TS.BS. NGUYỄN THẾ CƯỜNG
Trưởng khoa Thận – Lọc máu , BV Hữu nghị Việt Đức
Tăng kali máu là một rối loạn điện giải thường gặp ở người bệnh bệnh thận mạn và suy tim, đặc biệt khi sử dụng các liệu pháp nền tảng ức chế hệ renin–angiotensin–aldosterone (RAASi) và đối kháng thụ thể mineralocorticoid (MRA). Tăng kali máu liên quan mạnh đến nguy cơ rối loạn nhịp, tử vong, tái nhập viện và chi phí y tế cao cả trong giai đoạn nội viện và hậu xuất viện. Đồng thời, tăng kali máu là nguyên nhân phổ biến khiến bác sĩ giảm liều hoặc ngừng các liệu pháp nền tảng có lợi ích sống còn, làm mất đi hiệu quả bảo vệ tim–thận và gia tăng biến cố bất lợi. Bài viết tổng hợp gánh nặng dịch tễ, kinh tế và lâm sàng của tăng kali máu; làm rõ vai trò tối ưu hóa RAASi/MRA theo khuyến cáo quốc tế (KDIGO 2024, ESC 2021) và trong nước (Bộ Y tế/BYT) và trình bày cách tiếp cận xử trí tăng kali máu từ cấp cứu đến mạn tính, nhấn mạnh các chiến lược cho phép duy trì liệu pháp nền tảng, điều chỉnh chế độ ăn, lợi tiểu, và theo dõi định kỳ kali máu ở nhóm nguy cơ cao.
1. Gánh nặng của tăng kali máu về bệnh tật, tử vong, chi phí y tế trong giai đoạn nội viện và hậu xuất viện
Tăng kali máu định nghĩa theo đa số tài liệu là kali huyết thanh > 5,0 mmol/L; mức 5,1–5,9 mmol/L thường gọi là nhẹ, 6–6,4 mmol/L là trung bình và ≥ 6,5 mmol/L là nặng (xem Bảng 1). Ở người bệnh bệnh thận mạn, suy tim, đái tháo đường hoặc đang dùng RAASi/MRA, nguy cơ tăng kali máu cao hơn rõ rệt.
Bảng 1: Phân loại mức độ tăng kali máu theo một số khuyến cáo
| Mức độ tăng kali máu | Nhẹ | Trung bình | Nặng |
| ERC 2025 [2]
KDIGO 2024 [1] UKKA 2023 [3] |
5,1 – 5,9 | 6 – 6,4 | ≥ 6,5 |
| ESC 2018 [4] | 5,1 – 5,4 | 5,5 – 6 | > 6 |
| BYT Việt Nam 2015 [15] | Tăng kali máu > 5 mmoL/L. Chưa chia mức độ. | ||
ERC: European Resuscitation Council (ERC), ESC: European Society of Cardiology, KDIGO: Kidney Disease: Improving Global Outcomes, UKKA: United Kingdom Kidney Association
1.1. Gánh nặng bệnh tật, tái nhập viện, tử vong và chi phí y tế
Tần suất tăng kali máu khác nhau giữa người bệnh nội trú và ngoại trú. Tăng kali máu hiện diện ở 2–4% dân số chung và ở 10–55% người bệnh nhập viện vì bất kỳ lý do nào, tùy thuộc vào ngưỡng K+ được dùng để định nghĩa trong các nghiên cứu khác nhau [4]. Cả tỷ lệ hiện mắc tăng kali máu và nguy cơ tái phát đều tăng khi mức độ nặng và số lượng bệnh đi kèm tăng. Tỷ lệ xuất hiện tăng kali máu tăng theo mức độ suy giảm chức năng thận. Trong thực hành lâm sàng, tăng kali máu gặp ở tới 73% người bệnh bệnh thận mạn giai đoạn tiến triển và ở tới 40% người bệnh suy tim mạn [4].
Tăng kali máu gây thay đổi điện thế màng tế bào cơ tim, dẫn đến rối loạn dẫn truyền, rối loạn nhịp, block nhĩ–thất, rung thất, và ngưng tim. Tăng kali máu dẫn đến nhập viện thường xuyên hơn và tăng tỷ lệ tử vong, đặc biệt khi không được theo dõi chặt chẽ [4]. Tỷ lệ tử vong trong bệnh viện cao hơn rõ rệt ở người bệnh tăng kali máu (18,1%) so với người bệnh hạ kali máu (5,0%) hoặc kali máu bình thường (3,9%) [3]. Đã ghi nhận mối liên quan hình chữ U giữa nồng độ K+ huyết thanh và tỷ lệ tử vong, bao gồm cả ở người bệnh bệnh thận mạn chưa điều trị thay thế và đang điều trị thay thế thận. Những người bệnh tăng kali máu nặng (K+ > 6,5 mmol/l) có nguy cơ cao nhất và tỷ lệ tử vong trong bệnh viện >30% đã được báo cáo [3].
Ở nhóm người bệnh nội trú, tăng kali máu kéo dài hoặc tái phát làm tăng thời gian nằm viện, nhu cầu theo dõi, xét nghiệm lặp lại, và can thiệp cấp cứu. Sau xuất viện, tăng kali máu dai dẳng làm tăng tái nhập viện do rối loạn nhịp, suy tim mất bù, hoặc biến chứng thận. So với nhóm đối chứng không có tăng kali máu, nhóm người bệnh có ít nhất một biến cố tăng kali máu trong năm có mức sử dụng nguồn lực tại khoa Cấp cứu cao hơn 72%, tỷ lệ nhập viện nội trú tăng gấp 2 lần, thời gian nằm viện trung bình gấp 2 lần và số lần khám ngoại trú trung bình tăng khoảng 43% (p<0,001) [6]. So với nhóm người bệnh tim – thận không có tăng kali máu, nguy cơ nhập viện trong vòng 6 tháng cao hơn 3,8 lần ở người bệnh bệnh thận mạn kèm tăng kali máu [7] và cao hơn 2,8 lần ở người bệnh suy tim kèm tăng kai máu [8]. Những số liệu này phản ánh chăm sóc tốn kém kéo dài sau một đợt tăng kali máu, đặc biệt khi tăng kali máu dai dẳng hoặc tái phát.
1.2. Ảnh hưởng của tăng kali máu đến việc tối ưu hóa các liệu pháp điều trị nền tảng ở người bệnh tim mạch – thận
Các hướng dẫn điều trị hiện hành nhất quán nhấn mạnh tối ưu sớm liệu pháp điều trị nền tảng (GDMT) trong suy tim và bệnh thận mạn nhằm cải thiện sống còn và giảm nhập viện. Tuy nhiên, tăng kali máu là rào cản chính khiến bác sĩ trì hoãn, giảm liều hoặc ngừng các thuốc có lợi ích sống còn. Nghiên cứu đời thực trên quần thể lớn người bệnh tim–thận tại Vương quốc Anh cho thấy người bệnh có kali huyết thanh ≥ 5,0 mmol/L có nguy cơ bị giảm liều RAASi cao hơn (OR hiệu chỉnh: bệnh thận mạn 1,79 [KTC 95%: 1,64–1,96]; suy tim 1,33 [KTC 95%: 1,08–1,62]) [9]. Dữ liệu từ nghiên cứu đời thực ZORA bao gồm 25.963 người bệnh tại Hoa Kỳ và 8.722 người bệnh tại Nhật Bản mắc bệnh thận mạn và/hoặc suy tim cho thấy sau đợt tăng kali máu, các thuốc ức chế men chuyển angiotensin hoặc chẹn thụ thể angiotensin (ACEi/ARB) bị ngừng ở 23%–26% người bệnh và các thuốc đối kháng thụ thể mineralocorticoid (MRA) bị ngừng ở 33%–46% người bệnh [14]. Chỉ 10-15% người bệnh Hoa Kỳ và 6-8% người bệnh Nhật Bản khởi trị lại RAASi trong vòng 6 tháng [14]. Trong số những người bệnh khởi trị lại RAASi, 17% đến 37% người bệnh ở cả Hoa Kỳ và Nhật Bản bị giảm liều ACEi/ARB hoặc MRA trên 25%. Do đó, quản lý tăng kali máu không chỉ là kiểm soát một thông số điện giải mà còn là điều kiện tiên quyết để tối ưu GDMT.
Thực tế này phản ánh nhu cầu chiến lược quản lý kali máu dài hạn và hiệu quả để giảm chi phí, ngăn tái phát và cho phép duy trì liệu pháp nền tảng.
2. Vai trò của tối ưu hóa các liệu pháp nền tảng RAASi và MRA trên người bệnh tim mạch – thận
RAASi (ức chế men chuyển ACEi, chẹn thụ thể angiotensin ARB, ức chế renin trực tiếp ARNI) và MRA (spironolactone, eplerenone, finerenone) là trụ cột điều trị trong suy tim phân suất tống máu giảm (HFrEF), albumin niệu do đái tháo đường, và bệnh thận mạn, giúp giảm tử vong, tiến triển bệnh thận và nhập viện. Tuy nhiên, các thuốc này làm tăng nguy cơ tăng kali máu, nhất là ở bệnh thận mạn giai đoạn 3–5, đái tháo đường, dùng phối hợp thuốc, hoặc có toan chuyển hóa.
Trong thực hành, khi người bệnh xuất hiện tăng kali máu, bác sĩ thường giảm liều hoặc ngừng các thuốc ức chế hệ renin–angiotensin–aldosterone (RAASi: ACEi/ARB) và/hoặc kháng aldosterone (MRA). Tuy nhiên, nghiên cứu quan sát quy mô lớn trên 13.000 người bệnh suy tim và trên 100.000 người bệnh bệnh thận mạn mới mắc cho thấy việc điều trị RAASi/MRA dưới ngưỡng liều khuyến cáo (≤50% liều đích) hoặc ngừng thuốc làm tăng mạnh biến cố bất lợi. Ở nhóm suy tim mạn, giảm liều/ngừng RAASi liên quan với tăng tới khoảng 7,3 lần nguy cơ tử vong do mọi nguyên nhân [9]; còn ở bệnh thận mạn, nguy cơ này có thể tăng đến khoảng 5,6 lần [9]. Ngoài ra, việc ngừng hoặc giảm liều RAASi ở bệnh thận mạn làm tăng 74% hoặc 60% nguy cơ tiến triển đến bệnh thận giai đoạn cuối và việc ngừng hoặc giảm liều RAASi ở suy tim cho thấy 20,8% người bệnh có nguy cơ tái nhập viện hoặc nhập viện khẩn cấp vì suy tim (so với chỉ 14,6% người bệnh nếu bệnh nhân duy trì hoặc tối ưu liều RAASi) [10,11]. Điều này phản ánh vai trò quan trọng của RAASi/MRA của điều trị bảo vệ tim–thận: duy trì và tối ưu hóa liều mang lại lợi ích sống còn và làm chậm tiến triển bệnh, ngược lại giảm liều/ ngừng thuốc sớm vì tăng kali máu sẽ dẫn đến hậu quả nặng nề.
Các hướng dẫn hiện hành đều thống nhất cách tiếp cận “ưu tiên bảo tồn RAASi”. KDIGO 2024, ESC 2021, Đồng thuận Delphi quốc tế 2022 và Hướng dẫn Bộ Y tế về chẩn đoán và điều trị bệnh thận mạn 2024 khuyến cáo [1,5,12,13]:
1) Tối ưu hóa RAASi đến liều tối đa người bệnh dung nạp;
2) Chủ động theo dõi kali máu sau khi khởi trị và trong suốt quá trình điều trị;
3) Nếu xuất hiện tăng kali máu, cần xử trí tăng kali máu bằng các biện pháp hiệu quả để cho phép tiếp tục RAASi/MRA;
4) Chỉ khi các biện pháp kiểm soát kali thất bại mới cân nhắc giảm liều hoặc ngừng RAASi/MRA. Cách tiếp cận theo bậc thang này nhằm vừa bảo toàn lợi ích tim–thận của RAASi/MRA, vừa kiểm soát an toàn nguy cơ tăng kali máu, từ đó giảm nhập viện và tử vong.
Thông điệp từ khuyến cáo:
- ESC 2021 [5]: Tối ưu GDMT gồm ACEi/ARB/ARNI, β-blocker, MRA, SGLT2i càng sớm càng tốt. Tăng kali máu cần xử trí tích cực để tiếp tục MRA/RAASi và cân nhắc thuốc hạ kali thế hệ mới. Các thuốc hạ kali mới có thể cho phép khởi đầu hoặc tăng liều thuốc ức chế RAAS ở tỉ lệ lớn hơn người bệnh.
- Đồng thuận Delphi quốc tế về khuyến cáo thực hành tốt nhất trong quản lý tăng kali máu trên bệnh tim – thận 2022 [12]: Không nên giảm liều hoặc ngừng thuốc ức chế hệ renin–angiotensin–aldosterone (RAASi) chỉ vì tăng kali máu, trừ khi đã tối ưu các biện pháp khác để kiểm soát tăng kali máu mà vẫn không đạt mục tiêu. Các thuốc gắn kali mới (novel K+ binders) nên được ưu tiên sử dụng để kiểm soát tăng kali máu và nên dùng nhằm cho phép khởi trị, duy trì và tối ưu hóa liệu pháp RAASi.
- KDIGO 2024 [1]: Ưu tiên duy trì RAASi/MRA ở liều khuyến cáo. Theo dõi sát kali và chức năng thận sau khởi trị/tăng liều RAASi/MRA. Khi tăng kali máu, cần triển khai biện pháp kiểm soát kali hiệu quả (điều chỉnh ăn, lợi tiểu, bicarbonate nếu toan chuyển hóa, các tác nhân trao đổi kali) trước khi cân nhắc giảm/ngừng RAASi/MRA.
- Hướng dẫn Bộ Y tế về Chẩn đoán và điều trị bệnh thận mạn 2024 [13]: Xét nghiệm kali, creatinine máu sau 2-4 tuần khởi trị với thuốc ức chế RAAS. Khi có tăng kali máu cần áp dụng các biện pháp giảm kali máu trước khi giảm liều hay ngừng ức chế RAAS. Chỉ giảm liều hoặc ngừng ức chế RAAS khi người bệnh bị tụt huyết áp, tăng kali máu không thể kiểm soát được bằng các biện pháp nội khoa.
Tóm lại, chiến lược hiện đại là “bảo vệ GDMT” – kiểm soát kali để duy trì RAASi/MRA thay vì hy sinh liệu pháp nền tảng.
3. Xử trí tăng kali máu
3.1. Phân tầng mức độ và ngưỡng cần xử trí
Tăng kali máu nhẹ: Đánh giá nguyên nhân, thuốc, chế độ ăn; tăng cường theo dõi; thường không cần can thiệp cấp cứu.
Tăng kali máu trung bình: Can thiệp hạ kali, đặc biệt nếu có thay đổi ECG, suy thận tiến triển, toan chuyển hóa, hoặc đang dùng RAASi/MRA cần duy trì.
Tăng kali máu nặng hoặc có tăng kali máu có kèm biến đổi ECG: Là trường hợp cần can thiệp cấp cứu. Ưu tiên ổn định màng tế bào, chuyển kali vào nội bào và loại bỏ kali khỏi cơ thể; theo dõi liên tục.
Lưu ý: Diễn giải kali cần gắn với lâm sàng, tốc độ tăng, biểu hiện ECG và nguy cơ nền (bệnh thận mạn, suy tim, dùng digoxin, toan chuyển hóa).
3.2. Điều trị tăng kali máu cấp (Hướng dẫn Bộ Y Tế 2015)
Mục tiêu là nhanh chóng giảm độc tính trên tim và hạ kali huyết thanh.
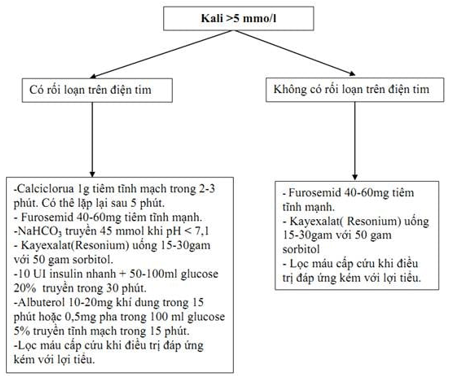
Hình 1: Sơ đồ xử trí tăng kali máu [15]
3.2.1. Ổn định màng tế bào cơ tim
Calciclorua giúp làm ổn định màng tế bào cơ tim, không có tác dụng làm giảm nồng độ kali máu, cần phải kết hợp với các biện pháp khác để điều trị tăng kali máu. Liều từ 0,5-2 g tùy từng người bệnh. Sau tiêm canxiclorua có tác dụng ngay và thời gian tác dụng kéo dài 30-60 phút.
3.2.2. Chuyển kali vào nội bào:
- Insulin và glusoce:
- Insulin có tác dụng chuyển kali từ ngoài vào trong tế bào tuy nhiên để tránh biến chứng hạ đường huyết chúng ta cần bổ sung thêm glucose.
- Hiệu quả của insulin bắt đầu sau 10 đến 20 phút, đạt đỉnh sau 30 đến 40 phút và kéo dài 4 đến 6 giờ. Ở hầu hết người bệnh nồng độ kali máu giảm 0,5-1,2 mmol/L.
- Natri bicarbonat:
Tăng pH máu làm ion H+ giải phóng vào máu như một phản ứng đệm, giúp cho kali di chuyển vào trong tế bào làm giảm kali máu. Thời gian bắt đầu có tác dụng sau 6 giờ. Không nên sử dụng natri bicarbonat đơn độc trong điều trị tăng kali máu cũng như các người bệnh toan chuyển hóa vừa và nhẹ. (HCO3 – > 18 mEq/L).
- Kích thích Beta-2 adrenergic (albuterol): cũng giống như insulin, albuterol có tác dụng vận chuyển kali máu vào trong tế bào. Thời gian tác dụng sau 10-15 phút và kéo dài 3-6 giờ.
3.2.3. Loại bỏ kali khỏi cơ thể
- Lợi tiểu quai (furosemid): có tác dụng đào thải kali qua nước tiểu, tuy nhiên những người bệnh suy thận nặng chức năng đào thải kali kém, hiệu quả điều trị hạ kali máu của lợi tiểu kém đáp ứng.
- Nhựa trao đổi cation: kali liên kết với nhựa trao đổi cation, giúp cho ngăn ngừa kali hấp thu qua ruột vào máu, từ đó kali sẽ được đào thải qua phân. Thời gian có tác dụng sau 1-2 giờ và kéo dài 4-6 giờ. Tuy nhiên, sodium polystyrene sulfonate hiện không được khuyến khích sử dụng vì hiệu quả kém và nguy cơ biến chứng đường tiêu hóa như hoại tử và thủng ruột [16,17]. Ngoài ra, gần đây hướng dẫn điều trị bệnh thận mạn của BYT có khuyến cáo các thuốc polymer gắn kali đường uống thế hệ mới, như muối silicate của zirconium, có thể điều chỉnh liều để duy trì nồng độ kali máu trong giới hạn an toàn, giúp có thêm các lựa chọn điều trị cho các người bệnh tăng kali máu [13].
- Lọc máu cấp cứu ngắt quãng: (thẩm tách máu hay còn gọi là thận nhân tạo – IHD) là biện pháp đào thải Kali có hiệu quả, nhanh có tác dụng sau 30 phút chỉ định ở người bệnh tăng kali máu nặng có biểu hiện trên điện tim hoặc trường hợp tăng kali máu điều trị kém đáp ứng với lợi tiểu. Phương thức lọc máu liên tục (CVVH) kết quả chậm hơn.
+ Ngừng/rà soát thuốc làm tăng kali: Tạm ngừng thuốc bổ sung kali, thuốc lợi tiểu giữ kali, NSAIDs, trimethoprim, heparin, thuốc ức chế calcineurin…; đánh giá ARNI/RAASi/MRA trong bối cảnh cấp, song mục tiêu vẫn là khôi phục và duy trì về sau khi kiểm soát được kali.
+ Theo dõi: Điện tim liên tục trên monitor. Nếu điện tim không thay đổi làm xét nghiệm kali 2 giờ/lần cho đến khi trở về bình thường. Nếu có biến đổi trên điện tim làm xét nghiệm kali ngay.
Khuyến cáo Bộ Y tế trong cấp cứu nhấn mạnh trình tự xử trí tăng kali máu cấp gồm bảo vệ tim bằng calci, sau đó chuyển kali vào nội bào, loại bỏ kali khỏi cơ thể, song song tìm và xử trí nguyên nhân và chuẩn bị chiến lược duy trì.
3.3. Điều trị tăng kali máu mạn: chiến lược ưu tiên và tối ưu hóa GDMT
Mục tiêu mạn tính là ngăn tái phát, cho phép duy trì hoặc tăng liều RAASi/MRA theo khuyến cáo, và giảm nhập viện.

Hình 2: Quản lý tăng kali máu ở người bệnh bệnh thận mạn [1]
+ Chế độ ăn
Bằng chứng chất lượng cao về hiệu quả của việc hạn chế kali trong chế độ ăn còn thiếu, và chế độ ăn ít kali có thể làm thiếu dưỡng chất, mâu thuẫn với chế độ ăn tốt cho tim như DASH. Ở người bệnh chạy thận, tăng ăn trái cây và rau giúp giảm tử vong do mọi nguyên nhân 5,0% và không do tim mạch 3,0%; tiêu thụ nhiều trái cây rau cũng liên quan đến chậm suy giảm chức năng thận. [17]
Điều chỉnh lượng kali theo bữa ăn, cân bằng với mục tiêu dinh dưỡng và lợi ích chế độ ăn giàu thực vật. Tư vấn cá thể hóa theo giai đoạn bệnh thận mạn. Trong giai đoạn đầu của bệnh thận mạn, thức ăn tự nhiên giàu kali dường như có tác dụng bảo vệ chống lại tiến triển bệnh [1]. Hạn chế tiêu thụ thực phẩm giàu kali (ví dụ: thực phẩm chế biến) đối với người bệnh bệnh thận mạn giai đoạn 3-5, những người có tiền sử tăng kali máu hoặc như một chiến lược phòng ngừa trong các giai đoạn bệnh mà nguy cơ tăng kali máu có thể là mối quan tâm. [1]
+ Rà soát thuốc không thuộc RAASi
Hạn chế NSAIDs, trimethoprim-sulfamethoxazole, heparin, thuốc ức chế calcineurin, lợi tiểu giữ kali và thuốc bổ sung kali; cân nhắc thay thế khi có thể.
+ Can thiệp bằng thuốc
- Lợi tiểu quai hoặc thiazide: Hữu ích khi có thừa dịch hoặc tăng huyết áp; tăng bài tiết kali ở thận còn chức năng. Theo dõi thể tích, điện giải để tránh làm nặng thêm hạ thể tích hoặc suy chức năng thận, dẫn đến tăng kali máu về sau.
- Natri bicarbonate đường uống có thể sử dụng cho người bệnh tăng kali máu có toan chuyển hóa. Tuy nhiên, bổ sung bicarbonat natri kéo dài có thể làm tăng tải natri, từ đó làm nặng thêm tình trạng quá tải dịch ở người bệnh bệnh thận mạn và suy tim. [17]
- Thuốc gắn kali thế hệ mới: Hầu hết các hướng dẫn như ESC 2021, Đồng thuận Dephil quốc tế về khuyến cáo thực hành tốt nhất trong quản lý tăng kali máu trên bệnh tim – thận 2022, UKKA 2023 và KDIGO 2024 đều ủng hộ sử dụng các chất gắn kali thế hệ mới để kiểm soát tăng kali máu đồng thời duy trì và tối ưu điều trị RAASi [1,3,5,17].
+ Quản lý RAASi/MRA song hành
- Thuốc ức chế thụ thể mineralocorticoid (MRA) làm tăng Kali máu, cần theo dõi kali sau khi khởi trị/tăng liều MRA. BN tăng kali > 5 mmol/L hoặc MLCT <30ml/phút/1,73m2 không nên sử dụng nhóm này. [13]
- Thuốc ức chế hệ renin angiotensin (RAASi): Xét nghiệm kali, creatinine máu sau 2-4 tuần. Khi có tăng kali máu cần áp dụng các biện pháp giảm kali máu trước khi giảm liều hay ngừng ức chế RAAS. Chỉ giảm liều hoặc ngừng ức chế RAAS khi người bệnh bị tụt huyết áp, tăng kali máu không thể kiểm soát được bằng các biện pháp nội khoa. [13]
- Kết hợp resin gắn kali khi kali tăng hoặc có nguy cơ; tránh ngừng RAASi/MRA trừ khi tăng kali nặng không kiểm soát. ESC 2021 có khuyến cáo cụ thể về việc sử dụng thuốc gắn kali mới và tăng/giảm/ngưng RAASi/MRA với từng mức nồng độ kali máu (xem Bảng 2).
- Cân nhắc ARNI (sacubitril/valsartan); SGLT2i (dapagliflozin, empagliflozin) giúp giảm nguy cơ tăng kali máu.
Bảng 2: Quản lý tăng kali máu mạn ở người bệnh suy tim [5]
| Ở người bệnh tăng kali máu mạn tính hoặc tái phát đang điều trị bằng thuốc ức chế RAAS, có thể bắt đầu sử dụng thuốc hạ kali được phê duyệt ngay khi nồng độ K⁺ > 5,0 mEq/L. Theo dõi chặt chẽ nồng độ K⁺. Duy trì điều trị trừ khi xác định được nguyên nhân khác có thể điều trị. |
| Ở người bệnh tăng kali máu mạn tính hoặc tái phát nhưng không dùng nạp liều tối đa theo khuyến cáo của thuốc ức chế RAAS, có thể bắt đầu sử dụng thuốc hạ kali được phê duyệt ngay khi nồng độ K⁺ > 5,0 mEq/L. Theo dõi chặt chẽ nồng độ K⁺. Duy trì điều trị trừ khi xác định được nguyên nhân khác có thể điều trị. Thuốc ức chế RAAS nên được tối ưu hóa khi nồng độ K⁺ < 5,0 mEq/L. |
| Ở người bệnh có nồng độ K⁺ từ 4,5–5,0 mEq/L và chưa dung nạp liều tối đa theo khuyến cáo, có thể khởi đầu hoặc tăng liều thuốc ức chế RAAS. Theo dõi chặt chẽ nồng độ K⁺. Nếu nồng độ K⁺ vượt quá 5,0 mEq/L, hãy bắt đầu sử dụng thuốc hạ kali được phê duyệt. |
| Ở người bệnh có nồng độ K⁺ từ >5,0–≤6,5 mEq/L và chưa dung nạp liều tối đa theo khuyến cáo nên bắt đầu sử dụng thuốc hạ kali được phê duyệt. Nếu nồng độ K⁺ < 5,0 mEq/L, tăng liều thuốc ức chế RAAS; nồng độ K⁺ cần được theo dõi chặt chẽ và duy trì điều trị hạ kali trừ khi xác định được nguyên nhân khác có thể điều trị. |
| Ở người bệnh có nồng độ K⁺ từ >5,0–≤6,5 mEq/L và đã dung nạp liều tối đa theo khuyến cáo của thuốc ức chế RAAS, nên bắt đầu sử dụng thuốc hạ kali được phê duyệt. Nồng độ K⁺ cần được theo dõi chặt chẽ và duy trì điều trị hạ kali trừ khi xác định được nguyên nhân khác gây tăng kali máu có thể điều trị. |
| Ở người bệnh có nồng độ K⁺ >6,5 mEq/L đã dùng liều tối đa hoặc dưới tối đa theo khuyến cáo của thuốc ức chế RAAS, nên ngừng hoặc giảm liều thuốc ức chế RAAS. Điều trị bằng thuốc hạ kali có thể bắt đầu ngay khi nồng độ K⁺ ≥ 5,0 mEq/L; cần theo dõi chặt chẽ nồng độ K⁺. |
+ Theo dõi định kỳ để phòng ngừa tái phát
- Kiểm tra kali và creatinine huyết thanh trong vòng 2–4 tuần sau khi khởi trị hoặc tăng liều RAASi/MRA [1]
- Người bệnh bệnh thận mạn, suy tim và/hoặc đái tháo đường, người bệnh có nguy cơ tăng kali máu (dùng các thuốc gây tăng kali máu như RAASi/MRA) cần được đánh giá kali máu 2–4 lần/năm tùy thuộc vào chức năng thận và mức độ protein niệu (1B). [3]
- Theo dõi người bệnh sau một đợt tăng kali máu nhẹ (K+ 5,5–5,9 mmol/L) phát hiện tại cộng đồng: UKKA 2023 khuyến nghị lặp lại xét nghiệm kali huyết thanh trong vòng 3 ngày, hoặc sớm nhất có thể (1C). [3]
- Theo dõi người bệnh sau một đợt tăng kali máu trung bình (K+ 6,0–6,4 mmol/L) phát hiện tại cộng đồng: UKKA 2023 khuyến nghị lặp lại xét nghiệm kali huyết thanh trong vòng 1 ngày (1C). [3]
- Theo dõi người bệnh sau một đợt tăng kali máu nặng phát hiện tại cộng đồng: UKKA 2023 khuyến nghị những người bệnh có tăng kali máu nặng (K+ ≥ 6,5 mmol/l) phát hiện tại cộng đồng nên được nhập viện để đánh giá và điều trị ngay lập tức (1B). [3]
Kết luận
Quản lý tăng kali máu là yếu tố cốt lõi để tối ưu hóa liệu pháp nền tảng ở người bệnh tim mạch–thận. Thay vì giảm liều hay ngừng RAASi/MRA, cách tiếp cận hiện đại nhấn mạnh kiểm soát kali chủ động bằng điều chỉnh chế độ ăn, rà soát thuốc, lợi tiểu, bicarbonate khi có toan chuyển hóa, và đặc biệt là sử dụng các thuốc gắn kali thế hệ mới để duy trì kali mục tiêu và bảo toàn lợi ích quan trọng của GDMT. Theo dõi định kỳ 2–4 lần/năm ở nhóm nguy cơ cao là cần thiết để phòng ngừa tái phát, giảm nhập viện và chi phí y tế. Kết hợp chăm sóc tim – thận – chuyển hóa, cùng với giáo dục người bệnh và chuẩn hóa quy trình, sẽ giúp hiện thực hóa mục tiêu kép: Kiểm soát toàn diện điện giải từ đó giúp tối ưu các điều trị nền tảng và gia tăng hiệu quả bảo vệ tim thận.
Tài liệu tham khảo:
- KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease, Kidney International (2024) 105 (Suppl 4S), S117–S314
- Lott, Carsten et al., European Resuscitation Council Guidelines 2025 Special Circumstances in Resuscitation, Resuscitation, Volume 215, 110753
- UKKA Clinical Practice Guideline – Management of Hyperkalaemia in Adults – October 2023
- Giuseppe M C Rosano et al., Expert consensus document on the management of hyperkalaemia in patients with cardiovascular disease treated with renin angiotensin aldosterone system inhibitors: coordinated by the Working Group on Cardiovascular Pharmacotherapy of the European Society of Cardiology, European Heart Journal – Cardiovascular Pharmacotherapy, Volume 4, Issue 3, July 2018, Pages 180–188
- Theresa A McDonagh et al., 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) With the special contribution of the Heart Failure Association (HFA) of the ESC, European Heart Journal, Volume 42, Issue 36, 21 September 2021, Pages 3599–3726
- Betts KA et al. The Cost of Hyperkalemia in the United States, Kidney Int Rep. 2018;3(2):385-393
- Thomsen RW et al. Elevated potassium levels in patients with chronic kidney disease: occurrence, risk factors and clinical outcomes-a Danish population-based cohort study, Nephrol Dial Transplant. 2018;33(9):1610-1620
- Thomsen RW et al. Elevated Potassium Levels in Patients With Congestive Heart Failure: Occurrence, Risk Factors, and Clinical Outcomes: A Danish Population-Based Cohort Study, J Am Heart Assoc. 2018;7(11):e008912.
- Cecilia Linde et al., Real‐World Associations of Renin–Angiotensin–Aldosterone System Inhibitor Dose, Hyperkalemia, and Adverse Clinical Outcomes in a Cohort of Patients With New‐Onset Chronic Kidney Disease or Heart Failure in the United Kingdom, J Am Heart Assoc. 2019;8:e012655
- Rastogi A et al., Association Between Reduced RAASi Therapy and Progression to ESKD in Hyperkalemic CKD Patients, Journal of the American Society of Nephrology 34(11S):p 379, November 2023
- Kanda, E., Rastogi, A., Murohara, T. et al. Clinical impact of suboptimal RAASi therapy following an episode of hyperkalemia. BMC Nephrol 24, 18 (2023)
- James O. Burton et al., An international Delphi consensus regarding best practice recommendations for hyperkalaemia across the cardiorenal spectrumEuropean, Journal of Heart Failure (2022) 24, 1467–1477
- Quyết định số 2388/QĐ-BYT ngày 12/8/2024 của Bộ Y tế về việc ban hành tài liệu chuyên môn “Hướng dẫn chẩn đoán và điều trị bệnh thận mạn và một số bệnh lý thận”
- Kanda, E., Rastogi, A., Murohara, T. et al. Clinical impact of suboptimal RAASi therapy following an episode of hyperkalemia. BMC Nephrol 24, 18 (2023).
- Quyết định số 1493/QD-BYT ngày 22/4/2015 của Bộ Y tế về việc ban hành tài liệu chuyên môn “Hướng dẫn chẩn đoán và xử trí hồi sức tích cực”
- Panchal AR et al. on behalf of the Adult Basic and Advanced Life Support Writing Group. Part 3: adult basic and advanced life support: 2020 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care, Circulation. 2020;142(suppl 2):S366–S468.
- De Nicola, L., Ferraro, P.M., Montagnani, A. et al. Recommendations for the management of hyperkalemia in patients receiving renin–angiotensin–aldosterone system inhibitors. Intern Emerg Med 19, 295–306 (2024).
2022 AHA/ACC/HFSA Guideline for the management of heart failure: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol 79:e263–e421







