BS. CKII. NGUYỄN HOÀNG DŨNG
Khoa Hồi sức Phẫu thuật tim, BV Chợ Rẫy
Hiệu đính: TS. BS. NGÔ MINH HÙNG
TÓM TẮT
Mục tiêu: Khảo sát mối liên quan giữa tần số tim và các kết cục ở bệnh nhân suy tim phân suất tống máu giảm có nhịp xoang và rung nhĩ được điều chỉnh theo nồng độ peptid bài natri niệu, một yếu tố tiên lượng quan trọng.
Phương pháp và kết quả: Trong số 13.562 bệnh nhân từ hai thử nghiệm lớn có suy tim phân suất tống máu giảm (HFrEF), 10.113 (74,6%) có nhịp xoang (SR) và 3449 (25,4%) có rung nhĩ (AF). Kết cục chính bao gồm tử vong do tim mạch hoặc nhập viện do suy tim. Nhịp tim được phân tích dưới dạng biến định tính (các nhóm, T1–3) và biến liên tục (mỗi 10 nhịp/phút), riêng biệt ở bệnh nhân SR và AF. Kết cục được điều chỉnh theo các biến tiên lượng, bao gồm tiền hormone peptid bài natri niệu týp B có chuỗi tận N (NT-proBNP) và cũng được kiểm tra bằng cách sử dụng sự thay đổi từ tần số tim nền đến 1 năm (≤ -10 nhịp/phút, ≥ + 10 nhịp/phút, <± 10 nhịp/phút). Bệnh nhân nhịp xoang với tần số tim cao hơn có các triệu chứng và chất lượng cuộc sống xấu hơn, thường mắc đái tháo đường nhiều hơn và nồng độ NT-proBNP cao hơn. Họ có nguy cơ của kết cục chính cao hơn [tỷ số nguy cơ (HR) điều chỉnh của T3 so với T1 là 1,5, 95% khoảng tin cậy (KTC) 1,35-1,66; P<0,001; mỗi 10 nhịp/phút là 1,12; KTC 95% 1,09 – 1,16; P<0,001]. Ở bệnh nhân nhịp xoang, tần số tim có liên quan đến nguy cơ suy bơm tương đối cao hơn đột tử [Tỉ số nguy cơ điều chỉnh mỗi 10 nhịp/phút là 1,17; KTC 95% 1,09 – 1,26; P <0,001 so với 1,07; KTC 95% 1,02 – 1.13; P = 0,011]. Tần số tim không dự báo được bất kỳ kết cục nào trong AF.
Kết luận: Trong suy tim phân suất tống máu giảm, tần số tim tăng là một yếu tố dự báo độc lập về kết cục tim mạch bất lợi ở bệnh nhân có nhịp xoang, ngay cả sau khi điều chỉnh theo NT-proBNP. Không có mối quan hệ giữa tần số tim và kết cục trong rung nhĩ.
Từ khoá: Suy tim phân suất tống máu giảm, Tần số tim
TỔNG QUAN:
Trong suy tim phân suất tống máu giảm (HFrEF) tăng tần số tim lúc nghỉ có liên quan đến tỉ lệ bệnh tật và tử vong cao hơn ở bệnh nhân có nhịp xoang. Hơn nữa ở những bệnh nhân này, tần số tim đã được chứng minh là một yếu tố nguy cơ có thể thay đổi được bằng cách sử dụng ivabradine, một chất ức chế kênh If của nút xoang, có tác dụng dược lý duy nhất làm giảm tần số tim. Tuy nhiên, vẫn còn một số câu hỏi liên quan đến mối quan hệ giữa tần số tim và các kết cục ở bệnh nhân suy tim phân suất tống máu giảm có nhịp xoang. Những phân tích hiện tại đã không điều chỉnh theo nồng độ peptid bài natri niệu, một yếu tố tiên lượng độc lập mạnh nhất trong suy tim và mức peptid bài natri niệu thường cao hơn ở bệnh nhân có tần số tim cao hơn. Những nghiên cứu trước đây có cở mẫu quá nhỏ nên không đánh giá được mối liên hệ giữa tần số tim và những dạng tử vong chính trong suy tim phân suất tống máu giảm, ví dụ đột tử và tử vong do suy tim nặng hơn. Hiện tại, những hiểu biết về sự thay đổi tần số tim liên quan đến các kết cục tim mạch vẫn còn hạn chế.
Mối liên quan giữa tần số tim và các kết cục trên bệnh nhân suy tim phân suất tống máu giảm có rung nhĩ chưa được nghiên cứu kỹ và rõ ràng. Rung nhĩ thường xuất hiện trong suy tim phân suất tống máu giảm và trở nên phổ biến hơn khi suy tim tiến triển. Mặc dù nhiều phân tích hậu kiểm của các nghiên cứu đoàn hệ quan sát và thử nghiệm đã báo cáo không có mối liên quan giữa tần số tim và kết cục ở bệnh nhân suy tim phân suất tống máu giảm và rung nhĩ, những nghiên cứu này có một số hạn chế. Ví dụ, không phải bệnh nhân nào cũng phân biệt được giữa tiền sử rung nhĩ và rung nhĩ ghi nhận trên điện tâm đồ tại thời điểm chọn bệnh. Điều này có liên quan đến một số lý do, bao gồm rung nhĩ kịch phát hoặc rung nhĩ mới khởi phát gần đây, chứ không phải rung nhĩ bền bỉ hoặc dai dẳng, đã được chứng minh là những dạng liên quan với kết cục xấu hơn ở bệnh nhân suy tim phân suất tống máu giảm. Quan trọng hơn, không có nghiên cứu nào trong số những nghiên cứu trước đây đo thường quy peptid bài natri niệu, đây là chất thường tăng cao hơn ở bệnh nhân rung nhĩ so với ở bệnh nhân nhịp xoang. Do đó, các nghiên cứu hiện tại không thể cho biết một cách chắc chắn liệu tần số thất lúc nghỉ có phải là một yếu tố tiên lượng độc lập về kết cục tim mạch bất lợi ở bệnh nhân suy tim phân suất tống máu giảm và rung nhĩ hay không. Tương tự như vậy, các nghiên cứu này cũng không thể so sánh mối quan hệ giữa tần số thất và các kết cục ở bệnh nhân rung nhĩ và nhịp xoang, điều quan trọng là nên tính đến mức độ khác nhau của peptid bài natri niệu trong hai nhóm này. Trên những bệnh nhân suy tim có nhịp xoang, người ta vẫn chưa biết thay đổi tần số tim liên quan như thế nào đến các kết cục.
Do đó, chúng tôi đã tìm hiểu mối liên quan giữa tần số tim căn bản thất lúc nghỉ (sau đây được gọi là “tần số tim”) và các kết cục trong hai thử nghiệm lâm sàng ngẫu nhiên lớn, đương đại, đa quốc gia, đa trung tâm, ở bệnh nhân suy tim phân suất tống máu giảm bằng cách sử dụng nhịp tim được xác định bằng điện tâm đồ ban đầu và điều chỉnh theo nồng độ tiền hormone peptid bài natri niệu týp B chuỗi tận N (NT-proBNP).
PHƯƠNG PHÁP:
Đối tượng và phương pháp nghiên cứu
Thiết kế, các đặc điểm cơ bản và kết quả của các thử nghiệm So sánh tiến cứu ARNI với ACEI để xác định tác động trên bệnh tật và tử vong toàn cầu trong suy tim (PARADIGM-HF) và Thử nghiệm Aliskiren để giảm thiểu kết cục ở bệnh nhân suy tim (ATMOSPHERE) đã được công bố chi tiết trước đây. Cả hai thử nghiệm đều được chấp thuận bởi Hội đồng Y đức ở mỗi trung tâm nghiên cứu và tất cả bệnh nhân đều đồng ý cung cấp thông tin bằng văn bản.
Các tiêu chuẩn tuyển vào nghiên cứu PARADIGM-HF và ATMOSPHERE gần giống nhau. Tóm lại, bệnh nhân đủ điều kiện để đưa vào nếu họ ≥18 tuổi, triệu chứng cơ năng theo phân loại của Hiệp hội Tim mạch New York (NYHA) từ II đến IV, có phân suất tống máu thất trái (LVEF) ≤35% (Hiệu chỉnh từ ≤40% ban đầu trong thử nghiệm PARADIGM-HF) và có mức peptide bài natri niệu tăng cao (điểm cắt không phụ thuộc vào sự hiện hữu hay không của rung nhĩ). Trước khi sàng lọc, điều trị bằng thuốc ức chế men chuyển hoặc thuốc chẹn thụ thể angiotensin với liều tương đương enalapril 10 mg mỗi ngày trong ít nhất 4 tuần là bắt buộc, cùng với thuốc chẹn beta (trừ khi có chống chỉ định hoặc không dung nạp được) và thuốc đối kháng thụ thể mineralocorticoid, nếu được chỉ định. Tiêu chuẩn loại trừ khi sàng lọc bao gồm hạ huyết áp có triệu chứng hoặc huyết áp tâm thu <95mmHg (<90mmHg trong thử nghiệm ATMOSPHERE), mức lọc cầu thận ước tính (eGFR) <30 mL/phút/1,73m2 (<35 mL/phút/1,73m2 trong thử nghiệm ATMOSPHERE ), và kali> 5,4 mmol/L (> 5,2 mmol/L trong thử nghiệm ATMOSPHERE).
Cả hai thử nghiệm đều liên quan đến giai đoạn điều trị nền bằng thuốc ức chế men chuyển hoặc thuốc chẹn thụ thể angiotensin, các điều trị này được dừng lại và những bệnh nhân khởi đầu bằng enalapril sau đó chuyển sang sử dụng sacubitril/valsartan trong thử nghiệm PARADIGM-HF và enalapril sau đó chuyển sang sử dụng kết hợp enalapril với aliskiren trong thử nghiệm ATMOSPHERE. Những bệnh nhân dung nạp được liều mục tiêu của thuốc sau đó được phân ngẫu nhiên vào liệu pháp mù đôi với sacubitril/valsartan 97/103 mg mỗi ngày 2 lần hoặc enalapril 10 mg mỗi ngày 2 lần theo tỷ lệ 1:1 trong thử nghiệm PARADIGM-HF, hoặc enalapril 10 mg mỗi ngày 2 lần, aliskiren 150 mg mỗi ngày (tăng lên đến 300 mg mỗi ngày sau 2 tuần nếu dung nạp được), hoặc cả hai loại thuốc theo tỷ lệ 1:1:1 trong thử nghiệm ATMOSPHERE.
Trong cả hai thử nghiệm, các điều tra viên được yêu cầu báo cáo về nhịp tim và tần số tim ghi trên điện tâm đồ nền. Một số lượng nhỏ bệnh nhân bị cuồng nhĩ cùng với những bệnh nhân có rung nhĩ trên điện tâm đồ nền của họ được đưa vào với mục đích nghiên cứu. Những bệnh nhân được ghi nhận có nhịp máy trên điện tâm đồ nền của họ đều bị loại khỏi phân tích này.
KẾT CỤC
Kết cục chính của cả hai thử nghiệm là tổng thời gian cho tới thời điểm tử vong do tim mạch hoặc nhập viện lần đầu do suy tim xảy ra. Trong phân tích này, chúng tôi đã nghiên cứu mối liên quan giữa tần số tim nền và nguy cơ của kết cục chính, từng thành phần tố đột tử, tử vong do suy bơm và tử vong do bất kỳ nguyên nhân nào. Chúng tôi thực hiện các phân tích riêng biệt này trên những bệnh nhân có nhịp xoang và những bệnh nhân có rung nhĩ trên ECG nền. Tất cả các kết cục đều được đánh giá cùng một hội đồng thẩm định các kết cục lâm sàng theo các tiêu chí được chỉ định trước.
PHÂN TÍCH THỐNG KÊ
Các đặc điểm cơ bản được trình bày theo các nhóm được xác định bởi các phân vị tần số tim (được tính riêng cho rung nhĩ và nhịp xoang), với trung bình ± độ lệch chuẩn (SD) hoặc trung vị (khoảng tứ phân vị) cho các biến liên tục, tần suất và tỷ lệ phần trăm cho các biến định tính. Sự khác biệt về các đặc điểm cơ bản theo các phân vị tần số tim từ sự phân bố tần số tim ghi trên ECG nền được đánh giá với một bài kiểm định xu hướng bằng phương pháp hồi quy bình phương có trọng số phương sai nhỏ nhất cho các biến liên tục và kiểm định phi tham số tìm xu hướng đối với các biến thứ bậc. Sự khác biệt về các đặc điểm cơ bản theo tần số tim nền được đánh giá bằng cách sử dụng kiểm định chi bình phương cho các biến thứ bậc và phân tích phương sai (ANOVA) hoặc kiểm định Kruskal-Wallis cho các biến liên tục.
Tỷ lệ xuất hiện các kết cục được biểu thị mỗi 100 người-năm. Đường cong thời gian tới lúc xảy ra biến cố được biểu thị bởi các phân vị tần số tim ghi trên ECG nền, được ước tính bằng phương pháp Kaplan – Meier và được so sánh bằng cách sử dụng kiểm định log-rank. Các hàm tỷ lệ mới mắc cộng dồn cho các kết cục cần quan tâm được tính dựa trên các nguy cơ tử vong cạnh tranh do mọi nguyên nhân và tử vong không do tim mạch. Không có sự khác biệt đáng kể nào được quan sát, do đó ước tính Kaplan-Meier mang tính đại diện. Các tỷ nguy cơ (HRs) với các khoảng tin cậy (KTC) 95% của các kết cục theo các phân vị tần số tim được tính toán sử dụng mô hình Cox lấy nhóm 1 làm tham chiếu. Một phân tích độ nhạy được thực hiện bằng cách sử dụng các phân vị tần số nhịp xoang được tính toán ở những bệnh nhân rung nhĩ trên ECG nền.
Tần số tim cũng được mô hình hóa như một biến liên tục với tỉ số nguy cơ ở khoảng tin cậy 95% được biểu thị cho mỗi 10 nhịp/phút. Mối quan hệ này được trình bày dưới dạng đồ thị trong một mô hình tuyến tính với tỉ số nguy cơ liên quan đến tần số tim nền là 80 nhịp/phút [được chọn trên cơ sở Hiệu quả Kiểm soát Tần số trong Rung nhĩ Bền bỉ: So sánh giữa thử nghiệm Lenient so với Kiểm soát Tần số nghiêm ngặt II (RACE II)]. Nếu có bất kỳ tương tác nào giữa tần số tim và nhịp tim trên các kết cục đều đã được kiểm định.
Các mô hình được hiệu chỉnh theo hướng điều trị ngẫu nhiên (enalapril, sacubitril/valsartan, aliskiren, hoặc kết hợp enalapril và aliskiren), và các đặc điểm cơ bản sau: tuổi, giới tính, chủng tộc, khu vực địa lý, phân loại triệu chứng cơ năng theo NYHA, LVEF, nguyên nhân thiếu máu cục bộ, huyết áp tâm thu, chỉ số khối cơ thể, eGFR, thời gian suy tim, tiền sử nhập viện do suy tim, tiền sử nhồi máu cơ tim, tiền sử đái tháo đường, tiền sử đột quỵ, điều trị bằng digoxin, điều trị bằng thuốc chẹn beta, điều trị bằng amiodarone và logarit của NT-proBNP. Dữ liệu về NT-proBNP nền bị thiếu ở 12 và 593 bệnh nhân tương ứng trong phân tích PARADIGM-HF và ATMOSPHERE. Đối với 593 bệnh nhân trong ATMOSPHERE, các giá trị thay thế được sử dụng để tính toán cho phân tích thử nghiệm sơ bộ và được trình bày chi tiết trong quy trình thử nghiệm. Giả định về các rủi ro tương ứng được kiểm định bằng cách sử dụng đường cong logarit [−log (sống còn)] và được nhận thấy hợp lệ cho tất cả các mô hình. Một phân tích độ nhạy được thực hiện đối với kết cục tổng hợp chính và kết cục đột tử do tim bằng việc bổ sung các đồng phương sai, chỉ định điều trị bằng thuốc đối kháng thụ thể mineralocorticoid và có cấy ghép máy khử rung tim và/hoặc liệu pháp tái đồng bộ tim cho các mô hình Cox đã điều chỉnh. Việc bổ sung các đồng phương sai này không làm thay đổi đáng kể kết quả được trình bày (dữ liệu ẩn). Một phân tích độ nhạy khác bao gồm những bệnh nhân có nhịp máy trên ECG nền có thiết bị điều trị tái đồng bộ tim cũng không ảnh hưởng đáng kể đến kết quả (dữ liệu ẩn).
Mối liên quan giữa sự thay đổi tần số tim theo thời gian và kết cục đã được nghiên cứu ở những bệnh nhân có ECG nền và 12 tháng và những người mà vẫn còn ở cùng nhịp với ECG ban đầu của họ. Ba nhóm được xác định: những người có tần số tim tăng 10 nhịp/phút trở lên, những người có tần số tim giảm 10 nhịp/phút trở lên và những người có tần số tim tăng hoặc giảm ít hơn 10 nhịp/phút. Kết cục được phân tích bằng cách sử dụng mô hình Cox cho các biến cố xảy ra ít nhất 12 tháng sau khi ngẫu nhiên hóa và được điều chỉnh cho cùng các đặc điểm cơ bản như đã trình bày ở trên và tần số tim nền, với nhóm tham chiếu là những người có tần số tim được ghi trên ECG thay đổi dưới 10 nhịp/phút qua hơn 12 tháng. Tỷ lệ bệnh nhân báo cáo sự thay đổi có ý nghĩa lâm sàng trong Bảng câu hỏi Bệnh cơ tim Thành phố Kansas (KCCQ) với điểm tổng kết lâm sàng (≥5 điểm) và sự khác biệt có ý nghĩa trong NT-proBNP (chỉ có sẵn ở bệnh nhân được chọn trong ATMOSPHERE) sau 12 tháng được tính toán và so sánh giữa ba nhóm sử dụng các phương pháp thống kê tương tự như đối với các đặc điểm cơ bản đã được trình bày ở trên.
Tất cả các giá trị đều là P hai đuôi và giá trị P <0,05 được xem là có ý nghĩa. Các phân tích được thực hiện bằng Stata phiên bản 15,1 (StataCorp, College Station, TX, USA).
KẾT QUẢ
Trong số 15 415 bệnh nhân được chọn ngẫu nhiên vào cả hai thử nghiệm, 1715 (11,1%) bệnh nhân được ghi nhận có nhịp máy trên ECG đều bị loại khỏi phân tích này (Hình S1 phụ lục trực tuyến). Ngoài ra, có 138 (0,9%) bệnh nhân không có ECG nền được ghi lại hoặc bị thiếu dữ liệu tần số tim. Như vậy, 13 562 bệnh nhân còn lại tuyển vào nghiên cứu, trong đó 3449 (25,4%) và 10 113 (74.6%) được báo cáo là có nhịp ECG nền là rung nhĩ và nhịp xoang theo thứ tự tương ứng.
Các đặc điểm cơ bản
Sự phân bố tần số tim nền được ghi trên ECG ở bệnh nhân nhịp xoang và những bệnh nhân rung nhĩ được trình bày trong Hình S2 phụ lục trực tuyến. Tần số tim trung bình cao hơn ở bệnh nhân rung nhĩ (79,9±17,2 nhịp/phút) so với nhịp xoang (70,1±13,1 nhịp/phút; P <0,001). Các nhóm tần số tim nền trong rung nhĩ được tính như sau: nhóm 1 (T1) ≤72 nhịp/phút, nhóm 2 (T2) 73 – 85 nhịp/phút và nhóm 3 (T3) ≥86 nhịp/phút. Mức tương ứng đối với bệnh nhân nhịp xoang lần lượt là ≤63 nhịp/phút, 64 – 75 nhịp/phút và ≥76 nhịp/phút.
Các đặc điểm cơ bản được tóm tắt trong Bảng phụ lục trực tuyến S1, theo các nhóm tần số tim và nhịp tim trên ECG nền. Sự khác biệt giữa những người có nhịp xoang hoặc rung nhĩ nền được tóm tắt trong Bảng phụ lục trực tuyến S2. Bất kể loại nhịp tim, bệnh nhân có tần số tim thấp hơn thường là nam giới, lớn tuổi và có eGFR thấp hơn, có triệu chứng cơ năng theo phân loại NYHA ít nghiêm trọng hơn, có thời gian suy tim lâu hơn, ít có khả năng phải nhập viện vì suy tim hơn, v.v. thường có một nguyên nhân chung là thiếu máu cục bộ. Điều trị bằng digoxin ít phổ biến hơn ở nhóm bệnh nhân có tần số tim thấp, tuy nhiên, amiodarone lại được sử dụng phổ biến hơn, và những bệnh nhân này có nhiều khả năng được cấy máy khử rung tim. Việc sử dụng thuốc lợi tiểu phổ biến hơn ở nhóm có tần số tim cao nhất và có nhịp xoang trong khi không thấy sự khác biệt đáng kể giữa các nhóm ở bệnh nhân rung nhĩ. Nhóm bệnh nhân nhịp xoang chứ không phải rung nhĩ lại sử dụng thuốc chẹn beta lại cao nhất ở phân vị có tần số tim thấp nhất (T1 so với T3 93,9% so với 89,0%, P <0,001). Tần số tim nền thấp hơn có liên quan đến phân suất thất trái cao hơn ở nhóm bệnh nhân có nhịp xoang chứ không phải nhóm rung nhĩ.
Tiền hormone Peptid bài natri niệu týp B có chuỗi tận N (NT-proBNP)
Nồng độ NT-proBNP tăng từ mức thấp nhất đến cao nhất của tần số tim ở bệnh nhân nhịp xoang (P <0,001), trong khi ở AF có xu hướng giảm mức NT-proBNP với tần số tim cao hơn, tuy nhiên điều này không đạt được ý nghĩa thống kê (P = 0,06).
Bảng câu hỏi Bệnh cơ tim Thành phố Kansas
Ở cả nhịp xoang và rung nhĩ, tần số tim thấp hơn có liên quan đến điểm KCCQ cao hơn (tốt hơn) (P <0,001 ở cả hai phía).
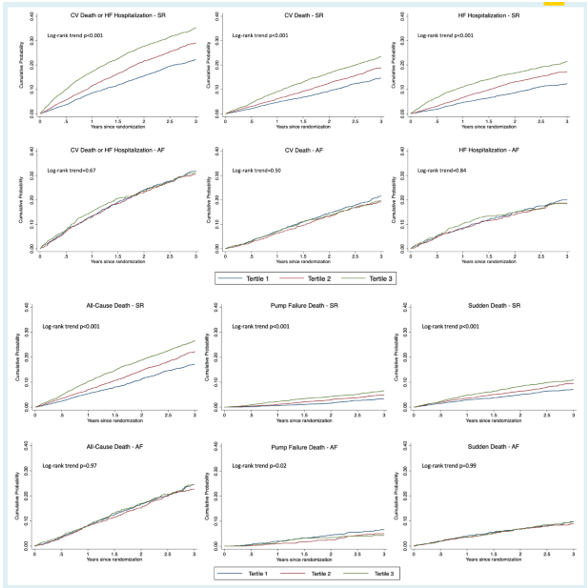
Hình 1. Phân tích sống còn Kaplan – Meier theo tần số tim và nhịp tim nền. Đường cong biến cố cho kết cục theo nhịp tim theo thời gian và các nhóm tần số tim nền (nhóm 1 thấp nhất/nhóm 3 cao nhất). AF: rung nhĩ; CV: tim mạch; HF: suy tim; SR: nhịp xoang.
KẾT CỤC LÂM SÀNG THEO CÁC PHÂN VỊ TẦN SỐ TIM
Nhịp xoang
Nguy cơ của tất cả các kết cục cao hơn đáng kể ở những bệnh nhân có tần số tim cao hơn trên ECG nền của họ (Hình 1 và bảng phụ lục trực tuyến S3). Nguy cơ gia tăng này vẫn có ý nghĩa đối với tất cả các kết cục sau khi điều chỉnh các biến có ý nghĩa tiên lượng khác (Hình 2 và Bảng phụ lục trực tuyến S3). Nguy cơ tương đối lớn nhất được ghi nhận với tử vong do suy bơm, trong đó nguy cơ tử vong do dạng này cao hơn 70% ở những người ở nhóm tần số tim cao nhất so với tần số tim thấp nhất (tỉ số chênh điều chỉnh 1,70; KTC 95% 1,30–2,22; P <0,001 ). Tỉ số nguy cơ điều chỉnh tương ứng cho đột tử là 1,28 (KTC 95% 1,06–1,54; P = 0,011).
Rung nhĩ
Ở những bệnh nhân có rung nhĩ trên điện tâm đồ nền của họ, chỉ có nguy cơ tử vong do suy bơm là khác nhau theo tần số tim, với nguy cơ thấp hơn ở các phân vị trên so với phân vị dưới.
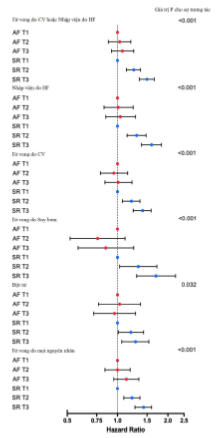
Hình 2. Biểu đồ phân bố về mối quan hệ giữa tần số tim nền và kết cục theo nhịp tim nền. Tỷ số rủi ro của kết cục theo nhịp tim [rung nhĩ (AF) hoặc nhịp xoang (SR)] sử dụng nhóm 1 trong mỗi nhóm làm tham chiếu.
Tỷ số rủi ro với khoảng tin cậy 95% được tính toán bằng cách sử dụng mô hình Cox được điều chỉnh cho các biến tương tự như được trình bày trong Bảng 1. Giá trị P cho sự tương tác giữa rung nhĩ và nhịp xoang với tần số tim được coi là một biến liên tục. (Tì số chênh không điều chỉnh T2 là 0,67; KTC 95% 0,47 – 0,97; P = 0,035 và Tỉ số chênh không điều chỉnh T3 0,67; KTC 95% 0,46 – 0,96; P = 0,031). Tuy nhiên, nguy cơ này không có ý nghĩa sau khi điều chỉnh các biến tiên lượng (Hình 2 và bảng phụ lục trực tuyến S3). Nguy cơ của tất cả các kết cục khác không khác biệt đáng kể giữa các nhóm tần số tim (Hình 1 và 2, và bảng phụ lục trực tuyến S3). Kết quả tương tự cũng được ghi nhận trong một phân tích độ nhạy đối với bệnh nhân có rung nhĩ nền bằng cách sử dụng phân vị tần số tim nhóm nhịp xoang (Bảng phụ lục trực tuyến S4).
KẾT CỤC LÂM SÀNG KHI SỬ DỤNG TẦN SỐ TIM NHƯ MỘT BIẾN LIÊN TỤC
Nhịp xoang
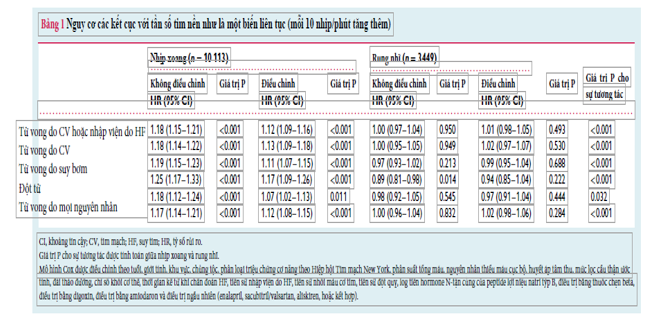
Khi được mô hình hóa như một biến liên tục, tần số tim nền tăng 10 nhịp/phút có liên quan đến nguy cơ cao hơn đáng kể về tất cả các kết cục đối với bệnh nhân nhịp xoang, ngay cả sau khi đã điều chỉnh các biến tiên lượng khác (Bảng 1 và Hình 3). Nguy cơ đột tử này thay đổi từ 7% (tỉ số nguy cơ điều chỉnh 1,07; KTC 95% 1,02 – 1,13; P = 0,011) lên 17% ở nhóm suy bơm (tỉ số nguy cơ điều chỉnh 1,17; KTC 95% 1,09–1,26; P <0,001). Nguy cơ nhập viện do suy tim cao hơn 13% khi tần số tim tang trên mỗi 10 nhịp/phút (tỉ số nguy cơ điều chỉnh 1,13; KTC 95% 1,09–1,18; P <0,001). Nguy cơ tử vong do tim mạch và do mọi nguyên nhân cũng cao hơn đáng kể khi nhịp tim tăng trên 10 nhịp/phút – tương ứng là 11% và 12% sau khi hiệu chỉnh các biến tiên lượng.
Rung nhĩ
Trong rung nhĩ, không có mối liên quan giữa sự gia tăng tần số tim nền trên 10 nhịp/phút và bất kỳ kết cục nào được quan tâm sau khi đã hiệu chỉnh các biến tiên lượng khác (Bảng 1). Có một sự tương tác đáng kể đối với tất cả các kết cục giữa nhịp tim nền (nhịp xoang hoặc rung nhĩ) và tần số tim nền trên phương diện biến liên tục (Bảng 1 và Hình 3).
MỐI QUAN HỆ GIỮA SỰ THAY ĐỔI TẦN SỐ TIM TẠI THỜI ĐIỂM 12 THÁNG SAU PHÂN NHÓM NGẪU NHIÊN VÀ CÁC KẾT CỤC
Dữ liệu về tần số tim và nhịp tim được ghi lại trên ECG vào thời điểm 12 tháng có sẵn ở 10 260 bệnh nhân (75,7%) vẫn giữ nguyên nhịp như trên ECG nền. Trong số này, 7756 (75,6%) nhịp xoang và 2504 (24,4%) rung nhĩ.
Nhịp xoang
Tần số tim trung bình vào thời điểm 12 tháng ở bệnh nhân nhịp xoang cao hơn 0,7 nhịp/phút so với nền (70,0 nhịp/phút so với 69,3 nhịp/phút, P <0,001). Đối với hầu hết bệnh nhân nhịp xoang [n = 4943 (63,7%)], tần số tim chênh lệch ít hơn 10 nhịp/phút so với nền. Tần số tim thấp hơn nền ít nhất 10 nhịp/phút ở 1274 bệnh nhân (16,4%) và cao hơn 10 nhịp/phút trở lên ở 1539 (19,8%).
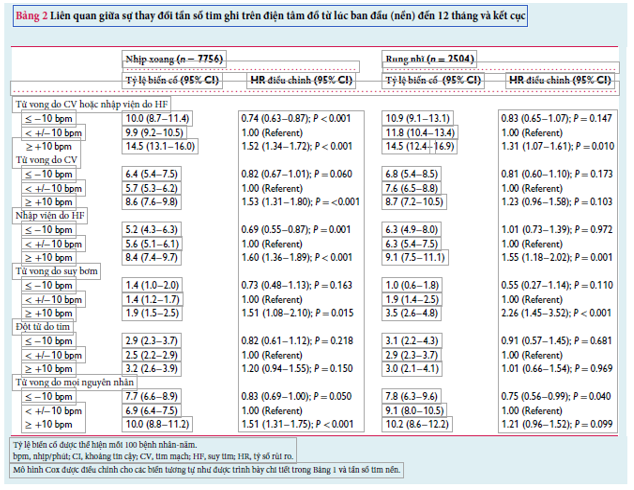
Mối liên quan giữa sự thay đổi tần số tim và các kết cục xảy ra sau 12 tháng theo dõi được báo cáo trong Bảng 2. Đối với nhịp xoang, nguy cơ của tất cả các kết cục được kiểm tra, ngoại trừ đột tử do tim, cao hơn đáng kể ở những người có tần số tim tăng 10 nhịp/phút trở lên, so với những người có tần số tim tăng ít hơn 10 nhịp/phút hoặc giảm. Nguy cơ thấp hơn về kết cục tổng hợp chính (và nhập viện do suy tim) đã được ghi nhận ở những người có tần số tim giảm ít nhất 10 nhịp/phút trong 12 tháng theo dõi. Tất cả các kết cục khác đều cho thấy xu hướng tương tự, tuy nhiên không có ý nghĩa thống kê.
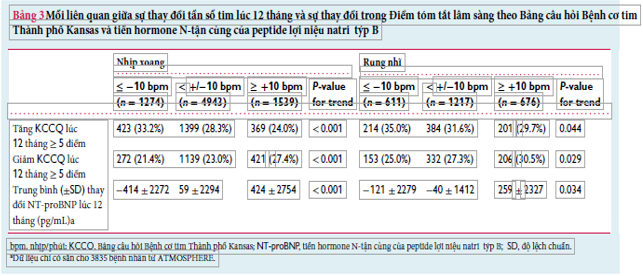
Sự gia tăng tần số tim từ 10 nhịp/phút trở lên tại thời điểm 12 tháng ở bệnh nhân nhịp xoang có liên quan đến sự gia tăng trung bình của NT-proBNP là 424 pg/mL [độ lệch chuẩn (SD) 2754], trong khi giảm tần số tim từ 10 nhịp/phút trở lên có liên quan với mức giảm 414 pg/mL (SD 2272) (P khuynh hướng <0,001) (Bảng 3). Một tỷ lệ lớn hơn những bệnh nhân có tần số tim giảm ít nhất 10 nhịp/phút đã báo cáo sự gia tăng có ý nghĩa lâm sàng trong điểm tổng kết lâm sàng KCCQ sau 12 tháng. Ngược lại, một tỷ lệ lớn hơn bệnh nhân tăng tần số tim từ 10 nhịp/phút trở lên báo cáo giảm điểm tổng kết lâm sàng KCCQ ít nhất 5 điểm (P khuynh hướng <0,001).
Rung nhĩ
Ở bệnh nhân rung nhĩ, tần số tim nền là 79,9 nhịp/phút và 80,5 nhịp/phút tại thời điểm 12 tháng (P = 0,05). Ở những bệnh nhân có rung nhĩ tại thời điểm 12 tháng, 1217 (48,6%) có sự khác biệt dưới 10 nhịp/phút, 611 (24,4%) có tần số tim thấp hơn (thấp hơn ít nhất 10 nhịp/phút) và 676 (27,0%) có tần số tim tăng ít nhất 10 nhịp/phút. Các xu hướng tương tự cũng được bắt gặp với nguy cơ cao hơn ở những người bị tăng tần số tim và nguy cơ thấp hơn liên quan đến việc giảm tần số tim, mặc dù chỉ một số trong số này có ý nghĩa thống kê: tăng tần số tim có liên quan đến nguy cơ cao hơn của kết cục chính tổng hợp, nhập viện do HF và tử vong do suy bơm; giảm tần số tim liên quan đến giảm nguy cơ tử vong do mọi nguyên nhân.
Những thay đổi về nồng độ NT-proBNP và điểm tổng kết lâm sàng KCCQ liên quan đến những thay đổi ở tim lúc 12 tháng ở bệnh nhân rung nhĩ tương tự như những thay đổi được mô tả ở trên ở bệnh nhân nhịp xoang (Bảng 3).
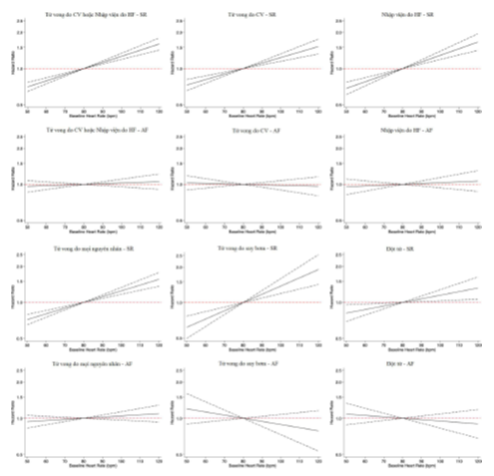
Hình 3. Mối liên hệ giữa tần số tim nền được mô hình hóa như một biến liên tục và kết cục. Tỷ số rủi ro đối với ảnh hưởng của tần số tim nền trên kết cục so với tần số tim nền là 80 nhịp/phút. Đường liền nét thể hiện ước tính điểm với đường đứt nét màu đen thể hiện khoảng tin cậy 95% và đường đứt nét màu đỏ thể hiện tỷ số rủi ro là 1,0. Mô hình Cox điều chỉnh cho các biến tương tự như được trình bày chi tiết trong Bảng 1. AF: rung nhĩ; bpm: nhịp/phút; CV: tim mạch; HF: suy tim; SR: nhịp xoang.
BÀN LUẬN
Phân tích này từ các thử nghiệm PARADIGM-HF và ATMOSPHERE, theo hiểu biết của chúng tôi, là phân tích đầu tiên mô tả mối quan hệ giữa tần số tim nền và kết cục tim mạch ở bệnh nhân suy tim phân suất tống máu giảm mãn tính hay biến đổi ở cả nhịp xoang và rung nhĩ, trong đó nguy cơ đã được điều chỉnh cho các mức peptide bài natri niệu. Những đặc trưng độc đáo khác trong nghiên cứu của chúng tôi là chúng tôi đã đánh giá chất lượng cuộc sống liên quan đến sức khỏe ở tất cả những người tham gia ở thời điểm ban đầu và bộ dữ liệu của chúng tôi đủ lớn để đánh giá cả hai dạng tử vong chính ở bệnh nhân suy tim phân suất tống máu giảm, tức là đột tử và tử vong do suy bơm.
Mặc dù nhiều phát hiện tiên lượng bất lợi lúc ban đầu ở những bệnh nhân nhịp xoang có tần số tim cao hơn phổ biến hơn, tần số tim vẫn là một yếu tố tiên lượng cho các kết cục sau khi điều chỉnh những khác biệt này. Chúng tôi cũng quan sát thấy rằng tần số tim cao hơn có liên quan đến nồng độ peptit bài natri niệu cao hơn ở những bệnh nhân này. Tuy nhiên, tầm quan trọng trong tiên lượng của tần số tim tăng vẫn tồn tại ngay cả sau khi điều chỉnh thêm nồng độ peptide bài natri niệu, xác nhận rằng tần số tim là một chỉ dấu mạnh mẽ, độc lập của các kết cục bất lợi ở bệnh nhân suy tim phân suất tống máu giảm nhịp xoang.
Một phát hiện quan trọng khác là ở những bệnh nhân nhịp xoang, tần số tim cao có liên quan đến nguy cơ tử vong do suy bơm tiến triển tương đối cao hơn so với đột tử, mặc dù nguy cơ tử vong của cả hai dạng này cao hơn ở những bệnh nhân có tần số tim cao hơn [tỉ số nguy cơ điều chỉnh trên mỗi 10 nhịp/phút tần số tim tăng: 1,17 (KTC 95% 1,09 – 1,26) so với 1,07 (KTC 95% 1,02–1,13)]. Mối liên quan tương đối mạnh hơn giữa tần số tim và suy bơm, so với đột tử, cũng được nhận thấy trong phân tích của chúng tôi về sự thay đổi tần số tim. Do đó, điều đáng quan tâm là trong điều trị Suy tim tâm thu với Thử nghiệm ivabradine ức chế IF (SHIFT), tử vong do suy bơm được giảm đáng kể bởi ivabradine (tỉ số nguy cơ 0,74; KTC 95% 0,58 – 0,94, P = 0,014) trong khi đột tử thì không (tỉ số nguy cơ 1,05; KTC 95% 0,87 – 1,26, P = 0,63). Nói chung, những phát hiện này cho thấy rằng những tác động hữu ích có chủ đích của việc giảm tần số tim, bao gồm bảo tồn năng lượng cơ tim, cải thiện lưu lượng máu mạch vành thứ phát do kéo dài tâm trương, cũng như cải thiện mối quan hệ tần số – lực co bóp dương (hiệu ứng Bowditch), có nhiều tác động hơn trên chức năng bơm đang xấu đi. Những phát hiện này cũng chỉ ra tác dụng bổ sung của thuốc chẹn beta ngoài việc giảm tần số tim thì thuốc chẹn beta còn làm giảm đáng kể đột tử. Điều này cho thấy rằng tăng hoạt động hệ adrenergic làm tăng nguy cơ loạn nhịp thất độc lập với tăng tần số tim và giảm đột tử là một lợi ích không liên quan đến tần số tim của thuốc chẹn beta.
Những phát hiện của chúng tôi liên quan đến việc nhập viện do suy tim (nguy cơ thấp hơn ở bệnh nhân có tần số tim thấp hơn) và chất lượng cuộc sống (điểm tổng kết lâm sàng KCCQ tốt hơn ở bệnh nhân có tần số tim thấp hơn) cũng phù hợp với lợi ích của việc giảm tần số tim ở bệnh nhân nhịp xoang có suy tim phân suất tống máu giảm được thể hiện trong nghiên cứu SHIFT. Các kết quả phân tích của chúng tôi về sự thay đổi tần số tim cũng phù hợp với SHIFT và một phân tích hậu kiểm của chương trình CHARM (Candesartan trong suy tim: Đánh giá giảm bệnh tật và tử vong). Cụ thể, trong nghiên cứu SHIFT, giảm tần số tim tổng thể trung bình được điều chỉnh bằng giả dược là 9,1 nhịp/phút với ivabradine sau 1 năm có liên quan với giảm 18% nguy cơ của kết cục tổng hợp chính; trong phân tích của chúng tôi, tần số tim giảm 10 nhịp/phút sau 1 năm có liên quan đến nguy cơ mắc kết cục tương tự thấp hơn 26%. Ở nhóm dùng giả dược trong nghiên cứu SHIFT, tần số tim tăng 5 nhịp/phút có liên quan đến nguy cơ kết cục tổng hợp chính cao hơn 16% và trong nghiên cứu của chúng tôi, tăng 10 nhịp/phút có liên quan đến nguy cơ cao hơn 52%. Hơn nữa, chúng tôi thấy rẳng giảm tần số tim có liên quan đến tỷ lệ bệnh nhân báo cáo cải thiện chất lượng cuộc sống cao hơn, được đo bằng điểm tổng kết lâm sàng KCCQ, tương tự như được thấy trong nghiên cứu SHIFT. Ngoài ra, chúng tôi báo cáo rằng tần số tim giảm cũng đi kèm với giảm mức NT-proBNP.
Trái ngược với những gì chúng tôi quan sát thấy ở những bệnh nhân nhịp xoang, tần số thất không có ý nghĩa tiên lượng ở những người có rung nhĩ trên ECG nền của họ. Có ý kiến cho rằng sự khác biệt này có thể được giải thích bởi bất kỳ lợi ích nào của việc giảm tần số tim trong rung nhĩ được bù đắp bởi sự gia tăng nguy cơ liên quan đến việc sử dụng thuốc giảm tần số tim ở những bệnh nhân này. Hai mối quan tâm chính là các phương pháp điều trị như vậy có thể làm trầm trọng thêm bệnh của hệ dẫn truyền nhĩ thất và làm trầm trọng thêm tình trạng huyết động ở những bệnh nhân dựa vào tần số thất cao hơn để duy trì cung lượng tim khi mất ‘nhát bóp tâm nhĩ’ (atrial kick). Mặt khác, chúng tôi nhận thấy rằng chất lượng cuộc sống (được đo bằng điểm tổng kết lâm sàng KCCQ) tốt hơn ở những bệnh nhân có tần số thất thấp hơn và phát hiện này được hỗ trợ bởi việc kiểm tra phân loại triệu chứng cơ năng theo NYHA. Hơn nữa, chúng tôi nhận thấy rằng sự gia tăng tần số thất theo thời gian ở bệnh nhân rung nhĩ có liên quan đến kết cục xấu hơn như đã được báo cáo trước đây trong phân tích của chương trình CHARM. Tăng tần số thất đi kèm với tăng mức NT-proBNP và giảm chất lượng cuộc sống. Điều này cho thấy mối quan hệ giữa tần số thất và tình trạng sức khỏe ở bệnh nhân suy tim phân suất tống máu giảm có rung nhĩ phức tạp hơn có lẽ được đánh giá cao hơn trước đây. Thậm chí có khả năng đạt được tần số thất tối ưu ở bệnh nhân suy tim phân suất tống máu giảm kèm rung nhĩ có thể liên quan đến sự đánh đổi giữa kiểm soát triệu chứng và nguy cơ tử vong và nhập viện. Tất nhiên, những phát hiện của chúng tôi mang tính chất quan sát và câu hỏi lâm sàng phức tạp và quan trọng này vẫn chưa được giải quyết trong một thử nghiệm lâm sàng ngẫu nhiên đầy đủ về các mục tiêu kiểm soát tần số ở bệnh nhân suy tim phân suất tống máu giảm và rung nhĩ. Trong thực tế, thiếu bằng chứng tổng hợp đã được phản ánh qua sự khác biệt giữa hướng dẫn của Hoa Kỳ ủng hộ tần số thất lúc nghỉ mục tiêu <80 nhịp/phút, hướng dẫn của Châu Âu về rung nhĩ đề xuất mục tiêu <110 nhịp/phút dựa trên thử nghiệm RACEII, mặc dù rất ít bệnh nhân trong thử nghiệm đó có suy tim và chủ yếu suy tim với phân suất tống máu bảo tồn (HFpEF), và các hướng dẫn của Châu Âu về suy tim cho thấy mục tiêu 60–100 nhịp/phút ở bệnh nhân rung và suy tim có thể thích hợp hơn.
NHỮNG ĐIỂM MẠNH VÀ HẠN CHẾ
Điểm mạnh chính của nghiên cứu này là quy mô, tính chất toàn cầu và chuẩn mực cao liệu pháp điều trị đương đại, cho phép tổng quát hóa kết quả cho một tỷ lệ lớn bệnh nhân suy tim phân suất tống máu giảm tương tự như những bệnh nhân được tham gia trong các thử nghiệm này. Tất cả các kết quả nghiên cứu trong cả hai thử nghiệm đều được đánh giá bởi cùng một ủy ban phụ trách kết cục lâm sàng. Việc sử dụng tần số tim đo bằng ECG sẽ loại bỏ các vấn đề về độ tin cậy trong việc ghi thủ công tần số thất trong rung nhĩ. Ngoài ra, số lượng bệnh nhân bị thiếu dữ liệu về NT-proBNP nhỏ, điều này giúp các mô hình điều chỉnh đa biến trong phần lớn đoàn hệ sau khi thay thế cho 593 bệnh nhân bị thiếu dữ liệu từ thử nghiệm ATMOSPHERE (không thay thế được thực hiện cho 12 bệnh nhân bị thiếu dữ liệu NT-proBNP từ PARADIGM-HF). Nghiên cứu của chúng tôi cũng có những hạn chế. Đây là một phân tích hồi cứu và chúng tôi chỉ tính đến tần số tim và sự hiện diện hay không của rung nhĩ khi ghi trên ECG nền. Phân tích của chúng tôi không tính đến sự phát triển, hoặc rung nhĩ kịch phát trong quá trình nghiên cứu. Phân tích tìm hiểu mối liên quan giữa những thay đổi theo thời gian của tần số tim và kết cục đã không tính đến những thay đổi trong việc sử dụng hoặc liều lượng thuốc giảm nhịp có thể ảnh hưởng đến tần số tim. Số lượng bệnh nhân có tần số tim rất cao hoặc rất thấp là rất ít. Chúng tôi đã nỗ lực điều chỉnh sự khác biệt về đặc điểm cơ bản giữa bệnh nhân rung nhĩ và nhịp xoang và giữa các phân vị tần số tim. Mặc dù đã cố gắng hạn chế, tuy nhiên, cũng như trong bất kỳ nghiên cứu phân tích nào, nguy cơ gây nhiễu vẫn cao và phát hiện của chúng tôi nên được giải thích trong bối cảnh này. Kết quả của chúng tôi không mở rộng cho những bệnh nhân không đủ điều kiện để đưa vào các thử nghiệm lâm sàng, ví dụ, những người bị suy tim phân suất tống máu bảo tồn hoặc suy thận nặng.
KẾT LUẬN
Ở những bệnh nhân bị suy tim phân suất tống máu giảm, tần số tim tăng trong nhóm nhịp xoang là một yếu tố tiên lượng độc lập của các kết cục tim mạch bất lợi gồm cả tử vong và không tử vong, ngay cả sau khi điều chỉnh mức peptide bài natri niệu. Tần số tim cao hơn có mối liên hệ chặt chẽ với tử vong do suy bơm hơn là đột tử. Không có mối liên hệ nào giữa tần số tim và kết cục ở bệnh nhân suy tim phân suất tống máu giảm và rung nhĩ.
THÔNG TIN PHỤ LỤC
Thông tin hỗ trợ bổ sung có thể được tìm thấy trực tuyến trong phần Thông tin hỗ trợ ở cuối bài viết.
Bảng S1. Đặc điểm cơ bản theo nhịp tim trên ECG nền và các nhóm tần số tim.
Bảng S2. Đặc điểm cơ bản theo nhịp tim trên điện tâm đồ nền. Bảng S3. Kết cục lâm sàng theo nhịp tim và các nhóm tần số tim nền.
Bảng S4. Phân tích độ nhạy – AF được phân tích trong các nhóm tần số tim nhịp xoang.
Hình S1. Lưu đồ bệnh nhân.
Hình S2. Phân bổ tần số tim nền được ghi trên ECG trong nhịp xoang và rung nhĩ.
Tài trợ
Các thử nghiệm ATMOSPHERE và PARADIGM-HF do Novartis tài trợ.
Xung đột lợi ích
Tiến sĩ Petrie, Abraham, Desai, Dickstein, Køber, Packer, Rouleau, Solomon, Swedberg, Zile, Jhund và McMurray hoặc các tổ chức của họ đã được Novartis trả tiền cho việc tham gia một hoặc cả hai thử nghiệm này. Tiến sĩ Petrie đã nhận được phí thuyết trình từ AstraZeneca, Novartis và Eli Lilly, hỗ trợ, phí hội đồng cố vấn và phí phục vụ trong một ủy ban kết cục từ Boehringer Ingelheim, phí hội đồng cố vấn, phí diễn thuyết và phí phục vụ ủy ban kết cục từ Novo Nordisk, phí ban cố vấn từ Napp Pharmaceuticals và phí phục vụ ủy ban kết cục từ Takeda Pharmaceutical và Bayer; Tiến sĩ Böhm đã nhận được phí giảng dạy từ Amgen, Bayer, Servier, Medtronic, Boehringer Ingelheim, Vifor Pharma, và Bristol-Myers Squibb, cấp hỗ trợ và phí giảng dạy từ AstraZeneca, và hỗ trợ từ Deutsche Forschungsgemeinschaft; Tiến sĩ Desai đã nhận được phí tư vấn từ Abbott, Biofourmis, Boston Scientific, Boehringer Ingelheim, DalCor Pharmaceuticals và Regeneron, hỗ trợ (trả cho Bệnh viện Brigham và Phụ nữ) và phí tư vấn từ Alnylam Pharmaceuticals và Novartis, và phí hội đồng tư vấn từ Corvidia và Relypsa; Tiến sĩ Køber đã nhận được phí giảng dạy từ Novartis và Bristol-Myers Squibb; Tiến sĩ Packer đã nhận được các khoản phí cá nhân từ Abbott, Amgen, Actavis, Bayer, Boehringer Ingelheim, Cardiorentis, Daiichi-Sankyo, Gilead, NovoNordisk, Relypsa, AstraZeneca, Sanofi, Synthetic Biologies và Theravance; Tiến sĩ Rouleau đã nhận được phí cá nhân từ Novartis và AstraZeneca; Tiến sĩ Solomon đã nhận được hỗ trợ tài trợ và phí tư vấn (tất cả các khoản phí được liệt kê trả cho Bệnh viện Phụ nữ và Brigham) từ Alnylam Pharmaceuticals, Amgen, AstraZeneca, Bristol-Myers Squibb, Gilead Sciences, GlaxoSmithKline, MyoKardia, Novartis, Theracos, Bayer, và Cytokinetics, hỗ trợ từ Bellerophon Therapeutics, Celladon, Ionis Pharmaceuticals, Lonestar Heart, Mesoblast, Sanofi Pasteur và Eidos Therapeu-tics, phí tư vấn từ Akros Pharma, Corvia Medical, Iron-wood Pharma, Merck, Roche, Takeda Pharmaceutical, Quantum Genomics, AOBiome, Cardiac Dimensions, Tenaya Therapeutics, và Daiichi Sankyo, và phí phục vụ trên bảng giám sát dữ liệu và an toàn từ Janssen; Tiến sĩ Thụy Điển đã từng là cố vấn và nhận được danh hiệu từ Astrazeneca, Novartis, Pfizer và Vifor Pharma; Tiến sĩ Zile đã nhận được các khoản phí cá nhân từ Novartis; Tiến sĩ Jhund đã nhận được phí tư vấn, phí ban cố vấn và phí thuyết trình từ Novartis, phí ban cố vấn từ Cytokinetics và hỗ trợ từ Boehringer Ingelheim. Tất cả các tác giả khác đã báo cáo rằng họ không có mối quan hệ nào liên quan đến nội dung của bài báo này để tiết lộ.
Tài liệu tham khảo
- Fox K, Ford I, Steg PG, Tendera M, Robertson M, Ferrari R; BEAUTIFUL Investigators. Heart rate as a prognostic risk factor in patients with coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL): a subgroup analysis of a randomised controlled trial. Lancet 2008;372:817–821.
- Böhm M, Swedberg K, Komajda M, Borer JS, Ford I, Dubost-Brama A, Lerebours G, Tavazzi L. Heart rate as a risk factor in chronic heart failure (SHIFT): the association between heart rate and outcomes in a randomised placebo-controlled trial. Lancet 2010;376:886–894.
- Castagno D, Skali H, Takeuchi M, Swedberg K, Yusuf S, Granger CB, Michelson EL, Pfeffer MA, McMurray JJ, Solomon SD; CHARM Investigators. Association of heart rate and outcomes in a broad spectrum of patients with chronic heart failure: results from the CHARM (Candesartan in Heart Failure: Assessment of Reduction in Mortality and morbidity) program. J Am Coll Cardiol 2012;59:1785–1795.
- Simpson J, Castagno D, Doughty RN, Poppe KK, Earle N, Squire I, Richards M, Andersson B, Ezekowitz JA, Komajda M, Petrie MC, McAlister FA, Gamble GD Whalley GA, McMurray JJ; Meta-Analysis Global Group in Chronic Heart Failure (MAGGIC). Is heart rate a risk marker in patients with chronic heart failure and concomitant atrial fibrillation? Results from the MAGGIC meta-analysis. Eur J Heart Fail 2015;17:1182–1191.
- Kotecha D, Flather MD, Altman DG, Holmes J, Rosano G, Wikstrand J, Packer M,Coats AJ, Manzano L, Böhm M, van Veldhuisen DJ, Andersson B, Wedel H, von Lueder TG, Rigby AS, Hjalmarson Å, Kjekshus J, Cleland JG; Beta-Blockers in Heart Failure Collaborative Group. Heart rate and rhythm and the benefit of beta-blockers in patients with heart failure. J Am Coll Cardiol 2017;69:2885–2896.
- Swedberg K, Komajda M, Böhm M, Borer JS, Ford I, Dubost-Brama A, Lerebours G, Tavazzi L; SHIFT Investigators. Ivabradine and outcomes in chronic heart failure (SHIFT): a randomised placebo-controlled study. Lancet 2010;376:875–885.
- Zile MR, Claggett BL, Prescott MF, McMurray JJ, Packer M, Rouleau JL, Swedberg K, Desai AS, Gong J, Shi VC, Solomon SD. Prognostic implications of changes in N-terminal pro-B-type natriuretic peptide in patients with heart failure. J Am Coll Cardiol 2016;68:2425–2436.
- Maisel WH, Stevenson LW. Atrial fibrillation in heart failure: epidemiology, pathophysiology, and rationale for therapy. Am J Cardiol 2003;91:2–8.
- Rienstra M, van Gelder IC, van den Berg MP, Boomsma F, Hillege HL, van Veldhuisen DJ. A comparison of low versus high heart rate in patients with atrial fibrillation and advanced chronic heart failure: effects on clinical profile, neurohormones and survival. Int J Cardiol 2006;109:95–100.
- Laskey WK, Alomari I, Cox M, Schulte PJ, Zhao X, Hernandez AF, Heidenreich PA, Eapen ZJ, Yancy C, Bhatt DL, Fonarow GC. Heart rate at hospital discharge in patients with heart failure is associated with mortality and rehospitalization. J Am Heart Assoc 2015;4:e001626.
- Cullington D, Goode KM, Zhang J, Cleland JG, Clark AL. Is heart rate important for patients with heart failure in atrial fibrillation? JACC Heart Fail 2014;2:213–220.
- Mulder BA, van Veldhuisen DJ, Crijns HJ, Tijssen JG, Hillege HL, Alings M, Rienstra M, Groenveld HF, van den Berg MP, van Gelder IC; RACE II Investigators.Lenient vs. strict rate control in patients with atrial fibrillation and heart failure: a post-hoc analysis of the RACE II study. Eur J Heart Fail 2013;15:1311–1318.
- Li SJ, Sartipy U, Lund LH, Dahlstrom U, Adiels M, Petzold M, Fu M. Prognostic significance of resting heart rate and use of ?-blockers in atrial fibrillation and sinus rhythm in patients with heart failure and reduced ejection fraction: findings from the Swedish Heart Failure Registry. Circ Heart Fail 2015;8:871–879.
- Mogensen UM, Jhund PS, Abraham WT, Desai AS, Dickstein K, Packer M, Rouleau JL, Solomon SD, Swedberg K, Zile MR, Køber L, McMurray JJ; PARADIGM-HF and ATMOSPHERE Investigators and Committees. Type of atrial
fibrillation and outcomes in patients with heart failure and reduced ejection fraction. J Am Coll Cardiol 2017;70:2490–2500.
- Kristensen SL, Jhund PS, Mogensen UM, Rørth R, Abraham WT, Desai A, Dickstein K, Rouleau JL, Zile MR, Swedberg K, Packer M, Solomon SD, Køber L, McMurray JJ. Prognostic value of N-terminal pro-B-type natriuretic peptide levels in heart failure patients with and without atrial fibrillation. Circ Heart Fail 2017;10:1–10.
- McMurray JJ, Packer M, Desai AS, Gong J, Lefkowitz MP, Rizkala AR, Rouleau J, Shi VC, Solomon SD, Swedberg K, Zile MR; PARADIGM-HF Committees and Investigators. Dual angiotensin receptor and neprilysin inhibition as an alternative to angiotensin-converting enzyme inhibition in patients with chronic systolic heart failure: rationale for and design of the Prospective Comparison of ARNI with ACEI to Determine Impact on Global Mortality and morbidity in Heart Failure trial (PARADIGM-HF). Eur J Heart Fail 2013;15:1062–1073.
- McMurray JJ, Packer M, Desai AS, Gong J, Lefkowitz M, Rizkala AR, Rouleau JL, Shi VC, Solomon SD, Swedberg K, Zile MR; PARADIGM-HF Committees and Investigators. Baseline characteristics and treatment of patients in Prospective Comparison of ARNI with ACEI to Determine Impact on Global Mortality and morbidity in Heart Failure trial (PARADIGM-HF). Eur J Heart Fail 2014;16:817–825.
- McMurray JJ, Packer M, Desai AS, Gong J, Lefkowitz MP, Rizkala AR, Rouleau JL, Shi VC, Solomon SD, Swedberg K, Zile MR; PARADIGM-HF Investigators and Committees. Angiotensin-neprilysin inhibition versus enalapril in heart failure. N Engl J Med 2014;371:993–1004.
- Krum H, Massie B, Abraham WT, Dickstein K, Kober L, McMurray JJ, Desai A, Gimpelewicz C, Kandra A, Reimund B, Rattunde H, Armbrecht J; ATMOSPHERE Investigators. Direct renin inhibition in addition to or as an alternative to angiotensin converting enzyme inhibition in patients with chronic systolic heart failure: rationale and design of the Aliskiren Trial to Minimize OutcomeS in Patients with HEart failuRE (ATMOSPHERE) study. Eur J Heart Fail 2011;13:107–114.
- Krum H, McMurray JJ, Abraham WT, Dickstein K, Køber L, Desai AS, Solomon SD, Chiang Y, Gimpelewicz C, Reimund B, Ali MA, Tarnesby G, Massie BM; ATMOSPHERE Committees and Investigators. The Aliskiren Trial to Minimize OutcomeS in Patients with HEart failuRE trial (ATMOSPHERE): revised statistical analysis plan and baseline characteristics. Eur J Heart Fail 2015;17: 1075–1083.
- 21. McMurray JJ, Krum H, Abraham WT, Dickstein K, Køber LV, Desai AS, Solomon SD, Greenlaw N, Ali MA, Chiang Y, Shao Q, Tarnesby G, Massie BM; ATMOSPHERE Committees Investigators. Aliskiren, enalapril, or aliskiren and enalapril in heart failure. N Engl J Med 2016;374:1521–1
- Cuzick J. A Wilcoxon-type test for trend. Stat Med 1985;4:87–90.
- Van Gelder IC, Groenveld HF, Crijns HJ, Tuininga YS, Tijssen JG, Alings AM, Hillege HL, Bergsma-Kadijk JA, Cornel JH, Kamp O, Tukkie R, Bosker HA, Van Veldhuisen DJ, Van den Berg MP; RACE II Investigators. Lenient versus strict rate control in patients with atrial fibrillation. N Engl J Med 2010;362:1363–1373.
- Mulder P, Barbier S, Chagraoui A, Richard V, Henry JP, Lallemand F, Renet S, Lerebours G, Mahlberg-Gaudin F, Thuillez C. Long-term heart rate reduction induced by the selective If current inhibitor ivabradine improves left ventricular function and intrinsic myocardial structure in congestive heart failure. Circulation 2004;109:1674–1679.
- Mulieri LA, Hasenfuss G, Leavitt B, Allen PD, Alpert NR. Altered myocardial force-frequency relation in human heart failure. Circulation 1992;85:1743–1750.
- Ekman I, Chassany O, Komajda M, Böhm M, Borer JS, Ford I, Tavazzi L, Swedberg K. Heart rate reduction with ivabradine and health related quality of life in patients with chronic heart failure: results from the SHIFT study. Eur Heart J 2011;32:2395–2404.
- Vazir A, Claggett B, Jhund P, Castagno D, Skali H, Yusuf S, Swedberg K, Granger CB, McMurray JJ, Pfeffer MA, Solomon SD. Prognostic importance of temporal changes in resting heart rate in heart failure patients: an analysis of the CHARM program. Eur Heart J 2015;36:669–675.
- Daoud EG, Weiss R, Bahu M, Knight BP, Bogun F, Goyal R, Harvey M, Strickberger SA, Man KC, Morady F. Effect of an irregular ventricular rhythm on cardiac output. Am J Cardiol 1996;78:1433–1436.
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, Castella M, Diener HC, Heidbuchel H, Hendriks J, Hindricks G, Manolis AS, Oldgren J, Popescu BA, Schotten U, Van Putte B, Vardas P. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J 2016;37:2893–2962.
- January CT, Wann LS, Alpert JS, Calkins H, Cigarroa JE, Cleveland JC, Conti JB, Ellinor PT, Ezekowitz MD, Field ME, Murray KT, Sacco RL, Stevenson WG, Tchou PJ, Tracy CM, Yancy CW, Anderson JL, Halperin JL, Albert NM, Bozkurt B, Brindis RG, Creager MA, Curtis LH, DeMets D, Guyton RA, Hochman JS, Kovacs RJ, Ohman EM, Pressler SJ, Sellke FW, Shen WK, Yancy CW; ACC/AHA Task Force Members. 2014 AHA/ACC/HRS guideline for the management of patients with atrial fibrillation: executive summary: a report of the American College of Cardiology/American Heart Association Task Force
on Practice Guidelines and the Heart Rhythm Society. Circulation 2014;130: 2071–2104. - 31. Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JG, Coats AJ, Falk V, González-Juanatey JR, Harjola VP, Jankowska EA, Jessup M, Linde C, Nihoyannopoulos P, Parissis JT, Pieske B, Riley JP, Rosano GM, Ruilope LM, Ruschitzka F, Rutten FH, van der Meer P. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed with the special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail 2016;18:891–975.
- Rush CJ, Campbell RT, Jhund PS, Petrie MC, McMurray JJ. Association is not causation: treatment effects cannot be estimated from observational data in heart failure. Eur Heart J 2018;39:3417–3438.
- Aguirre Dávila L, Weber K, Bavendiek U, Bauersachs J, Wittes J, Yusuf S, Koch A. Digoxin-mortality: randomized vs. observational comparison in the DIG trial. Eur Heart J 2019;40:3336–3341.







