Trưởng ban: PGS.TS. PHẠM NGUYỄN VINH
Tham gia biên soạn:
GS.TS. NGUYỄN LÂN VIỆT, PGS.TS. HỒ HUỲNH QUANG TRÍ,
TS.BS. TRẦN VŨ MINH THƯ, BS. CKII. LÊ THỊ ĐẸP,
BS. CKII. TRẦN THỊ TUYẾT LAN, ThS.BS. HUỲNH THANH KIỀU,
ThS.BS. PHẠM ĐỖ ANH THƯ, BS. CKI. PHẠM THỤC MINH THỦY
Biên tập: LƯƠNG BÍCH NHUNG, TRẦN THỊ THANH NGA
(…)
17.2. Liệu pháp bắc cầu
| Loại | MCC | Khuyến cáo về liệu pháp bắc cầu
trong thời gian tạm ngừng chống đông cho van nhân tạo |
| I | C | 1. Đối với bệnh nhân có van cơ học cần thực hiện thủ thuật nhỏ (ví dụ nhổ răng, lấy bỏ đục thủy tinh thể) mà chảy máu dễ kiểm soát, cần tiếp tục chống đông kháng vitamin K với mục tiêu INR được khuyến cáo. |
| I | C | 2. Đối với bệnh nhân thay van động mạch chủ cơ học 2 đĩa và không có yếu tố nguy cơ huyết khối tắc mạch cần thực hiện thủ thuật xâm nhập, khuyến cáo tạm ngừng kháng vitamin K, không cần bắc cầu khi INR dưới ngưỡng điều trị. |
| IIa | C | 3. Đối với bệnh nhân có van cơ học đang dùng kháng vitamin K cần ngưng lập tức để phẫu thuật cấp cứu hoặc thực hiện thủ thuật xâm nhập, dùng phức hợp yếu tố-4 prothrombin đậm đặc (hoặc dạng hoạt hóa của nó) là hợp lý. |
| IIa | C | 4. Đối với bệnh nhân có van nhân tạo hoặc tạo hình vòng van cần dùng chống đông vì rung nhĩ, cần cân nhắc dùng liệu pháp bắc cầu xung quanh thời gian thực hiện thủ thuật xâm nhập trên cơ sở điểm CHA2DS2-VASc phòng nguy cơ chảy máu. |
| IIa | C | 5. Đối với bệnh nhân cần thực hiện thủ thuật xâm nhập và có 1) Thay van động mạch chủ cơ học và bất kỳ yếu tố nguy cơ huyết khối tắc mạch nào, 2) Thay van động mạch chủ cơ học thế hệ cũ, hoặc 3) Thay van hai lá cơ học, hợp lý khi dùng liệu pháp bắc cầu chống đông trong khoảng thời gian trước phẫu thuật khi INR dưới ngưỡng điều trị dựa trên từng cá thể với sự cân nhắc giữa nguy cơ chảy máu và lợi ích của việc phòng ngừa huyết khối tắc mạch. |
Trong trường hợp cần thiết phải ngừng điều trị kháng vitamin K đường uống, thuốc chống đông thường được ngừng sử dụng từ 3 – 4 ngày trước khi tiến hành thủ thuật và được bắt đầu lại sau phẫu thuật ngay khi nguy cơ chảy máu cho phép. Chống đông bắc cầu với heparin không phân đoạn đường tĩnh mạch hoặc heparin trọng lượng phân tử thấp tiêm dưới da được bắt đầu khi INR giảm xuống dưới ngưỡng điều trị (tức là 2,0 hoặc 2,5 tùy vào bệnh cảnh lâm sàng), thường là từ 36 – 48 giờ trước khi phẫu thuật, và ngưng từ 4 – 6 giờ (đối với heparin không phân đoạn) hoặc 12 giờ (đối với heparin trọng lượng phân tử thấp) trước khi làm thủ thuật(137–143).
Ở bệnh nhân thay van động mạch chủ cơ học 2 đĩa và không có yếu tố nguy cơ nào khác, nguy cơ huyết khối tắc mạch sau ngừng chống đông kháng vitamin K là thấp nếu chỉ ngưng chống đông một vài ngày. Ở những bệnh nhân nguy cơ thấp này, có thể tránh được sự bất tiện và tốn kém của liệu pháp bắc cầu chống đông. Khi cần tạm ngừng kháng vitamin K, thuốc được ngưng 2 – 4 ngày trước khi làm thủ thuật và bắt đầu lại ngay khi nguy cơ chảy máu cho phép, thường là 24 giờ sau phẫu thuật (138,139).
Ở bệnh nhân có van cơ học dùng dài hạn kháng vitamin K cần phẫu thuật cấp cứu hoặc thủ thuật xâm nhập, có thể đảo ngược tác dụng của chống đông bằng cách truyền phức hợp yếu tố-4 prothrombin đậm đặc. Nó thay thế các yếu tố đông máu bị giảm bởi vitamin K và chứa toàn bộ các yếu tố đông máu, gồm II, VII, IX và X ở dạng bất hoạt. Hiệu lực bắt đầu trong vòng 5 – 15 phút, và thời gian tác dụng kéo dài từ 12 – 24 giờ. Với huyết tương tươi đông lạnh, thời gian bắt đầu tác dụng dài hơn (1 – 4 giờ) và thời gian tác dụng ngắn hơn (dưới 6 giờ), tùy thuộc vào liều dùng(140).
17.3. Quá liều thuốc chống đông và chảy máu nghiêm trọng ở bệnh nhân có van nhân tạo
| Loại | MCC | Khuyến cáo về xử lý quá liều thuốc chống đông và chảy máu nghiêm trọng ở bệnh nhân có van nhân tạo |
| IIa | C | 1. Đối với bệnh nhân có van cơ học và chảy máu không kiểm soát được, cần đảo ngược tác dụng của kháng đông tức thì, dùng phức hợp yếu tố-4 prothrombin (hoặc dạng hoạt hóa của nó) là hợp lý. |
| IIa | C | 2. Đối với bệnh nhân có van cơ học và chảy máu không kiểm soát được đã dùng phức hợp yếu tố-4 prothrombin đậm đặc, dùng thêm vitamin K đường tĩnh mạch là hợp lý nếu việc phục hồi liệu pháp kháng vitamin K dự định không bắt đầu trong 7 ngày tới. |
| IIa | B | 3. Đối với bệnh nhân có van cơ học hoặc tạo hình vòng van đã dùng chống đông đường uống trực tiếp và cần đảo ngược tác dụng của kháng đông tức thì vì chảy máu không kiểm soát được, điều trị bằng idarucizumab (đối với dabigatran) hoặc andexanet alfa (đối với thuốc ức chế Xa) là hợp lý (1 – 5). |
| IIb | C | 4. Đối với bệnh nhân có van cơ học và INR trên ngưỡng điều trị (trên 5,0) không đang chảy máu, lợi ích của việc điều trị theo từng cá thể bằng vitamin K đường uống ngoài việc tạm ngừng kháng vitamin K là không chắc chắn. |
Phức hợp yếu tố-4 prothrombin đậm đặc gồm yếu tố II, VII, IX và X. Thời gian bắt đầu có tác dụng trong vòng 5 – 15 phút, và thời gian tác dụng là 12 – 24 giờ. Đây là tác nhân đảo ngược tác dụng chống đông chuyên biệt và đáng tin cậy hơn huyết tương tươi đông lạnh.
Vitamin K là đồng yếu tố để gan sản xuất các yếu tố II, VII, IX và X. Thời gian phát huy tác dụng phụ thuộc vào đường dùng (đường tĩnh mạch hay uống), và liều dùng dự đoán dựa trên sự hiện diện của chảy máu, liều duy trì của kháng vitamin K, mức độ tăng của INR và khoảng điều trị mong muốn để giảm INR(144–147). Liều 10 mg đường tĩnh mạch được khuyến cáo đối với chảy máu đe dọa tính mạng khi không có dự định sẽ dùng lại kháng vitamin K vào tuần tới.
Idarucizumab (bolus tĩnh mạch 2,5 mg hai lần không cách nhau quá 15 phút) được dùng để đảo ngược tác dụng của dabigatran khi lâm sàng có chỉ định(148–151). Andexanet alfa (bolus và truyền tĩnh mạch trong 2 giờ, với liều lượng phụ thuộc thời điểm tiếp xúc và từng tác nhân) được sử dụng để đảo ngược tác dụng của kháng Xa đường uống(149–151). Phức hợp prothrombin đậm đặc (hay dạng hoạt hóa của nó) cũng được sử dụng cho chảy máu do chống đông đường uống.
17.4. Các biến cố huyết khối tắc mạch của van nhân tạo
| Loại | MCC | Khuyến cáo về xử lý các biến cố huyết khối tắc mạch của van nhân tạo |
| IIa | C | 1. Ở bệnh nhân thay van động mạch chủ cơ học đã từng bị đột quị hoặc biến cố huyết khối tắc mạch hệ thống khi vẫn trong ngưỡng điều trị của kháng vitamin K, hợp lý khi tăng mục tiêu INR từ 2,5 (khoảng điều trị 2,0 – 3,0) lên 3,0 (khoảng điều trị 2,5 – 3,5) hoặc thêm aspirin liều thấp mỗi ngày (75 – 100 mg) cùng với việc đánh giá nguy cơ chảy máu. |
| IIa | C | 2. Ở bệnh nhân thay van hai lá cơ học đã từng bị đột quị hoặc biến cố huyết khối tắc mạch hệ thống khi vẫn trong ngưỡng điều trị của kháng vitamin K, hợp lý khi tăng mục tiêu INR từ 3,0 (khoảng điều trị 2,5 – 3,5) lên 4,0 (khoảng điều trị 3,5 – 4,0) hoặc thêm aspirin liều thấp mỗi ngày (75 – 100 mg) cùng với việc đánh giá nguy cơ chảy máu. |
| IIb | C | 3. Ở bệnh nhân phẫu thuật thay van sinh học hoặc thay van động mạch chủ qua da hoặc thay van hai lá sinh học đã từng bị đột quị hoặc biến cố huyết khối tắc mạch hệ thống khi đang điều trị kháng tiểu cầu, dùng chống đông kháng vitamin K thay vì kháng tiểu cầu có thể cân nhắc sau khi đánh giá nguy cơ chảy máu(152,153). |
Đối với bệnh nhân có van cơ học bị biến cố tắc mạch, điều quan trọng là phải đánh giá mức độ đầy đủ của chống đông kháng vitamin K, ghi nhận Thời gian trong khoảng điều trị (TTR), loại trừ viêm nội tâm mạc nhiễm trùng, tìm rung nhĩ mới khởi phát, và xem xét tình trạng tăng đông tiềm ẩn góp phần. Tương tự, huyết khối tắc mạch ở bệnh nhân có van sinh học cũng gợi lên nghi ngờ về viêm nội tâm mạc nhiễm trùng và rung nhĩ mới khởi phát trong bệnh cảnh lâm sàng phù hợp. Huyết khối lá van thường xuất hiện hơn với thay van động mạch chủ sinh học qua da hơn thay van động mạch chủ bằng phẫu thuật(128,152–154). Tăng cường điều trị chống huyết khối luôn phải tính đến nguy cơ chảy máu của từng bệnh nhân (Hình 17).
17.5. Huyết khối van cơ học cấp
17.5.1. Chẩn đoán huyết khối van cơ học cấp
| Loại | MCC | Khuyến cáo về chẩn đoán huyết khối cấp van cơ học |
| I | B | 1. Ở bệnh nhân nghi ngờ huyết khối van nhân tạo, cần đánh giá khẩn cấp bằng SATQTN, SATQTQ, soi van, và/hoặc chụp cắt lớp vi tính đa dãy để đánh giá chức năng van, vận động lá van, và sự hiện diện và mức độ của huyết khối(155–161). |
Huyết khối van cơ học được chẩn đoán bằng vận tốc hoặc chênh áp ngang van nhân tạo tăng bất thường, với lá van vận động hạn chế hoặc dính vào khối di động phù hợp với huyết khối hoặc cả hai. Tắc nghẽn van nhân tạo thường xác định bằng chênh áp trung bình ngang van tăng trên 50% (hoặc tăng trên 10 mmHg ngang qua van nhân tạo động mạch chủ) so với mức nền, sau khi loại trừ các nguyên nhân khác, như tình trạng cung lượng tim cao. Khi nghi ngờ huyết khối van cơ học, hình ảnh và Doppler SATQTN cung cấp thông tin về chức năng van, ước lượng áp lực động mạch phổi, kích thước và chức năng tâm thu thất trái (162). Vận động lá van nên được xem với hình ảnh chụp CT hay SATQTQ (đặc biệt đối với van nhân tạo hai lá) hoặc soi van (đối với van nhân tạo động mạch chủ). Có thể cần thời gian quan sát lâu hơn khi soi van hoặc SATQTQ để chẩn đoán tắc nghẽn từng lúc. Đánh giá sự hiện diện, số lượng huyết khối và mô xơ bằng SATQTQ và chụp CT (160,161,163–165).
17.5.2. Can thiệp
| Loại | MCC | Khuyến cáo về điều trị huyết khối cấp van cơ học |
| I | B | 1. Ở bệnh nhân bị huyết khối van cơ học tim trái có triệu chứng tắc nghẽn van, khuyến cáo điều trị khởi đầu khẩn cấp bằng liệu pháp tiêu sợi huyết liều thấp, truyền chậm hoặc phẫu thuật cấp cứu (164,166–175). |
| IIa | B | 2. Tiêu sợi huyết (dùng rtPA 10 mg bolus + truyền 90 mg Heparin không phân đoạn trong 90 phút hay Streptokinase 1.500.000 UI trong 60 phút mà không có Heparin không phân đoạn) nên được cân nhắc khi phẫu thuật không có sẵn hoặc có nguy cơ rất cao, hoặc huyết khối van cơ học tim phải(168). |
Việc xử trí huyết khối van cơ học là có nguy cơ cao cho dù lựa chọn nào được thực hiện. Sử dụng tiêu sợi huyết có nguy cơ chảy máu, huyết khối tắc mạch, và huyết khối tái phát. Phẫu thuật thay van cấp cứu được khuyến cáo đối với huyết khối tắc nghẽn van nhân tạo ở bệnh nhân nguy kịch mà không có chống chỉ định phẫu thuật (18,168). Quyết định phẫu thuật hay dùng tiêu sợi huyết toàn thân đối với huyết khối van cơ học tim trái có triệu chứng nên được chọn theo từng cá nhân (Bảng 34) sau khi xem xét bởi nhóm van tim, tham khảo ý kiến của bệnh nhân và kinh nghiệm các chuyên gia. Tỉ lệ tử vong chung trong 30 ngày sau phẫu thuật là 10 – 15%, với tỉ lệ tử vong thấp hơn dưới 5% ở bệnh nhân NYHA I hoặc II (168,169,171) (108,109,112). Các nghiên cứu gần đây sử dụng phác đồ tiêu sợi huyết liều thấp, truyền chậm, có hướng dẫn bằng siêu âm tim đã cho thấy tỉ lệ thành công về huyết động trên 90%, với tỉ lệ biến cố tắc mạch dưới 2% và tỉ lệ chảy máu quan trọng dưới 2%(176). Do đó tiêu sợi huyết toàn thân là một giải pháp có thể chấp nhận được thay thế cho tái phẫu thuật ở bệnh nhân nguy cơ phẫu thuật cao hoặc rất cao và bệnh nhân có huyết khối nhỏ, triệu chứng suy tim nhẹ (NYHA I hoặc II), và nguy cơ chảy máu thấp. Sự vắng mặt chuyên gia phẫu thuật nên được cân nhắc trong việc ra quyết định chung, là một yếu tố ưu tiên cho tiêu sợi huyết, trái lại huyết khối van tái phát ưu tiên cho phẫu thuật (Bảng 34).
Bảng 34. Tiêu sợi huyết toàn thân hay phẫu thuật với huyết khối van nhân tạo (1)
| Ưu tiên phẫu thuật | Ưu tiên tiêu sợi huyết |
| Có sẵn chuyên gia phẫu thuật | Không có sẵn chuyên gia phẫu thuật |
| Nguy cơ phẫu thuật thấp | Nguy cơ phẫu thuật cao |
| Chống chỉ định tiêu sợi huyết | Không có chống chỉ định tiêu sợi huyết |
| Huyết khối van tái phát | Huyết khối van lần đầu |
| Suy tim NYHA IV | Suy tim NYHA I, II hoặc III |
| Huyết khối lớn (>0,8 cm2 hoặc >10 mm(18)) | Huyết khối nhỏ (≤ 0,8 cm2 hoặc ≤ 10 mm(18)) |
| Huyết khối nhĩ trái | Không có huyết khối nhĩ trái |
| Có bệnh mạch vành đồng mắc cần tái tưới máu | Không hoặc có bệnh mạch vành nhẹ |
| Có bệnh van khác | Không có bệnh van khác |
| Có thể là mô xơ | Hình ảnh huyết khối |
| Lựa chọn của bệnh nhân | Lựa chọn của bệnh nhân |
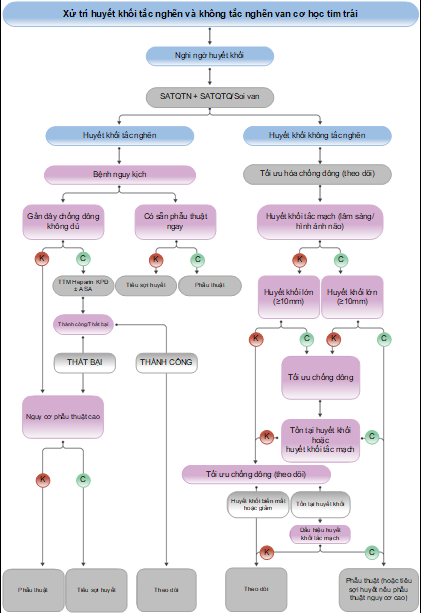
Hình 16. Xử trí huyết khối tắc nghẽn và không tắc nghẽn van cơ học tim trái (18)
ĐMC (động mạch chủ); Tăng mục tiêu INR (International Normalized Ratio – Tỉ lệ chuẩn hóa quốc tế) MDCT ( Multidetector computed tomography – chụp cắt lớp vi tính đa dãy); TSH (tiêu sợi huyết); SATQTQ (siêu âm tim qua thực quản); SATQTN (siêu âm tim qua thành ngực)
17.6. Huyết khối van sinh học
17.6.1. Chẩn đoán huyết khối van sinh học
| Loại | MCC | Khuyến cáo về chẩn đoán huyết khối van sinh học |
| IIa | C | 1. Ở bệnh nhân nghi ngờ huyết khối van sinh học, hình ảnh SATQTQ 3 chiều hoặc CT 4 chiều có thể hữu ích để loại trừ huyết khối lá van(128,129,152,153,177,178). |
Huyết khối van sinh học thường gặp nhất trong 3 tháng đầu sau thay van nhưng cũng được mô tả ở các bệnh nhân nhiều năm sau thay van (điển hình là 1 hoặc 2 năm), dài nhất là 6,5 năm(164). Van sinh học ít bị huyết khối hơn van cơ học. Huyết khối van sinh học phổ biến với thay van bằng thông tim hơn phẫu thuật thay van sinh học. Tuy nhiên chẩn đoán huyết khối van sinh học trên cận lâm sàng đã tăng lên khi sử dụng hình ảnh chụp CT và khi số lượng van sinh học được sử dụng đã tăng lên, kể cả thay van động mạch chủ qua da (128,152,153,177). Huyết khối van sinh học trên hình ảnh chụp CT có thể biểu hiện dưới dạng lá van dày giảm tỉ trọng với vận động lá van bình thường hoặc giảm vận động lá van nhưng chênh áp ngang van bình thường và huyết khối van trên lâm sàng với chênh áp ngang van tăng. Phân biệt giữa huyết khối và mô xơ bằng chụp CT là hướng dẫn quan trọng để quyết định điều trị (18). Khi có bằng chứng lâm sàng hẹp van, hình ảnh SATQTQ 3 chiều và CT 4 chiều có thể hữu ích để phát hiện lớp huyết khối van, có thể đáp ứng với điều trị chống đông đường uống.
17.6.2. Điều trị nội khoa
| Loại | MCC | Khuyến cáo về điều trị huyết khối van sinh học |
| IIa | B | 1. Ở bệnh nhân nghi ngờ hoặc đã xác định huyết khối van sinh học có huyết động ổn định và không có chống chị định kháng đông, khởi đầu điều trị bằng kháng vitamin K là hợp lý (129,152,179–182). |
Chống đông máu bằng kháng vitamin K và/hoặc heparin không phân đoạn là điều trị đầu tay với huyết khối van sinh học(18,183,184). Bệnh nhân bị tắc nghẽn van sinh học có thể có một lớp huyết khối mỏng gây giảm vận động lá van. Điều trị kháng vitamin K có thể làm ly giải huyết khối và cải thiện chức năng van. Nhiều nghiên cứu nhỏ không ngẫu nhiên đã ủng hộ việc sử dụng kháng vitamin K để điều trị bệnh nhân huyết khối van sinh học có triệu chứng lâm sàng và hình ảnh cận lâm sàng sau thay van động mạch chủ bằng phẫu thuật hoặc thay van động mạch chủ qua da (129,152,180,181,185). Chống đông kháng vitamin K có thể làm giảm đáng kể chênh áp ngang van, cải thiện vận động lá van và tình trạng lâm sàng (129,153,181). Vì huyết khối van sinh học có thể tái phát và liên quan đến thoái hóa sớm van sinh học, cân nhắc dùng chống đông vô thời hạn sau một đợt điều trị chống đông nhưng phải xem xét có làm tăng nguy cơ chảy máu hay không(18,183,184).
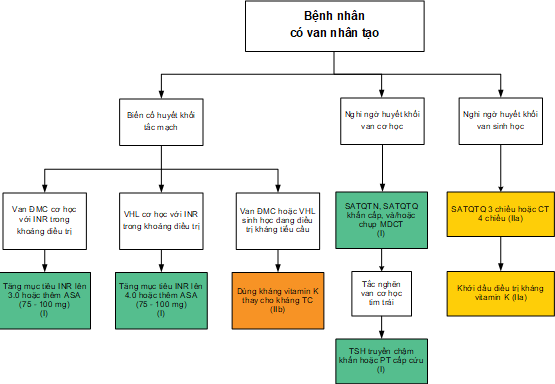
Hình 17. Xử trí các biến cố huyết khối tắc mạch và huyết khối van (1)
ĐMC (động mạch chủ); Tăng mục tiêu INR (International Normalized Ratio – Tỉ lệ chuẩn hóa quốc tế) MDCT ( Multidetector computed tomography – chụp cắt lớp vi tính đa dãy); TSH (tiêu sợi huyết); SATQTQ (siêu âm tim qua thực quản); SATQTN (siêu âm tim qua thành ngực)
17.7. Hẹp van nhân tạo
17.7.1. Chẩn đoán hẹp van nhân tạo
| Loại | MCC | Khuyến cáo về chẩn đoán hẹp van nhân tạo |
| I | B | 1. Ở bệnh nhân nghi ngờ hẹp van cơ học hay sinh học, SATQTN và SATQTQ được khuyến cáo để chẩn đoán nguyên nhân và độ nặng tắc nghẽn van, đánh giá chức năng van, và ước lượng áp lực động mạch phổi tâm thu(163,186). |
| I | C | 2. Ở bệnh nhân hẹp van cơ học, soi van hoặc CT hình ảnh động được khuyến cáo để đánh giá vận động của các lá van. |
| IIa | C | 3. Ở bệnh nhân hẹp van sinh học, hình ảnh SATQTQ 3 chiều hoặc CT 4 chiều có thể hữu ích để loại trừ huyết khối lá van(129,153,177,178). |
Hẹp van nhân tạo có thể xảy ra với van cơ học lẫn sinh học. Hẹp van nhân tạo được đặc trưng bởi một quá trình tăng dần vận tốc và chênh áp ngang van kết hợp với lá van dày bất thường/vôi hóa lá van (đối với van sinh học) hoặc bằng chứng hình thành mô xơ (đối với van cơ học). Tuy nhiên, hẹp van cũng có thể do một lớp huyết khối mỏng trên lá van, có thể hồi phục được khi điều trị chống đông đường uống. Khi hiện diện chênh áp ngang van tăng quá mức với vận động lá van bình thường và không có huyết khối, thì có sự tồn tại bất tương xứng bệnh nhân – van nhân tạo hoặc sự hình thành mô xơ (hoặc cả hai) (1).
Vận động của các đĩa van cơ học được đánh giá tốt nhất bằng soi van hoặc chụp CT hình ảnh động vì phản xạ mạnh từ van cơ học che khuất hình ảnh trên siêu âm tim, đặc biệt là SATQTN ở hầu hết bệnh nhân. Với soi van, góc ảnh phải được điều chỉnh để phù hợp với chuyển động của các đĩa van từ mặt bên, cho phép đo các góc đóng và mở, có thể được so sánh với các giá trị dự kiến cho loại van đó. Hình ảnh CT động thu được ở tốc độ khung hình cao tập trung vào van nhân tạo trong hình ảnh 3 chiều. So với phương pháp soi van, hình ảnh CT động 3 chiều ít phụ thuộc vào người vận hành hơn để đo góc mở và đóng. Thêm vào đó, hình ảnh CT động cho phép phát hiện mô xơ hoặc huyết khối trên van hoặc liền kề van, mà không thể thấy được khi soi van. Khi có bằng chứng lâm sàng về hẹp van sinh học, hình ảnh SATQTQ 3 chiều hoặc CT 4 chiều có thể hữu ích để phát hiện lớp huyết khối van là nguyên nhân gây tắc nghẽn (1).
17.7.2. Can thiệp hẹp van nhân tạo
| Loại | MCC | Khuyến cáo về điều trị hẹp van nhân tạo |
| I | B | 1. Ở bệnh nhân hẹp van cơ học hay sinh học có triệu chứng, có chỉ định can thiệp phẫu thuật lại, trừ khi nguy cơ phẫu thuật cao hoặc rất cao(187–189). |
| IIa | B | 2.Đối với bệnh nhân hẹp van động mạch chủ sinh học có triệu chứng và nguy cơ phẫu thuật cao hoặc rất cao, thủ thuật ghép van trong van qua ống thông là hợp lý khi thực hiện ở Trung tâm Van Chuyên sâu(190,191). |
| IIa | B | 3. Đối với bệnh nhân hẹp van sinh học nặng nghi ngờ hoặc đã ghi nhận do huyết khối van, dùng chống đông đường uống kháng vitamin K là hợp lý(128,179,180). |
Tái phẫu thuật cho hẹp van nhân tạo liên quan đến tỉ lệ tử vong và bệnh tật có thể chấp nhận được trong thời đại hiện nay, nhưng nguy cơ thường cao hơn so với ước tính tại thời điểm phẫu thuật ban đầu do bệnh nhân tuổi cao, tình trạng lâm sàng tại thời điểm can thiệp và tái phẫu thuật(80,188). Quyết định tiến hành phẫu thuật hay can thiệp qua da dựa trên kiến thức chuyên môn sẵn có, đặc điểm của từng bệnh nhân và van, cũng như quyết định chung.
Liệu pháp ghép van trong van qua ống thông nổi bật lên như một phương pháp thay thế chấp nhận được cho các bệnh nhân có nguy cơ phẫu thuật cao và rất cao bị hẹp van động mạch chủ sinh học (190,191). Mặc dù tắc nghẽn mạch vành phổ biến hơn với các thủ thuật ghép van trong van động mạch chủ so với thay van động mạch dủ qua da đối với hẹp van động mạch chủ tự nhiên, tỉ lệ hở cạnh van và đặt máy tạo nhịp vĩnh viễn thì thấp hơn với thủ thuật ghép van trong van so với thay van động mạch chủ qua da.
Can thiệp bằng bóng qua da nên tránh khi điều trị hẹp van sinh học tim trái. Tái thay van động mạch chủ bằng phẫu thuật qua da là lựa chọn an toàn và khả thi ở bệnh nhân được chọn, nhưng nguy cơ bất tương xứng bệnh nhân – van nhân tạo ở van nhỏ và nguy cơ tắc mạch vành, cũng như khả năng tiếp cận động mạch vành trong tương lai cần được xem xét(18).
Một số bệnh nhân có biểu hiện hẹp van sinh học do huyết khối lá van dẫn đến giảm vận động lá van. Huyết khối lá van có thể xảy ra từ một tháng đến nhiều năm sau ghép van. Nếu bệnh nhân ổn định và không có chống chỉ định chống đông lâu dài, dùng chống đông kháng vitamin K đường uống có thể giúp giải quyết huyết khối và cải thiện huyết động(128,153,179–182,185). Tuy nhiên, những bệnh nhân này tăng nguy cơ huyết khối tái phát (nếu ngừng chống đông) và thoái hóa cấu trúc van sớm, vì vậy cần theo dõi chặt chẽ(183).
17.8. Hở van nhân tạo
17.8.1. Chẩn đoán hở van nhân tạo
Hở van nhân tạo cơ học có thể trong van hoặc cạnh van. Hở trong van do giảm vận động đĩa van thứ phát do mô xơ, huyết khối, hoặc sùi làm cản trở việc đóng hoàn toàn lá van. Hở cạnh van do gián đoạn đường khâu liên quan đến lỗi kỹ thuật lúc thay van, lỗi khâu, đứt vòng van, hoặc viêm nội tâm mạc nhiễm trùng. Bệnh nhân có vôi hóa vòng van hai lá nặng dễ bị hở cạnh van muộn.
Hở van sinh học có thể cạnh van nhiều hơn trong van do giảm vận động lá van thứ phát do vôi hóa hoặc thủng lá van hoặc sa phất phơ lá van liên quan đến vùng vôi hóa khu trú(163).
| Loại | MCC | Khuyến cáo về chẩn đoán hở van nhân tạo |
| I | B | 1. Ở bệnh nhân nghi ngờ hở van cơ học hay sinh học, SATQTN và SATQTQ được khuyến cáo thực hiện để xác định nguyên nhân và độ nặng dòng hở, đánh giá chức năng thất trái, và ước lượng áp lực động mạch phổi tâm thu (163,186,192,193). |
| I | C | 2. Ở bệnh nhân phải thực hiện thủ thuật qua ống thông đóng dòng hở cạnh van nhân tạo, SATQTQ 3 chiều được khuyến cáo thực hiện để hướng dẫn trong thủ thuật (193–196). |
17.8.2. Điều trị nội khoa
Điều trị nội khoa hở van nhân tạo thích hợp với bệnh nhân không triệu chứng hoặc khi nguyên nhân hở van là huyết khối hoặc viêm nội tâm mạc nhiễm trùng, mặc dù cuối cùng có thể cần can thiệp thêm ở nhiều bệnh nhân này. Một số bệnh nhân dung nạp vời hở van nhân tạo không triệu chứng trong nhiều năm, tương tự như hở van tự nhiên. Ở bệnh nhân bị tán huyết nghi do hở cạnh van, điều trị nội khoa bổ sung sắt và axit folic hoặc có thể truyền máu định kỳ nếu thiếu máu không nặng, điều trị can thiệp dành riêng cho bệnh nhân thiếu máu khó trị có triệu chứng.
17.8.3. Can thiệp
| Loại | MCC | Khuyến cáo về điều trị hở van nhân tạo |
| I | B | 1. Ở bệnh nhân bị tán huyết khó trị hoặc suy tim do hở cạnh van hoặc trong van nhân tạo, phẫu thuật được khuyến cáo trừ khi phẫu thuật nguy cơ cao hoặc rất cao(80,188,189,197). |
| IIa | B | 2. Ở bệnh nhân hở van nhân tạo nặng không triệu chứng và nguy cơ phẫu thuật thấp, chỉ định phẫu thuật là hợp lý (80,188,189,197). |
| IIa | B | 3. Ở bệnh nhân hở cạnh van nhân tạo với những biểu hiện sau: 1) Tán huyết khó trị hoặc triệu chứng NYHA III/IV và 2) Có nguy cơ phẫu thuật cao hoặc rất cao và 3) Có đặc điểm giải phẫu phù hợp với liệu pháp qua ống thông, sửa chữa qua da đối với hở cạnh van là hợp lý khi thực hiện ở Trung tâm Van Chuyên sâu (198–202). |
| IIa | B | 4. Đối với bệnh nhân suy tim nặng do hở van nhân tạo có nguy cơ phẫu thuật cao hoặc rất cao, thủ thuật ghép van trong van qua ống thông là hợp lý khi thực hiện ở Trung tâm Van Chuyên sâu(190,203,204). |
Thoái hóa van nhân tạo có thể dẫn đến hở van do vôi hóa lá van, van áp không sát hoặc thoái hóa lá van với rách hoặc thủng van. Hở van cấp hay mạn có thể dẫn đến suy tim. Hở cạnh van có thể gây tán huyết với triệu chứng thiếu máu và suy tim. Hở cạnh van mới xuất hiện sau thay van làm tăng nghi vấn về viêm nội tâm mạc nhiễm trùng, cần được loại trừ vì sự hiện diện của nhiễm trùng cần điều trị kháng sinh trước phẫu thuật và là chống chỉ định thay van bằng thông tim. Bệnh nhân hở cạnh van nhân tạo có triệu chứng, tốt nhất nên được phẫu thuật, thủ thuật ghép van trong van qua ống thông nếu nguy cơ phẫu thuật cao hoặc rất cao. Vì hở van sinh học tiến triển nhanh, việc thay thế van sinh học bị hở nên được cân nhắc ngay cả khi bệnh nhân không triệu chứng.
Kaneko và cộng sự đã ghi nhận trên nhóm đoàn hệ 3380 bệnh nhân từ dữ liệu của Hội phẫu thuật lồng ngực (2011 – 2013) được tái thay van động mạch chủ bằng phẫu thuật đơn thuần theo chương trình, và họ đã chứng minh được tỉ lệ tử vong do tái phẫu thuật (nhưng chấp nhận được) so với phẫu thuật lần đầu (4,6% so với 2,2,%, P dưới 0,0001) và tỉ lệ biến chứng tương đối thấp(188). Gần đây hơn, Shah và cộng sự đã báo cáo tỉ lệ tử vong phẫu thuật là 3% trong số 495 bệnh nhân phẫu thuật vì hở cạnh van(205), với nguy cơ liên quan đến van hai lá cao hơn so với thủ thuật van động mạch chủ (OR: 1,66; KTC 95%: 1,25 – 2,20). Những phát hiện này phù hợp với phát hiện của Bouhout và cộng sự(206), đã báo cáo tỉ lệ tử vong phẫu thuật van hai lá là 8%, van động mạch chủ 3% và cả hai van là 14% trong tổng số 190 bệnh nhân được chỉ định phẫu thuật vì hở cạnh van. Ước tính rủi ro phẫu thuật cho từng bệnh nhân được tính bằng công cụ tính nguy cơ của Hội phẫu thuật lồng ngực (http://riskcalc.sts.org/stswebriskcalc/).
Trong một đoàn hệ đơn trung tâm lớn, sửa chữa qua da của 141 tổn thương hở cạnh van ở 115 bệnh nhân đã đạt tỉ lệ thành công 77% và tỉ lệ biến chứng trong 30 ngày là 8,7%(202). Trong một nghiên cứu khác với 126 bệnh nhân được sửa van qua do vì hở cạnh van, Sorajja và cộng sự đã báo cáo tỉ lệ sống còn sau 3 năm là 64,3%(198). Trong một đoàn hệ 231 bệnh nhân (2006 – 2017) đã được đóng hở cạnh van hai lá qua da, hở cạnh van giảm xuống mức độ nhẹ hoặc ít hơn đạt được ở 70% bệnh nhân, với tỉ lệ sống còn sau 3 năm là 61%, so với tỉ lệ 47% ở những bệnh nhân có mức độ hở cạnh van tồn lưu lớn hơn (P = 0,002) (200,201).
Cơ quan đăng ký Dữ liệu Quốc tế Van-Trong-Van đã kiểm tra kết quả của 459 bệnh nhân được làm thủ thuật ghép van trong van qua ống thông, trong đó khoảng 30% hở van đơn thuần và 30% có tổn thương phối hợp(190). Trong vòng 1 tháng sau thủ thuật, 7,6% bệnh nhân tử vong, 1,7% bị đột quị nặng, và 93% bệnh nhân sống sót có tình trạng chức năng tốt. Tỉ lệ sống còn sau 1 năm là 83,2% (190). Trong một báo cáo, thủ thuật ghép van trong van có kết quả huyết động tương tự tái phẫu thuật với nguy cơ đột quị và chảy máu thấp hơn tái phẫu thuật(203).
(Vui lòng xem tiếp trong kỳ sau)







