Mục tiêu nghiên cứu: đánh giá hiệu quả của phối hợp telmisartan và amlodipin ở các liều khác nhau trên tốc độ bài tiết albumin niệu (UAER) ở bệnh nhân tăng huyết áp kèm đái tháo đường và tiểu đạm vi thể.
Roberto Fogari, Giuseppe Derosa, Annalisa Zoppi, PaolaPreti, PierangeloLazzari, Maurizio Destro,
Elena Fogari, Andrea Rinaldi,and Amedeo Mugellini
Biên dịch: BS Nguyễn Thị Thuý Minh
Khoa Nội Tim mạch Bệnh viện Nhân Dân Gia Định
Phương pháp nghiên cứu: Sau 2 tuần điều trị bằng giả dược, 300 bệnh nhân đái tháo đường type 2 kèm tiểu đạm vi thể được điều trị bằng telmisartan 40 mg phối hợp amlodipin 2,5 mg. Sau 4 tuần, có 210 bệnh nhân không kiểm soát tốt huyết áp (>130/80 mmHg) được phân ngẫu nhiên thành hai nhóm. Một nhóm điều trị bằng telmisartan (lên đến 160 mg/ngày) phối hợp với amlodipin liều cố định 2,5 mg/ngày. Nhóm còn lại điều trị với amlodipin đến 10 mg/ngày phối hợp với liều telmisartan cố định 40 mg/ngày. Sau 12 tuần những bệnh nhân không kiểm soát được huyết áp được phối hợp thêm clonidin 0,1mg/ngày dán ngoài da. Sau 16 tuần những bệnh nhân vẫn chưa đạt huyết áp mục tiêu sẽ dừng khỏi nghiên cứu, những người còn lại tiếp tục được theo dõi đến tuần 48. Huyết áp, tốc độ bài tiết albumin niệu, độ thanh thải creatinin, nồng độ kali trong huyết tương, đường huyết đói, HbA1c, được đánh giá vào cuối giai đoạn điều trị telmisartan 40 mg phối hợp với amlodipin 2,5 mg và sau tuần thứ 48.
Kết quả: Huyết áp tâm thu và tâm trương giảm tương tự ở cả hai nhóm (-24/-21, -23/-21 và -24/-21 mmHg, p<0,001 ở nhóm tăng dần telmisartan; -25/-22, -25/-21 và-25/-22 mmHg, p<0,001 ở nhóm tăng dần amlodipin). Giảm tốc độ bài tiết albumin niệu 47,5% (p<0,01), 65,3% (p<0,001), và 77% (p<0,0001) tương ứng liều telmisartan 80-120-160 mg/amlodipin 2,5 mg/ngày. Trong khi đó giảm UAER 34% (p<0,03), 37% (p<0,03), và 33% (p<0,03) tương ứng với liều amlodipin 5-7,5 và 10 mg/telmisartan 40mg/ngày. Sự khác biệt giữa hai nhóm đáng kể và có ý nghĩa thống kê lần lượt là (p<0,05; p<0,01; và p<0,001)
Kết luận:Nghiên cứu này cho thấy, ở những mức làm giảm huyết áp tương đương, tốc độ bài tiết albumin qua nước tiểu giảm nhiều hơn khi điều trị liều telmisartan tăng dần .
Từ khoá: telmisartan, amlodipin, microalbuminuria, tăng huyết áp, đái tháo đường Type 2.
—————————————————————————————————-
Đặt vấn đề
Tiểu đạm vi thể khi tốc độ bài tiết albumin qua nước tiểu (UAER) 30-300 mg/24giờ. Tiểu đạm vi thể là một yếu tố tiên lượng mức độ tiến triển bệnh thận do đái tháo đường và sự gia tăng tỷ lệ bệnh và tử vong do bệnh lý tim mạch ở bệnh nhân đái tháo đường. Đạm niệu vi thể ở bệnh nhân đái tháo đường type 2 thường liên quan đến tăng huyết áp và mức độ tiến triển nhanh của tổn thương thận và tim mạch. Do vậy, mục tiêu điều trị là làm giảm huyết áp và tốc độ bài tiết albumin qua nước tiểu (UAER). Có nhiều bằng chứng cho thấy việc kiểm soát huyết áp sớm và tích cực là yếu tố bảo vệ thận ở bệnh nhân tăng huyết áp kèm đái tháo đường đặc biệt khi huyết áp dưới 130/80 mmHg và những bệnh nhân này thường phải phối hợp các loại thuốc điều trị tăng huyết áp để đạt được huyết áp mục tiêu.
Một đồng thuận chung đã cho thấy lợi ích của nhóm ức chế hệ renin-angiotensin làm giảm đạm niệu vi thể, làm chậm tiến triển suy thận và cải thiện sống còn. Do đó phối hợp thuốc trong điều trị tăng huyết áp nên bao gồm ức chế men chuyển hoặc ức chế thụ thể angiotensin để bảo vệ thận tích cực hơn. Các nghiên cứu gần đây cho thấy việc phối hợp giữa ức chế thụ thể angiotensin và ức chế men chuyển làm giảm albumin niệu nhiều hơn là đơn trị liệu ở bệnh nhân có bệnh thận do đái tháo đường. Tuy nhiên, việc phối hợp giữa 2 nhóm thuốc này gây nguy cơ bất lợi như: tăng nồng độ kali trong máu, làm nặng hơn tình trạng thiếu máu trong suy thận đặc biệt ở những bệnh nhân có suy chức nặng thận từ nhẹ đến trung bình. Do vậy điều trị phối hợp ức chế canxi và ức chế thụ thể angiotensin trên bệnh nhân tăng huyết áp kèm đái tháo đường type 2 sẽ tránh được các tác dụng phụ kể trên. Ức chế canxi là một nhóm thuốc hạ huyết áp trong khi đó nhóm ức chế thụ thể angiotensin hiệu quả làm giảm đạm niệu,vì vậy sự phối hợp này sẽ tăng khả năng bảo vệ chức năng thận. Tuy nhiên cho đến thởi điểm này vẫn còn ít nghiên cứu về hiệu quả phối hợp giữa ức chế canxi và ức chế thụ thể angiotensin trong điều trị tăng huyết áp kèm đái tháo đường cũng như liều tối ưu để làm giảm tối đa đạm niệu.
Với nền tảng nói trên, trong nghiên cứu này, chúng tôi đánh giá hiệu quả của phối hợp ức chế thụ thể telmisartan và amlodipin trên tốc độ bài tiết albumin qua nước tiểu ở những bệnh nhân tăng huyết áp kèm đái tháo đường type 2 có tiểu đạm vi thể qua so sánh hiệu quả giữa hai phác đồ điều trị (một nhóm sử dụng telmisartan liều cao/ amlodipin liều thấp và nhóm ngược lại).
Thiết kế nghiên cứu
Bệnh nhân tăng huyết áp kèm đái tháo đường type 2 đang điều trị ngoại trú tuổi từ 35-70, kiểm soát đường huyết tốt bằng chế độ ăn hoặc bằng thuốc hạ đường huyết uống, tiểu đạm vi thể khi albumin niệu từ 30-300 mg/ 24 giờ.
Tiêu chuẩn loại trừ: tăng huyết áp thứ phát, tiền sử nhồi máu cơ tim và đột quỵ trong vòng 6 tháng trước nghiên cứu, suy tim, ung thư, một số bệnh lý nghiêm trọng ảnh hưởng tới nghiên cứu, hút thuốc lá, BMI> 30 kg/m2, bệnh nhân không dung nạp với ức chế thụ thể hoặc ức chế canxi.
Nghiên cứu được tiến hành sau khi được sự đồng ý của bệnh nhân và đã được thông qua hội đồng y đức.
Sau 2 tuần điều trị bằng giả dược ở giai đoạn rửa trôi, ở giai đoạn này bệnh nhân phải ngưng thuốc hạ áp nhưng vẫn uống thuốc hạ đường huyết, bệnh nhân được uống telmisartan 40mg phối hợp 2,5 mg amlodipin. Sau 4 tuần những bệnh nhân chưa kiểm soát được huyết áp (HA>130/80 mmHg) được chọn ngẫu nhiên thành 2 nhóm điều trị bằng liều lượng khác nhau. Một nhóm bệnh nhân được sử dụng telmisartan tăng dần 40 mg mỗi 4 tuần cho đến 160 mg và liều amlodipin cố định 2,5 mg (nhóm T). Nhóm còn lại sẽ được tăng liều amlodipin 2,5 mg mỗi 4 tuần cho đến liều 10 mg và liều cố định telmisartan 40 mg (nhóm A). Sau 16 tuần những bệnh nhân không đáp ứng sẽ phối hợp thêm 0,1 mg ngày Clonidin dán ngoài da (Hình 1). Sau 20 tuần bệnh nhân không kiểm soát được huyết áp sẽ được dừng nghiên cứu. Những bệnh nhân đáp ứng sẽ được theo dõi thêm 48 tuần. Tất cả bệnh nhân đều duy trì chế độ ăn như là một phần của điều trị cùng với thuốc hạ đường huyết uống và không được sử dụng các loại thuốc khác trong suốt quá trình nghiên cứu.
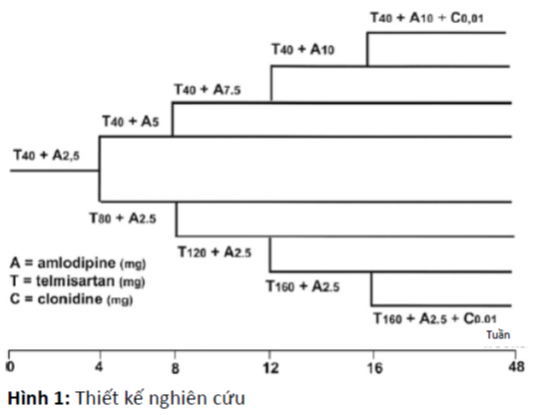
Đo và ghi nhận trị số huyết áp vào cuối giai đoạn điều trị telmisartan liều 40 mg phối hợp với amlodipin 2,5mg, cuối tuần lễ thứ 16 và sau 48 tuần điều trị. Độ thanh thải creatinin, UAER, nồng độ kali trong máu, đường huyết đói và HbA1C được đánh giá vào cuối giai đoạn telmisartan 40 mg phối hợp amlodipin 2,5 mg và sau 48 tuần .
Huyết áp được đo vào buổi sáng trước khi uống thuốc (tức là ở giai đoạn đáy, 22-24 giờ sau uống thuốc), sau nghỉ 5 phút ở tư thế ngồi và sử dụng máy đo huyết áp thuỷ ngân chuẩn. Đo 3 lần trên cùng một cánh tay cách nhau 2 phút. Trị số huyết áp được ghi nhận là số trung bình của 3 lần đo. UAER được đo bằng phương pháp miễn dịch phóng xạ. UAER được ghi nhận là trung bình của hai lần lấy nước tiểu 24 giờ trong vòng 1 tuần. Bệnh nhân cần được hướng dẫn lấy nước tiểu đúng cách và được khuyên hoạt động nhẹ trong thời gian lấy nước tiểu. Xét nghiệm sinh hoá máu và nước tiểu được thực hiện ở những phòng thí nghiệm đạt chuẩn. Nồng độ HbA1c được đo bằng phương pháp sắc ký lỏng hiệu năng cao (HPLC).

Phân tích thống kê
Số liệu được diễn giải bằng trung bìnhvà độ lệch chuẩn. Kiểm tra tính đồng nhất trong phân phối bệnh nhân giữa hai nhóm điều trị bằng x2 test. Kết quả được thống kê bằng cách sử dụng phương pháp thống kê phân tích phương sai và t test (so sánh trong nhóm và dưới nhóm). Tất cả các phép thống kê được kiểm định hai đầu và có ý nghĩa khi p< 0,05.
Kết quả
Có 300 bệnh nhân đạt tiêu chuẩn chọn bệnh ở cuối giai đoạn rửa trôi được điều trị bằng telmisaran 40 mg phối hợp với amlodipin 2,5 mg trong 4 tuần. Trong đó có 210 bệnh nhân không kiểm soát được huyết áp (> 130/80 mmHg) tiếp tục được đưa vào nghiên cứu và phân thành 2 nhóm ngẫu nhiên. 105 bệnh nhân ở nhóm T và 105 bệnh nhân ở nhóm A. Đặc điểm lâm sàng và nhân khẩu học được trình bày ở Bảng 1. Không có sự khác biệt có ý nghĩa thống kê giữa 2 nhóm ở các tham số phân tích. Kết quả ở giai đoạn chỉnh liều, ở nhóm T có 36 bệnh nhân cần điều trị liều cao nhất telmisartan, 33 bệnh nhân liều 120 mg và 36 duy trì ở liều 80 mg. Nhóm A có 26 bệnh nhân sử dụng amlodipin liều tối đa, 33 bệnh nhân liều 7,5 mg và 36 người liều 5 mg. Do không kiểm soát được huyết áp sau 12 tuần, có 16 bệnh nhân nhóm đang sử dụng telmisartan 160 mg phối hợp amlodipin 2,5 mg và 11 bệnh nhân ở nhóm telmisartan 40 mg phối hợp amlodipin 10 mg cần phải thêm clonidin ngoài da với liều 0,1 mg/ ngày. Đặc điểm lâm sàng tương đối tương đồng ở cả 2 nhóm. Sau 20 tuần theo dõi (kết thúc giai đoạn chỉnh liều), có 6 bệnh nhân (4 ở nhóm T, 2 ở nhóm A) không kiểm soát được huyết áp và bị loại khỏi nghiên cứu. Tuy vậy ở nhóm bệnh nhân này có UAER tương tự như ở nhóm tiếp tục được theo dõi. Hai bệnh nhân ở nhóm T và 1 bệnh nhân ở nhóm A bị mất khỏi nghiên cứu do vậy chỉ còn 99 ở nhóm T và 102 ở nhóm A hoàn thành 48 tuần theo dõi.
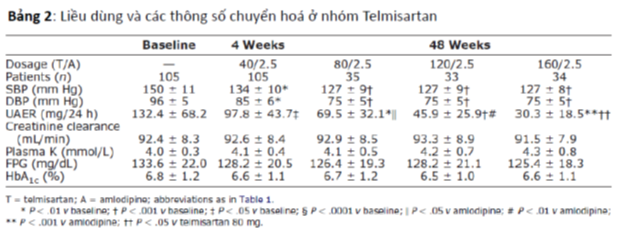
Kết quả chính của nghiên cứu được trình bày ở Bảng 2 và 3.
Ta nhận thấy rằng hiệu quả hạ áp tâm thu lẫn tâm trương tương tự nhau ở cả hai nhóm và sự khác biệt này không đáng kể giữa nhóm phối hợp telmisartan liều cao với amlodipin liều thấp và ngược lại ở một vài thời điểm nghiên cứu. Khi tăng dần liều telmisartan từ (40-80-120 và 160 mg), huyết áp tâm thu lẫn tâm trương đều giảm so với ban đầu lần lượt là 16/10 mmHg (p<0,01), 24/21 mmHg, 23/21 mmHg và 24/21 mmHg (tất cả có p<0,001). Huyết áp tâm thu lẫn tâm trương cũng giảm lần lượt 16/10 (p<0,01), 25/22 mmHg, 25/21mmHg và 25/22 mmHg (tất cả có p<0,001) ở nhóm điều trị với liều Amlodipin tăng dần ( 2,5-5- 7,5 và 10 mg).
UAER cũng giảm đáng kể ở cả hai nhóm điều trị phối hợp nhưng nhóm T giảm nhiều hơn. Giảm UAER lần lượt so với chứng là 34,6 mg/24 giờ (p<0,05), 62,9 mg/24giờ (p<0,01 so với chứng và p<0,05 so với nhóm A), 86,5mg/24giờ (p<0,001 so với chứng và p<0,01 so với nhóm A) và 102 mg/24 giờ (p<0,0001 so với chứng và p<0,001 so với nhóm A) ở nhóm điều trị với phác đồ phối hợp telmisartan 40-80-120 và 160mg/ amlodipin 2,5 mg/ngày. Giảm UAER so với chứng lần lượt là 35,1 mg/24 giờ (p<0,05); 46,2mg/24 giờ (p<0,03); 50,3mg/24giờ (p<0,03) và 45mg/24giờ (p<0,03) tương ứng ở nhóm điều trị với phác đồ amlodipin với liều tăng dần 2,5 – 5 – 7,5 và 10 mg/telmisartan 40 mg.
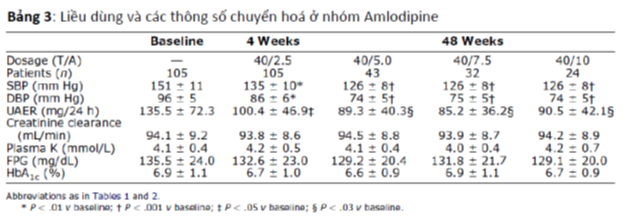
Trọng lượng cơ thể không thay đổi ở tất cả bệnh nhân. Độ thanh thải creatinin cũng không thay đổi đáng kể trong suốt 48 tuần nghiên cứu ở cả hai nhóm. Tương tự như vậy, không có tác động đáng kể lên nồng độ kali trong máu và đường huyết lúc đói ở cả hai nhóm. Nồng độ HbA1c cũng không bị ảnh hưởng đáng kể và không có bệnh nhân nào cần phải thay đổi phác đồ điều trị tăng đường huyết trong suốt thời gian nghiên cứu.
Bệnh nhân ở cả hai nhóm đều dung nạp tốt với thuốc. Ở nhóm T có 10 bệnh nhân (10%) được báo cáo có một hoặc nhiều hơn các tác dụng phụ (10%) và nhóm A có 15 bệnh nhân (14%), sự khác biệt này không có ý nghĩa thống kê giữa 2 nhóm. Các tác dung phụ được báo cáo như chóng mặt (n=5), buồn nôn (n=3), suy nhược (n=2) và đau đầu (n=1) ở nhóm T; phù chân (n=7), đau đầu (n=3) và hồi hộp (n=2) ở nhóm A. Không có bệnh nhân nào rút khỏi nghiên cứu vì có các biến cố nghiêm trọng.
Bàn luận
Từ những kết quả của nghiên cứu này chứng minh rằng ở những bệnh nhân không hút thuốc có tăng huyết áp kèm đái tháo đường type 2 và tiểu đạm vi thể khi điều trị phối hợp telmisartan liều cao với amlodipin liều thấp kiểm soát được huyết áp, không ảnh hưởng đến đường huyết, nồng độ các chất điện giải trong máu trong suốt 48 tuần. Hiệu quả này tương tự ở nhóm điều trị phối hợp telmisartan liều thấp với amlodipin liều cao. Điều này đã khẳng định lợi ích của viêc phối hợp điều trị giữa ức chế thụ thể angiotensin và ức chế canxi tác dụng kéo dài để đạt được huyết áp mục tiêu ở nhóm bệnh nhân có nguy cơ cao này.
Những phát hiện thú vị nhất của nghiên cứu này là ở cả hai nhóm điều trị đều có ảnh hưởng lên UAER. Điều trị phối hợp giữa telmisartan và amlodipin làm giảm đáng kể UAER, tuy nhiên trong nghiên cứu này cho thấy hiệu quả này tăng lên khi điều trị telmisartan liều cao dù cho hiệu quả hạ áp tương đương ở cả hai nhóm. Khi tăng liều amlodipin từ 7,5 mg lên đến 10 mg không làm giảm UAER thêm nữa, trong khi đó telmisartan liều cao 160 mg/ngày (liều cao hơn khuyến cáo 80mg/ngày) sẽ làm giảm thêm UAER (giảm 26% ở liều 40 mg; 47,5% liều 80 mg; 65% liều 120 mg và 77% liều 160mg). Trong nghiên cứu này, liều telmisartan trong điều trị tăng huyết áp gấp đôi liều khuyến cáo, tuy nhiên điều này phù hợp với các nghiên cứu trước đây về hiệu quả làm giảm đạm niệu càng tăng khi liều của nhóm thuốc ức chế men chuyển cũng như ức chế thụ thể angiotensin càng cao.
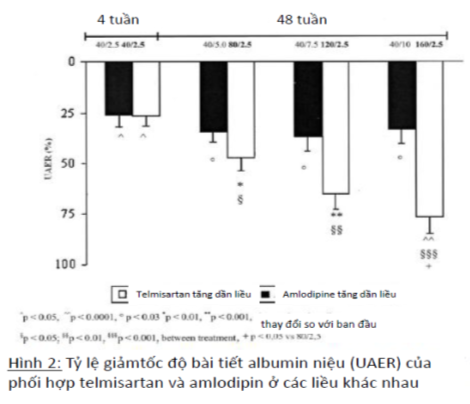
Hiệu quả làm giảm UAER nhiều hơn khi điều trị telmisartan liều cao độc lập với giảm huyết áp hệ thống. Có nhiều cơ chế giải thích tính độc lập về hiệu quả của ức chế thụ thể angiotensin trên huyết áp với hiệu quả trên UAER bao gồm: (1) giảm áp suất thuỷ lực trong hệ thống cầu thận bằng cách giãn tiểu động mạch đi; (2) cải thiện tính thấm có chọn lọc của màng lọc cầu thận; (3) giảm sự thiếu hụt bài tiết nephrin ở cầu thận, nephrin là một protein hiện diện ở màng khe của lớp tế bào biểu mô cầu thận đóng vai trò chính trong chức năng làm rào cản lọc thận; (4) giảm nồng độ các cytokin prosclerotic trong cầu thận như TGF-β (transforming growth factor-) và CTGF (connective tissue growth factor). Tăng hoạt động của hệ renin-angiotensin-aldosteron và tăng mật độ thụ thể angiotensin trong mô thận tổn thương cùng với giảm khả năng thâm nhập của thuốc lý giải cho thấy liều cao của thuốc là cần thiết để có thể ức chế hoàn toàn hệ renin-angiotensin-aldosteron ở mô, có hiệu quả chống đạm niệu so với nồng độ trong tuần hoàn để điều hoà huyết áp. Điều này cho thấy liều của các thuốc ức chế hệ renin-angiotensin-aldosteron để có hiệu quả tối đa làm giảm đạm niệu cao hơn liều cần thiết để làm hạ huyết áp.
Do vậy, khi phối hợp liều thấp telmisartan với liều cao amlodipin có hiệu quả chống đạm niệu thấp hơn. Khả năng làm giảm UAER khi điều trị theo phác đồ này có thể do tác dụng hạ áp của amlodipin. Điều này phù hợp với các nghiên cứu cho thấy khi kiểm soát huyết áp chặt chẽ ở giai đoạn sớm ở bệnh nhân bệnh thận do đái tháo đường là một trong những yếu tố quan trọng làm giảm UAER và ngăn ngừa tiểu đạm đại thể.
Kiểm soát tốt đường huyết đã được chứng minh là giảm đạm niệu ở bệnh nhân đái tháo đường Type 2. Trong nghiên cứu này không có phác đồ điều trị kết hợp nào làm thay đổi đáng kể đường huyết đói và nồng độ HbA1c.
Tiểu đạm ảnh hưởng đến tiến triển của tổn thương thận, giảm tốc độ bài tiết albumin niệu sẽ làm chậm khởi phát tiểu đạm trên lâm sàng và suy giảm chức năng thận do tiểu đạm vi thể. Trong nghiên cứu của chúng tôi, chức năng thận được đánh giá bằng độ thanh thải creatinin. Kết quả cho thấy không có thay đổi đáng kể ở cả hai nhóm sử dụng telmisartan liều cao và thấp phối hợp với amlodipin và không có sự khác biệt giữa hai nhóm. Tuy nhiên, thời gian nghiên cứu chỉ 48 tuần chưa đủ để làm thay đổi chức năng thận nhờ vào giảm tốc độ bài tiết albumin niệu ở bệnh nhân có bệnh lý thận giai đoạn sớm.
Từ nghiên cứu này cho thấy hiệu quả tăng liều dần ức chế thụ thể angiotensin trong phối hợp điều trị tăng huyết áp làm giảm tốc độ bài tiết albumin niệu tốt hơn tăng liều amlodipin ở bệnh nhân tăng huyết áp có đái tháo đường type 2 kèm tiểu đạm vi thể.
Tài liệu tham khảo
1. Mogensen CE: Microalbuminuria predicts clinical proteinuria and early mortality in maturity onset diabetes. N Engl J Med 1984;310:356–360.
2. Dinneen SF, Gerstein HC: The association of microalbuminuria and mortality in non-insulin-dependent diabetes mellitus. Arch Intern Med 1997;157:1413–1418.
3. Parving HH, Mauer M, Ritz E: Diabetic nephropathy, in Brenner BM (ed): Brenner and Rectors the Kidney, 7th ed. Philadelphia, Saunders, 2004, pp 1777–1818.
4. Schmitz A, Vaeth M, Mogensen CE: Systolic blood pressure relates to the rate of progression of albuminuria in NIDDM. Diabetologa 1994;37:1251–1258.
5. Sowers JR, Epstein M, Frohlic ED: Diabetes, hypertension and cardiovascular disease: an update. Hypertension 2001;37:1053–1059.
6. Bakris GL, Williams M, Dworkin L, Elliott WJ, Epstein M, Toto R, Tuttle K, Douglas J, Hsueh W, Sowers J: Preserving renal function in adults with hypertension and diabetes: a consensus approach. National Kidney Foundation Hypertension and Diabetes Executive Committees Working Group. Am J Kidney Dis 2000;36:646–661.
7. Hansson L, Zanchetti A, Carruthers SG, Dahlof B, Elmfeldt D,Julius S, Menard J, Rahn KH, Wedel H, Westerling S: Effects of intensive blood-pressure lowering and low-dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomised trial. Lancet 1998;351:1755–1762.
8. Chobanian AV, Bakris GL, Black HR, Cushman WC, Green LA, Izzo JL Jr, Jones DW, Materson BJ, Oparil S, Wright JT Jr, Roccella EJ, for the National Heart, Lung, and Blood Institute Joint National Committee on Prevention, Detection, Evaluation, and Treatment of
High Blood Pressure; National High Blood Pressure Education Program Coordinating Committee: The Seventh Report of the Joint National Committee on Prevention, Detection, Evaluation and Treatment of High Blood Pressure: the JNC 7 Report. JAMA 2003;289:2560 –2571.
9. Ravid M, Lang R, Rachmani R, Lishner M: Long-term renoprotective effect of angiotensin-converting enzyme inhibition in noninsulin-dependent diabetes mellitus. Arch Intern Med 1996;156:286–289.
10. Brenner BM, Cooper ME, de Zeeuw D, Keane WF, Mitch WE, Parving HH, Remuzzi G, Snapinn SM, Zhang Z, Shahinfar S, for the RENAAL Study Investigators: Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Engl J Med 2001;345:861– 869.
11. Parving HH, Lehnert H, Brochner-Mortensen J, Gomis R, Andersen S, Arner P: The effect of irbesartan on the development of diabetic nephropathy in patients with type 2 diabetes. N Engl J Med 2001;345:870–878.
12. Viberti G, Wheeldon NM: Microalbuminuria reduction with valsartan in patients with type 2 diabetes mellitus: a blood pressure independent effect. Circulation 2002;106:672– 678.
13. de Zeeuw D, Remuzzi G, Parving HH, Keane WF, Zhang Z, Shahinfar S, Snapinn S, Cooper ME, Mitch WE, Brenner BM: Proteinuria, a target for renoprotection in patients with type 2 diabetic nephropathy: lessons from RENAAL. Kidney Int 2004;65:2309–2320.
14. Mogensen CE, Neldam S, Tikkanen I, Oren S, Viskoper R, Watts RW, Cooper ME: Randomised controlled trial of dual blockade of renin-angiotensin system in patients with hypertension, microalbuminuria and non-insulin-dependent diabetes: the candesartan and lisinopril microalbuminuria (CALM) study. BMJ 2000;321:1440–1444.
15. Rossing K, Christensen PK, Jensen BR, Parving HH: Dual blockade of the renin angiotensin system in diabetic nephropathy. A randomised double-blind crossover study. Diabetes Care 2002;25:95–100.
16. Doulton TWR, He FJ, MacGregor GA: Systematic review of combined angiotensin-converting enzyme inhibition and angiotensin receptor blockade in hypertension. Hypertension 2005;45:880–886.
17. Sengul AM, Altuntas Y, Kurklu A, Aydin L: Beneficial effect of lisinopril plus telmisartan in patients with type 2 diabetes, microalbuminuria and hypertension. Diabetes Res Clin Pract 2006;71:210–219.
18. Jacobsen P, Andersen S, Rossing K, Hansen BV, Pareving HH:Dual blockade of the renin-angiotensin system in type 1 patients with diabetic nephropathy. Nephrol Dial Transplant 2002;17:1019–1024.
19. Kuriyama S, Tomonari H, Tokudome G, Horiguchi M, Hayashi H,Kobayashi H, Ishikawa M, Hosoya T: Antiproteinuric effects of combined antihypertensive therapies in patients with overt type 2 diabetic nephropathy. Hypertens Res 2002;25:849–855.
20. Andersen S, Rossing P, Juhl TR, Deinum J, Parving HH: Optimal dose of losartan for renoprotection in diabetic nephropathy. Nephrol Dial Transplant 2002;17:1413–1418.
21. Laverman GD, Navis G, Henning RH, de Jong PE, de Zeeuw D:Dual renin-angiotensin system blockade at optimal doses for proteinuria. Kidney Int 2002;62:1020 –1025.
22. Rossing K, Jacobsen P, Pietraszek L, Parving HH: Renoprotective effects of adding angiotensin II receptor blocker to maximal recommended doses of ACE inhibitor in diabetic nephropathy. A randomized double-blind cross-over trial. Diabetes Care 2003;26:2268–2274.
23. Rossing K, Schjoedt KJ, Jensen BR, Boomsa F, Parving HH:Enhanced renoprotective effects of ultrahigh doses of irbesartan in patients with type 2 diabetes and microalbuminuria. Kidney Int 2005;68:1190 –1198.
24. Schmieder RE, Klingbeil AU, Fleishmann EH, Veelken R, Delles C:Additional antiproteinuric effect of ultrahigh dose candesartan: a double-blind, randomized, prospective study. J Am Soc Nephrol 2005;16:3038 –3045.
25. Imanishi M, Yoshioka K, Konishi Y, Okumura M, Okada N, Sato T,Tanaka S, Fujii S, Kimura G: Glomerular hypertension as one cause of albuminuria in type II diabetic patients. Diabetologia 1999;42:999–1005.
26. Andersen S, Blouch K, Bialek J, Deckert M, Parving HH, Myers BD: Glomerular permselectivity in early stages of overt diabetic nephropathy. Kidney Int 2000;58:2129 –2137.
27. Bonnet F, Cooper ME, Kawachi H, Allen TJ, Boner G, Cao Z: Irbesartan normalises the deficiency in glomerular nephron expression in a model of diabetes and hypertension. Diabetologia 2001; 44:874–877.
28. MacIsaac RJ, Jerums G, Cooper ME: New insights into the significance of microalbuminuria. Curr Opin Nephrol Hypertens 2004; 13:83–91.
29. United Kingdom Prospective Diabetes Study (UKPDS) Group:Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes. BMJ 1998;317:703–713.







