I. Mở đầu:
Tỉ lệ xuất huyết não (XHN/ICH) hiệu chỉnh theo tuổi thay đổi khác nhau giữa 14,5 và 159,8/100.000 người/năm. Trong một tổng quan các nghiên cứu trên quần thể ở 21 quốc gia, tỉ lệ XHN là 24,6/100.000 người/năm và không có xu hướng giảm theo thời gian từ 1980-2007.
Bs Nguyễn Thanh Hiền
Bs Trần Dũ Đại
Bs Nguyễn Thị Lệ Trang
Bs Trần Thúy Anh Trang
Bs Ngô Văn Vinh
Tỉ lệ tử vong trung vị trong nhóm này khoảng 40 % trong tháng đầu và 55 % trong 1 năm (1).
Tỉ lệ XHN ở bệnh nhân đang dùng kháng đông thay đổi từ 0,6 – 1% mỗi năm. Trong một phân tích 52.993 bệnh nhân bị xuất huyết não nhập viện ở Mỹ, tỉ lệ tử vong trong bệnh viện thay đổi giữa 40% bệnh nhân bị XHN liên quan tới Warfarin và 29 – 31% bệnh nhân bị XHN không liên quan tới Warfarin. Xu hướng tử vong trong bệnh nhân không đổi theo thời gian ở nhóm XHN liên quan Warfarin, còn nhóm XHN không liên quan Warfarin có xu hướng giảm (1).
Lợi ích lâm sàng của dùng lại kháng đông sau XHN liên quan tới kháng đông còn nhiều tranh cãi và không có thực nghiệm lâm sàng ngẫu nhiên nào đánh giá về vấn đề này. Cả nguy cơ XHN lại nếu dùng kháng đông và nguy cơ thuyên tắc huyết khối nếu ngưng kháng đông đều phải đánh giá cẩn thận và quyết định tùy thuộc vào từng người bệnh cụ thể dựa trên yếu tố nguy cơ và tùy tình trạng bệnh nhân (2-4). Bài viết này nhằm đưa ra cách tiếp cận hiện nay khi dùng lại kháng đông sau XHN.
II. Nguy cơ XHN tái phát khi dùng lại kháng đông:
XHN tái phát khoảng 2- 3%/năm, khoảng 10 lần so với quần thể chung. Sau XHN, không dùng kháng đông sau 3 tháng khoảng 1%. Dùng kháng đông nguy cơ tái phát tăng
3 -5 lần (kháng vitamin K), máu tụ nhiều hơn và tiên lượng xấu hơn so với XHN ban đầu. Kết hợp kháng đông và ASA tăng nguy cơ XHN từ 2- 4 lần so với kháng vitamin K đơn độc ànên tránh phối hợp ở bệnh nhân sau XHN (3).
Nguy cơ này có thể dự đoán dựa trên loại XHN, nguy cơ của bệnh nhân cũng như hình ảnh đặc biệt trên MRI (1, 3).
II.1. Tỉ lệ XHN và nguy cơ tái phát (1,2,5):
XHN được phân loại theo vị trí gồm XHN nhu mô (nội sọ), dưới nhện và máu tụ ngoài màng cứng hay dưới màng cứng. Trên cùng một bệnh nhân có thể bị một hay nhiều vị trí.
Theo nguyên nhân, chia thành XHN tự phát và thứ phát. XHN thứ phát (chiếm 15-20% trong tổng số xuất huyết não) thường do chấn thương, dị dạng động tĩnh mạch (AVM), u não, thuốc và bệnh lý rối loạn đông máu (di truyền hay mắc phải). Nguy cơ tái phát sau XHN thứ phát có thể giảm sau khi điều chỉnh các yếu tố khởi phát. XHN tự phát (80 -85% trong tổng số XHN) chủ yếu liên quan với bệnh mạch máu nhỏ, do hậu quả của rối loạn toàn thân, chủ yếu do tăng huyết áp và bệnh mạch máu dạng tinh bột (Amyloid angiopathy).
Về hình ảnh thần kinh, XHN tự phát chia ra 2 loại: sâu (deep) và thùy (lobar). XHN “sâu” khi xảy ra xuất huyết ở hành não, thân não, đồi thị, bao trong, tiểu não hay thân não. Nguyên nhân là do thái hóa hyaline động mạch xiên trong não thường do hậu quả tăng huyết áp. XHN “thùy” khi tổn thương nằm ở vùng vỏ và vỏ – dưới vỏ, thùy trán, đỉnh, thái dương hay chầm. Máu tụ (hematoma) thùy thường xảy ra riêng lẻ hoặc có bệnh động mạch não thoái hóa dạng tinh bột gia đình (Familial cerebral amyloid angiopathy- CAA). Bệnh này do lắng động fibril dạng bột (Amyloid fibril) ở các động mạch vỏ từ nhỏ đến trung bình và động mạch màng nuôi. Tỉ lệ CAA tăng theo tuổi từ 2,3% bệnh nhân 65-74 tuổi đến hơn 12% ở người hơn 85 tuổi và còn cao hơn ở bệnh nhân Alzheimer. Nguy cơ tử vong và tái phát của xuất huyết “sâu” và “thùy” khác nhau. Xuất huyết “thùy” có biểu hiện lâm sàng nặng hơn, thể tích máu tụ nhiều hơn và lan rộng hơn so với xuất huyết “sâu”. Tỉ lệ tái phát xuất huyết thùy cũng cao hơn (15%/ 2 năm xuất huyết thùy so với 2% xuất huyết “sâu”/2 năm). Tỉ lệ tử vong xuất huyết “thùy” cũng cao hơn xuất huyết “sâu”. Uống kháng đông thường gây xuất huyết thùy nhiều hơn (hình 1).
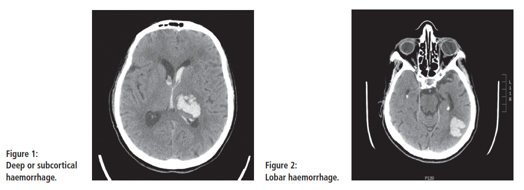
Hình 1.XHN sâu (trái) so với 2% tái xuất huyết /2 năm và XHN thùy (phải) với 15% tái XH/2 năm (1).
Phân loại SMASH-4 dựa trên SLB, nguyên nhân, kiểu tổn thương mạch máu, thuốc, bệnh động mạch thoái hóa tinh bột, bệnh hệ thống, tăng huyết áp, hay nguyên nhân không xác định được. Theo đó, XHN do bệnh động mạch thoái hóa dạng tinh bột và tăng huyết áp chiếm 20-30% (tương ứng), điều trị kháng đông chiếm 14%, tổn thương mạch não cấu trúc và bệnh toàn thân (xơ gan, giảm tiểu cầu vá các tình trạng hiếm khác) chiếm 5% mỗi loại và 21% không xác định được nguyên nhân. Bệnh nhân do tổn thương cấu trúc có máu tụ nhỏ nhất và tiên lượng tốt nhất (tử vong 3 tháng gần 4%) trong khi bệnh nhân xuất huyết não do kháng đông có xuất huyết lớn nhất và tiên lượng xấu nhất ( tử vong 3 tháng khoảng 54%).
II. 2. Nguy cơ bệnh nhân và yếu tố tái phát XHN (3,5-10):
Số liệu hiện nay về nguy cơ tái phát XHN còn hạn chế. Nguy cơ tái phát tăng ở nam, tăng huyết áp, mang van nhân tạo, đột quỵ trước đây, suy thận, ung thư và biến cố XHN tự phát. Tăng huyết áp không kiểm soát và điều trị kháng đông lại là yếu tố nguy cơ quan trọng nhất gây XHN tái phát (bảng 1).
Bảng 1. YTNC gây XHN khi sử dụng kháng đông (5)
|
YTNC chắc chắn BN cao tuổi (đặc biệt >75 tuổi) THA (HATT >160mmHg) Tiền sử bệnh mạch máu não Dùng kháng đông mạnh |
|
YTNC không chắc chắn Sử dụng Aspirin Bệnh mạch máu não thoái hóa dạng bột (amyloid) Chủng tộc: Châu Á hoặc người Mỹ gốc Mexico (Mexican-American) Hút thuốc lá Nghiện rượu nặng, K |
|
Hình ảnh học và dấu ấn di truyền Xơ cứng rải rác được xác chẩn bằng CT/MRI não Vi xuất huyết trên hình ảnh MRI Kiểu gen APOE epsilon II or IV |
Hiện có nhiều thang điểm để ước lượng nguy cơ chảy máu, nhưng không có một thang điểm nào tập trung vào riêng XHN và các kết quả cũng khác nhau về dự báo XHN. Trong 1 nghiên cứu XHN tự phát lần đầu, nguy cơ tái phát tăng theo thang điểm HASBLED (từ 1,37% bệnh nhân- năm với HASBLED một điểm tới 3 điểm, và 39% bệnh nhân/năm nếu HASBLED ≥3 điểm). Tuy nhiên điều trị lại với kháng vitamin K chỉ chiếm 2,5% bệnh nhân trong số này. Ngoài ra, bệnh nhân nguy cơ chảy máu liên quan với kháng vitamin K theo thang điểm HASBLED cũng có nguy cơ cao thuyên tắc huyết khối. Chính vì vậy cần cân nhắc kỹ để quyết định dùng lại kháng đông. Điều trị kháng đông ở bệnh nhân thuyên tắc tĩnh mạch, thang điểm RIETE dự đoán chảy máu tiêu hóa tốt hơn XHN.
Bệnh nhân mang van nhân tạo, tỉ lệ XHN liên quan kháng vitamin K khoảng 5% bệnh nhân- năm. Tỉ lệ tái phát còn chưa rõ số liệu.
II. 3. Dấu hiệu MRI và nguy cơXHN (5, 11-13):
MRI giúp xác định XHN vi thể(cerebral microbleeds)qua kỹ thuật gradient-Echo trên MRI. Tổn thương gồmlắng đọng hemosiderin và chứng tỏ hiện diện tổn thươngbệnh mạch máu nhỏ nặng do hậu quả củatăng huyết áp và CAA. Chảy máu vithểthường kết hợp tăng nguy cơ và tỉ lệ tái XHN (hình 2).
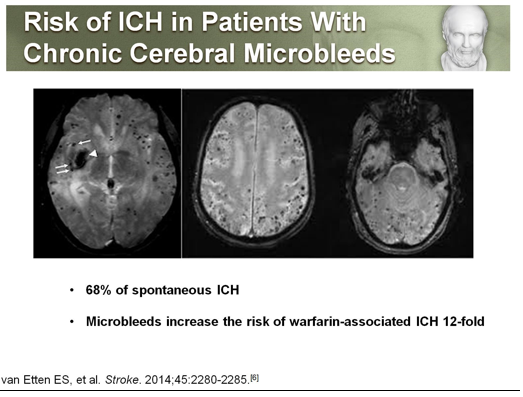
Hình 2. XHN vi thể mạn tính
MRI cũng có thể xác định tổn thương chất trắng(Leucoaraions) , chứng tỏ khả năng dấu hiệubịbệnh mạch máu nhỏ vàđược coi như là yếu tố nguy cơ độc lập cho XHN khi dùng kháng đông.
III. Nguy cơ huyết khối nếu không dùng kháng đông(1, 14-15):
Chỉ định dùng kháng đông trong lâm sàng gồm mang van nhân tạo (đặc biệt cơ học), rung nhĩ, huyết khối tĩnh mạch và thuyên tắc phổi, huyết khối trong buồng tim.
Nguy cơ biến chứng thuyên tắc huyết khối khi không dùng kháng đông khác nhau tùy theo tình trạng bệnh lýriêng biệt(Bảng 2).
Rung nhĩ là bệnh dùng kháng đông phổ biến nhất hiện nay. Rung nhĩ làm tăng nguy cơ đột quỵ tim mạch lên 5 lần nếu không điều trị. Theo mộtphân tích tổng hợp 29 thực nghiệm lâm sàng bệnh nhân rung nhĩ không do bệnh van tim, warfarin liều điều chỉnh làm giảm đột quỵ 64% so với không điều trị, trong khi thuốc chống tiểu cầu chỉ giảm được 22%. Các hướng dẫn điều trị hiện nay đều thống nhất điều trị kháng đông cho bệnh nhân rung nhĩ không do bệnh van tim với nguy cơ thuyên tắc huyết khối trung bình-cao (CHA2DS2 -VASc ≥1 điểm ở nam và ≥ 2 điểm ở nữ).
Nguy cơ VTE tái phát sau ngưng kháng đông phụ thuộc 3 yếu tố: vị trí huyết khối tĩnh mạch sâu (VTE) lúc chẩn đoán, thời gian điều trị kháng đông và còn yếu tố nguy cơ gây VTE hay không. Nguy cơ tái phát cao hơn nếu thời gian điều trị ngắn và có tình trạng ưahuyết khối (Thrombophilic conditions). Sau VTE có triệu chứng cơn đầu, nguy cơ thuyên tắc phổi tử vong ở bệnh nhân điều trị ít nhất 3 tháng với kháng vitamin K khoảng 0,19% – 0,49% bệnh nhân-nămvà tỉ lệ tử vong theo case (case fatility rate) khoảng 4-9%. Các yếu tố khác bao gồm tuổi cao, VTE vùng chân đùi.Ởbệnh nhân không dùng được kháng đông dự phòng, lưới lọc tĩnh mạch chỉ làm giảm được tỉ lệ thuyên tắc phổi, nhưng có thể làm tăng tỉ lệ DVT.
Ở bệnh nhân van cơ học, tỉ lệ biến chứng thuyên tắc khoảng 4% bệnh nhân-nămnếu không dùng kháng đông. Nguy cơ thuyên tắc huyết khối liên quan đến cả vị trí valve (2 lá hoặc động mạch chủ),loại van cũng như có rung nhĩ,tiền sử huyết khối van trước đây và các yếu tốnguy cơ đột quỵ khác hay không. Ngoài ra, thời gian sau mổ thay van cũng rất quan trọng, trong tháng đầu là nguy cơ cao nhất, đặc biệt là bệnh nhân thay van 2 lá cơ học.
Bảng 2:Nguy cơ ĐQ thiếu máu và hướng dẫn thời điểm chỉ định lại kháng đông sau xuất huyết não (XHN) (1)
|
Tình trạng lâm sàng |
Nguy cơ đột quị thiếu máu |
Kháng đông uống sau XHN |
Thời điểm bắt đầu |
|
Rung nhĩ |
0,8-20% (Bảng 2) |
Xem xét/nguy cơ thuyên tắc TB-cao |
>14 ngày sau XHN |
|
Bệnh cơ tim – Giảm CNTT không RN – Giảm CNTT kèm RN – Huyết khối TT
– Huyết khối nhĩ/tiểu nhĩ trái |
– 1,6-4%/năm – 2-18%/năm – 15%/3 tháng |
– Không – Tương tự BN rung nhĩ – Chỉ định sau XHN lần đầu or XHN với YTNC đã điều chỉnh được
– Xem xét đóng tiểu nhĩ |
– >14 ngày sau XHN – Sớm nhất có thể. Máu tụ ổn định trên CT não. Bắt đầu với liều thấp. – Sớm nhất có thể nếu không đóng tiểu nhĩ được. |
|
Bệnh van tim – Bệnh van 2 lá hậu thấp – Hai lá hậu thấp có RN – Hai lá hậu thấp có HK nhĩ trái hoặc thuyên tắc |
– 5%/năm – >5%/năm – #9% |
– Không – Dùng sau XHN lần đầu – Chỉ định sau XHN lần đầu |
– >14 ngày sau XHN – Sớm nhất có thể
|
|
Van tim nhân tạo – Van2lá/ĐMC sinh học Không rung nhĩ
Có rung nhĩ – Van hai lá cơ học – Van ĐMC cơ học – Van hai lá và ĐMC cơ học |
– 1-2%/0,4-1,9% (17%/3 tháng) – Giống rung nhĩ – 22%/năm – ≥12%/năm – 91% |
Không
– Giống rung nhĩ – Dùng sau XHN lần đầu – Dùng sau XHN lần đầu – Dùng sau XHN lần đầu |
/
– >14 ngày sau XHN – Sớm nhất có thể – Sớm nhất có thể – Sớm nhất có thể |
IV. Cân bằng lợi ích và nguy cơ(1, 3, 14, 15, 16):
Quyết định dùng lại kháng đông sau XHN sớmcầncân bằng lợi ích/nguy cơ trên mỗi bệnh nhân. Hiện chưa có nghiên cứu tiền cứu nào đánh giá lợi ích lâm sàng của dùng lại kháng đông sauXHN.
Một số nghiên cứu dùng lại kháng đông sau XHN tóm tắt ở bảng 3. Nhìn chung tỉ lệ dùng lại kháng đông là thấp (khoảng 19-35%, trung bình khoảng 24%). Thời gian dùng lại trung bình thay đổi từ 18-65 ngày, trung bình khoảng 31 ngày. Hầu hết bệnh nhân dùng lại là mang van cơ học (khoảng 68%) và rung nhĩ (10%). Đối tượng dùng lại thường trẻ hơn, XHN không nặng theo đánh giá lâm sàng (NIHSS vàthangđiểmxuất huyết não- ICH score) và đánh giá chức năng (mRS cải tiếntừ 0-3). Trong các nghiêncứu này, vị trí xuất huyết không ảnh hưởng đến quyết định dùng lại kháng đông. Trong năm theo dõi đầu tiên, nhóm bệnh nhân điều trị có tỉ lệ thiếu máu cục bộ thấphơn (5,2 so với 15% P<0,001) và tăng nguy cơ chảy máu không có ý nghĩa thông kê (8,1% so với 6,%, P=0,48). Sau 5 năm, nhóm dùng lại kháng đông giảm tỉ lệ tử vong (8,5% so với 18%, HR 0,56;95% CI 0,46 – 0,71),đột quỵ thiếu máu (3,5 so với 36% HR hiệu chỉnh 0,55;95% CI 0,37 – 0,81) và tái xuất huyết não không có ý nghĩa thống kê giữa 2 nhóm (3,6 so với 5,1%, HR 0,79;95% CI 0,59 – 1,19). Phân nhóm bệnh nhân rung nhĩ dùng lại kháng đông có tỉ lệ biến cố thiếu máu cục bộ thấp hơn và tăng không có ý nghĩa biến chứng chảy máu so với bệnh nhân rung nhĩ không dùng lại kháng đông.
Bảng 3:Các nghiên cứu sử dụng kháng đông sau XHN liên quan kháng đông (1)
|
Nghiên cứu |
Cỡ mẫu |
% BN dùng lại |
Nguy cơ XHN tái phát/1 năm |
Nguy cơ TEE/1 năm |
Tử suất/1 năm |
|
Nielsen PB et al. (2015) |
1752NVAF |
621(35,4) |
8,0% vs 8,6% |
5,3% vs 10,4% |
9,7% vs 19,1% |
|
Kuramatsu et al. (2015) |
566AF |
110(19,4) |
3,9% vs 3,9% |
5,5% vs 14,9% |
8,2% vs 37,1% |
|
Witt DM et al. (2015) |
160 |
54(33,8) |
3,7% vs 7,6% |
0% vs 1,9% |
18,5%vs 31,1% |
|
Yung D et al. (2012) |
284 |
91(32) |
<2% vs 0% |
Không báo cáo |
48% vs 61% |
|
Poly D et al. (2014) |
267 |
267 |
2,6% |
1,9% |
5,6% |
V. Chiến lượcdùng lại kháng đông sauXHN:
V.1. Đánh giá nguy cơchảy máu lại khi dùng kháng đông:
Nguy cơ này có thể dự đoán dựa trên loại XHN, nguy cơ của bệnh nhân cũng như hình ảnh đặc biệt của MRI (phần trên).Ở BN XHN thùy hay bệnh MM não tích tụ amyloid, nguy cơ XHN liên quan kháng đông cao hơn biến cố huyết khối thuyên tắc, vì vậy nên thận trọng khi dùng lại kháng đông ở nhóm bệnh nhân này (1,3).
V.2. Đánh giá tình trạng bệnh phải dùng kháng đông:
Tùy theo tình trạng bệnh lý, việc dùng lại kháng đông sẽ khác nhau vì nguy cơ /lợi ích của các bệnh lý nay khác nhau. Hướng dẫn dùng kháng đôngsau XHN tóm tắt ở hình 3.
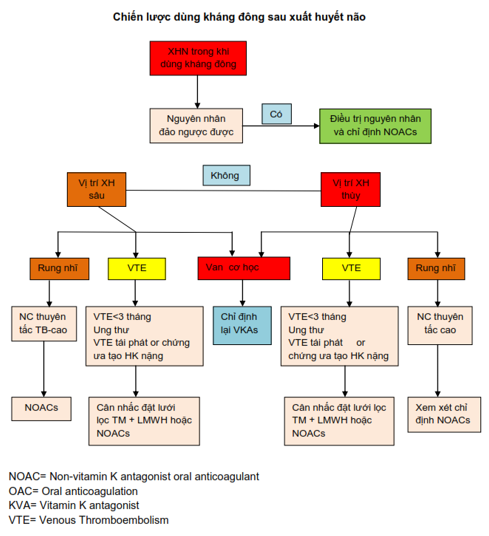
Hình 3. Chiến lược dùng KĐ sau XHN (1)
Nhóm bệnh nhân nên dùng lại kháng đông (16-20):
– XH khi đang sử dụng KVA hoặc quá liều kháng đông
– Do chấn thương hoặc nguyên nhân điều trị được
– Bệnh nhân trẻ tuổi
– Kiểm soát HA tốt
– XH nhân nền
– Không hoặc tổn thương nhẹ chất trắng ở não
– Đã phẫu thuật lấy khối máu tụ
– Đã can thiệp dị dạng mạch máu
– Nguy cơ đột qụi cao
Nhóm bệnh nhân không nên dùng kháng đông (16-20):
– XH trong khi uống kháng đông chưa đạt liều điều trị
– Đang sử dụng NOAC hoặc gián đoạn hay không đủ liều kháng đông
– Bệnh nhân cao tuổi
– Không kiểm soát tốt HA
– XH vùng vỏ não
– XHN nghiêm trọng
– Nhiều ổ vi xuất huyết
– Không điều trị được nguyên nhân xuất huyết
– Nghiện rượu
– Bắt buộc kháng KTTC kép sau PCI
V.2.1.Van nhân tạo (1,3, 17, 21-23) :
– Bắt buộc phải dùng lại kháng đông bất chấp nguy cơ chảy máu lại (hình 4, bảng 4)
– Đề nghị kháng đông khác nhau tùy theo loại van, có hay không yếu tố hình thànhcục máu đông (rung nhĩ, huyết khối trước đây…) và vị trí của van (2 lá, đông mạch chủ).
– Bệnh nhân mang van cơ học, động mạch chủ On-x (bileaflet) và không có yếu tố nguy cơ thuyên tắc huyết khối, dùng kháng vitamin K đạt INR# 2 – 3 trong 3 tháng đầu sau phẫu thuật, sau 3 tháng mục tiêu INR # 1,5 – 2.
– Bệnh nhân van 2 lá khác không phải On-x hay van động mạch chỉ cơ học dạng đỉa nghiêng đơn thế hệ gần đây và không có yếu tố nguy cơ thuyên tắc huyết khối, dùng kháng vitamin K INR # 2,5.
– Bệnh nhân mang van động mạch chủ cơ học (không phải On-x) và có yếu tố nguy cơ thuyên tắc huyết khối (rung nhĩ, tiền sử thuyên tắc, huyết khối trước đây, suy chức năng tâm thu thất trái, tình trạng tăng đông…) hay van động mạch chủ cơ học thế hệ cũ (van ball-in-cage) đề nghị dùng kháng vitamin K INR # 3.
– Bệnh nhân thay van 2 lá cơ học (kể cả van On-x) đề nghị dùng kháng vitamin K với INR # 3.
– Bệnh nhân mang van 3 lá cơ học, đề nghị dùng kháng vitamin K đạt INR #3
– Van sinh học: Đề nghị 3 tháng đầu dùng kháng đông, sau đó dùng ASA dài hạn
V.2.2. Rung nhĩ:
– Bệnh nhân rung nhĩ có chỉ định dùng kháng đông tùy theo nguy cơ thuyên tắc huyết khối (điểm CHA2DS2 – VASc) (hình 5).
– Ở bệnh nhân rung nhĩ không do bệnh van tim và tiền căn XHN, các nghiên cứu cho thấy kháng vitamin K không có lợi ở bệnh nhân sau XHN đặc biệt là XHN thùy. Không nên dùng kháng huyết khối ở bệnh nhân rung nhĩ sống sót sau XHN thùy tự phát nhưng có thể dùng sau XHN sâu vẫn còn các yếu tố nguy cơ thuyên tắc huyết khối. BN XHN sâu một bên bán cầu và nguy cơ ban đầu của đột quỵ thiếu máu > 6.5%/năm, tương ứng với CHADS2 ≥ 4 hay CHA2DS2-VASc ≥ 5, có thể có lợi khi dùng lại kháng đông. Nên dùng NOAC vì ít nguy cơ XHN hơn (17,19,20).
– Những bệnh nhân không thể dùng lại kháng đông, biện pháp thay thế là thắt tiểu nhĩ trái (24-26).
V.2.3. VTE:
– Nếu bị XHN khi đangdùng kháng đông để dự phòng tái phát VTE, có thể ngưng nếuđã điều trịđủ 3 tháng và hết yếu tố nguy cơgây VTE. Nếu bệnh nhân bị VTE tự phát và nguy cơ gây VTE còn dài hạn hoặc chưa uống đủ 3 tháng từ khi bị XHN, quan tâm dùng liều kháng đông dự phòngvà có thểkết hợp với lưới lọc tĩnh mạch(3, 27,28).
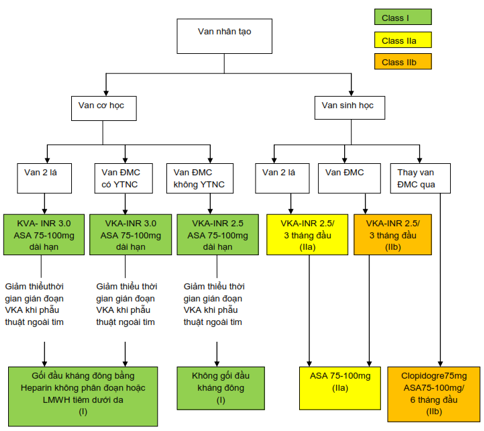
Hình 4.Chiến lược dùng kháng đông trong van nhân tạo (23).
Bảng 4.
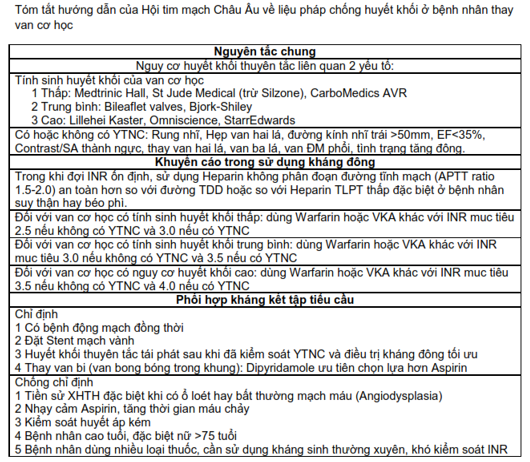
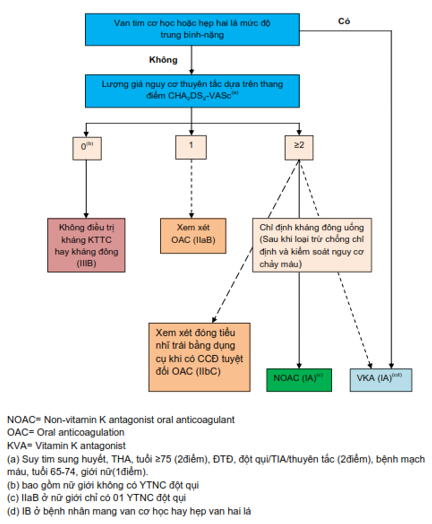
Hình 5. Hướng dẫn dùng KĐ trong rung nhĩ (17)
V.3. Chiến lược dùng thuốc:
Dùng kháng vitamin K: dùng lại liều như các khuyến cáo, không khuyến khích dùng liều thấp hơn vì sẽ tăng nguy cơ biến cố thiếu máu cục bộ. Nếu bệnh nhân nguy cơ XHN cao và không có chống chỉ định dùng NOAC, nên chuyển sang dùng NOAC(1, 17).
Dùng NOAC: Các thuốc NOAC ức chế trực tiếp yếu tố IIa (Dabigatran) hay Xa (Rivaroxa ban, apixaban và epixaban), là một biện pháp điều trị lựa chọn cho bệnh nhân XHN liên quan với kháng đông kháng vitamin K. NOAC đã được nghiên cứu và đưa vào thực hành lâm sàng để dự phòng thuyên tắc huyết khối ở bệnh nhân rung nhĩ không do bệnh van tim và điều trị VTE, PE. Ở bệnh nhân rung nhĩ không do bệnh van tim, NOAC làm giảm nguy cơ XHN > 50% so với kháng vitamin K (bảng 5). Cơ chế giảm XHN của NOAC có thể do hoạt tính sinh học của thuốc chỉ tác động lên khâu cuối cùng của quá trình đông máu, giảm thâm nhập qua hàng rào máu não và có thể với cơ chế phụ thuộc yếu tố tổ chức (29, 30,).
Dựa trên kết quả này, hướng dẫn hiện nay đề nghị nên dùng NOAC cho bệnh nhân bị XHN liên quan kháng đông kháng vitaminn K ở bệnh nhân rung nhĩ không do bệnh van tim hay VTE/PE nếu không có chống chỉ định (17,20,28).
Lưu ý:không dùng NOAC cho bệnh nhân van cơ học và các chống chỉ định của thuốc (suy thận…)
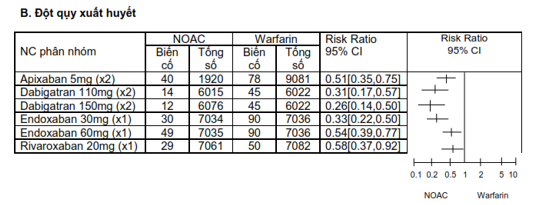
Bảng 5.So sánh biến cố XHN giũa NOAC và kháng vitamim K (29)
V.4. Thời gian tối ưu dùng lại KĐ (hình 6) (1,17, 28, 31):
Nguy cơ lan rộng máu tụ cao nhiều trong những giờ đầu và vài ngày sau xuất huyết não, trong khi yếu tố thuyên tắc huyết khối và xuất huyết não tăng dần theo thời gian. Dùng càng sớm kháng đông nguy cơ tái phát XH càng cao. Nhìn chung, khi dùng lại kháng đông nguy cơ tái phát XHN tăng lên 5 lần và làm giảm 90% nguy cơ thiếu máu cục bộ.
Thời gian đề nghị là rất khác nhau từ 2 – 10 tuần.Một số đề nghị dùng sớm hơn (dưới 7 ngày) hoặc muộn hơn (hơn 10 tuần). Điều này tùy thuộc vào từng bệnh lý cụ thể và nguy cơ mỗi người bệnh dựa trên kích thước và vị trí hấp thụ, và yếu tố nguy cơ lan rộng máu tụ, nguy cơ thuyên tắc và hậu quả của nó…
Theo các hướng dẫn hiện nay, cũng như quan điểm của chúng tôi, hạn chế dùng trước 2 tuần (trừ trường hợp van cơ học), thường là sau 4 tuần nếu xuất huyết não đã cầm hay ở bệnh nhân xuất huyết não nhỏ và nguy cơ thuyên tắc huyết khối cao, dùng lại sau 8 – 10 tuần hay muộn hơn ở bệnh nhân xuất huyết não vùng thân não, tiểu não hay xuất huyết não lớn
Nếu phải dùng dưới 7 ngày, nên chuyển sang chiến lược bắc cầu bằng Heparin, sau đó mới chuyển sang dùng kháng đông uống.
Lưu ý: các biện pháp tránh XHN khi dùng KĐ (bảng 6).

Bảng 6.Các biện pháp giảm tai biến XHN khi dùng KĐ (3)
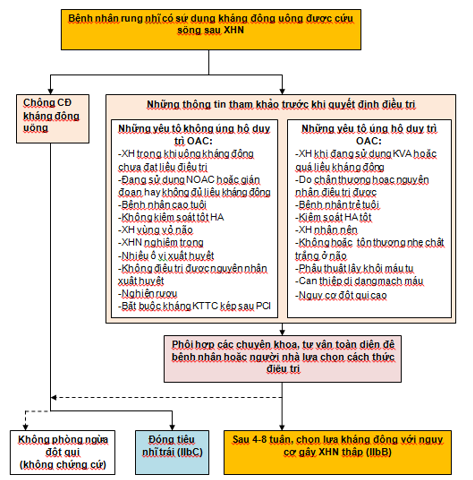
Hình 6.Tóm tắt chiến lược lại và thời gian tối ưu dùng KĐ sau XHN (17)
VI. Kết luận:
– XHN là một biến chứng khiến cả bệnh nhân và thầy thuốc cùng lo lắng.
– Cần cân nhắc giữa lợi ích và nguy cơ khi quyết định dùng lại kháng đông sau XHN.
– Các yếu tố cần tính toán khi quyết định dùng lại là: loại XHN, nguy cơ của bệnh nhân cũng như hình ảnh đặc biệt trên MRI.
– Những bệnh nhân nguy cơ thuyên tắc huyết khối cao cần dùng lại là bệnh nhân mang van cơ học, rung nhĩ không do bệnh van tim với thang điểm đột quỵ cao (CHA2DS2-VASc ≥ 5).
– Khi dùng lại: chọn thời điểm, thuốc kháng đông và liều lượng phù hợp. Ưu tiên dùng NOAC cho bệnh nhân rung nhĩ không do bệnh van tim. Không nên phối hợp thêm với kháng tiểu cầu.
– Cần có sự thống nhất giữa bác sĩ Tim mạch và Đột quỵ
Tài liệu tham khảo
1. Becattini. C , Sembolini. A, Paciaron. M: Resuming anticoagulant therapy after intracerebral bleeding. Vascular Pharmacology 84 (2016): 15–24.
2. Claassen. DO et al: Restarting Anticoagulation Therapy After Warfarin-Associated Intracerebral Hemorrhage. Arch Neurol. 2008;65 (10):1313-1318.
3. Wijdicks. EFM: The use of antithrombotic therapy in patients with an acute or prior intracerebral hemorrhage. Uptodate 2016.
4. Punthakee. X, Doobay. J, Anand. SS: Oral-anticoagulant-related intracerebral hemorrhage. Thrombosis Research 108 (2003) 31– 36.
5. Freeman. WD et al: Risk of intracerebral bleeding in patients treated with anticoagulants. Uptodate 2016.
6. Zia. E: Three-Year Survival and Stroke Recurrence Rates in Patients With Primary Intracerebral Hemorrhage. Stroke. 2009;40:3567-3573.
7. Passero. S: Recurrence of Bleeding in Patients With Primary Intracerebral Hemorrhage . From the Istituto di Clinica delle Malattie Nervose e Mentali, Universita di Siena (Italy). 1995.
8. Butler and. AC & Tait. RC: Restarting anticoagulation in prosthetic heart valve patients after intracranial haemorrhage: a 2-year follow-up. British Journal of Haematology, 1998; 103: 1064–1066.
9. Bejot.Y et al: Intracerebral haemorrhage profiles are changing: results from the Dijon population-based study. Brain 2013: 136; 658–664.
10. S. De Vleeschouwer: Risk Analysis of Thrombo-Embolic and Recurrent Bleeding Events in the Management Of Intracranial Haemorrhage Due to Oral Anticoagulation. Acta chir belg, 2005; 105: 268-274.
11. Lim. JS: Cerebral Microbleeds and Early Recurrent Stroke After Transient Ischemic Attack: Results From the Korean Transient Ischemic Attack Expression Registry. JAMA Neurol. 2015;72(3):301-308.
12. Imaizum. Ti et al: Antithrombotic Drug Uses and Deep Intracerebral Hemorrhages in Stroke Patients With Deep Cerebral Microbleeds. Journal of Stroke and Cerebrovascular Diseases, Vol. 22, No. 6 (August), 2013: pp 869-875.
13. Wang. Z et al: Cerebral Microbleeds:Is Antithrombotic Therapy Safe to Administer? Stroke. 2014;45:2811-2817.
14. Eckman. MH et al: Can Patients Be Anticoagulated After Intracerebral Hemorrhage? A Decision Analysis. Stroke. 2003;34:1710-1716.
15. Phan.TG: safety of discontinuation of anticoagulation in patients with ICH at high thromboembolic risk. Arch Neuro 2000; 57: 1710-1713.
16. Paciaroni. M al: Should oral anticoagulants be restarted after warfarin-associated cerebral haemorrhage in patients with atrial fibrillation? Thromb Haemost 2014; 111: 14–18.
17. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS
18. Poli. P et al: Recurrence of ICH after resumption of anticoagulation with VK antagonists CHIRONE Study. Neurology® 2014;82:1–7.
19. Nielsen. PB et al: Restarting Anticoagulant Treatment After Intracranial Hemorrhage in Patients With Atrial Fibrillation and the Impact on Recurrent Stroke, Mortality, and Bleeding A Nationwide Cohort Study. Circulation. 2015;132:517-525.
20. Kovacs. RJ: Practical Management of Anticoagulation in Patients With Atrial Fibrillation. J Am Coll Cardiol 2015;65:1340–60.
21. Romualdi. E et al: Oral anticoagulant therapy in patients with mechanical heart valve and intracranial haemorrhage: A systematic review. Thromb Haemost 2009; 101: 290–297.
22. Gerard P Aurigemma, et al: Antithrombotic therapy for prosthetic heart valves: Indications. Uptodate 2016.
23. 2014 AHA/ACC Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines
24. Horstmann. S et al: Left atrial appendage occlusion in atrial fibrillation after intracranial hemorrhage. Neurology® 2014;82:135–138.
25. Holmes. DR et al: Prospective Randomized Evaluation of the Watchman Left Atrial Appendage Closure Device in Patients With Atrial Fibrillation Versus Long-Term Warfarin Therapy: The PREVAIL Trial. J Am Coll Cardiol 2014;64:1–12.
26. Redd. VY et al: Percutaneous Left Atrial Appendage Closure vsWarfarin for Atrial Fibrillation A Randomized Clinical Trial. JAMA. 2014;312(19):1988-1998.
27. PaciaronI. AM: Efficacy and safety of anticoagulants in the prevention of venous thromboembolism in patients with acute cerebral hemorrhage: a meta-analysis of controlled studies. Journal of Thrombosis and Haemostasis, 2009: 893–898.
28. Guidelines for the Management of Spontaneous Intracerebral Hemorrhage. Stroke 2015
29. Chatterjee. S et al: New Oral Anticoagulants and the Risk of Intracranial Hemorrhage Traditional and Bayesian Meta-analysis and Mixed Treatment Comparison of Randomized Trials of New Oral Anticoagulants in Atrial Fibrillation. JAMA Neurol. 2013;70(12):1486-1490.
30. Hagii. J et al: Characteristics of Intracerebral Hemorrhage During Rivaroxaban Treatment Comparison With Those During Warfarin. Stroke. 2014;45:2805-2807.
31. Majeed. A et al: Optimal Timing of Resumption of Warfarin After Intracranial Hemorrhage. Stroke. 2010;41:2860-2866.







