TS. BS. NGUYỄN THỊ MỸ HẠNH
ThS. BS. NGUYỄN THỊ NGỌC HÂN
BV Đa khoa Tâm Anh
I. MỞ ĐẦU:
Siêu âm tim là kỹ thuật hình ảnh hàng đầu cho bệnh van tim trong phần lớn các trường hợp, tuy nhiên trong một số trường hợp, hình ảnh cộng hưởng từ tim (Cardiac Magnetic Resonance imaging – CMR) có thể cung cấp thêm thông tin, thậm chí là những thông tin vượt trội siêu âm tim, đặc biệt trong sang thương hở van. Không bị giới hạn mặt phẳng khảo sát, CMR cho hình ảnh các van và các buồng thoát rõ ràng, kể cả những trường hợp khó (như biến dạng lồng ngực, béo phì) hay những ca giải phẫu hoặc vị trí tim bất thường (sau phẫu thuật tim, bệnh tim bẩm sinh), hoặc khi cần xác định chính xác vị trí dòng chảy bị hạn chế ở buồng thoát. Chất lượng hình ảnh tốt kết hợp với kỹ thuật bản đồ tương phản của dòng máu theo pha (phase contrast flow mapping) cho phép định lượng lưu lượng và tốc độ dòng máu, giúp đánh giá định lượng mức độ hẹp và hở van, cũng như đánh giá hậu quả của rối loạn chức năng van thông qua định lượng chính xác thể tích, khối cơ và chức năng thất tương ứng. Hình ảnh xơ sẹo cơ tim trên hình LGE và T1 mapping bổ sung thêm thông tin về đặc tính mô cơ tim. Cuối cùng, với kỹ thuật phim (hình cine) và hình ảnh mạch máu 3 chiều (3D angiography), CMR cho hình ảnh rất tốt về giải phẫu của các mạch máu lớn, có thể cần thiết cho xác định nguyên nhân của rối loạn chức năng van, các bệnh lý kết hợp của mạch máu lớn như dãn, hẹp eo động mạch (ĐM) chủ, tiên lượng nguy cơ cũng như lập kế hoạch phẫu thuật.
Những ưu thế này của CMR cần được khai thác trong đánh giá bệnh van tim, hơn là lặp lại siêu âm tim hoặc chụp cắt lớp vi tính đa dãy đầu dò (Multidetector computed tomography – MDCT) cho bệnh nhân. Đồng thời, cần hiểu những hạn chế của CMR để chọn các chuỗi xung một cách khôn khéo, phân tích cẩn thận để có được thông tin chính xác.
Trong bài tổng quan này, chúng tôi dùng nguồn tài liệu chính cập nhật của Hội Hình ảnh Tim mạch Châu Âu, cho thấy cách đánh giá cũng như cách phân mức độ nặng của các bệnh lý van tim, ưu nhược điểm của kỹ thuật này trong bệnh lý van tim. Đồng thời, chúng tôi cũng trình bày vị trí của CMR theo các khuyến cáo của các Hiệp hội tim mạch hiện nay trong bệnh van tim.
II. QUY TRÌNH CHỤP CMR:
Bề dày lát cắt 4 – 5 mm.
Chủ yếu dùng chuỗi xung SSFP và phase contrast trong bệnh lý van tim.
Chuỗi xung SSFP khảo sát hình cine (hình 1): cine trục ngắn đánh giá thể tích và chức năng 2 thất. Cine trục dọc và trục ngắn qua đỉnh van để thấy rõ van ĐM chủ, van hai lá và van ba lá. Van ĐM chủ khảo sát thêm cine buồng tống thất trái, van ĐM phổi khảo sát thêm cine buồng tống thất phải.
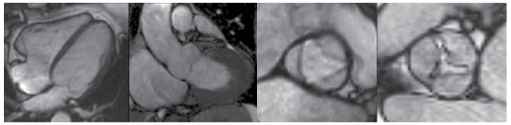
Hình 1. Cine 4 buồng đánh giá van hai lá, cine mặt phẳng đứng ngang buồng tống thất trái đánh giá van ĐM chủ (2 hình bên trái), mặt cắt trục ngắn qua van ĐMC thì tâm thu trường hợp van ĐM chủ bình thường và hẹp ĐM chủ (2 hình bên phải).
Phase contrast: đo vận tốc dòng máu qua van, lưu lượng hở van. Mặt phẳng khảo sát thường đặt ngay dưới van (hình 2).
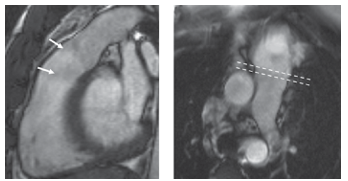
Hình 2. Cine buồng tống thất phải và vị trí mặt phẳng khảo sát phase contrast dưới van ĐM phổi [5].
III. ĐẶC ĐIỂM CMR TRONG BỆNH VAN TIM:
1. Đánh giá hẹp van:
CMR có thể đánh giá chính xác mức độ hẹp van ĐM chủ và van ĐM phổi. Hình cine các mặt phẳng qua buồng tống thất trái, buồng tống thất phải và các mặt phẳng vuông góc với buồng tống giúp đánh giá định tính tốt tình trạng hẹp van (hình 3, 4), đồng thời có thể xác định được hẹp dưới và trên van.
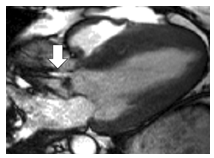
Hình 3. Hình cine chuỗi xung SSFP 3 buồng thì tâm thu trên bệnh nhân hẹp van ĐM chủ nặng. Hạn chế mở van, dòng phụt (jet) qua van hẹp thì tâm thu vận tốc cao với dòng chảy lớp (lamina) trung tâm có màu trắng (mũi tên) và dòng chảy rối (turbulent) xung quanh vùng trung tâm có màu đen [5].
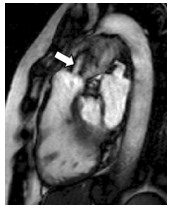
Hình 4. Hình cine SSFP buồng tống thất phải thì tâm thu: dòng phụt tốc độ cao qua van ĐM phổi [5].
- Đánh giá định lượng diện tích mở van: cine SSFP mặt phẳng ngang qua đỉnh (tip) của lỗ van là tối ưu để đo diện tích mở van. Có thể cắt nhiều lát mỏng song song để xác định lát tối ưu (hình 5)
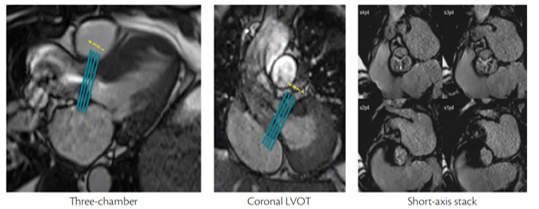
Hình 5. Định vị chuỗi các lát cine dựa trên 2 mặt phẳng vuông góc khảo sát van ĐM chủ để xác định mặt phẳng tối ưu đi qua đỉnh van đo diện tích mở van (giữa tâm thu) [5].
- Xác định vận tốc tối đa qua van bằng bản đồ vận tốc phase contrast: mặt phẳng phase contrast trên van tối ưu song song với tip van, ngang mức vena contracta (hình 6).
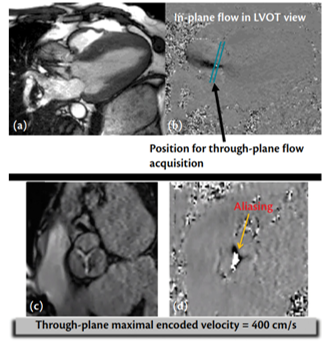
Hình 6. Phase contrast 2 chiều đo vận tốc tối đa qua van ĐM chủ. Mặt phẳng in-plane phase contrast 3 buồng (nín thở) được thực hiện trước, với nhiễu do dòng rối (flow turbulence) thấy ở vùng vena contracta (a) và (b). (c) và (d): mặt phẳng phase contrast trực tuyến ở vị trí trước nhiễu (prior aliasing) và nhiễu (continued aliasing) với VENC 400 cm/s, chứng tỏ hẹp van ĐM chủ nặng với vận tốc tối đa qua van ĐM chủ > 4 m/s [5].
Phase contrast có thể kém chính xác khi vận tốc tối đa dòng máu qua van ĐMC > 3.5–4 m/s do hiệu ứng thể tích phần (partial volume effects) với dòng xịt (flow jet) rất hẹp gây mất tín hiệu do dòng rối và lỗi thay đổi pha (phase shift errors) do sự tăng tốc nhanh của dòng máu và mất pha trong voxel (intravoxel dephasing). Do đó, phương pháp đo diện tích mở van trực tiếp là phương pháp đáng tin cậy nhất. Trên siêu âm, đánh giá vận tốc hữu ích trong hẹp van ĐM chủ và van ĐM phổi do khó đo diện tích mở van trực tiếp. CMR đo diện tích mở van trực tiếp đáng tin cậy, với diện tích thường lớn hơn so với phương pháp gián tiếp qua đo vận tốc.
- Đánh giá hậu quả của hẹp van ĐM chủ: tình trạng phì đại và chức năng thất trái. Đánh giá xơ hoá thất trái trên hình bắt thuốc thì muộn (Late gadolinium enhancement – LGE) xơ hoá kiểu đốm (patchy) gặp trong khoảng 1/3 các trường hợp hẹp van ĐM chủ nặng có phì đại thất trái. Có hai nghiên cứu cho thấy mối quan hệ của xơ hoá cơ tim với tiên lượng xấu hơn [1,2]. Một thử nghiệm lâm sàng đang được tiến hành để xác định xơ hoá cơ tim có phải là yếu tố nguy cơ cao để xác định các bệnh nhân hẹp van ĐM chủ không triệu chứng có thể có lợi với điều trị thay thế van sớm [3].
- Phân mức độ hẹp van ĐM chủ dựa vào phân độ trên siêu âm. Dữ liệu trên các thông số của CMR liên quan đến kết cục khá hạn chế. Mối liên quan giữa khối cơ thất trái và kết cục có kết quả không đồng nhất giữa các nghiên cứu. Tình trạng xơ hoá thất trái khu trú trên LGE có liên quan đến việc cần phải phẫu thuật trong tương lai. T1 mapping đánh giá tình trạng xơ hoá lan toả có triển vọng ứng dụng trong tương lai, với kết quả của một nghiên cứu cho thấy thời gian thư giãn cơ tim T1 cao hơn ở nhóm bệnh nhân có triệu chứng, tuy nhiên giá trị T1 bị chồng chéo giữa nhóm hẹp van trung bình và nặng.
- Hẹp van hai lá và van ba lá có thể đánh giá trên CMR, đo diện tích mở van 2D trực tiếp trên hình cine SSFP, mặt phẳng trục ngắn trực tuyến với đỉnh van thì tâm trương. Nên cắt nhiều lát mỏng song song để xác định mặt phẳng tối ưu đo diện tích mở van do cả lá van và vòng van đều di động nhiều (hình 7).
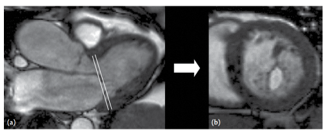
Hình 7. Đánh giá hẹp van hai lá. Đặt các lát trực tuyến với đỉnh van hai lá (a) trong thì tâm trương. Diện tích mở van đo được dễ dàng trên trục ngắn (b) [5].
2. Đánh giá hở van:
Đánh giá định tính trên hình cine SSFP: lát dọc (hình 8) đánh giá hở van ĐM chủ và van ĐM phổi. Van hai lá và van ba lá cần thêm nhiều lát tương ứng với các phần của van (hình 9).
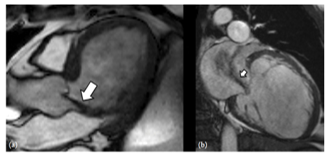
Hình 8. (a) Hình cine SSFP 3 buồng thì tâm trương cho thấy dòng hở van ĐM chủ lệch tâm (mũi tên). (b) SSFP 2 buồng thì tâm thu trường hợp hở van hai lá thứ phát trong bệnh cơ tim thiếu máu cục bộ [5].
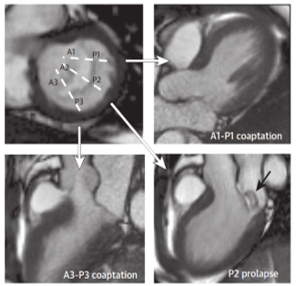
Hình 9. Mặt phẳng trục ngắn qua mép van hai lá được dùng để định vị các mặt cắt trực tuyến với mép van để đánh giá phần (scallops) bị sa của các lá van trước và sau [4].
Các lát mỏng trực tuyến với các phần của van cần thiết để quan sát cấu trúc giải phẫu và chức năng của tất cả các van. Hở van hai lá dòng hở lệch tâm, nhiều lát song song (stack) 3 buồng giúp xác định cơ chế hở van và các cấu trúc giải phẫu liên quan, đồng thời đánh giá mức độ hở van. Dấu hiệu vận động ra trước thì tâm thu (Systolic Anterior Motion – SAM) trong bệnh cơ tim phì đại cũng dùng mặt cắt này (hình 10).
Có thể thấy và đo được lỗ dòng hở van (hình 11). Dòng hở biểu hiện trên hình SSFP bằng hình ảnh mất tín hiệu do dòng rối (turbulent flow), nhưng nếu dòng hở rộng và chảy thành lớp (laminar), đặc biệt đối với hở van ĐM phổi, dấu mất tín hiệu có thể ít, dễ sót hở van nặng. Bản đồ dòng in-plane (in-plane flow mapping) có thể hữu ích trong trường hợp này.
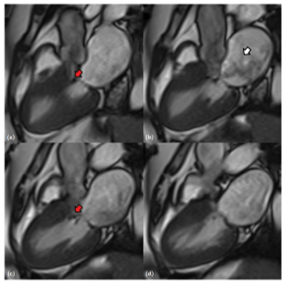
Hình 10. Hình stack cine SSFP 3 buồng – gồm 4 mặt cắt song song từ (a) đến (d), cho thấy dấu SAM của lá trước van hai lá (mũi tên đỏ hình a và c) và dòng hở van hai lá hướng về phía lá sau (mũi tên trắng hình b) [5].
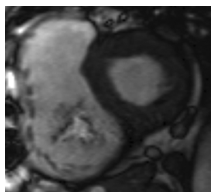
Hình 11. Hở van ba lá: hình cine SSFP trực tuyến với đỉnh van thì tâm thu: Lỗ hở van do các lá van áp không sát [5].
- Định lượng hở van: là ưu thế của CMR, xác định được thể tích dòng hở (regurgitant volume), phân suất dòng hở (regurgitant fraction), thể tích thất trái và thất phải cho thấy đáp ứng của thất với tổn thương van. Đánh giá chức năng và cấu trúc thành thất bao gồm cả vị trí cơ trụ tiếp nối vào thành thất có thể là chìa khoá cho xác định cơ chế hở van hai lá thứ phát. LGE xác định vùng nhồi máu có thể hữu ích trong hở van hai lá thứ phát
- Định lượng hở van ĐM chủ và van ĐM phổi được bằng phase contrast đặt ngay phía trên van (hình 12): đo được thể tích dòng tới (forward) dòng trào ngược (regurgitant) và phân suất dòng hở (regurgitant fraction = (regurgitant volume/forward volume × 100%).
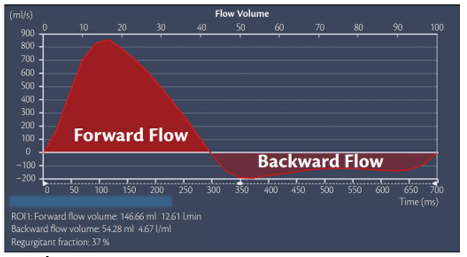
Hình 12. Biểu đồ thể tích dòng máu qua van ĐM chủ trên một bệnh nhân hở van ĐM chủ nặng mạn tính. Vùng nằm dưới trục X đại diện cho thể tích trào ngược của hở van ĐM chủ (dòng dội ngược toàn tâm trương – holodiastolic backward flow) [5].
- Định lượng hở van hai lá và van ba lá thường tính bằng phương pháp gián tiếp (hình 13): là hiệu số của thể tích 1 nhát bóp của thất trái / thất phải bằng phương pháp thể tích (volumetric) với thể tích 1 nhát bóp bằng phương pháp phase contrast qua ĐM chủ / ĐM phổi. Phương pháp đo trực tiếp bằng lưu lượng máu qua van kém chính xác do van hai lá và ba lá di động nhiều và nhiễu do dòng rối.
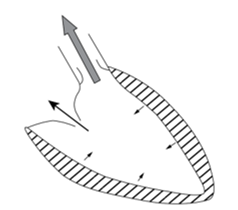
Hình 13. Định lượng hở van hai lá bằng phương pháp gián tiếp trên CMR. Trong thời kỳ tâm thu, thể tích một nhát bóp của thất trái đi vào ĐM chủ (mũi tên xám lớn) hoặc đi qua van hai lá do hở van (mũi tên đen nhỏ). Thể tích dòng hở là hiệu số của thể tích 1 nhát bóp của thất trái bằng phương pháp thể tích (volumetric) với thể tích 1 nhát bóp bằng phương pháp phase contrast qua ĐM chủ [5].
- Định lượng hở van ĐM chủ có thể không chính xác do các lỗi bù pha nền (background phase offset errors) hoặc đánh giá thấp hở van ĐM chủ do chuyển động của vòng van (hình 14) hoặc do vẽ đường để đo thể tích không chính xác. Các lưu ý khi đo thể tích bằng phase contrast: chọn VENC đúng, định vị mặt phẳng phase contrast ở vùng đẳng từ, hiệu chỉnh nền khi cần thiết để làm giảm tối đa lỗi bù lưu lượng (flow offset errors), đo thể tích thất trái / thất phải cẩn thận để có được các số liệu đúng về thể tích.
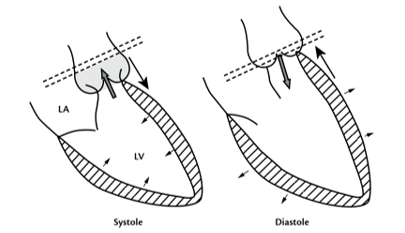
Hình 14. Cơ chế đánh giá thấp hở van ĐM chủ. Khoảng cách giữa van và mặt phẳng đánh giá phase contrast mở rộng ra do: 1/chuyển động của van ĐM chủ về phía mỏm; 2/ xoang và gốc ĐM chủ dãn do đàn hồi. Lượng máu vào khoang này thì tâm thu (vùng xám) trở về thất trái thì tâm trương do hở van ĐM chủ mà không mà không đi qua mặt phẳng đánh giá phase contrast và có thể không được tính. Các yếu tố làm gia tăng khoảng cách thể tích bao gồm: 1/ Tăng khoảng cách giữa van và mặt phẳng khảo sát lưu lượng; 2/ Co thắt mạnh theo trục dọc của thất trái (thường gặp trong hở van ĐM chủ nặng); 3/ Dãn xoang vành (là nguyên nhân thường gặp trong hở van ĐM chủ). Những yếu tố làm giảm bớt khoảng cách thể tích bao gồm: 1/ Vị trí mặt phẳng khảo sát lưu lượng gần van nhất có thể; 2/ Mặt phẳng khảo sát lưu lượng di chuyển cùng chuyển động của vòng van – ‘slice tracking’ – chỉ có ở một số hãng máy [5].
- Mặc dù có những hạn chế, các số liệu nghiên cứu của Myerson và cộng sự cho thấy phương pháp đo thể tích và phân suất dòng hở van và đo thể tích thất trái cuối tâm trương có giá trị cao trong tiên lượng xuất hiện triệu chứng và cần phải phẫu thuật trong tương lai ở nhóm bệnh nhân hở van hai lá và van ĐM chủ không triệu chứng theo dõi trung bình 6 ± 2.1 năm (biểu đồ 1) [5,6]. Điểm cắt của phân suất hở van ĐM chủ > 33% có giá trị tiên lượng bệnh nhân tiến triển đến có triệu chứng và cần phải phẫu thuật trong tương lai với độ nhạy 85% và độ đặc hiệu 92%, cho thấy khả năng dung nạp với tình trạng hở van ĐM chủ kém hơn hở van hai lá (phân suất hở van > 40 – 50%). Các nghiên cứu này cũng cho thấy giá trị phân biệt hở van ĐM chủ trung bình với nặng của siêu âm kém hơn CMR và có khuynh hướng đánh giá quá mức hở van hai lá.
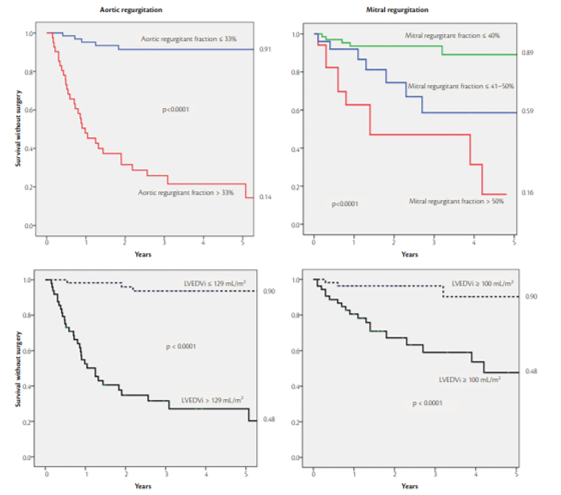
Biểu đồ 1. Tiên đoán tiến triển cần phải phẫu thuật của các bệnh nhân hở van hai lá hoặc hở van ĐM chủ trung bình đến nặng không triệu chứng (nguồn: J Am Coll Cardiol Img 2021;14:2020–2032)
- Các ngưỡng để phân độ hở van hiện tại dựa trên siêu âm. Tuy nhiên, kết quả của các nghiên cứu gần đây cho thấy các ngưỡng của CMR có thể thích hợp hơn và liên quan sát hơn với các hậu quả lâm sàng. Phân độ nặng hở van của CMR theo bảng 1.
Bảng 1. Phân độ nặng hở van của CMR
| Nhẹ | Trung bình | Nặng | |
| Hở van ĐM chủ và van ĐM phổi | |||
| Phân suất hở – Regurgitant fraction (%) | 0 – 15 | 16 – 30 | > 30 |
| Thể tích dòng hở -Regurgitant volume
(mL/cycle) |
0 – 20 | 21 – 40 | > 40 |
| Chỉ số thể tích thất trái cuối tâm trương (mL/m2) (cho hở van ĐM chủ) | > 130 | ||
| Hở van hai lá và van ba lá | |||
| Phân suất hở – Regurgitant fraction (%) | 0 – 20 | 21 – 40 | > 40 |
| Thể tích dòng hở -Regurgitant volume
(mL/cycle) |
0 – 30 | 31 – 60 | > 60 |
| Chỉ số thể tích thất trái cuối tâm trương (mL/m2) (cho hở van hai lá) | > 100 | ||
3. Bệnh van hỗn hợp:
Bệnh van hỗn hợp bao gồm cả hẹp và hở van. Thường tổn thương hẹp hoặc hở van sẽ trội hơn và là yếu tố để quyết đinh chiến lược điều trị.
Đối với bệnh van ĐM chủ hoặc ĐM phổi, siêu âm tim và CMR đều có thể đánh giá bệnh van hỗn hợp, mỗi phương pháp đều có những hạn chế nhất định. Đối với siêu âm tim, đánh giá bằng phương pháp vận tốc (siêu âm doppler), do hở van làm gia tăng dòng máu tới (forward) qua van, làm gia tăng vận tốc dòng máu độc lập với tình trạng hẹp van. CMR có thể đo diện tích mở van để đánh giá thành phần hẹp van, không bị ảnh hưởng bởi mức độ hở van. Thành phần hở van đánh giá bằng phương pháp phase contrast nhưng thường bị sai số do dòng hở ở vị trí ĐM chủ lên sau chỗ hẹp van thường có vận tốc cao và có dòng rối (turbulent), là giảm độ chính xác so với siêu âm doppler. Hơn nữa, VENC được chọn cao khi có hẹp van ĐM chủ để xoá nhiễu do vận tốc dòng máu thì tâm thu cao, VENC này lại tương đối cao so với vận tốc dòng máu thì tâm trương để khảo dòng hở van ĐM chủ, do đó sẽ đánh giá sai thể tích thì tâm trương. Có thể dùng 2 VENC khác nhau, một cho thì tâm thu, một cho thì tâm trương, tuy nhiên phương pháp này có sai số khi tính phân suất dòng hở còn nhiều hơn so với chọn 1 VENC. Có thể kết hợp các phương pháp đánh giá gián tiếp khác để củng cố thêm bằng chứng của hở van ĐM chủ nặng như đo chênh lệch thể tích 1 nhát bóp giữa thất trái và thất phải (nếu chỉ hở 1 van), hoặc có dòng nghịch đảo toàn tâm thu (holodiastolic flow reversal) ở ĐM chủ xuống trong hở van ĐM chủ.
Bệnh van hai lá và van ba lá không bị những hạn chế nêu trên, do hở van được đánh giá gián tiếp bằng phase contrast qua ĐM chủ hoặc ĐM phổi, do đó không bị ảnh hưởng bởi dòng rối do vận tốc cao, hẹp van đánh giá trực tiếp bằng đo diện tích mở van.
4. Đánh giá ĐM chủ trong bệnh van ĐM chủ:
Bệnh van ĐM chủ thường có bất thường của ĐM chủ ngực đi kèm. Trong hẹp van ĐM chủ, hướng dòng máu xịt bất thường trong thì tâm thu có thể gây dãn ĐM chủ sau hẹp. Trong van ĐM chủ 2 mảnh, cả 2 yếu tố bất thường về gen và thay đổi về huyết động có thể gây phình ĐM chủ lên, và bệnh này có quan hệ mạnh với hẹp eo ĐM chủ. Dãn gốc ĐM chủ cũng có thể gây hở van ĐM chủ do các lá van áp không sát. Sau phẫu thuật van ĐM chủ, như kỹ thuật Ross, ĐM chủ có thể dãn.
Vì vậy, trong bệnh lý van ĐM chủ luôn cần đánh giá ĐM chủ ngực.
CMR có thể đánh giá ĐM chủ ngực bằng một số kỹ thuật (hình 15):
- Hình cine: loạt xung SSFP hoặc HASTE song song trục ngang (transverse) thường là đủ cho đánh giá ĐM chủ ngực.
- Hình ảnh ECG-gated 3D SSFP (không thuốc tương phản từ): giúp đo chính xác đường kính vòng van, gốc ĐM chủ và chỗ nối xoang – ống.
- Hình 3D có thuốc tương phản từ: thường không cần thiết.
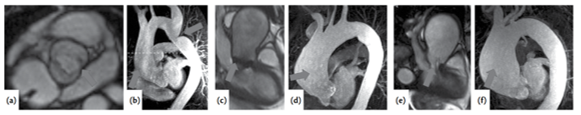
Hình 15. Hình ảnh ĐM chủ (a) Van ĐM chủ hai mảnh; (b) Phối hợp với phình ĐM chủ lên và hẹp eo ĐM chủ; (c) và (d) Van ĐM chủ cơ học với phình ĐM chủ lên; (e) và (f) Phình lớn ĐM chủ lên gây hở van ĐM chủ do các lá van áp không sát [5].
5. Van nhân tạo:
CMR là kỹ thuật có giá trị để đánh giá van nhân tạo khi siêu âm tim qua thành ngực hoặc siêu âm qua thực quản không kết luận được. Các kỹ thuật và mặt cắt tương tự van tự nhiên. Chỉ thép an toàn với CMR và không gây trở ngại đáng kể lên chất lượng hình ảnh (hình 16) trừ khi vùng khảo sát rất gần với chỗ bị nhiễu do chỉ thép. Gần như tất cả các van sinh học và cơ học cũng như các van nhân tạo đặt qua ống thông (Transcatheter aortic valve implantation – TAVI), vòng van nhân tạo đều có mã an toàn hoặc an toàn có điều kiện (MR-safe hoặc MR-conditional) trong trường MRI 1.5T và phần lớn cũng an toàn trong môi trường 3T.
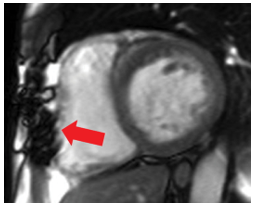
Hình 16. Nhiễu chỉ thép [5].
Đánh giá van nhân tạo bằng CMR khả thi với một số van sinh học tuỳ thuộc chất liệu khung van và lưới (stent) van. Các mặt cắt tương tự van tự nhiên (hình 17). Khó đánh giá lỗ của các van nhân tạo hoặc TAVI do nhiễu cảm từ (susceptibility artefacts – nhiễu gây ra do sự không đồng nhất của từ trường). Tuy nhiên có thể đánh giá lưu lượng bằng mặt cắt trực tuyến tương đối xa van nhân tạo, từ đó phát hiện được các bất thường về dòng máu và vận tốc. Hở van ĐM phổi hoặc ĐM chủ có thể đánh giá bằng phase contrast (hình 18) với mặt phẳng trực tuyến đặt phía trên van nhân tạo một khoảng ngắn, do đó có thể đánh giá thấp hơn thể tích hở van so với van tự nhiên (tăng khoảng cách từ mặt phẳng khảo sát đến van), nhưng chênh lệch không gây ảnh hưởng nhiều đến kết quả.
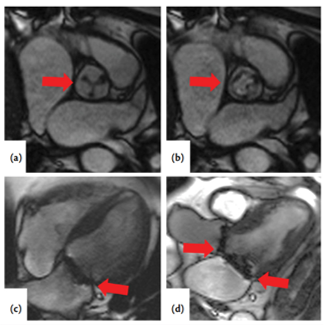
Hình 17. Van ĐM chủ nhân tạo thì tâm trương (a) và tâm thu (b). (c) van hai lá nhân tạo, (d) van hai lá và van ĐM chủ nhân tạo [5].
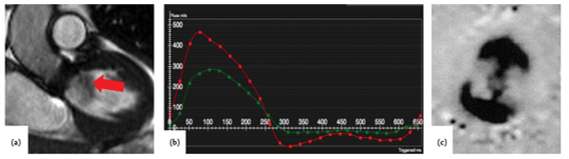
Hình 18. (a) Hình cine SSFP trong thì tâm trương cho thấy hở van ĐM chủ với dòng hở gần van nhân tạo SAPIEN XT TAVI; (b) Dòng phase contrast ở ĐM chủ lên (đường biểu đồ màu đỏ) cho thấy phân suất hở 22% (mức độ trung bình – nhẹ) và không có dòng trào ngược toàn tâm thu rõ ở ĐM chủ xuống (màu xanh lá); c/ Kiểu hình ảnh dòng trực tuyến điển hình của van kim loại 2 đĩa nghiêng (bileaflet tilting disc). Hình ảnh 2 dòng máu (flow) hình lưỡi liềm, nối nhau bởi 1 dòng xịt (jet) biểu hiện bằng một đường nhỏ hơn ở trung tâm lỗ van, gợi ý van Star Wars [5].
CMR còn có thể giúp phân biệt dòng hở tại van với dòng hở cạnh van trong một số trường hợp bằng cách đánh giá vùng có dòng hở (hình 19).
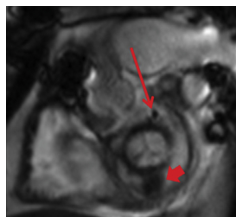
Hình 19. Hình cine SSFP của bệnh nhân bị tán huyết trên nền có van hai lá nhân tạo sinh học. Có 2 dòng hở cạnh van có màu đen (mất tín hiệu – signal loss): 1/ Vị trí 6 giờ (mũi tên đỏ ngắn) gần với dụng cụ đóng thông liên thất; 2/ Vị trí 12 giờ (mũi tên đỏ dài) [5].
Khó phân biệt dòng hở tại van với dòng hở cạnh van TAVI do nhiễu stent/frame của van. Tuy nhiên, các nghiên cứu cho thấy CMR đáng tin cậy hơn siêu âm trong đánh giá mức độ hở van TAVI (siêu âm đánh giá thấp hở van). Định lượng hở cạnh van sau TAVI 40 ngày bằng CMR có tương quan mạnh hơn với các kết cục lâm sàng so với siêu âm 6 ngày sau TAVI. Phân suất hở > 30% thuộc nhóm có nguy cơ cao suy tim phải nhập viện và tử vong do mọi nguyên nhân [4].
Phương pháp định lượng hở van hai lá và ba lá van nhân tạo tương tự van tự nhiên.
- Nốt sùi và huyết khối van nhân tạo: CMR ít có giá trị, do các cấu trúc này rất di động và do hạn chế về độ phân giải về không gian và thời gian của CMR.
6. Các khuyến cáo của các Hiệp hội tim mạch về chỉ định CMR trong bệnh van tim:
- Khuyến cáo của Hội tim Mỹ năm 2020 và Hội tim châu Âu năm 2021 về chẩn đoán và điều trị bệnh van tim [10,11]: khi chất lượng hình ảnh siêu âm tim không thích hợp, hoặc khi kết quả siêu âm không tương thích với triệu chứng lâm sàng của bệnh nhân, CMR được chỉ định để đánh giá độ nặng của tổn thương van, đặc biệt là hở van, đánh giá thể tích và chức năng tâm thu thất, bất thường của ĐM chủ lên, xơ hoá cơ tim. CMR đặc biệt hữu ích cho đánh giá hậu quả của hở van ba lá do các thông số về thể tích và chức năng tâm thu thất phải trên CMR có giá trị tham chiếu. Ngày càng có nhiều chứng cứ cho thấy giá trị của CMR trong đánh giá hở van hai lá và van ĐM chủ.
- Khuyến cáo năm 2020 của SCMR (Hội CMR quốc tế):
Bảng 2. Chỉ định của CMR trong bệnh van tim
| Chỉ định | Class |
| 1. Hẹp van ĐM chủ
2. Xác định hẹp dưới và trên van 3. Hở van ĐM chủ 4. Hẹp van ĐM chủ lưu lượng thấp ở ĐM chủ lên (Ascending aortic low patterns in aortic stenosis) 5. Hẹp van hai lá 6. Hở van hai lá 7. Hẹp van ĐM phổi 8. Hở van ĐM phổi 9. Hẹp van ba lá 10. Hở van ba lá 11. Van nhân tạo |
II
I II Inv
III II I I III II II |
7. Triển vọng của các kỹ thuật phát triển trong tương lai:
- Ngưỡng CMR đánh giá độ nặng, hướng dẫn can thiệp: các ngưỡng để phân độ nặng bệnh van tim hiện tại dựa trên siêu âm. Các ngưỡng này phần lớn được xác định từ ý kiến đồng thuận chuyên gia, và ngay cả siêu âm tim cũng chỉ có vài nghiên cứu xác định ngưỡng tối ưu. Đôi khi kết quả siêu âm tim và CMR không nhất quán, cho thấy sự cần thiết xác định ngưỡng của các thông số chuyên biệt cho CMR. CMR có khả năng cung cấp các thông số định lượng bệnh lý van (như thể tích dòng hở, thể tích và khối cơ, thể tích thất trái…), có triển vọng trong đánh giá độ nặng có liên quan đến kết cục lâm sàng.
- Đánh giá xơ hoá cơ tim với T1 mapping: mức độ tăng thời gian thư giãn T1 có mối liên quan với mức độ xơ hoá mô kẽ cơ tim trong hẹp van ĐM chủ, đồng thời có tương quan với độ nặng của hẹp van ĐM chủ. Một số nghiên cứu cũng cho thấy ECV tăng trong hẹp van ĐM chủ so với nhóm chứng. Tuy nhiên, có sự chồng chéo của giá trị T1 mapping giữa các nhóm và cần có nhiều số liệu nghiên cứu hơn nữa để xác định giá trị của T1 maping trong bệnh lý van tim.
- 4D flow: cho thông tin về kiểu dòng chảy (hình 20), phân bố lực biến dạng thành (wall shear stress) trên ĐM chủ trong bệnh van ĐM chủ 2 mảnh và hẹp van ĐM chủ. Vùng có biến đổi về mô học của thành ĐM chủ tương ứng với vùng có áp lực biến dạng thành cao nhất.
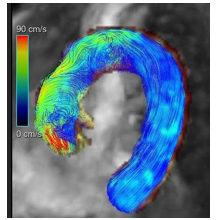
Hình 20. 4D flow cho thấy dòng chảy kiểu xoắn ốc ở ĐM chủ lên trong một trường hợp van ĐM chủ hai mảnh
KẾT LUẬN
CMR cung cấp thêm các thông tin quan trọng trong bệnh van tim. Những ưu thế nổi bật của CMR bao gồm: không hạn chế mặt phẳng khảo sát trong đánh giá hình thái van bằng kỹ thuật cine, định lượng hẹp – hở van, đánh giá hậu quả của hẹp – hở van trên khối cơ, thể tích và chức năng thất.
TÀI LIỆU THAM KHẢO
- Dweck MR, Joshi S, Murigu T, et al. Mid-wall fibrosis is an independent predictor of mortality in patients with aortic stenosis . Heart. 2011;97:A94.
- Musa TA, Treibel TA, Vassiliou VS, et al. Myocardial scar and mortality in severe aortic stenosis. Circulation. 2018;138:1935–1947.
- Bing R, Everett RJ, Tuck C, et al. Rationale and design of the randomized, controlled Early Valve Replacement Guided by Biomarkers of Left Ventricular Decompensation in Asymptomatic Patients with Severe Aortic Stenosis (EVOLVED) trial. Am Heart J. 2019;212:91–100.
- Ribeiro HB, et al. Cardiovascular magnetic resonance to evaluate aortic regurgitation after transcatheter aortic valve replacement. J Am Coll Cardiol. 2016;68:577–85.
- Cavalcante JL, Knobelsdorff FV, Myerson S. Introduction EACVI text book of cardiovascular magnetic resonance 2018. Section 8, Valve disease, page 443- 462.
- Myerson SG. CMR in Evaluating Valvular Heart Disease: Diagnosis, Severity, and Outcomes. J Am Coll Cardiol Img 2021;14:2020–2032.
- Myerson SG, et al. Determination of clinical outcome in mitral regurgitation with cardiovascular magnetic resonance quantification. Circulation 2016;133:2287–96.
- Myerson SG, et al. Aortic regurgitation quantification using cardiovascular magnetic resonance: association with clinical outcome. Circulation 2012;126:1452–60.
- Ribeiro HB, et al. Cardiovascular magnetic resonance to evaluate aortic regurgitation after transcatheter aortic valve replacement. J Am Coll Cardiol. 2016;68:577–85.
- Vahanian A, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease European Heart Journal (2021) 00,1-72. doi:10.1093/eurheartj/ehab395.
- Otto CM, et al. 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. Volume 143, Issue 5, 2 February 2021; Pages e72-e227.
- Leiner T, Bogaert J, Matthias GF, et al. SCMR Position Paper (2020) on clinical indications for cardiovascular magnetic resonance. J Cardiovasc Magn Reson (2020) 22:76.







