Management of antithrombotic therapy afterbleeding in patients with coronary artery disease and/or atrial fibrillation
I. GIỚI THIỆU
Xuất huyết liên quan thuốc chống huyết khối (CHK) là một biến chứng thường gặp khi điều trị bệnh nhân (BN) với bệnh động mạch vành (BMV), đặc biệt là những người có hội chứng mạch vành cấp (HC MVC) hoặc trải qua can thiệp mạch vành qua da (PCI) và những BN điều trị rung nhĩ (RN).
BS. NGUYỄN THANH HIỀN
BS. TRẦN NGUYỄN THU THỦY
Các nghiên cứu (NC) ngẫu nhiên cho thấy nguy cơ xuất huyết nặng chiếm 1 – 18% sau 30 ngày ở BN HC MVC, và 2 – 5% mỗi năm ở những BN bị RN được điều trị bằng thuốc chống đông đường uống (OAC). Nhiều NC quan sát cho thấy nguy cơ xuất huyết thậm chí còn cao hơn. Xuất huyết nặng có liên quan đến làm tăng nguy cơ cả về tử vong ngắn và dài hạn. Ngay cả xuất huyết tối thiểu cũng có ảnh hưởng vì thường dẫn đến gián đoạn của liệu pháp điều trị kháng đông.
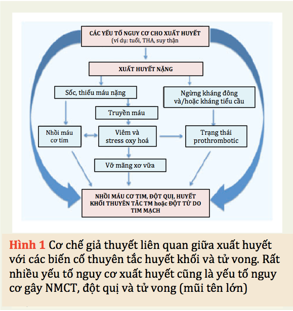
Nhiều cơ chế đã được đưa ra để giải thích mối quan hệ giữa xuất huyết nặng và tăng tỷ lệ tử vong (Hình 1). Ngoài ra, trên cùng một BN, các yếu tố nguy cơ gây xuất huyết cũng có thể là yếu tố nguy cơ gây huyết khối (tuổi, THA, tiền căn đột quỵ…). Việc ngừng sử dụng thuốc CHK có thể dẫn đến tăng tỷ lệ biến cố thuyên tắc huyết khối do sự phục hồi dần của chức năng tiểu cầu và hoạt động đông máu. Thêm vào đó, xuất huyết có thể hoạt hoá đáp ứng của prothrombotic ngoài những cơ chế liên quan đến việc ngừng thuốc kháng đông. Rõ ràng, cân bằng các nguy cơ xuất huyết so với các biến cố huyết khối có thể gây tử vong là rất quan trọng cho các quyết định về việc trường hợp nào và khi nào bắt đầu điều trị thuốc CHK sau khi xuất huyết, đặc biệt xuất huyết não, tiêu hóa.
Mặc dù rất nhiều khuyến cáo đã được công bố có liên quan đến việc kiểm soát tình trạng xuất huyết cấp tính ở những BN được điều trị bằng thuốc CHK, nhưng hướng dẫn cách điều trị CHK sau khi xuất huyết xảy ra vẫn còn là vấn đề tranh cãi hiện nay. BN mới bị xuất huyết đã được loại trừ khỏi hầu hết các thử nghiệm ngẫu nhiên về điều trị CHK và có rất ít các bằng chứng nghiêm ngặt để đưa ra quyết định điều trị.
Trong khi chờ dữ liệu từ các NC quan sát và ngẫu nhiên, bài viết này đưa ra quan điểm và chiến lược liệu pháp CHK sau xuất huyết ở BN BMV và/hoặc RN, bao gồm cả việc dừng thuốc, dùng lại thuốc gì và khi nào.
II. MỘT SỐ KHÁI NIỆM
1. Phân loại độ nặng xuất huyết
Với mục đích của tài liệu này, xuất huyết nặng đã được định nghĩa theo Hiệp hội nghiên cứu học thuật xuất huyết (BARC, Hộp 1),
2. Dừng điều trị:
Bỏ điều trị kháng đông đã được xác định theo Mehran và cộng sự như ngừng thuốc (theo khuyến cáo, ngưng thuốc theo chỉ định của bác sĩ)
Gián đoạn (ngừng điều trị kháng tiểu cầu tạm thời do cần thiết phải phẫu thuật trong vòng 14 ngày)
Ngưng đột ngột (ngừng ĐT kháng tiểu cầu do xuất huyết hoặc không tuân thủ).
Hộp 1. Phân loại xuất huyết của BARC
|
Type 0: không XH |
|
Type 1: XH vi thể và không khiến BN đến khám ngoài lịch hẹn của nghiên cứu hoặc cần nhập viện hay điều trị với chuyên gia chăm sóc sức khỏe, có thể bao gồm cả những đợt BN tự ngưng thuốc điều trị mà không tham vấn ý kiến của bác sĩ. |
|
Type 2: bất kỳ XH nặng hay XH thấy rõ trên LS (ví dụ như XH nhiều hơn dự kiến trong một trường hợp LS nhất định, bao gồm cả XH chỉ thấy trên hình ảnh học), không phù hợp với các tiêu chuẩn của type 3, 4 hay 5, nhưng có ít nhất một trong các tiêu chuẩn sau: (1) cần chuyên gia y tế can thiệp không phẫu thuật hay dùng thuốc điều trị, (2) cần nhập viện hay tăng mức độ chăm sóc, (3) cần được đánh giá. |
|
Type 3: – Type 3a: + XH thấy rõ kèm giảm Hb từ 3 đến < 5g/dL (có bằng chứng do XH) cần truyền máu. + Bất kỳ XH thấy rõ nào cần truyền máu – Type 3b: + XH thấy rõ kèm giảm Hb ≥ 5g/dL (có bằng chứng do XH) cần truyền máu. + Chèn ép tim + XH cần can thiệp phẫu thuật để kiểm soát (ngoại trừ XH trong nha khoa, bệnh lý xoang, bệnh ngoài da, trĩ) + XH cần điều trị bằng thuốc vận mạch – Type 3c: + XH nội sọ (ngoại trừ vi XH hay chuyển dạng XH), XH trong cột sống + Các loại XH được xác nhận qua giải phẫu tử thi, hình ảnh học hay chọc dò tủy sống + XH nội nhãn làm giảm thị lực Type 4: XH liên quan đến CABG: – XH nội sọ trong 48 giờ quanh phẫu thuật – Tái phẫu thuật với mục đích cầm máu sau khi đã đóng xương ức – Truyền ≥ 5 đơn vị máu toàn phần hay HCL trong vòng 48 giờ – Lưu lượng dẫn lưu phổi > 2 L trong vòng 24 giờ |
|
Type 5: XH gây TV: – Type 5a: XH có thể gây TV, không được xác nhận bằng giải phẫu tử thi hay hình ảnh học, nhưng có nghi ngờ trên LS. – Type 5b: XH chắc chắn gây TV, XH trầm trọng được xác nhận bằng giải phẫu tử thi hay hình ảnh học. |
3. Các nguy cơ huyết khối và xuất huyết sau xuất huyết
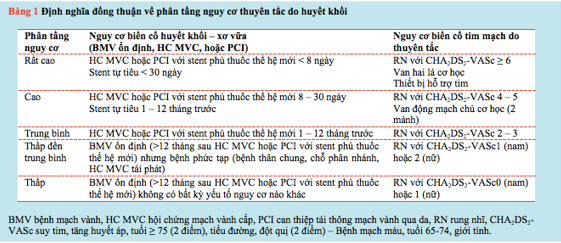
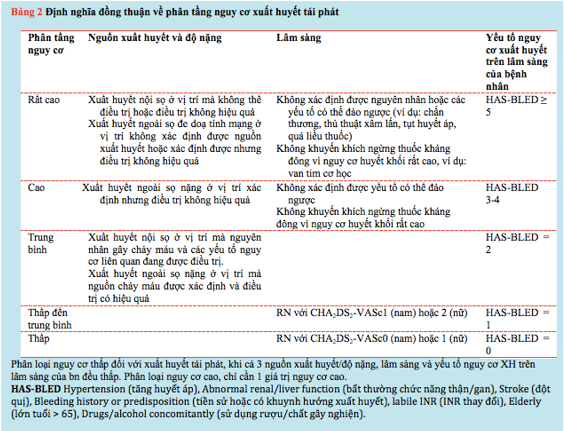
Bảng 2 và 3 trình bày các nguy cơ huyết khối và xuất huyết trên BN BMV và RN. Nguy cơ được chia thành năm loại: thấp, thấp đến trung bình, trung bình, cao và rất cao. Các định nghĩa dựa trên các thông số lâm sàng đơn giản và xác địnhđiểm số.Mặc dù giá trị của xét nghiệm chức năng tiểu cầu để dự đoán nguy cơ thiếu máu cục bộ và xuất huyết gần đây đã được chứng minh trong một NCđoàn hệ trên 20 000 BN, việc điều trị cá thể hoá dựa trên chức năng tiểu cầu và/hoặc các xét nghiệm di truyền học không được khuyến cáo trong thực hành lâm sàng thông thường do không đủ dữ liệu.
III. CHIẾN LƯỢC CHUNG ĐIỀU TRỊ THUỐC CHK SAU XUẤT HUYẾT
Quyết định điều trị thuốc CHK sau khi bị chảy máu là rất khó khăn vì nguy cơ huyết khối và nguy cơ xuất huyết đều rất cao ở BN bị xuất huyết. Với sự gia tăng nguy cơ các biến cố huyết khối sau khi ngừng thuốc CHK sớm, các tác giả thống nhất nên xem xét nối lại điều trị thuốc CHK đường uống trong tất cả các tình huống mà có chỉ địnhbắt buộc (van cơ học, huyết khối trong tim…), ngay cả trong trường hợp xuất huyết nặng, miễn là xuất huyết trong hoặc ngoài sọ không đe dọa tính mạng. Khi nguy cơ huyết khối cao hơn nguy cơ xuất huyết tái phát (Bảng 2 và 3), các tác giả đề nghị tiếp tục điều trị thuốc CHK.Khi nguy cơ huyết khối xảy rangang bằng với nguy cơ xuất huyết, chỉ đề nghị ngưng một khoảng thời gian ngắn hoặc tạm thời điều trị thuốc CHK. Khi nguy cơ xuất huyết cao hơn nguy cơ huyết khối, đề nghị xem xét, tùy từng trường hợp, giảm số lượng và/hoặc liều thuốc kháng đông. Chúng ta nên đặt BN vào diện theo dõi chặt chẽ để kịp giải quyết các vấn đề phát sinh trong quá trình điều trị
IV. ĐIỀU TRỊ CHK SAU XUẤT HUYẾT NGOÀI SỌ
IV.1. Điều trị kháng tiểu cầu sau xuất huyết ngoài sọ
1. Bệnh nhân mắc hội chứng mạch vành cấp và/hoặc can thiệp mạch vành qua da gần đây (<12 tháng)
Nguy cơ mắc các biến cố tim mạch mới tăng lên ở những BN mắc HC MVC gần đây, đặc biệt là trong 3 tháng đầu và vẫn tăng lên đến 1 năm sau biến cố cấp. Vì vậy, nên sử dụng kháng tiểu cầu kép (DAPT) với aspirin và thuốc ức chế P2Y12 lên đến 1 năm đối với những BN này.
Sau khi xuất huyết, không có thử nghiệm ngẫu nhiên nào đánh giá liệu dừng hoặc sử dụng lại một hoặc cả hai thuốc chống kết tập tiểu cầu là lựa chọn tốt nhất.Ở những BN được đặt stent mạch vành gần đây, gián đoạn sớm của một hoặc cả hai thuốc chống kết tập tiểu cầu (đặc biệt là chất ức chế P2Y12) đã được chứng minh là yếu tố dự báo mạnh nhất của huyết khối trong stent.
Nguy cơ huyết khối trong stent cũng tăng cùng với thời gian ngưng điều trị, đặc biệt hơn 5 ngày, nhất là khi ngưng trong tháng đầu sau khi làm thủ thuật. Tỷ lệ tử vong trong vòng một năm đối với huyết khối trong stent vẫn ở mức cao khoảng 10 – 14%. Trong đăng ký sổ bộ của hơn 5000 BN được điều trị PCI, nguy cơ tim mạch đã tăng đáng kể khi ngừng DAPT là do không tuân thủ hoặc xuất huyết. Nguy cơ cao nhất trong 7 ngày đầu sau khi ngưng, nhưng vẫn còn cao trong vòng 30 ngày. Do đó, điều này rất quan trọng cho các bác sĩ lâm sàng để đánh giá rõ ràng việc tăng nguy cơ của các biến cố thiếu máu cục bộ sau khi ngừng điều trị kháng tiểu cầu sớm ở BN có stent mạch vành.
a. Thời gian điều trị kháng tiểu cầu kép theo loại stent ở bệnh nhân có nguy cơ xuất huyết cao đã can thiệp mạch vành qua da <12 tháng
Các NC ngẫu nhiên gần đây sử dụng stent phủ thuốc thế hệ mới (everolimus- hoặc zotarolimus-eluting) (DES) ủng hộ rút ngắn thời gian dùng DAPT ở BN có nguy cơ xuất huyết cao; trong số nghiên cứu này, không có bằng chứng cho thấy việc sử dụng 3 – 6 tháng của DAPT có hiệu quả thấp hơn với so với 12 tháng. Vì vậy, khi có xuất huyết nặng xảy ra sau 3 – 6 tháng sử dụng DAPT, các nghiên cứu này ủng hộ việc ngừng thuốc ức chế P2Y12 và tiếp tục dùng aspirin đơn độc, đặc biệt ở những BN không có tiền sử HC MVC. Thêm vào đó, NC so sánh ngẫu nhiên LEADER FREE về stent phủ thuốc BioFreedomBiolimus A9 so với stent Gazelle không phủ thuốc ở những BN có nguy cơ xuất huyết cao cho thấy rằng stent phủ biolimus không có polymer có thể cho phép thời gian sử dụng DAPT ngắn hơn (1 tháng). Do đó, quyết định về việc có hay không và khi nào nên tiếp tục điều trị kháng tiểu cầu sau khi xuất huyết cũng nên xem xét loại stent BN sử dụng.
Trong khi nguy cơ chung huyết khối trong stent với DES thế hệ mớilà thấp nhất, nhưng nguy cơ huyết khối lại cao hơn với stent tự tiêu (BVS), do sự hình thành huyết khối có liên quan đến độ dày của khung stent và bề mặt tiếp xúc với máu. Do đó, thời gian dùng DAPT dài hơn và nhu cầu cấp thiết hơn để sử dụng lại các thuốc chống kết tập tiểu cầu sau khi xuất huyết có thể cần thiết với BVS, mặc dù các NC cụ thể hơn với loại stent này là cần thiết để xác định thời gian điều trị DAPT tối ưu.
b. Bệnh nhân dùng prasugrel, ticagrelor hoặc vorapaxar
Ở những BN HC MVC được điều trị bằng thuốc ức chế P2Y12 mới như prasugrel hoặc ticagrelor, không có dữ liệu có sẵn để sử dụng lại sau khi xuất huyết. Nguy cơ xuất huyết trên những BN không CABG có dùng các thuốc này cao hơn đáng kể so với clopidogrel. Mặc dù có ít bằng chứng, clopidogrel (làm ức chế tiểu cầu ít hơn và nguy cơ xuất huyết tự phát thấp hơn) có thể được sử dụng làm thuốc ức chế P2Y12 sau xuất huyết đã xảy ra ở những BN đã được điều trị bằng prasugrel hoặc ticagrelor, càng sớm càng tốt ngay khi có thể bắt đầu lại điều trị kháng tiểu cầu. Khả năng gắn kết không thể đảo ngược của prasugrel và gắn kết thuận nghịch của ticagrelor nên được xem xét để quyết định khi nào bắt đầu lại thuốc ức chế P2Y12 ở những bệnh nhân này. Không khuyến cáo giảm liều từ 10 – 5 mg lần/ngày đối với prasugrel hoặc từ 90mg xuống 60mg 2lần/ngày với ticagrelor do thiếu bằng chứng về tính hiệu quả ở những bệnh nhânmới mắc HC MVC gần đây. Tuy nhiên, đáng lưu ý, hai liều ticagrelor đều có mức độ ức chế tiểu cầu tương đối cao.
Nguy cơ xuất huyết cũng tăng lên với chất đối kháng thụ thể thrombinvorapaxar, là thuốc có thời gian bán hủy cực kỳ kéo dài, thuốc này nên được ngưng sử dụng vĩnh viễn ở BN sau khi có xuất huyết xảy ra (hiện chúng ta chưa có thuốc này).
2. Bệnh nhân chỉ điều trị nội khoa hội chứng mạch vànhcấp
Các NC và những thống kê cho thấy một tỷ lệ đáng kể BN mắc HC MVC được điều trị nội khoa mà không cần tái thông mạch vì nhiều lý do khác nhau. Trung bình những BN này có dự hậu vềtim mạch kém hơn so với những người trải qua điều trị tái thông mạch vành. Các khuyến cáo về điều trị CHK sau khi xuất huyết cũng tương tự như BN có can thiệp, ngoại trừ việc không có nguy cơ huyết khối trong stent.
3. Bệnh nhân có bệnh mạch vành ổn định (> 12 tháng sau can thiệp mạch vành qua da hoặc hội chứng mạch vành cấp)
Hai phân tích tổng hợp, chủ yếu dựa trên dữ liệu quan sát, cho thấy rằng liệu pháp kháng tiểu cầu đơn độc chỉ định để phòng ngừa thứ phát ở bệnh nhân BMV ổn định nên được dùng lại trong vòng vài ngày sau khi xuất huyết. Phân tích đầu tiên bao gồm 50 279 BN đang dùng aspirin: ngừng hoặc không tuân thủ điều trị với aspirin có nguy cơ mắc các biến cố tim mạch lớn cao gấp ba lần so với những BN tiếp tục sử dụng [OR = 3,14 (1,75 – 5,61), P=0,0001]. Nguy cơ này tăng lên gấp nhiều lần ở những BN có đặt stent mạch vành.
NC phân tích tổng hợp thứ hai đánh giá những BN ngưng aspirin quanh phẫu thuật. Thời gian trung bình của các biến cố mạch vành sau khi ngưng aspirin là 8,5 ngày, biến cố xảy ra sớm nhất là 5 ngày sau khi ngưng. Mặt khác, một NC ngẫu nhiên lớn (POISE-2), so sánh dùng aspirin quanh phẫu thuật so với giả dược ở những BN được coi là có nguy cơ biến cố tim mạch và trải qua phẫu thuật không tim mạch, cho thấy không có tác dụng có ý nghĩa của aspirin đối với tỷ lệ tử vong trong vòng30 ngày hoặc nhồi máu cơ tim không gây tử vong, nhưng tăng nguy cơ xuất huyết nặng so với giả dược. Đáng chú ý là chỉ có dưới một phần ba dân số POISE-2 bị bệnh mạch máu trước đó và chỉ 23% có BMV.
4. Tiếp tục điều trị kháng tiểu cầu sau xuất huyết tiêu hóa
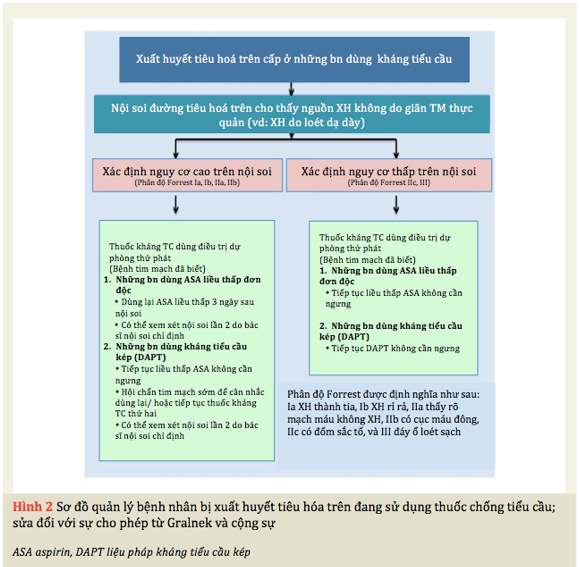
Đường tiêu hóa là một trong những vị trí xuất huyết thường gặp nhất ở BN mắc BMV. Một thử nghiệm ngẫu nhiên có đối chứng nhỏ đã đánh giá hiệu quả của việc tái sử dụng sớm aspirin, 80mg mỗi ngày, so với giả dược trong số 156 BN bị xuất huyếtdo loét dạ dày trong khi dùng aspirin. Xuất huyết tái phát do loét trong vòng 30 ngày xảy ra ở 10,3% BN dùng aspirin và 5,4% dùng giả dược (P=0,25). Tuy nhiên, tỷ lệ tử vong do mọi nguyên nhân ở tuần thứ 8 ở nhóm dùng aspirin thấp hơn rõ rệt so với nhóm giả dược (1,3 với 12,9%, P=0,005). Ở những BN dùng aspirin liều thấp để phòng ngừa tim mạch thứ phát bị xuất huyếtdo loét dạ dày, Hiệp hội Nội soi Tiêu hóa Châu Âu (ESGE) gần đây đã khuyến cáo dùng aspirin ngay lập tức sau khi nội soi nếu nguy cơ xuất huyết tái phát thấp (xác định nguy cơ thấp trên nội soi: phân loại Forrest IIc hoặc III) . Ở những BN bị loét dạ dày có nguy cơ cao (Forrest Ia, Ib, IIa, IIb), nên dùng lại aspirin sớm vào ngày thứ 3, với điều kiện là phải cầm máu đầy đủ (Hình 2). Ở những BN dùng DAPT, nên tiếp tục DAPT mà không bị gián đoạn nếu nội soi cho thấy có dấu hiệu nguy cơ thấp. Với dấu hiệu có nguy cơ cao, khuyến cáo nên bắt đầu điều trị đơn lẻ bằng aspirin liều thấp, sau đó hội chẩn sớm với bác sĩ tim mạch cho khuyến cáo về việc sử dụng lại thuốc chống kết tập tiểu cầu thứ hai. Dùng liều cao thuốc ức chế bơm proton (PPI) được khuyến cáo ở tất cả các BN bị xuất huyết do loét dạ dày, vì kì vọng sẽ nhanh chóng làm lành vết thương. Xét nghiệm nội soi lặp lại sau biến cốxuất huyết có thể giúp đảm bảo an toàn khi dùng lại clopidogrel ngoài aspirin.
5. Tóm tắt đồng thuận về điều trị kháng tiểu cầu sau xuất huyết ngoài sọ
a. Đối với những BN có nguy cơ huyết khối cao hoặc rất cao (xem Bảng 2: HC MVC hoặc đặt stent mạch vành <30 ngày) bị xuất huyết nhỏ hoặc xuất huyết nặng, chúng tôi đề nghị tiếp tục dùng aspirin liều thấp mà không bị gián đoạn. Việc dùng lại thuốc chống kết tập tiểu cầu thứ hai nên được xem xét càng sớm càng tốt sau khi BN ổn định.
b. Đối với những BN có nguy cơ huyết khối trung bình (xem Bảng 2: HC MVC hoặc PCI với thế hệ thứ hai DES 1- 12 tháng trước) bị xuất huyết nhẹ hoặc nặng, chúng tôi khuyến cáo nên dùng lại aspirin liều thấp ngay khi xuất huyết được kiểm soát, tốt nhất là trong vòng 3 ngày. Sử dụng lại thuốc chống kết tập tiểu cầu thứ hai nên được xem xét nếu nguy cơ huyết khối cao hơn nguy cơ xuất huyết tái phát. Đối với những BN bị xuất huyết khi đang điều trị DAPT trong vòng 3 tháng sau khi đặt stent mạch vành thế hệ mới, chúng tôi khuyến cáo nên dùng lại DAPT tối đa 3 tháng. Nếu BN bị xuất huyết hơn 3 tháng sau khi đặt stent thế hệ mới và vẫn có nguy cơ xuất huyết tái phát, chúng tôi đề nghị dùng lại chỉ một thuốc chống kết tập tiểu cầu (aspirin hoặc clopidogrel).
c. Ở những BN bị xuất huyết sau khi đặt stent BVS, DAPT có thể cần thiết đến 12 tháng sau thủ thuật.
d. Clopidogrel, vì ít hiệu quả hơn nhưng cũng có xu hướng giảm tỷ lệxuất huyết, có thể được sử dụng làm thuốc ức chế P2Y12 sau khi xuất huyết xảy ra trênBN đã dùng prasugrel hoặc ticagrelor. Thời gian tác dụng của prasugrel (7 – 10 ngày) hoặc ticagrelor (3 – 5 ngày) nên được xem xét quyết định khi nào nên dùng lại thuốc ức chế P2Y12 ở những BN này.
e. Ở những BN bị xuất huyết nặng dovorapaxar, chúng tôi đề nghị ngừng thuốc vĩnh viễn sau đó.
f. Ở những BN HC MVC điều trị nội khoa bị xuất huyết nặng trên DAPT, liệu pháp kháng tiểu cầu đơn lẻ có thể được xem xét, trong trường hợp không có nguy cơ huyết khối trong stent.
g. Đối với những BN có BMV hoặc HC MVC ổn định bị xuất huyết đường tiêu hoá trên (không giãn tĩnh mạch), có thể tiếp tục điều trị kháng tiểu cầu (đơn hoặc kép) mà không bị gián đoạn nếu nội soi xác định tình trạng xuất huyết nguy cơ thấp (Hình 2). Nếu xác định nguy cơ xuất huyết nguy cơ cao và xuất huyết đã được kiểm soát bằng nội soi can thiệp, aspirin có thể được dùng lại trong vòng 3 ngày. Nếu các dấu hiệu nguy cơ cao được xác định ở bệnh nhân dùng DAPT, việc sử dụng lại thuốc chống tiểu cầu thứ hai nên dựa vào việc cân nhắc cẩn thận nguy cơ huyết khối và xuất huyết trên từng BN.
h. Bổ sung PPI được khuyến nghị trong mọi trường hợp xuất huyết đường tiêu hoá trên. PPI cũng nên được sử dụng ở những BN dùng DAPT có nguy cơ xuất huyết tiêu hoá cao trên mức trung bình. Tương tác dược lực học giữa PPI (đặc biệt là omeprazole) và clopidogrel cho đến nay không cho thấy có mối liên quan rõ ràng với kết cục lâm sàng xấu hơn, nhưng nên ưu tiên sử dụng những thuốc PPI có ức chế CYP2C19 yếu hơn (ví dụ pantoprazole).
IV.2. Điều trị chống đông bằng đường uống (OAC) sau xuất huyết ngoài sọ
Điều trị bằng OAC làm giảm nguy cơ đột quỵ và thuyên tắc hệ thống ở BN RN. Ngừng OAC đã được chứng minh là có liên quan đến tăng nguy cơ đột quỵ ngay cả sau thời gian ngắn gián đoạn.
1. Thuốc đối kháng vitamin K (VKA)
Một phân tích tổng hợp gần đây của các nghiên cứu trênnhững BN dùng VKA dài hạn đã chứng minh rằng việc dùng lại warfarin sau khi bị gián đoạn do xuất huyết tiêu hoá có liên quan đến việc giảm các biến cố huyết khốivà tỷ lệ tử vong mà không có gia tăng đáng kể xuất huyết tái phát. Trong một nghiên cứu hồi cứu nhữngBN bị RN không do van tim, dùng lại warfarin sau khi xuất huyết tiêu hoá nặng có liên quan độc lập với giảm tỷ lệ tử vong so với ngừng warfarin vĩnh viễn. Không có sự khác biệt đáng kể trong tỷ lệ xuất huyết tiêu hoá mới được tìm thấy khi warfarin được dùng lại sau 1 tuần so với 1 tháng; tuy nhiên, khi warfarin được sử dụng lại trước tuần đầu tiên sau khi xuất huyết tiêu hoá đã qua, nguy cơ xuất huyết tái phát tăng đáng kể. Dựa trên những dữ liệu này, với một chỉ định rõ ràng, liệu pháp VKA nên được sử dụng lại trong vòng 1 tuần sau khi xuất huyết tiêu hoá nặng.
Ở những BN có van tim cơ học, ngừng sử dụng VKA có liên quan đến nguy cơ huyết khối cao và thường phải cố gắng dùng lại.
2. Thuốc chống đông máu không đối kháng vitamin K (NOAC)
NOAC chưa được thử nghiệm ở BN RN bị mới bị xuất huyếtvà thời gian tối ưu để khởi động lạiNOAC sau khi xuất huyết là không rõ. Trong một NC gần đây với thuốc giải độc idarucizumab cho BN dùng dabigatran bị xuất huyết đe dọa tính mạng hoặc cần phẫu thuật khẩn cấp, xảy ra các biến cố huyết khối trong vòng 6 ngày sau dùng idarucizumab khi thuốc kháng đông không được dùng lại. Điều này tương tự như khuyến cáo đối với thuốc VKA, lưu ý rằng tác dụng chống đông máu đầy đủ của NOAC xảy ra sớm hơn (trong vòng 2- 4 giờ) so với VKA (vài ngày).
Khi tái sử dụng NOAC, cần đánh giá và theo dõi chức năng thận cẩn thận để tránh tích lũy thuốc. Khoảng thời gian được khuyến cáo trong quá trình theo dõi chức năng thận phụ thuộc vào mức độ của chức năng thận: nếu độ thanh thải creatinin (CrCl) dưới 60mL/phút, nên kiểm tra lại chức năng thận mỗi x tháng, trong đó x được xác định x = CrCl /10. Tuy nhiên, nếu sau xuất huyết nặng, khoảng thời gian này nên được ngắn lại.
Một số NOAC có liên quan đến tăng nguy cơ xuất huyết tiêu hoá so với warfarin (rivaroxaban, dabigatran). Có thể được xem xét chuyển sang warfarin hoặc NOAC mà không tăng nguy cơ xuất huyết tiêu hoá so với warfarin (ví dụ apixaban).
Tóm tắt đồng thuận về điều trị chống đông máu sau xuất huyết ngoài sọ
a. Sau khi xuất huyết ngoài sọ, OAC nên được dùng ngay khi nguy cơ huyết khối thuyên tắc tim mạch liên quan đến ngừng thuốc được cho là lớn hơn nguy cơ xuất huyết tái phát khi sử dụng lại thuốc, trong hầu hết các trường hợp trong vòng 1 tuần.
b. Khi tái sử dụng NOAC, chức năng thận cần được đánh giá và giám sát cẩn thận để tránh tích lũy thuốc.
c. Nếu thuốc giải độc (idaruzicumab) đã được sử dụng để đảo ngược tác dụng chống đông máu của NOAC, thì nên dùng lại NOAC càng sớm càng tốt, tốt nhất là trong vòng 3 – 4 ngày nếu nguy cơ xuất huyết trên từng BN cho phép.
d. Ở những BN có van tim cơ học, ngừng sử dụng VKA có liên quan đến nguy cơ huyết khối cao và không được khuyến khích, đặc biệt đối với vị trí van hai lá.NOAC hiện đang chống chỉ định cho BN có van tim cơ học.
IV. 3. Tiếp tục điều trị chống huyết khối ở bệnh nhân có chỉ định cho cả thuốc chống tiểu cầu và thuốc chống đông đường uống
Một thách thức đặc biệt về điều trị CHK là trên những BN có cả RN và HC MVC / đặt stent mạch vành, hầu hết trong số họ đều có chỉ định cho cả DAPT và OAC. Khoảng thời gian điều trị ba thuốc được khuyến cáo ở hầu hết các BN, sau đó là liệu pháp kép (OAC cộng với kháng tiểu cầu đơn lẻ) lên đến một năm; sau đó tiếp tục OAC dài hạn.Kết hợp DAPT với OAC (VKA hoặc NOAC) làm tăng đáng kể nguy cơ xuất huyết, bất kể sự kết hợp nào. NC tối ưu hoá điều trị kháng tiểu cầu và điều trị chống đông máu ở BN dùng OAC và có đặtstent mạch vành (WOEST) trên 573 BN đã chứng minh rằng liệu pháp hai thuốc (VKA cộng với clopidogrel) an toàn hơn đối với xuất huyết BARC so với điều trị bằng ba thuốc, các NC trên dữ liệu đăngký cũng cho thấy kết quả tương tự. NC ISAR TRIPLEtrên 614 BN sử dụng VKA có đặt stent DEScho thấy kết quả tương tự nếu clopidogrel, cùng với VKA và aspirin, được chỉ định trong 6 tuần hoặc 6 tháng. Cả hai thử nghiệm này đều quá nhỏ để đánh giá dự hậu thiếu máu cục bộ, cũng như BN đều ổn định và không bị xuất huyết. Tuy nhiên, như một phép ngoại suy từ các nghiên cứu này, chúng tôi khuyên nên ngừng dùng aspirin hoặc clopidogrel khi bệnh nhân bị xuất huyết nặng trong khi điều trị CHK ba thuốc. Ở những BN bị xuất huyết nặng khi điều trị hai thuốc (OAC cộng với kháng tiểu cầu đơn), việc ngừng sử dụng thuốc chống tiểu cầu có thể được cân nhắc trước 1 năm, miễn là nguy cơ huyết khối ở mức trung bình hoặc thấp hơn (Bảng 2).
Hiện đã có các NC so sánh VKA với NOAC trên những bn RN với HC MVC / PCI, và có các hướng dẫn cho thấy có thể sử dụng kết hợp NOAC với các liệu pháp điều trị kháng tiểu cầu (PIONER-AF PCI, REDUAL PCI, AUGUST). Liên quan đến việc lựa chọn liệu pháp kháng tiểu cầu, hướng dẫn ESC khuyến cáo nên hạn chế sử dụng prasugrel hoặc ticagrelor như là một phần của liệu pháp ba thuốc. Việc sử dụng ticagrelor kết hợp với NOAC hiện đang được thử nghiệm trong các nghiên cứu ngẫu nhiên tiến cứu (NCT02164864,NCT02415400).
Khi NOAC được kết hợp với thuốc chống tiểu cầu, nên sử dụng liều thấp nhất có hiệu quả để phòng ngừa đột quỵ, nghĩa là dùng dabigatran 110mg 2 lần/ngày (Rivaroxaban 15 mg 1 lần/ngày, apixaban 2,5 mg 2 lần/ngày, hoặc edoxaban 30 mg 1 lần/ngày, chỉ khi có tiêu chuẩn giảm liều). Hiệu quả của rivaroxaban 2,5mg 2 lần/ngày chưa được chứng minh trong phòng ngừa đột quỵ ở BN RN và không thể được khuyến cáo cho chỉ định này.
Tóm tắt đồng thuận về chỉ định cho cả thuốc chống tiểu cầu và thuốc chống đông đường uống sau khi xuất huyết ngoài sọ
a. Khi BN được điều trị bằng PCI có RN không do bệnh vantim bị xuất huyết đang dùng 3 thuốc CHK, chúng tôi khuyến cáo nên ngừng dùng aspirin hoặc clopidogrel (clopidogrel không ngừng trong vòng tháng đầu tiên sau đặt stent) đến khi cho phép dùng lại. Đối với OAC, chúng tôi đề xuất INR mục tiêu là 2,0– 2,5 với VKA và liều thấp nhất có hiệu quả để phòng ngừa đột quỵ cho NOAC.
b. Ở những BN bị xuất huyết nặng khi điều trị hai thuốc (OAC cộng với kháng tiểu cầu đơn), việc ngừng sử dụng thuốc kháng tiểu cầu có thể được xem xét trước 1 năm.
c. Chúng tôi đề nghị DAPT (không có OAC) trong 1 năm sau HC MVC / PCI khi BN bị RN không do bệnh van tim và nguy cơ đột quỵ thấp (CHA2DS2-VASc 1 điểm đối với nam, 2 đối với nữ) bị xuất huyết khi điều trị CHK ba thuốc.
V. ĐIỀU TRỊ CHỐNG HUYẾT KHỐI SAU XUẤT HUYẾT NỘI SỌ
V.1. Điều trị kháng tiểu cầu
Khoảng 0,2- 0,6% bệnh nhân HC MVC bị xuất huyết nội sọ (XHNS) hàng năm khi điều trị bằng kháng tiểu cầu. Bằng chứng về việc có hay không dừng thuốc vô thời hạn hoặc tiếp tục điều trị kháng tiểu cầu còn rất hạn chế.
Cần xem xét cẩn thận nguy cơ huyết khối và nguy cơ xuất huyết. Nói chung, điều trị lại sau khi ngừng thuốc tạm thời nên được xem xét nếu nguy cơ huyết khối, như được xác định trong Bảng 2, là rất cao hoặc cao. Các NC cho thấy dùng lại một thuốc kháng tiểu cầu là an toàn. Một thử nghiệm ngẫu nhiên có đối chứng về việc dùng lại so với tránh dùng thuốc chống tiểu cầu sau khi XHNS liên quan đến thuốc CHK đang diễn ra (ISRCTN71907627).
V.2. Thuốc chống đông đường uống
XHNS là một trong những biến chứng đáng sợ nhất của OAC, xảy ra ở 0,5 – 1,0% BN điều trị OAC hàng năm. Ở những BN sống sót sau XHNS liên quan đến dùng kháng đông (<60%), câu hỏi được đặt ra là có nên sử dụng lại OAC hay không. Theo một tóm tắt hệ thống của các NC quan sát trên BN có van tim nhân tạo bị XHNS kết luận rằng ở những BN có van tim cơ học, việc chống đông bằng heparin có thể được dùng lại an toàn 3 ngày sau XHNS và chuyển sang VKA sau 7 ngày. Đối với BN không có van tim cơ học, vấn đề khó khăn là liệu có nên táisử dụng OAC sau XHNS.Mặc dù tóm tắt những đặc điểm của các thuốc kháng đông đều cho rằng XHNS là chống chỉ định với OAC, một số NC quan sát đã so sánh việc tái sử dụng so với không dùng OAC sau XHNS. Có ba nghiên cứu cung cấp nhiều thông tin nhất nghiên cứu trên đối tượng BN người lớn với các loại XHNS khác nhau và nhiều chỉ định cho OAC (chủ yếu là RN), và định lượng nguy cơ của XHNS tái phát hoặc biến cố nguy cơ thiếu máu cục bộ cho BN đã ngưng dùng hoặc dùng lại warfarin. Dữ liệu từ các NC này cho thấy có sự giảm các biến cố thiếu máu cục bộ, XHNS tái phát và tỷ lệ tử vong liên quan đến việc dùng lại warfarin.
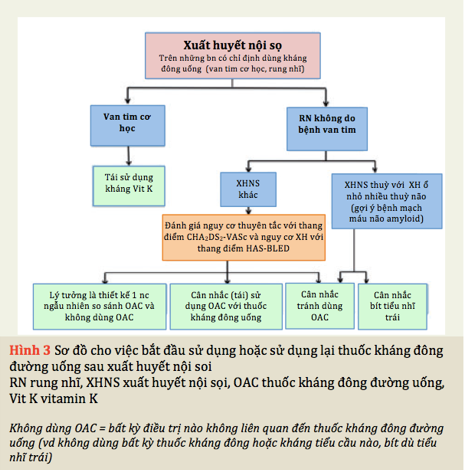
Khả năng huyết khối đối với tình trạng bệnh nền đòi hỏi OAC, như được phân tầng trong Bảng 2, vị trí của XHNS, sự hiện diện của các ổ xuất huyết nhỏ trên hình ảnh cộng hưởng từ và nguy cơ xuất huyết chung của BN (Bảng3) nên được xem xét trước khi quyết định (Hình 3, bảng 4). XHNS tái phát khá phổ biến với những BN XHNS vỏ não, XH não ổ nhỏ đa thùy, tiền sử gia đình có XHNS, bệnh lý mạch máu do amyloid và thiếu các yếu tố thuận nghịch/kết tủa. Các nguyên nhân có thể đảo ngược hoặc có thể điều trị được của XHNS, hoặc nhu cầu cấp thiết về kháng đông ở BN có vantim cơ học (Hình 3), nên ưu tiên sử dụng lại. Nếu quyết định sử dụng lại thuốc chống đông máu, thời gian dùng lại tối ưu là không chắc chắn. Thời gian đề nghị là rất khác nhau từ 2 – 10 tuần. Một số đề nghị dùng sớm hơn (dưới 7 ngày) hoặc muộn hơn (hơn 10 tuần). Điều này tùy thuộc vào từng bệnh lý cụ thể và nguy cơ mỗi người bệnh dựa trên kích thước và vị trí hấp thụ, và yếu tố nguy cơ lan rộng máu tụ, nguy cơ thuyên tắc và hậu quả của nó. Theo các hướng dẫn hiện nay, cũng như quan điểm của chúng tôi, hạn chế dùng trước 2 tuần (trừ trường hợp van cơ học), thường là sau 4 tuần nếu xuất huyết não đã cầm hay ở BN xuất huyết não nhỏ và nguy cơ thuyên tắc huyết khối cao, dùng lại sau 8 – 10 tuần hay muộn hơn ở BN xuất huyết não vùng thân não, tiểu não hay xuất huyết não lớn. Nếu phải dùng dưới 7 ngày, nên chuyển sang chiến lược bắc cầu bằng Heparin, sau đó mới chuyển sang dùng kháng đông uống
Tất cả các bằng chứng hiện có chỉ liên quan đến VKA. Các NOAC xuất hiện đầy hứa hẹn vì nguy cơ XHNS thấp hơn warfarin trong các thử nghiệm ở BN RN không có van tim, nhưng những thuốc này chưa được thử nghiệm ở BN đã XHNS trước đó. Ở những BN RN có XHNS và/ hoặc xuất huyết ở nhỏ nhiều thuỳ và/hoặc điểm CHA2DS2-VASc ≥ 4, thủ thuật bít tiểu nhĩ trái là một lựa chọn.
Một nghiên cứu ngẫu nhiên về apixaban so với không dùng thuốc chống đông sau khi XHNS liên quan đến chống đông máu đang diễn ra (NTR4526).
Tóm tắt đồng thuận về thuốc chống đông đường uống sau XHNS
a. Có nên quyết định sử dụng lại OAC sau XHNS hay không và khi nào tùy thuộc vào nguy cơ huyết khối của BN và nguy cơ xuất huyết tái phát (Hình 3). Cần có sự hợp tác chặt chẽ giữa các bác sĩ thần kinh và bác sĩ tim mạch để đưa ra quyết định trên từng BN.
b. Trong trường hợp không có van tim cơ học, NOAC có thể thích hợp hơn với warfarin sau XHNS, với tỷ lệ XHNS thấp hơn. Nếu dùng NOAC, nên sử dụng liều thấp nhất có hiệu quả để phòng ngừa đột quỵ trong RN. Chức năng thận, trọng lượng cơ thể, tuổi tác và tương tác thuốc nên được xem xét cẩn thận để tránh dùng thuốc quá liều.
Bảng 4:Các yếu tố cần cân nhắc trước khi quyết định dùng lại kháng đông.
|
Nhóm bệnh nhân nên dùng lại kháng đông |
Nhóm bệnh nhân không nên dùng kháng đông |
|
– XH khi đang sử dụng KVA hoặc quá liều kháng đông – Do chấn thương hoặc nguyên nhân điều trị được – Bệnh nhân trẻ tuổi – Kiểm soát HA tốt – XH nhân nền – Không hoặc tổn thương nhẹ chất trắng ở não – Đã phẫu thuật lấy khối máu tụ – Đã can thiệp dị dạng mạch máu – Nguy cơ đột qụy cao |
– XH trong khi uống kháng đông chưa đạt liều điều trị – Đang sử dụng NOAC hoặc gián đoạn hay không đủ liều kháng đông – Bệnh nhân cao tuổi – Không kiểm soát tốt HA – XH vùng vỏ não – XHN nghiêm trọng – Nhiều ổ vi xuất huyết – Không điều trị được nguyên nhân xuất huyết – Nghiện rượu – Bắt buộc kháng KTTC kép sau PCI
|
PHẦN KẾT LUẬN
Việc sử dụng ngày càng nhiều thuốc CHK mạnh và phối hợp thuốc làm tăng thách thức cho các bác sĩ lâm sàng trong việc điều trị BN bị biến chứng xuất huyết. Điều cần thiết là các bác sĩ lâm sàng nhận thức được nguy cơ cao của các biến cố thiếu máu cục bộ sau xuất huyết và điều chỉnh các quyết định của họ về việc tiếp tục hoặc tái sử dụng liệu pháp chống huyết khối cho phù hợp. Mặc dù ưu tiên là thu thập thêm bằng chứng từ các thử nghiệm ngẫu nhiên, chúng tôi đề xuất hướng dẫn quản lý điều trị chống huyết khối sau khi xuất huyết khi tham gia vào một thử nghiệm lâm sàng có liên quan là không khả thi, nhấn mạnh tầm quan trọng thường xuyên của việc tiếp tục hoặc tái sử dụng điều trị chống huyết khối.
Tài liệu tham khảo
1. Daniel M. Witt: What to do after the bleed: resuming anticoagulation after major bleeding. American Society of Hematology 2016: 620-624.
2. Halvorsen.S et al: Management of antithrombotic therapy after bleeding in patients with coronary arterydisease and/or atrial fibrillation: expert consensus paper of the European Society ofCardiology Working Group on Thrombosis. European Heart Journal (2017) 38, 1455–1462
3. 2017 ESC focused update on dual antiplatelettherapy in coronary artery disease developedin collaboration with EACTS
4. Gimbel. ME, Minderhoud. SCS, ten Berg. JM: A practical guide on how to handle patients with bleeding events while on oral antithrombotic treatment. Neth Heart J (2018) 26:341–351
5. Di Minno.A et al: Gastrointestinal bleeding in patients receiving oral anticoagulation: Current treatment and pharmacological perspectives. Thrombosis Research 136 (2015) 1074–1081
6. Kido. K et al: Management of Oral AnticoagulationTherapy AfterGastrointestinal Bleeding: Whether to, When to, and How to Restartan Anticoagulation Therapy. Annals of Pharmacotherapy. 2017, 51 : 11 1000-1007
7. Pannach. J et al: Management and outcome of gastrointestinal bleeding in patients taking oral anticoagulants or antiplatelet drugs. J Gastroenterol (2017) 52:1211–1220
8. Veitch Andrew M et al. Endoscopy in patients on antiplatelet or anticoagulant therapy, includingdirect oral anticoagulants: British Society of Gastroenterology (BSG) and European Society of Gastrointestinal Endoscopy (ESGE) guidelines. Endoscopy 2016; 48: 1–18
9. Chai-Adisaksopha. A et al: Thromboembolic events, recurrent bleeding and mortality after resuming anticoagulant following gastrointestinal bleeding A meta-analysis. Thromb Haemost 2015; 114: 819–825
10. Qureshi. W et al: Restarting Anticoagulation and Outcomes After Major Gastrointestinal Bleeding in Atrial Fibrillation. Am J Cardiol 2014; 113:662e668
11. Pilis.A et alL: Gastrointestinal Bleeding in Patients Receiving Antiplatelet and Anticoagulant Therapy: Practical Guidance for Restarting Therapy and Avoiding Recurrences. Hellenic J Cardiol 2014; 55: 499-509
12. The 2018 European Heart Rhythm AssociationPractical Guide on the use of non-vitamin Kantagonist oral anticoagulants in patientswith atrial fibrillation
13. 2016 ESC Guidelines for the management of atrialfibrillation developed in collaboration with EACTS
14. 2015 Guidelines for the Management of SpontaneousIntracerebral Hemorrhage
15. 2017 ACC Expert Consensus DecisionPathway on Management of Bleeding in Patients on Oral Anticoagulants Potpara. TH, Lip.GYH: Oral Anticoagulant Therapy in Atrial Fibrillation Patients at High Stroke and Bleeding Risk. Progress in Cardiovascular Diseases (2015), doi: 10.1016/j.pcad.2015.07.003
16. Al-Shahi Salman. R et al: Antiplatelet Therapy May Be Continued After Intracerebral Hemorrhage. Stroke. 2014;45:3149-3150
17. Zazulia. A: Antiplatelet and Anticoagulant after Intracerebral Hemorrhage. Neurol Clin 33 (2015) 329–345
18. Bs Nguyễn Thanh Hiền et al: Dùng lại kháng đông sau xuất huyết não. Chuyên đề tim mạch học 2017
19. Becattini. C, Sembolini. A, Paciaron. M: Resuming anticoagulant therapy after intracerebral bleeding. Vascular Pharmacology 84 (2016): 15–24.
20. Wijdicks. EFM: The use of antithrombotic therapy in patients with an acute or prior intracerebral hemorrhage. Uptodate 2019
21. Lim. JS: Cerebral Microbleeds and Early Recurrent Stroke After Transient Ischemic Attack: Results From the Korean Transient Ischemic Attack Expression Registry. JAMA Neurol. 2015;72(3):301-308
22. Imaizum. Ti et al: Antithrombotic Drug Uses and Deep Intracerebral Hemorrhages in Stroke Patients With Deep Cerebral Microbleeds. Journal of Stroke and Cerebrovascular Diseases, Vol. 22, No. 6 (August), 2013: pp 869-875.
23. Nielsen. PB et al: Restarting Anticoagulant Treatment After Intracranial Hemorrhage in Patients With Atrial Fibrillation and the Impact on Recurrent Stroke, Mortality, and Bleeding A Nationwide Cohort Study. Circulation. 2015;132:517-525
24. Majeed. A et al: Optimal Timing of Resumption of Warfarin After Intracranial Hemorrhage. Stroke. 2010;41: 2860-2866.
25. .Ding. X et al: Resumption of antiplatelet therapy in patients with primary intracranial hemorrhage-benefits and risks: A meta-analysis of cohort studies. Journal of the Neurological Sciences 384 (2018) 133–138
26. Murthy. SB et al: Restarting Anticoagulant Therapy After Intracranial Hemorrhage A Systematic Review and Meta-Analysis. Stroke. 2017;48:1594-1600.
27. Chandra. D et al: When should you restart anticoagulation in patients who suffer an intracranial bleed who also have a prosthetic valve? Interactive CardioVascular and Thoracic Surgery 16 (2013) 520–524
28. Kuramatsu. JB et al: Anticoagulant Reversal, Blood Pressure Levels, and Anticoagulant Resumption in Patients With Anticoagulation-Related Intracerebral Hemorrhage. JAMA. 2015; 313(8):824-836.
29. Bs Nguyễn Thanh Hiền, Bs Dương Hiệp Hồ, Bs Trần Nguyễn Thu Thủy: chăm sóc bệnh nhân dùng kháng đông đường uống mới (NOAC) trong tình huống cấp tính. Chuyên đề tim mạch học 2018







