 Tái lưu thông ĐMV là điều trị chính đối với bệnh nhân ĐMV. Có 3 biện pháp tái lưu thông ĐMV: thuốc tiêu sợi huyết, nong ĐMV qua da và phẫu thuật bắc cầu ĐMV. Quan điểm trước kia cho là đối với bệnh nhân ĐTĐ, phẫu thuật BCĐMV tốt hơn nong ĐMV.
Tái lưu thông ĐMV là điều trị chính đối với bệnh nhân ĐMV. Có 3 biện pháp tái lưu thông ĐMV: thuốc tiêu sợi huyết, nong ĐMV qua da và phẫu thuật bắc cầu ĐMV. Quan điểm trước kia cho là đối với bệnh nhân ĐTĐ, phẫu thuật BCĐMV tốt hơn nong ĐMV.
Bệnh viện Tim Tâm Đức
Đại Học Y Phạm Ngọc Thạch
Viện Tim TP.HCM
Tài liệu do Servier cung cấp
6.2. Tái lưu thông động mạch vành
Tái lưu thông ĐMV là điều trị chính đối với bệnh nhân ĐMV. Có 3 biện pháp tái lưu thông ĐMV: thuốc tiêu sợi huyết, nong ĐMV qua da và phẫu thuật bắc cầu ĐMV. Quan điểm trước kia cho là đối với bệnh nhân ĐTĐ, phẫu thuật BCĐMV tốt hơn nong ĐMV. Từ thời đại có thuốc chống kết tập tiểu cầu như abxicimab và stent, sau đó là stent phủ thuốc (td: sirolimus) quan điểm này có thay đổi.
Trước khi có stent và thuốc đối kháng GP IIb/IIIa, tỷ lệ tái hẹp sau nong ĐMV trên bệnh nhân ĐTĐ lên tới 47 – 71%. Nghiên cứu EPISTENT cho thấy, có stent kèm abciximab, tỷ lệ tái hẹp chỉ là 8,1% ở bệnh nhân ĐTĐ được can thiệp ĐMV (22). Nghiên cứu Arterial Revascularization Trial Study (ARTS) so sánh nong nhiều nhánh ĐMV với phẫu thuật BCĐMV trên 1245 bệnh nhân ĐTĐ cho thấy không khác biệt giữa 2 nhóm về tử vong, NMCT và đột quỵ sau 1 năm (30)
Các nghiên cứu RAVEL và SIRIUS chứng minh tỷ lệ tái hẹp ở bệnh nhân BĐMV kèm ĐTĐ được nong kèm đặt stent phủ thuốc (sirolimus) chỉ là 8,3% so với 48,5% ở nhóm đặt stent không phủ thuốc (31) (32). Do đó, từ thời đại có stent phủ thuốc, chỉ định nong ĐMV ở bệnh nhân ĐTĐ rộng hơn.
7. SUY TIM TRÊN BỆNH NHÂN ĐÁI THÁO ĐƯỜNG
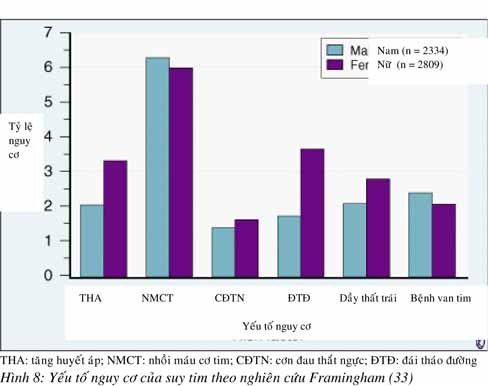
ĐTĐ là yếu tố nguy cơ độc lập của suy tim. Nghiên cứu Framingham cho thấy nam bị ĐTĐ có nguy cơ 1,82 lần so với nam không ĐTĐ; với bệnh nhân nữ còn cao hơn 3,73 lần (31). Khoảng 33% bệnh nhân nhập viện vì suy tim có ĐTĐ.

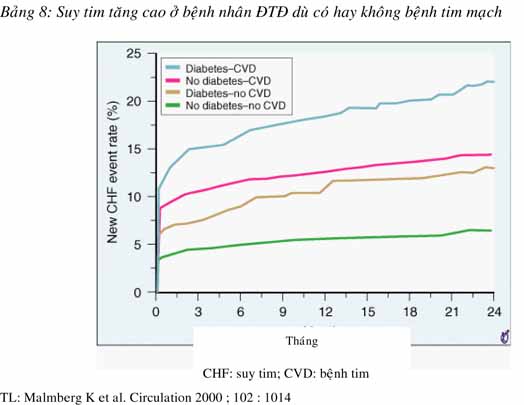
Hai yếu tố góp phần tăng suy tim ở bệnh nhân ĐTĐ là bệnh ĐMV mạn và tái cấu trúc thất sau NMCT. Dựa trên nghiên cứu OASIS, Malmberg phân tích thấy dù có hay không bệnh ĐMV, bệnh nhân ĐTĐ vẫn có tần suất suy tim cao hơn bệnh nhân không ĐTĐ (bảng 8)
7.1. Kiểm soát chặt đường huyết và tăng huyết áp giúp giảm nguy cơ suy tim trên bệnh nhân ĐTĐ
7.1.1. Đường huyết
Hai nghiên cứu chứng minh sự tương quan giữa đường huyết với suy tim. Iribarren và c/s theo dõi 48858 bệnh nhân ĐTĐ không suy tim trong trung bình 2,2 năm. Tần suất nhập viện hay tử vong vì suy tim, tùy thuộc vào mức độ HbA1C. Tương quan chặt chẽ hơn ở bệnh nhân nam, gia tăng 1% nồng độ HbA1C sẽ làm tăng 12% suy tim (34)
Nghiên cứu UKPDS trên 4585 bệnh nhân ĐTĐ type 2. Trong 7,5 – 12,5 theo dõi, mỗi gia tăng 1% HbA1C sẽ làm tăng 16% tần suất suy tim (p = 0,021) (35)
Như vậy kiểm soát kém đường huyết trên bệnh nhân ĐTĐ sẽ làm gia tăng nguy cơ suy tim.
7.1.2. Huyết áp
Trong nghiên cứu UKPDS có 1148 bệnh nhân THA kèm ĐTĐ type 2 được phân ra nhóm kiểm soát chặt huyết áp (HA mục tiêu < 150/85 mmHg) và nhóm kiểm soát kém chặt huyết áp (HA mục tiêu < 180/105 mmHg) theo dõi trong 8,4 năm. HA trung bình đạt được của nhóm kiểm soát chặt chẽ là 144/82 mmHg, của nhóm kiểm soát kém chặt chẽ là 154/87 mmHg. Nhóm được kiểm soát chặt HA có tần suất suy tim giảm 56% so với nhóm còn lại (p = 0,0043) (15)
Nghiên cứu Antihypertensive and Lipid- Lowering Treatment to Prevent Heart Attack Trial (ALLHAT) đặt ra vấn đề từng nhóm thuốc hạ áp có thể ngăn suy tim nhiều hơn trên bệnh nhân THA kèm ĐTĐ. Có 3 thuốc được sử dụng: amlodipine, lisinopril và chlorthalidone. Sau thời gian theo dõi trung bình 4,9 năm; nhóm sử dụng chlorthalidone có tần suất suy tim mới xuất hiện thấp nhất so với 2 nhóm còn lại (36)
7.1.3. Các thuốc sử dụng nhằm phòng ngừa hay điều trị suy tim do đái tháo đường
– Chẹn bêta:
Các chẹn bêta có thể sử dụng trong điều trị suy tim bao gồm: metoprolol, carvedilol, bisoprolol và bucindolol.
Nghiên cứu Carvedilol or Metoprolol European Trial (COMET) sử dụng chẹn bêta điều trị suy tim có NYHA 2 đến 4 trong thời gian trung bình 5 năm. Có 24% bệnh nhân ĐTĐ trong nghiên cứu này. Kết quả cho thấy lợi điểm của carvedilol giảm tử vong có ý nghĩa tương tự giữa 2 nhóm bệnh nhân suy tim có ĐTĐ và nhóm suy tim không ĐTĐ (37) 80
– Ức chế men chuyển
Nghiên cứu GISSI – 3 chứng minh lisinopril giảm tử vong vào tuần 6 và tháng 6 khi dùng sớm sau NMCT cấp. Tuy nhiên lisinopril không giảm tần suất suy tim. Nghiên cứu TRACE sử dụng trandolapril vào ngày 2 – 6 sau NMCT cấp ở nhóm bệnh có PXTM < 35%. So với nhóm placebo, nhóm có trandolapril giảm 62% tiến triển đến suy tim nặng ở nhóm có ĐTĐ (p < 0,001). Lợi điểm này không thấy ở nhóm không ĐTĐ (38) 32
– Chẹn thụ thể angiotensin II
Nghiên cứu Reduction in Endpoints in NIDDM with the Angiotensin II Antagonist Losartan (RENAAL) thực hiện trên bệnh nhân ĐTĐ týp 2 có kèm bệnh thận và không tiền sử suy tim. Các bệnh nhân được chia ra 2 nhóm, nhóm losartan và nhóm placebo; nhóm placebo có kèm thuốc điều trị THA quy ước khác. Sau 4 năm, tần suất suy tim ở nhóm losartan giảm 32% (p = 0,005) (39).
Trong nghiên cứu Losartan Intervention For Endpoint Reduction (LIFE), 1195 bệnh nhân ĐTĐ kèm dầy thất trái được chia 2 nhóm, nhóm có losartan và nhóm aténolol nhằm điều trị THA. Sau thời gian trung bình 4,7 năm; nhóm losartan giảm các tiêu chí chính (tử vong tim mạch, NMCT và đột quỵ) và giảm 41% số lần nhập viện vì suy tim (p = 0,013) (40)
– Chất đối kháng aldosterone
Nghiên cứu Eplerenone Post – Acute Myocardial Infarction Heart Failure Efficacy and Survival Study (EPHESUS), sử dụng eplerenone thêm vào điều trị tối đa suy tim (UCMC, chẹn bêta, lợi tiểu, aspirin) so sánh với placebo. Nhóm có eplerenone giảm tử vong tim mạch hoặc nhập viện có ý nghĩa thống kê (p = 0,002). Lợi điểm này có cả ở 32% ĐTĐ trong nghiên cứu này (41)
8. ĐIỀU TRỊ ĐÁI THÁO ĐƯỜNG TRÊN BỆNH NHÂN BỆNH ĐMV, HỘI CHỨNG ĐMV CẤP HOẶC SUY
TIM
8.1. Sulfonylureas
Trong thập niên 70, có quan ngại là một số sulfonylureas như tolbutamide có thể làm tăng tử vong tim mạch và bệnh ĐMV trên bệnh nhân ĐTĐ typ 2 khi so sánh với insulin.
Tuy nhiên nghiên cứu UKPDS (15, 35) chứng minh sulfonylureas không làm tăng thiếu máu cơ tim. Trong 10 năm điều trị của nghiên cứu này, nhóm bệnh nhân sử dụng chlorpropamide hoặc glibenclamide có tần số NMCT và đột tử tương đương nhóm sử dụng insulin.
Nghiên cứu mới ADVANCE, thực hiện trên 11140 bệnh nhân ĐTĐ týp 2 (47), các bệnh nhân được phân phối ngẫu nhiên ra 2 nhóm: nhóm kiểm soát chặt đường huyết bằng glicazide MR (Diamicron MR®) (HbAc = 6.5%) và nhóm kiểm soát tiêu chuẩn (các sulfonylurea khác, ngoại trừ glicazide) HbA1c 7.3%. Thời gian theo dõi trung bình là 5 năm. Kết quả thu được là nhóm kiểm soát chặt đường huyết bằng glicazide MR đã giảm biến cố mạch máu lớn và mạch máu nhỏ phối hợp (p= 0,013), đặc biệt giảm 21% biến chứng thận.
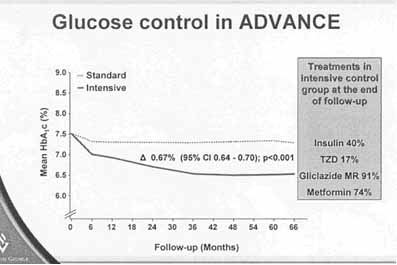
Hình 9: Kiểm soát đường máu trong nghiên cứu ADVANCE
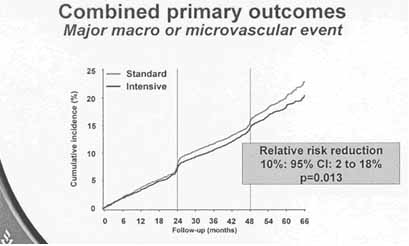
Hình 10: Biến cố mạch máu lớn và vi mạch phối hợp/ nghiên cứu ADVANCE
8.2. Thiazolidinediones
Hai thiazolidinediones (TZDs) sử dụng trong lâm sàng là rosiglitazone và pioglitazone. Nhóm thuốc này tăng nhạy cảm insulin ở các mô mục tiêu. Ngoài tác dụng làm giảm đường máu, TZDs còn có hiệu quả chống huyết khối, chống viêm, cải thiện chức năng nội mạc do cơ chế tác dụng qua hoạt hóa thụ thể PPAR gamma.
Không nên sử dụng TZDs ở bệnh nhân ĐTĐ có suy tim độ 3 hay 4, do thuốc làm tăng giữ nước và phù. Có thể phối hợp TZDs với sulfonylureas, metformin và insulin (42). Khi phối hợp TZDs với insulin, có thể giảm từ 2 lần tiêm insulin xuống 1 lần/ ngày.
8.2. Metformin
Metformin giảm đường máu qua 2 tác dụng: tăng nhậy cảm insulin và giảm sản xuất glucose từ gan. Nghiên cứu gần đây theo dõi trung bình 5,1 năm cho thấy metformin đơn độc hay metformin phối hợp sulfonylureas giảm tử vong có ý nghĩa hơn nhóm sulfonylurea đơn độc (43).
Nguy cơ lactic acidosis của bệnh nhân bệnh phổi nặng, suy thận mạn (tăng creatinine máu, > 1,4mg% ở nữ và > 1,5mg% ở nam) và suy tim làm giảm oxy máu. Không nên sử dụng metformin ở bệnh nhân suy tim cần điều trị bằng thuốc (43).
8.3. Thuốc ức chế alpha-glucosidase
Hai chất acarbose và miglitol tác động ở ruột non, ngăn cản hoạt động của men alpha-glucosidase ở niêm mạc ruột; do đó làm chậm hấp thu carbohydrate. Chỉ khoảng 1% thuốc hấp thu vào máu. Các thuốc này giảm khoảng 30% đường máu sau ăn và giảm 10% đường máu lúc đói. Dùng đơn độc thường không đủ hiệu quả, cần kết hợp với các thuốc trị ĐTĐ khác.
8.4. Repaglinide
Thuốc mới, có tác dụng tăng tiết insulin qua tác dụng trên thụ thể khác với thụ thể tác dụng của sulfonylureas trên kênh K-ATP. Thời gian bán hủy của thuốc khoảng 3,7 giờ; do đó có hiệu quả hạ đường máu sau ăn cao hơn là hạ đường máu lúc đói. Thuốc được dùng ở người cao tuổi và ở bệnh nhân ĐTĐ có kèm suy thận mạn.
8.5. Insulin
Dù là ĐTĐ týp 2, tiến triển tự nhiên của loại này cũng sẽ là suy tế bào bêta. Do đó, sau khoảng 10 năm điều trị có hiệu quả bằng sulfonylureas, các b/n ĐTĐ týp 2 cũng sẽ cần insulin phụ trợ. Có thể sử dụng đơn độc insulin hoặc phối hợp với các thuốc uống điều trị ĐTĐ. Khác với hiện tượng tăng insulin nội sinh; insulin ngoại lai dùng điều trị ĐTĐ không làm tăng tật bệnh hoặc tử vong tim mạch.
8.6. Nguyên tắc điều trị đái tháo đường trên bệnh nhân tim mạch
Dựa vào các nghiên cứu UKPDS (td: UKPDS 34, UKPDS 35, UKPDS 39…); nghiên cứu ADVANCE và một số nghiên cứu khác, các nguyên tắc sau cần thực hiện khi điều trị ĐTĐ trên bệnh nhân tim mạch:
– Đối với ĐTĐ týp 2, cần giảm đường máu tích cực (đường máu lúc đói < 108mg/dl), tối ưu hóa mức HbA1C bằng sulfonylureas, các thuốc tăng nhậy cảm insulin hoặc phối hợp với insulin khi cần có thể giữ HbA1C ở mức 6.5%
– Đối với ĐTĐ týp 1, nên áp dụng kiểu điều trị tiêm insulin nhiều lần trong ngày hoặc sử dụng bơm insulin.
– Cần kiểm soát chặt chẽ huyết áp, giữ mức < 130/80mmHg.
– Không sử dụng nhóm TZDs ở bệnh nhân suy tim độ 3 hay 4.
– Cẩn thận khi sử dụng metformin ở bệnh nhân suy tim suy thận, suy hô hấp mạn để tránh biến chứng lactic acidosis.
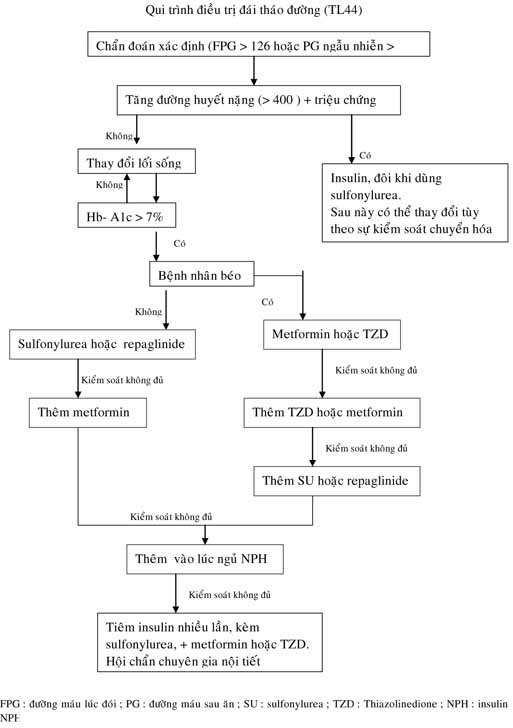
Qui trình sau (sơ đồ) có thể được áp dụng điều trị ĐTĐ (TL 44).
TÀI LIỆU THAM KHẢO
1. Malmberg K, Yusuf S, Gerstein HC et al. Impact of diabetes on long – term prognosis in patients with unstable angina and non Q – wave myocardial infarction: results of the OASIS (Organization to Assess Strategies for Ischemic Syndromes) Registry. Circulation 2000; 102: 1014
2. Nichols GA, Hillier TA, Erbey JR et al. Congestive heart failure in type 2 diabetes: Prevalence, incidence and risk factors. Diabetes Care 2001; 24: 1614
3. Report of the Expert Committee on the Diagnosis and Classification of Diabetes Mellitus. Diabetes Care 1997; 20: 1183 – 1197
4. Haffner SM, Lehto S, Ronnemaa T et al. Mortality from coronary heart disease in subjects with type 2 diabetes and in nondiabetic subjects with and without prior myocardial infarction. N Engl J Med 1998; 339: 229 – 234
5. Stamler J, Vaccaro O, Neaton JD et al. Diabetes, other risk factors and 12 year cardiovascular mortality for men screened in the Multiple Risk Factor Intervention Trial. Diabetes Care 1993; 16: 434 – 444
6. Hart CL, Hole DJ, Smith GD. Risk factors and 20 year stroke mortality in men and women in the Renfrew/ Paisley Study in Scotland. Stroke 1999; 30: 1999 – 2007
7. Beckman JA, Creager MA, Libby P. Diabetes and atherosclerosis: epidemiology, pathophysiology and management. JAMA 2002; 287: 2570 – 2581
8. Kannel WB, McGee DL. Update on some epidemiologic features of intermittent claudication: the Framingham Study. J Am Geriatr. Soc 1985; 33: 13 – 18
9. Beckman JA, Libby P, Creager MA. Diabetes Mellitus, the Metabolic Syndromes and Atherosclerotic Vascular Disease.
In Brauwald’s Heart Disease; ed by D. Zipes, P. Libby, R. Bonow, E. Braunwald. WB Saunders 2005, 7th ed, p. 1035 – 1046
10. Collins R, Armitage J, Parish S et al. MRC/ BHF Heart Protection Study of Cholesterol lowering with simvastatin in 5963 people with diabetes: a randomized placebo – controlled trial. Lancet 2003; 361: 2005 – 2010
11. Rubins HB, Robins SJ, Collins D et al. Gemfibrozil for the secondary prevention of coronary heart disease in men with low levels of high density lipoprotein cholesterol. Veterans Affairs HDL – Cholesterol Intervention Trial Study Group. N Engl J Med 1999; 341: 410 – 418
12. Neve BP, Corseaux D, Chinette G et al. PPARalpha agonists inhibit tissue factor expression in human monocytes and macrophages. Circulation 2001; 103: 207 – 212
13. JNC 7 Report. JAMA 2003; 289: 2560 – 2572
14. Mehler PS, Coll JR, Estacio R et al. Intensive blood pressure control reduces the risk of cardiovascular events in patients with peripheral arterial disease and type 2 diabetes. Circulation 2003; 107: 753 – 756
15. UKPDS Group. Efficacy of atenolol and captopril in reducing risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 39. BMJ 1998; 317: 713 – 720
16. Staessen JA, Fagard R, Thijs L et al. Randomised double – blind comparison of placebo and active treament for older patients with isolated systolic hypertension. The Systolic Hypertension in Europe (Syst – Eur) Trial Investigators. Lancet 1997; 350: 757 – 764
17. Colwell JA. Aspirin therapy in diabetes. Diabetes Care 2003; 26: S87
18. CAPRIE steering committee. A randomised, blinded trial of clopidogrel versus aspirin in patients at risk of ischemic events. Lancet 1996; 348: 1329
19. Bhatt DL, Marso SP, Hirsch AT et al. Amplified benefit of clopidogrel versus aspirin in patients with diabetes mellitus. Am J Cardiol 2002; 90: 625
20. Yusuf S, Zhao F, Mehta SR et al. Effects of clopidogrel in addition to aspirin in patients with acute coronary syndrome without ST segment elevation. N Engl J Med 2001; 345: 494
21. Kereiakes DJ, Lincoff AM, Anderson KM et al. Abciximab survival advantages following percutaneous coronary intervention is predicted by clinical risk profile. Am J Cardiol 2002, 90: 628
22. Topol EJ, Mark DB, Lincoff AM et al. Outcomes at 1 year and economic implications of platelet glycoprotein IIb/IIIa blockade in patients undergoing coronary stenting: results from a multicenter randomised trial. EPISTENT investigators. Lancet 1999; 354: 2019
23. Labinaz M, Madan M, O’shea JO et al. Comparison of one – year outcomes following coronary artery stenting in diabetic versus non – diabetic patients (from the Enhanced Suppression of the Platelet IIb/IIIa Receptor with Integrilin Therapy (ESPRIT) Trial). Am J Cardiol 2002; 90: 585
24. Chen J, Marcinicak TA, Radford MF et al. Beta blocker therapy for secondary prevention of myocardial infarction in elderly diabetic patients. Results from the National Cooperative Cardiovascular Project. J Am Coll Cardiol 1999; 34: 1388
25. Zuanetti G, Latini R, Maggioni AP et al. Effect of the ACE inhibitor lisinopril on mortality in diabetic patients with acute myocardial infarction: data from the GISSI – 3 study. Circulation 1997; 96: 4239
26. Effects of ramipril on cardiovascular and microvascular outcomes in people with diabetes mellitus: results of the HOPE study and MICRO – HOPE substudy. Lancet 2000; 355: 253
27. McFarlane SI, Kumar A, Sowers JR. Mechanisms by which angiotensin – converting enzyme inhibitors prevent diabetes and cardiovascular disease. Am J Cardiol 2003; 91: 30H
28. Malmberg K, Norhammar A, Wedel H et al. Longterm results from the Diabetes and Insulin Glucose Infusion in Acute Myocardial Infarction (DIGAMI) study. Circulation 1999; 99: 2626
29. Furnary AP, Gao G, Grunhemeier GL et al. Continuous insulin – infusion reduces mortality in patients with diabetes undergoing coronary artery bypass grafting. J Thorac Cardiovasc Surg 2003; 125: 1007
30. Abizaid A, Costa MA, Centemero M et al. Clinical and economic impact of diabetes mellitus on percutaneous and surgical treatment of multivessel coronary disease patients: Insights from the Arterial Revascularization Therapy (ARTS) trial. Circulation 2001; 104: 533 – 538
31. Moses JW, Leon MB, Popma JJ et al. Sirolimus – eluting stents versus standard stents in patients with stenosis in a native coronary artery. N Engl J Med 2003; 349: 1315 – 1323
32. Moses J, Leon M, Popma J et al. Angiographic and clinical outcomes after a sirolimus- eluting stent compared to a standard stent in patients with complex coronary stenoses. N Engl J Med 2003; 349: 1315
33. Levy D, Larson MG, Vasan RS et al. The progression from hypertension to congestive heart failure. JAMA 1996; 275: 1557
34. Iribarren C, Karter AJ, Go AS et al. Glycemic control and heart failure among adult patients with diabetes. Circulation 2001; 103: 2668
35. Stratton IM, Adler AI, Neil HA et al. Association of glycemia with macrovascular and microvascular complications in type 2 diabetes (UKPDS 35): prospective observational study. BMJ 2000; 321: 405
36. The ALLHAT Investigators. Major outcomes in high – risk hypertensive patients randomized to angiotensin converting enzyme inhibitor or calcium channel blocker vs diuretic: the ALLHAT trial. JAMA 2002; 288: 2981
37. Poole- Wilson PA, Swedberg K, Cleland JG et al. Comparison of carvedilol and metoprolol on clinical outcomes in patients with chronic heart failure. The Carvedilol or Metoprolol European Trial (COMET). Lancet 2003; 362: 7
38. Gustafsson I, Torp – Pedersen C, Kober L et al. Effect of the angiotensin – converting inhibitor trandolapril on mortality and morbidity in diabetic patients with left ventricular dysfunction after acute myocardial infarction. J Am Coll Cardiol 1999; 34: 83
39. Brenner BM, Cooper ME, de Zeeuw D et al. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Engl J Med 2001; 345: 861
40. Lindholm LH, Ibsen H, Dahlof B et al. Cardiovascular morbidity and mortality in patients with diabetes in the Losartan Intervention For Endpoints reduction in hypertension study (LIFE). Lancet 2002; 359: 1004
41. Pitt B, Remme W, Zannad F et al. Eplerenone, a selective aldosterone blocker in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med 2003; 348: 1309
42. Wooltorton E. Rosiglitazone (Avandia) and pioglitazone (Actoz) and heart failure. Can Med Assoc J 2002; 166; 219
43. Bailey CJ, Turner RC. Metformin. N Engl J Med 1996; 334: 574
44. Farkouh ME, Elliot JR, Fuster V. Diabetes and cardiovascular disease. In Hurst’s The Heart ed by V.Fuster, RW Alexander, RA O’Rourke. McGraw Hill 2004, 11th ed, p.2098 – 2125
45. Mancia G et al. European Society of Cardiology and European Society of Hypertension 2007 Guidelines for the management of Arterial Hypertension. Eur. H. Journal, June 11,2007
46. The ADVANCE Collaborative Group. Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomized controlled trial. Lancet 2007; 370: 829-840
47. The ADVANCE Collaborative Group. Intensive blood glucose control in patients with type 2 Diabetes N. Engl J Med 358:24 www. NEJM. ORG June, 12, 2008. XEM PHẦN I