Tái thông hoàn toàn nên được thực hiện ngay lập tức trong STEMI: Ưu và nhược điểm
Giới thiệu
Bệnh đa mạch vành thường xảy ra ở những bệnh nhân bị nhồi máu cơ tim ST chênh lên (STEMI). Các hướng dẫn hiện hành của Châu Âu về hội chứng mạch vành cấp (ACS) khuyến cáo tái thông hoàn toàn ở những bệnh nhân này, nhưng không có sự đồng thuận về thời điểm tối ưu. Như vậy, can thiệp mạch vành qua da (PCI) của các nhánh không phải động mạch thủ phạm (IRA) có thể được thực hiện ngay lập tức (trong thì đầu PCI) hoặc theo chương trình (trong vòng 45 ngày). Mặc dù tái thông mạch hoàn toàn ngay lập tức có thể làm giảm việc sử dụng thuốc cản quang và nhiễm xạ và có thể thực tế hơn khi làm thủ thuật ngoài giờ, nhưng có những yếu tố ủng hộ cách tiếp cận theo chương trình, bao gồm nguy cơ viêm huyết khối cao, đánh giá chưa đầy đủ về nhánh mạch vành không thủ phạm (non-IRAs) và thiếu thông tin về tiền sử bệnh nhân và bệnh đi kèm khi sử dụng chiến lược can thiệp tức thì. Cả hai chiến lược này đều có ưu và nhược điểm và thời điểm tối ưu để tái thông mạch hoàn toàn vẫn còn là chủ đề tranh luận.
Ưu điểm (Theo Adnan Kastrati, MD; Thorsten Kessler, MD)
PCI tiên phát điều trị sang thương thủ phạm là tiêu chuẩn điều trị cho bệnh nhân STEMI. Các bằng chứng hiện tại ủng hộ lợi ích của tái thông mạch máu hoàn toàn (CR- complete revascularisation) so với chỉ PCI sang thương thủ phạm trong STEMI có bệnh đa mạch máu (MVD- multiple vessel disease) và các hướng dẫn hiện hành đưa ra khuyến cáo loại I. Mặc dù có sự nhất trí rộng rãi rằng CR là chiến lược tốt nhất cho bệnh nhân STEMI và MVD nhưng vẫn chưa có sự đồng thuận về thời điểm thực hiện PCI nhánh không thủ phạm khi bệnh nhân được làm thủ thuật hay nhập viện. Cho đến gần đây, vẫn còn thiếu bằng chứng so sánh trực tiếp giữa chiến lược CR tức thì và chiến lược CR chương trình. Lợi ích chính đáng của CR tức thì bao gồm làm ổn định các mảng xơ vữa dễ đứt vỡ, thường gặp hơn ở các sang thương không phải thủ phạm trong bối cảnh viêm huyết khối cấp tính ở STEMI và tránh phải nhập viện nhiều lần, giảm chi phí và sự bất tiện cho bệnh nhân. Mặt khác, CR ngay lập tức được coi là có liên quan đến việc tăng sử dụng chất cản quang, liều bức xạ cao hơn và có thể là thách thức lớn hơn đối với nhóm can thiệp khi làm thủ thuật ngoài giờ. Do đó, hướng dẫn của hiệp hội Tim mạch Châu Âu (ESC) năm 2023 về quản lý hội chứng vành cấp không cụ thể về thời điểm tối ưu của PCI đối với các sang thương không thủ phạm ở bệnh nhân STEMI và khuyến cáo rằng nên được thực hiện theo chương trình hoặc trong vòng 45 ngày.
Kết quả của 2 thử nghiệm ngẫu nhiên có đối chứng (RCT) so sánh trực tiếp CR tức thì và CR chương trình ở bệnh nhân ACS có MVD đã được công bố gần đây. Định nghĩa CR bao gồm can thiệp tất cả các tổn thương có đường kính hẹp ≥70%. Bệnh nhân bị sốc tim, đã làm phẫu thuật bắc cầu động mạch vành trước đây và tắc mạn hoàn toàn bị loại khỏi các thử nghiệm này. Trong cả hai thử nghiệm, tiêu chí chính sau 1 năm bao gồm tử vong do mọi nguyên nhân, nhồi máu cơ tim không tử vong, đột quỵ và tái thông mạch máu do thiếu máu cục bộ ngoài kế hoạch và trong thử nghiệm MULTISTARS AMI là nhập viện vì suy tim. Đánh giá chức năng của đoạn hẹp hoặc hình ảnh nội mạch được sử dụng ở 10-20% bệnh nhân và thường được thực hiện hơn ở nhóm CR chương trình. Tổng lượng thuốc cản quang, liều lượng/thời gian bức xạ, thời gian thực hiện thủ thuật và thời gian nằm viện ở nhóm CR chương trình đều cao hơn.
Thử nghiệm BIOVASC bao gồm toàn bộ bệnh nhân có ACS và trong đó STEMI chiếm khoảng 40% trong số 1,525 bệnh nhân tham gia. Các thủ thuật ngoài giờ được thực hiện ở 28% bệnh nhân và đạt được CR trong 96% trường hợp. Thời gian trung bình để thực hiện thủ thuật theo chương trình là 15 ngày (bách phân vị thứ 25 và 75 tương ứng là: 4 và 28). Sau 1 năm, không có sự khác biệt đáng kể về xuất huyết nặng hoặc tử vong do mọi nguyên nhân (1.9% ở nhóm CR ngay lập tức và 1.2% ở nhóm CR theo chương trình).
Thử nghiệm MULTISTARS AMI xem xét cụ thể vai trò của CR tức thì ở bệnh nhân STEMI (n=840). Tiêu chuẩn loại trừ bổ sung cho thử nghiệm này bao gồm sang thương ở nhánh trái chính và suy thận nặng. Thời gian trung vị để tiến hành can thiệp theo chương trình là 37 ngày (30-43). Thủ thuật đã đạt được CR ở 91% bệnh nhân. Tỷ lệ suy thận cấp hoặc cần điều trị thay thế thận là khoảng 3% và không khác biệt có ý nghĩa giữa hai nhóm. Sau 1 năm, không có sự khác biệt có ý nghĩa về xuất huyết nặng và tử vong do mọi nguyên nhân (2.9% ở nhóm CR ngay lập tức và 26% ở nhóm CR chương trình).
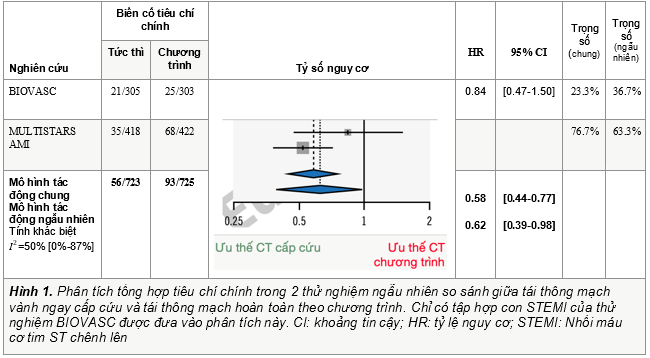
Như trong mô hình tác động ngẫu nhiên ở Hình 1, chiến lược CR tức thì đã giảm đáng kể (38%) nguy cơ về tiêu chí chính. Giảm tỷ lệ nhồi máu cơ tim tái phát, chủ yếu là quanh thủ thuật và giảm tỷ lệ tái thông ngoài kế hoạch là những yếu tố của lợi ích quan sát được. Mặc dù có hạn chế trong độ chính xác chẩn đoán nhồi máu tái phát trong STEMI cấp so với các giai đoạn sau, cả hai thử nghiệm đều cho thấy rõ ràng rằng ít nhất không có sự đánh đổi nào về kết cục khi thực hiện CR tức thì, bao gồm hậu cần, chi phí và sự thuận tiện cho bệnh nhân. Một RCT khác gần đây, thử nghiệm FIRE, cho thấy chiến lược CR tức thì là khả thi, an toàn và hiệu quả, ngay cả ở những bệnh nhân từ 75 tuổi trở lên.
Tóm lại, không có RCT nào có thể thay thế cho việc đánh giá lâm sàng cẩn thận và ra quyết định điều trị cho từng bệnh nhân. Tuy nhiên, bằng chứng mới được đưa ra vào năm 2023 cung cấp sự hỗ trợ đầy đủ cho CR ngay lập tức như một chiến lược tái thông mạch máu được ưu tiên ở phần lớn bệnh nhân STEMI và MVD.
Nhược điểm (theo Salvatore Brugaletta, MD, Tiến sĩ; Riccardo Rinaldi, MD)
Hướng dẫn mới nhất của ESC về hội chứng mạch vành cấp khuyến cáo xem xét tái thông mạch máu hoàn toàn thường quy ở bệnh nhân STEMI mắc bệnh đa mạch máu trong vòng 45 ngày, nhưng không có thông cáo rõ ràng nào về việc liệu nên thực hiện ngay sau khi điều trị sang thương thủ phạm hay muộn hơn, trước hoặc sau khi xuất viện. Tuy nhiên, ở những bệnh nhân ACS có biểu hiện sốc tim và bệnh nhiều nhánh mạch máu, các hướng dẫn hiện hành rõ ràng khuyến cáo điều trị ngay lập tức tổn thương thủ phạm và PCI chương trình cho những sang thương không thủ phạm sau đó. Khuyến cáo này dựa trên kết quả của thử nghiệm CULPRIT SHOCK, cho thấy tỷ lệ tử vong do mọi nguyên nhân hoặc điều trị thay thế thận trong 30 ngày cao hơn khi so sánh chiến lược CR tức thì so với chiến lược CR theo chương trình.
Ngoài những dữ liệu này, có một số điểm cần lưu ý đối với việc tái thông hoàn toàn ngay lập tức đối với STEMI đa nhánh mạch máu (Hình 2).
Thứ nhất, người ta biết rằng có một mức độ co mạch nhất định trong giai đoạn cấp của STEMI có thể dẫn đến đánh giá quá mức tình trạng hẹp mạch vành và khả năng dùng các stent nhỏ hơn mức độ hẹp thực của mạch vành một cách không cần thiết, do đó, có thể tạo ra các biến cố lâm sàng sau đó.
Điểm thứ hai liên quan đến việc làm thế nào để quyết định, tại thời điểm thực hiện thủ thuật cấp cứu, liệu các sang thương non-IRA có nên được điều trị hay không. Quyết định lúc đó dựa trên dữ liệu hạn chế thường có sẵn tại thời điểm đó liên quan đến bệnh sử lâm sàng của bệnh nhân (chẳng hạn như tiền sử các cơn đau thắt ngực, phân suất tống máu thất trái, v.v.); thêm vào đó là các chỉ số sinh lý (ví dụ: lưu lượng dự trữ vành) trong giai đoạn cấp tính của STEMI có rất ít giá trị và hoàn toàn không được khuyến nghị theo hướng dẫn ESC ACS 2023.
Điểm thứ ba liên quan đến liệu pháp kháng tiểu cầu. Mặc dù nhìn chung stent phủ thuốc thế hệ mới an toàn với tỷ lệ huyết khối thấp, ngay cả các thuốc kháng tiểu cầu đường uống mạnh nhất cũng cần thời gian để đạt được sự ức chế tiểu cầu tối ưu, ngụ ý rằng thực hiện tái thông mạch máu hoàn toàn tức thì cho STEMI có thể là tình huống kháng tiểu cầu làm việc dưới mức tối ưu.
Cuối cùng nhưng không kém phần quan trọng, tiến hành các thủ thuật PCI phức tạp (chỗ chia nhánh, tắc mạn hoàn toàn, sang thương dài và vôi hóa) trong giai đoạn cấp ngay sau khi tái thông sang thương thủ phạm làm chậm trễ việc điều trị tích cực, chưa có dữ liệu chứng minh rằng thời gian và nỗ lực dành thêm cho PCI bổ sung có thể chuyển thành lợi ích lâm sàng rõ ràng về các tiêu chí chính như tử vong hoặc nhồi máu cơ tim tái phát hay không.
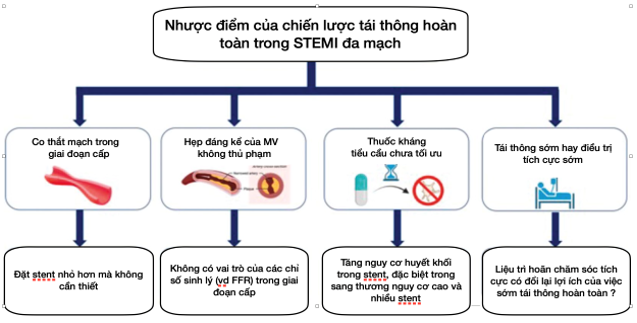
Hình 2. Nhược điểm của chiến lược tái thông mạch máu hoàn toàn ngay lập tức trong STEMI nhiều nhánh. FFR: lưu lượng dự trữ vành; STEMI: Nhồi máu cơ tim ST chênh lên
Lược dịch từ Complete revascularisation should be immediate in STEMI: pros and cons
Một thế kỷ của suy tim phân suất tống máu giảm: Ban đầu không có gì mới, sau đó là sự phát triển nhanh chóng
Hội chứng lâm sàng của suy tim (HF), bao gồm một tập hợp các dấu hiệu và triệu chứng đã được công nhận trong hơn một thế kỷ. Những bước phát triển trong hơn 100 năm trước khá mờ nhạt như: khám phá từ nghiên cứu cơ bản, việc sử dụng các loại thuốc nghiên cứu, các thử nghiệm lâm sàng quan trọng. Tuy nhiên, thế kỷ này đã chứng kiến sự giảm tỷ lệ mắc bệnh và tử vong ở nhóm bệnh nhân có số lượng lớn này. Thật vậy, các đánh giá gần đây đã ước tính rằng việc sử dụng tối ưu các liệu pháp điều trị suy tim với phân suất tống máu giảm (HFrEF) có thể kéo dài thêm 2 đến 8 năm không tử vong do tim mạch hoặc nhập viện do suy tim, tùy thuộc vào độ tuổi của bệnh nhân khi khởi phát bệnh.
SỰ PHÁT TRIỂN NỀN TẢNG
Năm 1924, Willem Einthoven đoạt giải Nobel Y học cho sự phát triển của máy điện tâm đồ, dẫn đường cho ngành tim mạch. Nguyên nhân phổ biến nhất của HFrEF: bệnh động mạch vành, xuất hiện như một tai họa của thời hiện đại. Werner Forssman, một bác sĩ tiết niệu, đã tự thực hành đặt catheter thông tim lần đầu tiên trên người ông vào năm 1929. Quy trình này được André Frédéric Cournand và Dickinson W. Richards phát triển như một phương pháp thường quy trong những năm sau đó (cả 3 người đều nhận được giải Nobel năm 1956). Tuy nhiên, phải đến năm 1953, mô tả đầu tiên về siêu âm tim mode M của Inge Edler và Hellmuth Hertz mới đánh dấu khởi đầu của sự phát triển một kỹ thuật không xâm lấn quan trọng trong suy tim.
Những hiểu biết về sinh lý bệnh
Charles A. Chidsey, Donald C. Harrison và Eugene Braunwald đã mô tả phản ứng tăng cường catecholamine khi tập thể dục ở bệnh nhân suy tim trong các ấn phẩm từ năm 1962 và 1963. Họ và những người khác đã chứng minh vai trò then chốt của hệ thần kinh giao cảm trong sinh bệnh học trong hội chứng suy tim, mở ra những thử nghiệm lâm sàng đầu tiên về ức chế β của Finn Waagstein và các đồng nghiệp ở Thụy Điển được báo cáo vào năm 1975. Braunwald, John Ross Jr, và Edmund H. Sonnenblick đã xuất bản một loạt bài gồm 5 phần trên tạp chí New England Journal of Medicine về cơ chế co bóp của tim bình thường và tim suy vào năm 1967. Chatterjee và cộng sự đã viết một nghiên cứu mang tính bước ngoặt vào năm 1973 với tựa đề “Đáp ứng huyết động và chuyển hóa với liệu pháp giãn mạch trong nhồi máu cơ tim cấp”. Phương pháp điều trị mới này cho bệnh nhân suy tim cấp thứ phát sau nhồi máu cơ tim là phương pháp điều trị chính cho đến khi tiêu sợi huyết trở thành thường quy.
Những tiến bộ về trị liệu y tế
Năm 1977, Cohn và Franciosa đã phác thảo cơ sở lý luận cho liệu pháp giãn mạch đối với HFrEF trong một loạt bài gồm 2 phần, tiếp theo là bắt đầu thử nghiệm đa trung tâm đầu tiên ở bệnh nhân suy tim mạn vào năm 1980: V-HeFT I (Vasodilator–Heart Failure Trial- Thử nghiệm giãn mạch-Suy tim). Thử nghiệm này cho thấy tỷ lệ tử vong ở bệnh nhân dùng hydralazine và isosorbide dinitrate (H-I) giảm 23% so với giả dược sau 3 năm, đánh dấu sự khởi đầu hy vọng điều trị thành công bệnh suy tim. Mặc dù chủng tộc và sắc tộc ban đầu không được mô tả cho 630 bệnh nhân, nhưng 29% số người tham gia là người da đen và bị tăng huyết áp nhiều hơn cũng như ít mắc bệnh mạch vành hơn so với những người da trắng. Tỷ lệ tử vong không khác nhau giữa những người tham gia da đen và da trắng khi dùng giả dược. Chỉ những bệnh nhân da đen dùng H-I cho thấy tỷ lệ tử vong giảm; ở bệnh nhân da trắng thì không có sự khác biệt khi so sánh với giả dược. Quan sát đáng chú ý này không được báo cáo cho đến năm 1999 và nhấn mạnh nhu cầu cấp thiết về sự đa dạng trong quần thể thử nghiệm lâm sàng. Nếu tất cả bệnh nhân trong thử nghiệm đều là người da trắng thì khái niệm liệu pháp giãn mạch mạn tính cho HFrEF có thể đã bị loại bỏ.
Dzau và cộng sự đã tóm tắt vai trò của hệ thống renin-angiotensin-aldosterone trong suy tim vào năm 1981 và đến năm 1985, CONSENSUS (Cooperative North Scandinavian Enalapril Survival Study- Nghiên cứu tỷ lệ sống sót của Enalapril trên cộng đồng Bắc Scandinavia) đã tuyển chọn bệnh nhân, cũng như SOLVD (Studies of Left Ventricular Dysfunction -Nghiên cứu về rối loạn chức năng thất trái) cho bệnh nhân suy tim có triệu chứng vào năm 1986. Cả hai thử nghiệm đều đánh giá vai trò của thuốc ức chế men chuyển angiotensin (ACEi), một nhóm thuốc ban đầu được sử dụng để điều trị tăng huyết áp. Đồng thời, vai trò của ức chế β trong bệnh suy tim mạn đã được khám phá trong một số thử nghiệm với metoprolol tác dụng kéo dài hoặc carvedilol, bắt đầu từ năm 1993.
Sự kết hợp giữa thuốc ức chế men chuyển và thuốc chẹn beta đã thành công trong việc giảm tỷ lệ mắc bệnh và tử vong cũng như tỷ lệ đột tử do tim, đến mức các bác sĩ lâm sàng không thể tin rằng một loại thuốc cũ như spironolactone lại có thể mang lại nhiều lợi ích lâm sàng. Việc không kiểm soát được hệ thống aldosterone trong suy tim đã được giải quyết bằng một số chất đối kháng thụ thể mineralocorticoid, đáng chú ý nhất trong thử nghiệm RALES (Randomized Aldactone Evaluation Study- Nghiên cứu ngẫu nhiên đánh giá Aldactone), bắt đầu thu nhận bệnh nhân vào năm 1995, cho thấy tỷ lệ tử vong và tỷ lệ đột tử giảm đáng kinh ngạc. Vào cuối thế kỷ 20, việc điều trị HFrEF mạn đã được thiết lập vững chắc bao gồm thuốc ức chế men chuyển (hoặc thuốc ức chế thụ thể angiotensin), thuốc chẹn β và thuốc đối kháng thụ thể mineralocorticoid.
Nhiều nhóm thuốc khác nhau đã được đánh giá trong 2 thập kỷ qua, bao gồm một số thuốc tăng co bóp đường uống. Tranh luận về hiệu quả điều trị của digitalis và các thuốc tăng co bóp khác vẫn tiếp tục. Một loại thuốc mới ức chế endopeptidase đã được công bố và thử nghiệm trong một thử nghiệm sử dụng omapatrilat, xuất bản năm 2002. Kết quả không mấy hứa hẹn. Omapatrilat chặn 3 con đường thoái gián bradykinin, dẫn đến tỷ lệ phù mạch cao. Tuy nhiên, đến năm 2014, thử nghiệm PARADIGM-HF (Prospective Comparison of ARNI with ACEI to Determine Impact on Global Mortality and Morbidity in Heart Failure- So sánh tiến cứu giữa ARNI với ACEI để xác định tác động đối với tỷ lệ tử vong và bệnh tật toàn cầu trong suy tim) đã được công bố, cho thấy hiệu quả đáng kinh ngạc của một loại thuốc kết hợp, sacubitril và valsartan (sau này được biết đến như một chất ức chế thụ thể angiotensin/neprilysin), so với thuốc ức chế ACE trong HFrEF. Thuốc này mang lại lợi ích trong việc ức chế đồng thời hệ thống renin-angiotensin-aldosterone và ức chế neprilysin đồng thời giảm thiểu sự xuất hiện của phù mạch.
Tiến bộ trị liệu phẫu thuật
Năm 1967, ca ghép tim người thành công đầu tiên được thực hiện. Năm 1968, bác sĩ Sharon Hunt vẫn còn là sinh viên y khoa khi ca cấy ghép đầu tiên được thực hiện tại cơ sở của bà, đại học Stanford. Sau đó, bà và các đồng nghiệp của mình đã phát triển và xác định nguyên tắc chăm sóc bệnh nhân trước và sau ghép tim. Năm 2010, kỳ thi cấp chứng chỉ đầu tiên về suy tim chuyên sâu và ghép tim được tổ chức cho các bác sĩ chuyên khoa tim mạch.
Máy tạo nhịp tim điện tử đầu tiên được Rune Senning và Åke Elmqvist cấy ghép ở Thụy Điển vào năm 1958 bằng cách sử dụng phương pháp phẫu thuật lồng ngực. Năm 1980, bác sĩ Michel Mirowski và nhóm của ông đã đặt máy phá rung tim cấy được đầu tiên trên một bệnh nhân. Sự hiểu biết về các cơ chế sinh lý bệnh cơ bản trong điện sinh lý dần dần được xây dựng do tỷ lệ đột tử do tim cao ở bệnh nhân HFrEF. Việc cấy ghép thành công thiết bị hỗ trợ thất trái đầu tiên được bác sĩ Michael E. DeBakey hoàn thành vào năm 1966; 35 năm sau, vào năm 2001, kết quả thử nghiệm REMATCH (Randomized Evaluation of Mechanical Assistance for the Treatment of Congestive Heart Failure – Đánh giá ngẫu nhiên hỗ trợ cơ học trong điều trị suy tim sung huyết) được công bố so sánh việc điều trị bằng thiết bị hỗ trợ thất trái với điều trị nội khoa. Tỷ lệ sống sót sau 1 và 2 năm ở nhóm nội khoa của bệnh nhân suy tim nặng lần lượt là 25% và 8%; ngược lại, tỷ lệ sống sót khi dùng thiết bị là 52% và 23%.
Hướng dẫn điều trị nội khoa tối ưu
Cơ quan nghiên cứu và chính sách chăm sóc sức khỏe Hoa Kỳ đã công bố một trong những hướng dẫn thực hành lâm sàng sớm nhất về chăm sóc và đánh giá bệnh nhân HFrEF vào năm 1994. Một bảng các loại thuốc thường được sử dụng liệt kê 9 loại thuốc lợi tiểu, bao gồm cả spironolactone, 4 thuốc ức chế ACE, digoxin và H-I. Hướng dẫn thực hành lâm sàng đầu tiên của Hiệp hội tim mạch Hoa Kỳ/Trường môn tim mạch Hoa Kỳ về suy tim xuất hiện vào năm 1995. Tài liệu này đề cập đến cả HFrEF và “suy tim tâm trương”, đồng thời thúc giục sử dụng thuốc ức chế ACE ở tất cả bệnh nhân HFrEF (H-I là lựa chọn thay thế cho bệnh nhân không dung nạp thuốc ức chế ACE) và sử dụng thận trọng thuốc chẹn β sau nhồi máu cơ tim. Ghép tim đã được thảo luận như một lựa chọn, suy tim ở trẻ sơ sinh và trẻ em cũng được đề cập, cũng như vai trò của viêm cơ tim và một phác thảo dài về quản lý bệnh suy tim cấp cũng được đưa vào. Độ dài của toàn bộ hướng dẫn là 55 trang.
Ngày nay, liệu pháp điều trị theo hướng dẫn cho HFrEF bao gồm “tứ trụ” (thuốc chẹn β, thuốc ức chế men chuyển hoặc thụ thể angiotensin/thuốc ức chế neprilysin, chất đối kháng thụ thể mineralocorticoid và chất ức chế SGLT2). Các khuyến cáo cũng bao gồm cân nhắc sử dụng máy phá rung cấy được hoặc liệu pháp tái đồng bộ tim, phòng khám suy tim đa chuyên khoa hoặc kỹ thuật theo dõi từ xa. Bệnh nhân mắc bệnh cơ tim không do thiếu máu cục bộ hiện được đánh giá bằng một loạt phân tích di truyền. Ngay cả những lưu ý cuối đời trong HFrEF cũng đã được cải thiện.
KẾT LUẬN
Hai mươi năm trước, người viết bài này là đồng tác giả của một bài đánh giá về suy tim. Một số vấn đề lâm sàng phổ biến cho đến nay đã được giải quyết. Nhưng vẫn còn nhiều vấn đề chưa được giải quyết, bao gồm cách xác định bệnh nhân bệnh cơ tim có yếu tố gia đình ở giai đoạn sớm hơn, cách xác định bệnh nhân có nguy cơ đột tử cao, cách xác định ai sẽ được phù hợp nhất sử dụng các thiết bị hỗ trợ cơ học và cách chăm sóc tối ưu cho số lượng bệnh nhân suy tim ngày càng tăng. Một thách thức lớn đó là nỗ lực hết sức để kiểm soát tăng huyết áp và các yếu tố nguy cơ tim mạch nhằm ngăn ngừa hội chứng suy tim – hiện đạt được rất ít tiến bộ.
Lược dịch từ A Century of Heart Failure With Reduced Ejection Fraction: Mostly Drought, Followed by Rapid Progress







