BS. NGUYỄN THANH HIỀN
BS. LÊ NGỌC CÁT TƯỜNG*
BS. NGUYỄN ĐÌNH SƠN NGỌC**
*BS thực tập BV Đại Học Y Dược TP.Hồ Chí Minh
** BS Khoa nội Tim Mạch, BV ĐHYD TP.Hồ Chí Minh
Một số từ viết tắt
BSI – Bloodstream Infective: Nhiễm trùng huyết
CIED – Cardiac Implantable Electronic Device: Dụng cụ điện học cấy ghép ở tim
CIED-IE – Cardiac Implantable Electronic Device-related Infective Endocarditis: Viêm nội tâm mạc nhiễm trùng liên quan dụng cụ điện học cấy ghép trong tim.
EHRA – European Heart Rhythm Association: Hội Nhịp học Châu Âu
ICD – Implantable Cardioverter-Defibrillator: máy phá rung tim cấy ghép
IE – Infective Endocarditis: Viêm nội tâm mạc nhiễm trùng
non-SA GPC – non– Staphylococcus aureus gram- positive cocci
PET-CT – [18F]-fluorodeoxyglucose Positron Emission Tomography- Computed Tomography
SAB – Staphylococcus aureus Bacteremia: Vi khuẩn Staphyloccocus
TEE – Transesophageal echocardiography: Siêu âm tim qua thực quản
PCR – Polymerase Chain Reaction: Phản ứng chuỗi polymerase
SIRS – Systemic Inflammatory Response Syndrome: Hội chứng đáp ứng viêm toàn than
Tóm tắt
Viêm nội tâm mạc nhiễm trùng liên quan đến cấy ghép dụng cụ điện học tim (Cardiac implantable electronic device-related infective endocarditis – CIED-IE) bao gồm một loạt các hội chứng lâm sàng, gồm nhiễm trùng van tim, thiết bị dây dẫn và nhiễm trùng huyết. Tuy nhiên, chẩn đoán chính xác CIED-IE vẫn còn nhiều thách thức. Một phần do các biểu hiện lâm sàng đa dạng, thiếu định nghĩa chuẩn hóa và có nhiều sự khác biệt trong các khuyến cáo hướng dẫn. Hơn nữa, trong các phương thức chẩn đoán hiện tại, chẳng hạn như siêu âm tim qua thực quản (Transesophageal Echocardiography – TEE) và chụp cắt lớp vi tính phát xạ positron [18F]-fluorodeoxy-glucose ([18F]-fluorodeoxyglucose positron emission tomography computed tomography – PET-CT) có độ nhạy và độ đặc hiệu hạn chế, từ đó góp phần vào sự không chắc chắn trong chẩn đoán. Điều này còn có khả năng dẫn đến các biến chứng và chi phí không cần thiết liên quan đến gỡ bỏ thiết bị do chỉ định không phù hợp. Sáu trường hợp lâm sàng giả định sau đây sẽ minh họa cho các biểu hiện về sự đa dạng của CIED-IE. Thông qua những trường hợp này, chúng tôi nhấn mạnh tầm quan trọng của việc tối ưu hóa trong chẩn đoán và điều trị chính xác, hiểu các rủi ro cụ thể của các nguồn nhiễm trùng khác nhau đối với nhiễm trùng huyết, hướng dẫn loại bỏ thiết bị thích hợp và ngăn ngừa CIED-IE, đồng thời bổ sung những kiến thức mới về vấn đề này.
I. Mở đầu
Việc cấy ghép CIED đã tăng lên do mở rộng chỉ định và sự xuất hiện đồng thời nhiều bệnh lý đi kèm ở cả người lớn và trẻ em. Việc tăng cường sử dụng thiết bị để cải thiện tuổi thọ và chất lượng cuộc sống của bệnh nhân trong thực tế hiện nay có liên quan đến việc tăng nguy cơ nhiễm trùng CIED – một biến chứng có khả năng đe dọa tính mạng cùng với các gánh nặng về chi phí chăm sóc sức khỏe liên quan1,2.
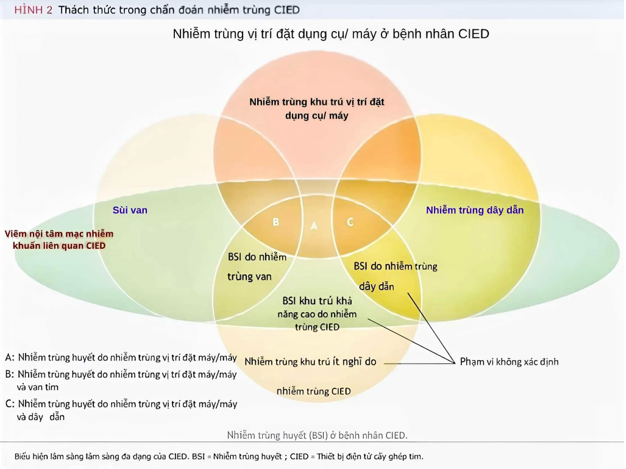
Định nghĩa về CIED-IE đã phát triển theo thời gian trong các hướng dẫn lâm sàng (Bảng 1, Hình 1). Định nghĩa của CIED-IE bao gồm một loạt các bệnh cảnh kết hợp hoặc riêng lẻ, bao gồm:
- Nhiễm trùng huyết (Bloodstream infection – BSI) với ổ sùi tại van (Valve Vegetation).
- Nhiễm trùng huyết với ổ nhiễm trùng tại dây dẫn (Lead Vegetation).
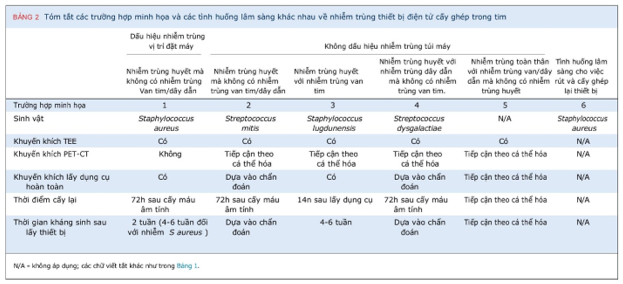
- Nhiễm trùng huyết đơn độc (Isolated BSI) mà không có bằng chứng nhiễm trùng tại van tim hay dây dẫn (hình 2)3.
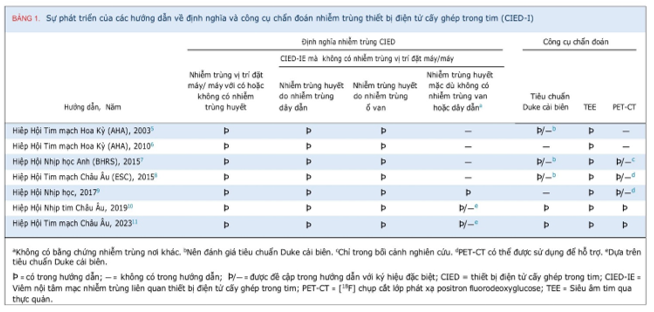
Năm 2023, hội tim mạch Hoa kỳ cũng đưa ra bảng tiêu chuẩn về chẩn đoán (xác định, khả năng, loại trừ) của tình trạng này (bảng 2)4. Qua các trường hợp lâm sàng giả định, bài viết này làm nổi bật các khía cạnh thách thức của CIED-IE (Bảng 3), nhằm bổ sung những thiếu hụt và xác định những hạn chế hiện tại trong sự hiểu biết của chúng ta về hội chứng này.
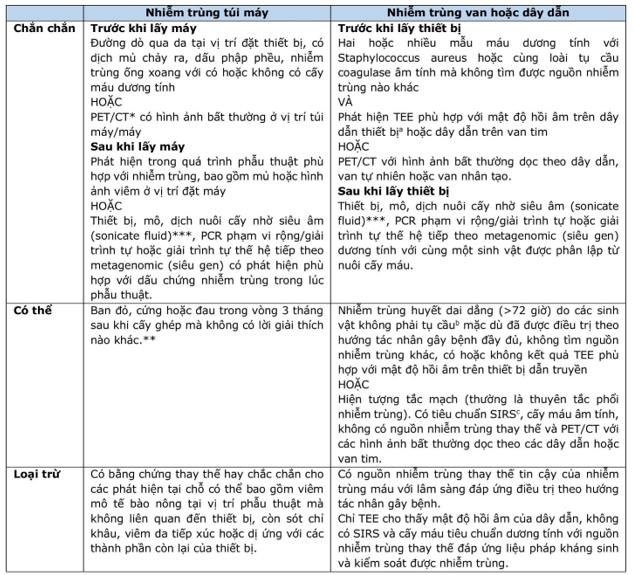
* Không yêu cầu để xác định chẩn đoán.
** Các giải thích thay thế có thể bao gồm viêm tế bào bề mặt tại vị trí phẫu thuật mà không liên quan đến thiết bị, sót chỉ khâu, viêm da tiếp xúc hoặc dị ứng với các thành phần của thiết bị.
***Sonicate fluid: dịch nuôi cấy nhờ siêu âm, là kỹ thuật nuôi cấy/phân tích vật liệu di truyền bằng cách siêu âm để giải phóng vi khuẩn bám trên bề mặt vật liệu nhân tạo ra dịch nuôi cấy
a TEE âm tính với các mật độ hồi âm của dây dẫn không loại trừ nhiễm trùng dây dẫn thiết bị điện tử cấy ghép tim.
b Chủ yếu bao gồm các sinh vật gram dương không phải staphylococcus, Pseudomonas aeruginosa, Serratia marcescens và các loài Candida.
c Tiêu chí SIRS được định nghĩa là có ≥ một trong các tiêu chí sau: nhiệt độ ≥ 38.3°C hoặc ≤ 36°C, nhịp tim > 90 lần/phút, nhịp thở > 20 lần/phút, và số lượng bạch cầu ngoại vi > 12000/μL hoặc < 4000/μL hoặc > 10% bạch cầu non.
II. CÁC TÌNH HUỐNG LÂM SÀNG
II.1. TRƯỜNG HỢP MINH HỌA 1: NHIỄM TRÙNG HUYẾT LIÊN QUAN ĐẾN CIED DO NHIỄM TRÙNG VỊ TRÍ ĐẶT MÁY.
Một phụ nữ 50 tuổi được cấy ghép máy tạo nhịp vĩnh viễn 10 tháng trước. Bệnh sử có sốt, nổi mẩn đỏ và sưng 3 ngày tại vị trí đặt dụng cụ. Hai bộ cấy máu cho kết quả mọc Staphylococcus aureus. TEE không thấy nhiễm trùng tại van tim hay dây điện cực.
Thảo luận/Câu hỏi lâm sàng
Chẩn đoán nhiễm trùng CIED trong trường hợp này rất đơn giản, được gợi ý bởi dấu nhiễm trùng khu trú và cấy máu dương tính. Chẩn đoán xác định CIED-IE với biểu hiện rõ ràng của nhiễm trùng tại chỗ và toàn thân.
Phương thức chẩn đoán
TEE là công cụ được dùng để chẩn đoán loại trừ viêm nội tâm mạc nhiễm trùng do dây điện cực hay van tim. Chụp PET-CT sẽ không được chỉ định trong trường hợp này, vì kết quả sẽ không làm thay đổi điều trị. Tuy nhiên, hướng dẫn của Hiệp hội Nhịp tim Châu Âu (European Heart Rhythm Association – EHRA) năm 2019 khuyến cáo rằng tất cả bệnh nhân nhiễm khuẩn huyết do Staphylococcus aureus (Staphylococcus aureus Bacteremia – SAB) đã CIED đều nên thực hiện PET-CT để loại trừ nhiễm trùng di căn. Mặc dù các nghiên cứu trước đây đã chứng minh lợi ích của PET-CT đối với Staphylococcus aureus bacteremia (SAB), nhưng bằng chứng gần đây cho thấy nên đánh giá lại lợi ích của nó và làm nổi bật mối lo ngại về khả năng sai lệch thời gian sống còn, với những bệnh nhân đã thực hiện PET-CT dường như có tiên lượng tốt hơn vì ở những bệnh nhân được thực hiện PET-CT thì có thời gian sống lâu hơn5,6.
Điều trị
Khuyến cáo loại bỏ thiết bị hoàn toàn với làm sạch ổ máy ở tất cả các bệnh nhân nhiễm trùng CIED. Sau khi loại bỏ CIED, việc cấy lại thiết bị mới có thể sớm nhất là 72 giờ sau cấy máu âm tính. BSI có liên quan đến vị trí đặt máy mà không có bằng chứng liên quan đến thiết bị dây điện cực hoặc van tim thì cần điều trị IE trong 2 tuần sau lấy máy. Tuy nhiên, thực hành lâm sàng thường liên quan đến một đợt điều trị kháng sinh kéo dài (4-6 tuần) sau khi lấy thiết bị trong trường hợp nhiễm SAB có nhiều biến chứng mặc dù TEE âm tính nhưng nghi ngờ cao về các biến chứng trên dây điện cực hoặc van tim3,4.
Những điểm quan trọng rút ra từ case lâm sàng
- TEE là công cụ chẩn đoán thường dùng để loại trừ IE do dây điện cực hoặc van tim.
- PET-CT ít có giá trị ở nhiễm trùng vị trí đặt máy/máy do SAB, trừ khi nghi ngờ có biến chứng.
- Nên cắt lọc, loại bỏ hoàn toàn thiết bị ở vị trí đặt máy bị nhiễm trùng.
- Trong các ca bệnh SAB, một đợt điều trị kháng sinh thường dùng dài hơn (4-6 tuần), ngay cả khi TEE loại trừ IE do dây dẫn, van tim và chưa ghi nhận các biến chứng di căn.
II.2. TRƯỜNG HỢP MINH HỌA 2: BSI LIÊN QUAN ĐẾN CIED MÀ KHÔNG NHIỄM TRÙNG TẠI VỊ TRÍ ĐẶT MÁY.
Một phụ nữ 50 tuổi được đặt máy tạo nhịp tim vĩnh viễn 3 năm, nhập viện với biểu hiện mệt mỏi và sốt 2 tuần nay. Khám lâm sàng thấy không có dấu hiệu nhiễm trùng vị trí đặt máy. Hai mẫu cấy máu phát hiện Streptococcus mitis. Du khuẩn huyết vẫn tồn tại kéo dài trong 3 ngày dù đã điều trị kháng sinh thích hợp. TEE không cho thấy hình ảnh nhiễm trùng van tim hay dây điện cực.
Thảo luận/Câu hỏi lâm sàng
Nhiễm trùng CIED trong trường hợp không có gợi ý lâm sàng tại vị trí đặt máy là một thách thức. Khi gặp trường hợp BSI, điều quan trọng là phải xem xét 3 khả năng chính:
- Nhiễm trùng huyết có thể là dấu chứng của nhiễm trùng CIED.
- Một nguồn lây nhiễm khác, chẳng hạn như da và mô mềm, ống thông tĩnh mạch trung tâm, hoặc từ đường tiết niệu, có thể là nguyên nhân chính của BSI, với biểu hiện thứ phát tại CIED.
- BSI có thể bắt nguồn từ một nguồn khác và CIED thật sự không bị nhiễm bệnh, gây khó khăn trong chẩn đoán.
Nguy cơ nhiễm trùng CIED khác nhau tùy thuộc vào từng cá thể và các yếu tố liên quan đến thiết bị hoặc thủ thuật và tác nhân gây bệnh BSI. SAB có liên quan đến nhiễm CIED được xác định trong 14%-55% ca bệnh, cầu khuẩn gram dương không phải Staphylococcus aureus (non-Staphylococcus aureus gram-positive cocci: non-SA GPC) trong 7% đến 38% ca bệnh và mầm bệnh gram âm chỉ trong 2% đến 17% ca bệnh. Do đó, cách tiếp cận lâm sàng và quyết định tầm soát thêm về nhiễm trùng CIED phụ thuộc vào nguy cơ dựa trên mầm bệnh. Khuyến cáo bổ sung xét nghiệm đối với S aureus hoặc BSI non-SA GPC, đặc biệt là enterococci, staphylococci không tính đông máu (coagulase-negative staphylococci) và streptococci nhóm viridans. Ngược lại, nhiễm khuẩn huyết gram âm thường không cần xét nghiệm bổ sung. Một số nghiên cứu đã nhấn mạnh một xu hướng cao hơn của Pseudomonas aeruginosa và các loài Serratia gây nhiễm trùng CIED so với các vi khuẩn gram âm khác, do đó cần tăng cường đánh giá chẩn đoán ở bệnh nhân mắc BSI do 2 vi khuẩn này. Thời gian bị BSI, khởi phát tại cộng đồng và bằng chứng thuyên tắc mạch nên được xem xét trong việc xác định chiến lược chẩn đoán vì chúng làm tăng xác suất nhiễm CIED3.
Phương thức chẩn đoán
Mặc dù TEE không cho thấy hình ảnh nhiễm trùng van tim hay dây điện cực. Trường hợp này là một trường hợp “có thể nhiễm trùng CIED” theo hướng dẫn EHRA và AHA, bởi vì dây điện cực có thể bị nhiễm khuẩn hoặc không. Phân loại này dựa trên nuôi cấy máu dương tính với mầm bệnh CIED-IE điển hình (một tiêu chí chính) và sốt (một tiêu chí phụ). Ngoài ra, trường hợp này có các đặc điểm nguy cơ cao đối với nhiễm CIED như khởi phát trong cộng đồng và không có nguồn lây nhiễm thay thế.
Hầu hết bệnh nhân nhiễm S aureus và GPC không phải SA bị sốt sẽ tự động được phân loại là “có thể nhiễm trùng CIED”. Khi suy đoán rằng chẩn đoán chỉ là “có thể” có độ đặc hiệu thấp làm dấy lên lo ngại về việc đánh giá chính xác CIED nguy cơ nhiễm trùng sau BSI, vì các nghiên cứu thường bao gồm khả năng nhiễm trùng CIED tương đương như nhiễm trùng CIED thực tế. Tuy nhiên, dự đoán này có thể đánh giá quá cao rủi ro thực sự và có khả năng dẫn đến việc loại bỏ không cần thiết các thiết bị không bị nhiễm3.
Hướng dẫn EHRA 2019 và ESC 2023 đều công nhận tầm quan trọng của PET-CT dương tính như một tiêu chí để chẩn đoán nhiễm trùng CIED. Tuy nhiên, vẫn còn những hạn chế. Mặc dù đánh giá có hệ thống và phân tích tổng hợp cho thấy độ nhạy 83% và độ đặc hiệu 89% để phát hiện nhiễm trùng CIED ở 492 bệnh nhân trong 14 nghiên cứu, độ nhạy đối với nhiễm dây dẫn thấp hơn ở mức 76%, với độ đặc hiệu là 83%. Trong một nghiên cứu gần đây, độ nhạy của PET- CT để phát hiện nhiễm trùng là 79% tại vị trí đặt máy. Tuy nhiên, khi khoảng cách tới túi máy tăng lên, độ nhạy giảm đáng kể, có thể xuống thấp tới 10%. Và khi PET-CT được kết hợp với TEE, hiệu suất chẩn đoán tăng từ 34% lên 56%5,7,8.
Điều trị
Quyết định có nên chẩn đoán BSI do CIED mà không có bằng chứng của nhiễm trùng vị trí đặt máy, dây điện cực. hoặc van tim là một thách thức và yêu cầu thảo luận một nhóm các chuyên khoa. Bởi vì, giữ lại CIED bị nhiễm bệnh có thể dẫn đến tỷ lệ nhiễm trùng và tử vong đáng kể, trong khi việc loại bỏ thiết bị không cần thiết có thể dẫn đến tăng các biến chứng và chi phí.
Hướng dẫn EHRA khuyến nghị loại bỏ thiết bị cho tất cả bệnh nhân bị SAB hoặc nhiễm nấm bất kể có bằng chứng về nhiễm trùng thiết bị hay không và phải dựa trên ý kiến chuyên gia. Một số nghiên cứu đã chứng minh lợi ích về tử vong trong các ca nhiễm S aureus ngay cả khi không có bằng chứng nhiễm trùng thiết bị. Tuy nhiên, vai trò của loại bỏ thiết bị trong nhiễm trùng huyết do nấm vẫn chưa chắc chắn.
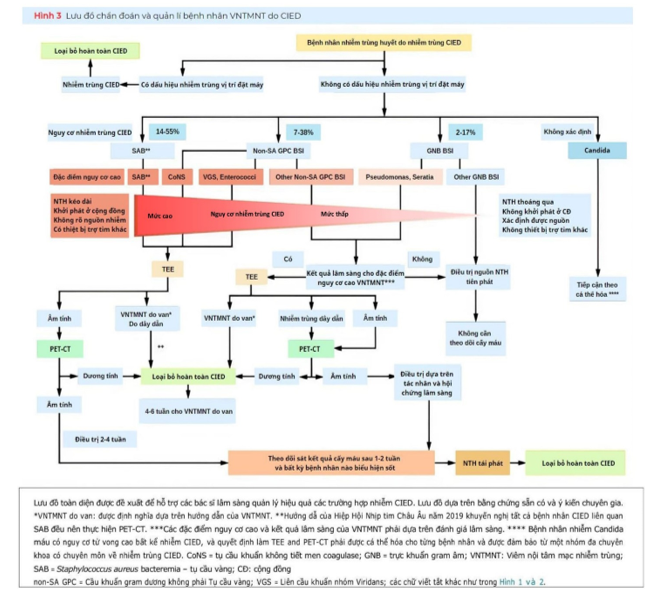
Đối với GPC non-SA, nếu đánh giá ban đầu không cho thấy bằng chứng về CIED-IE, nhưng có nghi ngờ cao về nhiễm trùng CIED, làm lại TEE là rất quan trọng. Các tác giả đưa ra tiêu chuẩn thực hành bao gồm tiến hành nuôi cấy máu và theo dõi từ 1 đến 2 tuần sau khi hoàn thành liệu pháp kháng sinh ở bệnh nhân giữ thiết bị, vì nhiễm trùng tái phát sẽ làm tăng lo ngại về nhiễm trùng thiết bị. Tuy nhiên, lợi ích của thực tiễn này vẫn còn gây tranh cãi. Do đó, các tác giả đề xuất một lưu đồ quản lý để hướng dẫn việc ra quyết định trong những trường hợp như vậy (hình 3)3,4.
Những điểm quan trọng từ ca lâm sàng
- Chẩn đoán nhiễm trùng CIED trong các ca bệnh BSI không có dấu hiệu nhiễm trùng vị trí đặt máy là một thách thức.
- Nguy cơ nhiễm trùng CIED khác nhau tùy thuộc vào tác nhân gây bệnh.
- Các quyết định về loại bỏ CIED đòi hỏi một cách tiếp cận đa chuyên khoa.
- Giữ lại CIED bị nhiễm trùng có thể dẫn đến tử vong và việc loại bỏ thiết bị không cần thiết có thể dẫn đến tăng các biến chứng và chi phí.
II.3. TRƯỜNG HỢP MINH HỌA 3: VAN TỰ NHIÊN LIÊN QUAN ĐẾN CIED-IE, KHÔNG NHIỄM TRÙNG VỊ TRÍ ĐẶT MÁY
Một phụ nữ 80 tuổi bị bệnh thận giai đoạn cuối đang chạy thận nhân tạo và đã được đặt máy tạo nhịp tim vĩnh viễn 5 năm có biểu hiện mệt mỏi và sốt 3 ngày. Không có dấu hiệu nhiễm trùng vị trí đặt máy. Hai bộ nuôi cấy máu mọc Staphylococcus lugdunensis. TEE cho thấy một ổ sùi 0,8 cm trên van hai lá tự nhiên. Không có ổ nhiễm khuẩn nào được nhìn thấy trên dây điện cực CIED hoặc các van khác.
Thảo luận/câu hỏi lâm sàng
Nguy cơ nhiễm trùng CIED cao đáng kể khi có tụ cầu khuẩn với coagulase âm tính. Tuy nhiên, S Lugdunensis, không giống như các tụ cầu khuẩn coagulase âm tính khác, nó thể hiện xu hướng lây nhiễm các van tự nhiên và tương tự như S aureus cũng được xem là mầm bệnh nguy hiểm. Do đó, TEE rất quan trọng trong quy trình chẩn đoán này để đánh giá xem tình trạng nhiễm trùng có phức tạp hay không.
Phương thức chẩn đoán
Tiêu chuẩn chẩn đoán cho IE đã phát triển theo thời gian với một bản cập nhật lớn được xuất bản bởi Trung tâm Y tế Đại học Duke và Hiệp hội Quốc tế về Bệnh Truyền nhiễm Tim mạch vào năm 2023. Đáng chú ý, cả hai tiêu chí chính và phụ đã được mở rộng để bao gồm hoạt động trao đổi chất bất thường của PET-CT từ van, ghép động mạch chủ mà có bằng chứng về sự tham gia của van, dây dẫn thiết bị trong tim hoặc các vật liệu giả khác (chủ yếu nếu thiết bị được đặt cách đây hơn 3 tháng). Sự hiện diện của CIED đã được thêm vào các tiêu chí phụ như một yếu tố có thể gây ảnh hưởng9.
Điều trị
Khi đã chẩn đoán xác định CIED-IE, loại bỏ CIED là cần thiết. Chúng ta cần tư vấn của bác sĩ phẫu thuật tim-lồng ngực nếu bệnh nhân có chỉ định thay van tim. Tuy nhiên, ở một số bệnh nhân lớn tuổi hoặc có nhiều bệnh lý đi kèm, việc loại bỏ thiết bị hoặc phẫu thuật tim hở có thể không khả thi. Hơn nữa, việc tuân thủ chỉ định loại bỏ hoàn toàn thiết bị như được khuyến nghị trong hướng dẫn thường không đầy đủ. Một nghiên cứu gần đây sử dụng cơ sở dữ liệu tái nhập viện toàn quốc đã chứng minh rằng chỉ có 11,5% bệnh nhân bị CIED-IE đã được loại bỏ thiết bị, với người cao tuổi, bệnh nhân nữ, sa sút trí tuệ và suy thận ít có khả năng chịu đựng được phẫu thuật lấy dụng cụ. Do đó, liệu pháp kháng sinh có tầm quan trọng hơn trong những trường hợp này. Tiêu chuẩn chăm sóc cho IE thường đòi hỏi tối thiểu 6 tuần điều trị. Tuy nhiên, nếu thiết bị không được gỡ bỏ, thì kháng sinh dài hạn có thể được xem xét để thay thế, miễn là thiết bị được giữ lại đúng chỉ định. Trong một nghiên cứu liên quan đến 48 bệnh nhân bị nhiễm trùng CIED (10% trong số đó có dấu hiệu của nhiễm trùng vị trí đặt máy) được coi là không đủ điều kiện để loại bỏ thiết bị, lúc này kế hoạch điều trị là kháng sinh đường uống dài hạn. Lưu giữ thiết bị có liên quan với tỷ lệ tái phát nhiễm trùng cao và tử vong do mọi nguyên nhân trong 1 năm. Tuy nhiên, những kết quả này có thể đã bị ảnh hưởng, ít nhất là một phần, bởi các bệnh đi kèm của bệnh nhân3,4.
Những điểm quan trọng
- Bệnh nhân có các bệnh đồng mắc đáng kể không thể trải qua phẫu thuật loại bỏ thiết bị thì nên được xem xét sử dụng kháng sinh dài hạn, mặc dù lựa chọn này không triệt để và có liên quan đến tỷ lệ tái phát và tử vong cao hơn.
- Khuyến cáo theo dõi chặt chẽ ở những bệnh nhân sử dụng kháng sinh đường uống dài hạn khi có nguy cơ tái phát nhiễm trùng ở mức cao.
II.4. TRƯỜNG HỢP MINH HỌA 4: DÂY DẪN CIED LIÊN QUAN ĐẾN CIED-IE, KHÔNG NHIỄM TRÙNG VỊ TRÍ ĐẶT MÁY
Một người đàn ông 30 tuổi (được nuôi ăn qua đường tĩnh mạch hoàn toàn mãn tính và được cấy ICD) vào viện vì sốt và ớn lạnh 4 ngày. Không có dấu hiệu nhiễm trùng vị trí đặt ICD. Cấy máu mọc Streptococcus dysgalactiae từ cả ống thông tĩnh mạch trung tâm và ngoại vi. Cả hai ống đều được loại bỏ và cấy máu ngoại vi vẫn dương tính trong 1 ngày sau khi loại bỏ ống. TEE cho thấy hồi âm không xác định mật độ dọc theo dây điện cực CIED, nhưng không thấy sùi ở van.
Thảo luận/ câu hỏi lâm sàng
Biểu hiện của bệnh nhân mắc BSI liên quan đến ống thông trung tâm kèm theo bất thường mật độ hồi âm trên dây dẫn CIED mà không có dấu hiệu nhiễm trùng vị trí túi hoặc bằng chứng về sùi tại van là một tình huống lâm sàng phổ biến. Đầu tiên, TEE đã chứng minh độ đặc hiệu thấp trong việc phân biệt giữa hôi âm trên dây dẫn bị nhiễm và không bị nhiễm bệnh, thường gặp ở CIED không bị nhiễm bệnh. Thứ hai, mặc dù nguy cơ GPC không phải SA ngoài tụ cầu khuẩn âm tính với coagulase âm tính, streptococci nhóm viridans và enterococci gây nhiễm CIED là trung bình, nhưng nó cao hơn so với BSI gram âm, mặc dù không phải là cao nhất trong số tất cả các mầm bệnh. Thứ ba, mặc dù trường hợp này có đặc điểm là BSI khởi phát từ cộng đồng, BSI đã quyết định cắt bỏ ống thông trung tâm, gợi ý không nhiễm trùng CIED. Thứ tư, cần lưu ý rằng việc áp dụng các tiêu chí EHRA cho tình huống này sẽ phân loại bệnh nhân là có “nhiễm trùng CIED xác định” dựa trên sự hiện diện của 2 tiêu chí chính (BSI và kết quả siêu âm tim dương tính) và 1 tiêu chí phụ (sốt), cần phải loại bỏ thiết bị. Tuy nhiên, điều quan trọng là phải xem xét hậu quả tiềm ẩn của việc loại bỏ thiết bị không cần thiết, bao gồm cả tử vong. Với 4 khía cạnh thách thức này, việc xác định liệu độ đặc hiệu về thiết bị CIED có bị nhiễm trùng hay không là một câu hỏi hóc búa về chiến lược điều trị.
Phương thức chẩn đoán
Nhiễm trùng dây dẫn, đặc trưng bởi sự hiện diện của một khối di động dọc theo phần nội tâm mạc dây điện cực, thường được quan sát thấy ở các khu vực như tâm nhĩ phải, van ba lá hoặc điểm tiếp xúc dây điện cực trong tâm thất phải. Sự hiện diện của nó thường cho thấy nghi ngờ lâm sàng cao đối với nhiễm trùng CIED trong bối cảnh BSI do mầm bệnh nguy cơ cao hoặc nhiễm trùng vị trí đặt máy. Trong một nghiên cứu, các bệnh thận và rối loạn chuyển hóa, suy tim, dây điện cực khử rung tim và vòng lặp của các dây điện cực (loops of the leads) là yếu tố nguy cơ đối với nhiễm trùng dây điện cực lớn có thể dẫn đến các biến chứng đáng kể như thuyên tắc phổi. Ngoài ra, nhiễm trùng dây điện cực thường gặp hơn ở những bệnh nhân không bị nhiễm trùng túi máy hơn là ở những bệnh nhân bị nhiễm trùng túi máy10,11.
Ngược lại, việc phân biệt một người bị nhiễm bệnh với huyết khối không bị nhiễm trùng hoặc cục máu đông đơn thuần đặt ra một thách thức đáng kể. Một cuộc kiểm tra mù liên tiếp 25 trường hợp nhiễm trùng dây điện cực CIED và 25 bệnh nhân không có nhiễm trùng CIED có mật độ ECHO không đặc hiệu trên dây điện cực cho thấy độ nhạy của việc xem xét TEE bị mù trong việc phát hiện ổ sùi chỉ là 31,5% đến 37,5%. Trong một nghiên cứu khác trên 231 bệnh nhân CIED đã thực hiện TEE vì nhiều lý do, bao gồm loại trừ IE, mật độ ECHO dọc theo dây điện cực đã được quan sát thấy trong 50 trường hợp (21,6%), nhưng chỉ có 16 trong số đó (32%) cuối cùng được chẩn đoán nhiễm CIED. 2 nghiên cứu này với nguyên lý được công nhận rõ ràng rằng cục máu đông nhạt (bland clots) là phổ biến (tùy thuộc vào phương pháp chẩn đoán) trên các dây điện cực và làm dấy lên lo ngại về tính đặc hiệu của chẩn đoán “nhiễm trùng dây dẫn” trong các trường hợp nghi ngờ lâm sàng thấp về nhiễm CIED12,13.
Điều trị
Trong trường hợp này, rủi ro của nhiễm trùng CIED ở mức trung bình và TEE cho thấy những phát hiện không chắc chắn về nguồn gốc, nên có 3 cách tiếp cận khả thi có thể xem xét. Cách tiếp cận đầu tiên liên quan đến thực hiện PET-CT. Nếu kết quả PET-CT dương tính với nhiễm trùng, thì nên tháo thiết bị do PET-CT có độ đặc hiệu cao. Mặt khác, nếu PET-CT cho kết quả không rõ ràng hoặc âm tính, nghĩa là không đủ bằng chứng để kết luận rằng CIED bị nhiễm bệnh, lúc này nên điều trị BSI theo hướng dẫn và theo dõi chặt chẽ sự tái phát. Cách tiếp cận thứ hai là quản lý với điều trị kháng sinh là bước đầu tiên với theo dõi chặt chẽ để đánh giá tái phát nhiễm trùng. Cách tiếp cận thứ ba là cách tích cực nhất, liên quan đến giả định rằng CIED bị nhiễm, đòi hỏi phải loại bỏ thiết bị. Cách tiếp cận này có thể phù hợp với các trường hợp có các đặc điểm nguy cơ cao, chẳng hạn như BSI kéo dài mà không có nguồn gốc rõ ràng. Quyết định loại bỏ thiết bị nên được đánh giá cẩn thận, xem xét các lợi ích và rủi ro tiềm ẩn liên quan, để ngăn ngừa tác hại không cần thiết cho bệnh nhân. Bởi vì hiện tại không có bằng chứng dựa trên tài liệu ủng hộ hoặc bác bỏ các phương pháp này, điều quan trọng là phải áp dụng một tiếp cận cá thể hóa và được hướng dẫn bởi một cuộc hội chẩn liên chuyên khoa, kết hợp với thông báo, ra quyết định và được sự hợp tác của bệnh nhân, là vô cùng quan trọng3,4.
Những điểm quan trọng từ ca lâm sàng
- TEE có độ đặc hiệu thấp trong việc phân biệt giữ cục máu đông bị nhiễm trùng và không bị nhiễm trùng.
- Áp dụng các tiêu chí EHRA 2019 có thể dẫn đến việc loại bỏ thiết bị không cần thiết và các kết quả bất lợi tiềm ẩn.
- PET-CT có những hạn chế trong việc hỗ trợ chẩn đoán nhiễm trùng CIED, và cần nghiên cứu thêm để nâng cao độ chính xác.
- Quan điểm điều trị nên dựa trên đánh giá lâm sàng và cá thể hóa trên từng bệnh nhân dựa trên sự hội chẩn liên chuyên khoa.
II.5. TRƯỜNG HỢP MINH HỌA 5: NHIỄM TRÙNG DÂY ĐIỆN CỰC CIED VỚI CẤY MÁU ÂM TÍNH
Một phụ nữ 50 tuổi bị sốt và khó chịu đã 4 tuần. Người bệnh không có các triệu chứng khu trú và không được dùng thuốc kháng sinh. Khám thực thể cho thấy không có dấu hiệu nhiễm trùng vị trí đặt máy. Hai bộ cấy máu đều âm tính. Tăng bạch cầu và các dấu hiệu viêm tăng cao đã được ghi nhận. TEE đã phát hiện thấy khối hồi âm 12 mm bám vào dây điện cực của thiết bị.
Thảo luận/ câu hỏi lâm sàng
Các bác sĩ lâm sàng phải đối mặt với những thách thức đáng kể khi xử lý CIED-IE mà cấy máu âm tính, đặc biệt khi không có những thay đổi viêm có thể quan sát được ở vị trí đặt máy. Mặc dù chiếm 7% đến 13% các trường hợp, vẫn thiếu hướng dẫn chẩn đoán và quản lý cụ thể để giải quyết hội chứng này14,15.
Bệnh nhân có CIED-IE cấy âm tính thường có hội chứng đáp ứng viêm toàn thân và nồng độ các dấu hiệu viêm tăng cao. Cấy máu âm tính có thể là kết quả của việc sử dụng kháng sinh trước khi lấy máu xét nghiệm, đặc biệt trong các trường hợp liên quan đến các vi khuẩn có độc lực thấp hoặc sự hiện diện của các mầm bệnh không thể nuôi cấy hoặc khó nuôi cấy. Hơn nữa, việc xác định hồi âm bất thường trên dây dẫn có thể làm tăng mối lo ngại về khả năng CIED có liên quan đến nguồn lây nhiễm3,14.
Tuy nhiên, xem xét mức độ tương đối hiếm gặp của hội chứng này, việc chẩn đoán CIED-IE ở những bệnh nhân có dấu hiệu nhiễm trùng toàn thân, cấy máu âm tính và có hồi âm bất thường trên dây điện cực nên được tiếp cận như một “chẩn đoán loại trừ”. Bác sĩ lâm sàng nên điều tra kỹ lưỡng và loại trừ các nguồn lây nhiễm khác hoặc loại trừ các yếu tố làm sai lệch kết quả trước khi xác định chẩn đoán này và khuyến cáo việc loại bỏ một thiết bị có khả năng không bị nhiễm trùng. Như đã thảo luận trước đây, mật độ hồi âm của dây điện cực tương đối đặc trưng ở những bệnh nhân mắc CIED và có thể được quy cho là cản âm của dây điện cực (lead reverberations) hay những thay đổi thoái hóa hoặc huyết khối12.
Do những trường hợp này rất phức tạp nên việc tham khảo ý kiến của bác sĩ chuyên khoa về bệnh truyền nhiễm là điều cần thiết. Việc kiểm tra nên tập trung vào các nguồn lây nhiễm thay thế và các tình trạng không lây nhiễm dựa trên bệnh sử và thăm khám. PET-CT đặc biệt hữu ích trong những trường hợp chẩn đoán không chắc chắn hoặc không rõ ràng. Ngoài ra, PET-CT có thể đóng vai trò là công cụ có giá trị trong việc xác định các nguồn lây nhiễm thay thế và chẩn đoán các tình trạng không lây nhiễm. Metagenomic shotgun sequencing* trong máu có thể hỗ trợ xác định vi khuẩn gây bệnh trong các trường hợp nghi ngờ nhiễm CIED mà nuôi cấy âm tính. Tuy nhiên, giá trị tiên đoán âm tính trong bối cảnh lâm sàng này và tác động của liệu pháp kháng sinh trước đó có thể làm ảnh hưởng đến kết quả xét nghiệm và có thể không loại trừ dứt khoát nguồn lây này16.
Điều quan trọng cần lưu ý là CIED-IE âm tính với nuôi cấy cũng có thể liên quan đến nhiễm trùng do nấm hoặc vi khuẩn mycobacteria. Tuy nhiên, do sự hiếm gặp của những bệnh nhiễm trùng này nên việc xét nghiệm thường quy đặc biệt đối với những mầm bệnh này không được khuyến khích, và việc xét nghiệm phải được chỉ định bởi chuyên gia về bệnh truyền nhiễm. Tương tự, mặc dù các trường hợp brucella và coxiella là nguyên nhân hiếm gặp gây nhiễm CIED đã được báo cáo, tuy nhiên việc tầm soát chỉ nên được xem xét ở những người có lịch sử phơi nhiễm thích hợp.
Quá trình chẩn đoán nhằm xác định nhiễm trùng và xác định thời gian điều trị sau khi tháo thiết bị thường bao gồm nhiều phương pháp khác nhau. Mô bệnh học của khối cản âm có thể là một công cụ có giá trị cho chẩn đoán xác định, mặc dù hiếm khi hình thành. Thiết bị chiết xuất xoáy nước/siêu âm (Vortexing/sonication of an extracted device) là một kỹ thuật trong phòng thí nghiệm có thể nâng cao năng suất vi sinh vật trong quá trình nuôi cấy vi khuẩn và xét nghiệm phân tử thông thường. Nếu nuôi cấy cho kết quả âm tính sau 48 giờ, phản ứng/giải trình tự chuỗi polymerase 16S rRNA hoặc kỹ thuật giải trình tự tập hợp gen thế hệ mới (metagenomic next-generation sequencing) có thể được thực hiện trên dịch nuôi cấy nhờ siêu âm (sonicate fluid). Xét nghiệm phân tử và xét nghiệm huyết thanh bổ sung đối với các mầm bệnh không điển hình hoặc nuôi cấy vi khuẩn hoặc nấm có thể được xem xét dựa trên các yếu tố nguy cơ riêng lẻ15.
Điều trị
Trong những trường hợp nhiễm trùng đã được xác định, nên điều trị bằng kháng sinh trong 2 tuần sau khi tháo thiết bị. Nếu nuôi cấy bệnh phẩm từ các dây điện cực, ổ nhiễm trùng hoặc xét nghiệm phân tử cho thấy S.aureus thì thời gian điều trị nên được kéo dài lên đến 4 đến 6 tuần. Việc điều chỉnh thuốc kháng sinh phải dựa theo việc xác định các mầm bệnh cụ thể tại địa phương, tiền sử của bệnh nhân. Trong trường hợp không có sẵn dữ liệu sinh học hoặc nuôi cấy có kết quả âm tính được cho là do điều trị bằng kháng sinh trước đó, liệu pháp kháng sinh sau khi loại bỏ thiết bị có thể được dùng giống như trước khi lấy thiết bị mà không cần dùng kháng sinh phổ rộng hơn3,4.
Những điểm quan trọng từ ca lâm sàng
- Cấy máu âm tính có thể do tiếp xúc với kháng sinh gần đây trước khi lấy mẫu bệnh phẩm (nguyên nhân phổ biến nhất) hoặc do sự hiện diện của các sinh vật không thể nuôi cấy hoặc khó nuôi cấy.
- Siêu âm tim có giá trị trong việc xác định IE do van tim, nhưng không khuyến cáo chẩn đoán nhiễm trùng dây dẫn CIED ở bệnh nhân cấy máu âm tính.
- PET-CT là phương pháp chẩn đoán được ưu tiên trong những trường hợp này.
II.6. TRƯỜNG HỢP MINH HỌA 6: TRƯỜNG HỢP CẦN CÂN NHẮC LOẠI BỎ CIED
Một người đàn ông 43 tuổi bị bệnh cơ tim phì đại và đặt ICD vì ngừng tim ngoài bệnh viện khoảng 11 năm trước, nhập viện với tiền sử sốt và ban đỏ vị trí đặt ICD 5 ngày. Kết quả cấy máu dương tính với S.aureus. Siêu âm tim cho thấy sùi van kích thước 0,7×0,5cm trên van động mạch chủ, và sùi 1,2 cm trên dây dẫn cạnh vách nhĩ thất . Bệnh nhân được phẫu thuật lấy CIED qua da.
Các yếu tố chính khi cân nhắc loại bỏ CIED
Có một số yếu tố cần xem xét khi xác định cách tiếp cận, rủi ro và lợi ích của việc loại bỏ CIED. Các yếu tố bệnh nhân báo hiệu nguy cơ cao hơn khi thực hiện loại bỏ thiết bị bao gồm tuổi cao, yếu, chỉ số khối cơ thể thấp và phẫu thuật cắt xương ức trước đó. Các yếu tố liên quan đến thiết bị bao gồm loại, số lượng và tuổi của dây điện cực, còn hiện diện dây máy còn sót lại hay bị cắt cụt (abandoned or capped leads), độ thông thoáng tĩnh mạch, sự hiện diện của đường tĩnh mạch trung tâm và nhiễm trùng CIED trước đó đã lấy bỏ mà có thể ảnh hưởng đến vị trí hệ thống mới. Hơn nữa, sự hiện diện của van nhân tạo, mức độ va chạm của dây điện cực và mức độ nghiêm trọng của trào ngược van ba lá là các yếu tố quan trọng cần xem xét. Nhận biết chi tiết bệnh nhân liên quan đến phẫu thuật xương ức trước đó, loại phẫu thuật và hình ảnh giải phẫu là rất quan trọng để lập kế hoạch chiến lược. Nếu cơ sở y tế không được trang bị cơ sở hạ tầng và kỹ năng để loại bỏ dây điện cực cũng như dự phòng phẫu thuật tim mạch nếu cần, thì bệnh nhân nên được chuyển đến một trung tâm với đầy đủ những loại chuyên môn đó3.
Các biến chứng tiềm ẩn cần xem xét khi lấy CIED
Biến chứng thường gặp nhất kết hợp với loại bỏ CIED là rách tĩnh mạch chủ trên. Điều này là do tĩnh mạch chủ trên không được bảo vệ bởi màng ngoài tim, vì vậy rách có thể dẫn đến xuất huyết ồ ạt vào trung thất. Tỷ lệ mắc bệnh này là <1%. Thông thường, sẽ bơm bóng ở vị trí chảy máu để cầm máu tạm thời cho đến khi một đội ngũ phẫu thuật giàu kinh nghiệm có thể thực hiện phẫu thuật cắt xương ức, cầm máu và đảm bảo hỗ trợ huyết động của bệnh nhân. Các biến chứng lớn khác có thể gặp phải là: tràn máu ngoải ngoài tim và chèn ép màng ngoài tim cần chọc màng ngoài tim. Ngoài ra, có thể làm xấu đi tình trạng hở van ba lá với khả năng hở van 3 lá rất nặng cần can thiệp phẫu thuật ngay sau khi rút dây điện cực17,18.
Các yếu tố cần xem xét để tái cấy CIED
Cân nhắc đầu tiên là xác định xem bệnh nhân có chỉ định tiếp tục CIED phù hợp hay không. Những chỉ định chính sẽ là nhu cầu tạo nhịp tim liên tục, chỉ định tiên phát hay thứ phát của đặt ICD, bao gồm xu hướng hoặc tiền sử rối loạn nhịp thất trước đó, xu hướng đột tử do tim hoặc nếu bệnh nhân tiếp tục đáp ứng các tiêu chí điều trị tái đồng bộ tim. Cân nhắc thứ hai là thời điểm tái cấy ghép để tối ưu khả năng ngăn ngừa nhiễm trùng hệ thống mới được cấy ghép. Khi có nhiễm trùng vị trí đặt máy hoặc sùi van, việc tái cấy ghép tại vị trí đối diện có thể thực hiện sớm nhất là 72 giờ sau khi loại bỏ CIED với sạch vi trùng (nếu hiện diện) và túi máy bị nhiễm trùng đã được cắt lọc triệt để. Nếu có nhiễm trùng van tim, thì nên trì hoãn việc cấy lại sau 14 ngày.
Trong một số trường hợp IE van tim, bệnh nhân được xuất viện trước 14 ngày mà không cần thiết bị vĩnh viễn. Nếu bệnh nhân không có nhu cầu kiểm soát nhịp nhưng vẫn có nguy cơ cao bị rối loạn nhịp thất, hãy sử dụng máy khử rung tim đeo tạm thời để chờ cấy ghép lại thiết bị vĩnh viễn. Nếu bệnh nhân có nhu cầu cần tạo nhịp (pacing) nhưng không có nguy cơ cao bị rối loạn nhịp thất, bệnh nhân có thể sử dụng máy tạo nhịp tim không dây hoặc máy tạo nhịp tim tạm thời với bộ theo dõi bên ngoài. Ngoài ra, nếu bệnh nhân không cần tạo nhịp, và không hưởng lợi từ liệu pháp kích nhịp chống nhịp nhanh (antitachycardia pacing therapy), có thể đặt ICD dưới da để tránh cấy ghép vào mạch máu, đặc biệt là ở những bệnh nhân có xu hướng nhiễm trùng tái phát cao. Cuối cùng, đối với bệnh nhân những người có cả nhu cầu kiểm soát nhịp và có nguy cơ cao phát triển rối loạn nhịp thất, quản lý ngoại trú có thể không thuận lợi và kiểm soát nội viện lâu dài đôi khi là cần thiết3,4.
III. PHÒNG NGỪA
III.1. Dự phòng nhiễm trùng
III.1.1. Bằng chứng
Dự phòng tại vị trí phẫu thuật là khía cạnh duy nhất trong quản lý và phòng ngừa CIED-IE dựa trên dữ liệu thử nghiệm lâm sàng. Điều này bao gồm thực hành phòng ngừa và kiểm soát nhiễm trùng và sử dụng kịp thời kháng sinh trước phẫu thuật, thường là cefazolin.
Có 2 khía cạnh của phòng chống CIED-IE đã thu hút sự chú ý gần đây. Đầu tiên, có sự đồng thuận rằng tiền sử dị ứng penicillin của bệnh nhân không nhất thiết là lý do để tránh sử dụng cefazolin như biện pháp dự phòng tại chỗ phẫu thuật. Thứ hai, sự hình thành khối máu tụ, bất kể kích thước tại vị trí túi máy, đã được xác định là yếu tố nguy cơ cao liên quan đến CIED-IE. Do đó, các can thiệp trong phẫu thuật để giảm nguy cơ nhiễm trùng đồng nghĩa với việc phải giảm hình thành khối máu tụ. Điều này bao gồm tránh cắt nang (capsulectomy) -tránh làm tổn thương bao gan cơ ngực lớn và không cắt bao túi máy khi thaay máy, và tránh heparin trong giai đoạn phẫu thuật.
Hai thử nghiệm ngẫu nhiên lớn phải được kể đến. Thử nghiệm lớn thứ nhất, thử nghiệm PADIT (Thử nghiệm phòng ngừa nhiễm trùng thiết bị rối loạn nhịp tim; NCT01002911), bao gồm hơn 19.000 bệnh nhân, so sánh phác đồ dự phòng tích cực với một phác đồ Cefazolin đơn độc trong dự phòng trước phẫu thuật. Đó là ngoài Cefazolin trước phẫu thuật thông thường, nhóm can thiệp còn được dùng Vancomycin trước phẫu thuật, trong thủ thuật rửa túi máy bằng Bacitracin, và một liệu trình Cephalexin sau thủ thuật 2 ngày. Kết quả cho thấy không có khác nhau liên quan đến nhiễm trùng giữa 2 nhóm nghiên cứu19.
Thử nghiệm ngẫu nhiên lớn thứ hai, WRAP-IT (Thử nghiệm dự phòng nhiễm trùng bằng túi bọc kháng sinh tự tiêu ngẫu nhiên toàn cầu; NCT02277990), bệnh nhân ngẫu nhiên được dự phòng bằng túi bọc tự tiêu kháng sinh (antimicrobial-impregnated envelope: minocycline và rifampin) hoặc không. Gần 7.000 bệnh nhân, trong đó những bệnh nhân nhận được dự phòng bằng túi máy bọc kháng sinh đã giảm 40% nguy cơ nhiễm trùng CIED tương đối trong thời gian theo dõi 12 tháng. Vấn đề quan trọng hiện nay là xác định bệnh nhân nào sẽ được hưởng lợi khi cân bằng giữa chi phí -hiệu quả của chiến lược dự phòng kháng sinh này20.
III.1.2. Thực hành lâm sàng
Việc sử dụng Cefazolin trước thủ thuật là một phương pháp chuẩn đã được nghiên cứu.
Vancomycin là một lựa chọn thay thế trong một số tình huống cụ thể, chẳng hạn như khi bệnh nhân có dị ứng với penicillin hoặc β-lactam, có tiền sử nhiễm trùng do Staphylococcus aureus kháng methicillin, hoặc khi cơ sở y rế có tỷ lệ nhiễm trùng do Staphylococcus aureus kháng methicillin hoặc Staphylococcus koagulaza âm tính kháng methicillin cao bất thường dựa trên dữ liệu trước đó. Quan trọng là phải tiêm vancomycin 120 phút trước khi rạch và liều dựa trên cân nặng là 20 mg/kg. Cần thêm sự tư vấn của dược sĩ đối với bệnh nhân có suy thận hoặc béo phì.
Rửa vết mổ bằng dung dịch muối là hợp lý cho bệnh nhân thực hiện cấy ghép thiết bị điện tử tim (CIED) hoặc máy tạo nhịp tim
Việc sử dụng kháng sinh sau phẫu thuật thường không được hỗ trợ theo như các dữ liệu đã công bố.
Việc sử dụng túi máy tẩm kháng sinh có thể được xem xét cho bệnh nhân có nguy cơ cao về CIED-IE, bao gồm bệnh nhân có nguy cơ cao về hình thành huyết khối trong phẫu thuật.
III.2. Có cần ngừng hoặc thay đổi liệu pháp chống đông khi cấy ghép/sửa đổi CIED không?
Cả việc tiếp tục hay tạm ngừng thuốc chống đông đường uống trực tiếp (DOAC) đều được chấp thuận khi thực hiện cấy ghép hoặc sửa đổi CIED, vì cả hai phương pháp đều có liên quan đến nguy cơ hình thành huyết khối thấp.
Đối với bệnh nhân đang sử dụng Warfarin, việc thực hiện cấy ghép CIED với tỷ lệ chuẩn hóa quốc tế (INR) nên trong khoảng từ 2 đến 3,54.
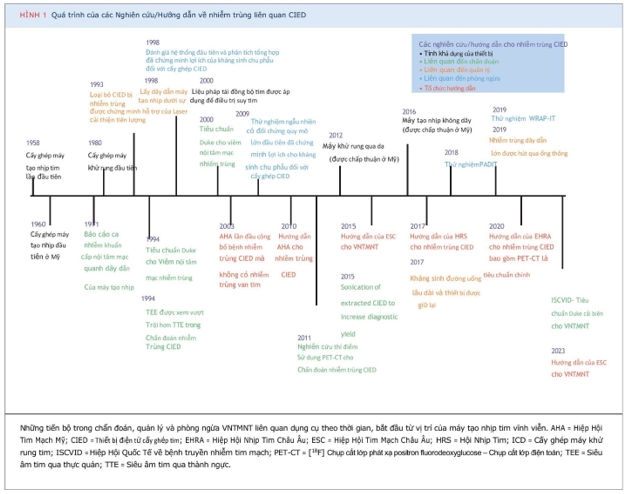
IV. HƯỚNG TƯƠNG LAI VÀ KẾT LUẬN
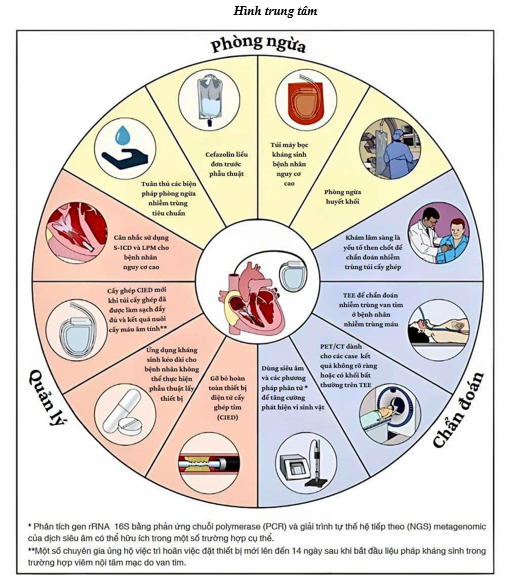
Chẩn đoán và quản lý CIED-IE vẫn còn nhiều thách thức, như minh họa ở đây trong nhiều trường hợp lâm sàng. Nhiều khía cạnh cần nghiên cứu thêm khi lĩnh vực này đang có xu hướng phát triển. Thứ nhất, mặc dù sử dụng PET-CT có tăng lên trong những năm gần đây và cho thấy hứa hẹn trong chẩn đoán CIED-IE, tuy nhiên độ nhạy và độ đặc hiệu của nó vẫn chưa hoàn hảo. Các chiến lược như kết hợp PET-CT với TEE, khám phá các chất đánh dấu mới ngoài [18F]-fluorodeoxyglucose, áp dụng trí tuệ nhân tạo và kết hợp các dấu hiệu ngoài tim, chẳng hạn như thuyên tắc mạch nhiễm trùng, có thể cải thiện độ chính xác chẩn đoán của PET-CT. Thứ hai, các kỹ thuật phân tử mới hơn như DNA không có tế bào và kỹ thuật giải trình tự tập hợp gen (metagenomic sequencing) từ cả máu và dịch nuôi cấy nhờ siêu âm của các thiết bị chiết xuất có thể tăng cường chẩn đoán vi sinh của CIED-IE khi nuôi cấy âm tính, nhưng cần nhiều nghiên cứu hơn về độ nhạy, độ đặc hiệu, tác động của chúng đối với việc lựa chọn liệu pháp kháng sinh cũng như là hiệu quả. Thứ ba, lợi ích của việc sử dụng kháng sinh lâu dài khi các thiết bị được giữ lại là không rõ ràng và cần được nghiên cứu thêm. Thứ tư, cần cải thiện các công cụ phân tầng nguy cơ để xác định những bệnh nhân có nguy cơ cao có thể được hưởng lợi từ việc theo dõi, dự phòng hoặc can thiệp sớm tích cực hơn (hình trung tâm).
V. GIẢI THÍCH THÊM MỘT SỐ THUẬT NGỮ TRONG BÀI
– Metagenomics is the study of the structure and function of entire nucleotide sequences isolated and analyzed from all the organisms (typically microbes) in a bulk sample. Metagenomics is often used to study a specific community of microorganisms, such as those residing on human skin, in the soil or in a water sample: Metagenomics là nghiên cứu về cấu trúc và chức năng của toàn bộ trình tự nucleotide được phân lập và phân tích từ tất cả các sinh vật (thường là vi khuẩn) trong một mẫu lớn. Metagenomics thường được sử dụng để nghiên cứu một cộng đồng vi sinh vật cụ thể, chẳng hạn như những vi khuẩn cư trú trên da người, trong đất hoặc trong mẫu nước
– Metagenomic next-generation sequencing (mNGS): kỹ thuật giải trình tự tập hợp gen thế hệ mới so với kỹ thuật giải trình tự lâu đời của Sanger từ 1977 (dựa trên phương pháp giản đoạn chuỗi hay chain-determination). Giải trình tự Sanger tốn kém, chậm, không hiệu quả cho metagenomic. mNGS được sử dụng chủ yếu để tìm ra tác nhân gây bệnh trong mẫu. mNGS bao gồm nhiều kỹ thuật giải trình tự khác nhau:
+ Whole metagenome shotgun sequencing: giải trình tự toàn bộ hệ gen trong mẫu không nhắm vào gen hay vi sinh vật cụ thể nào (untargeted mNGS method), cho cái nhìn toàn cảnh về toàn bộ vật liệu di truyền trong mẫu của tất cả vi khuẩn, virus, nấm và ký sinh trùng, phân tích đa dạng vi sinh, chức năng với nhau và con đường chuyển hoá của chúng, bằng cách phân mảnh (shotgun or fragment) ngẫu nhiên các mảnh DNA và giải trình tự -> mục đích phân loài và phân tích chức năng, tương tác của chúng trong cộng đồng vi sinh vật
+ Giải trình tự amplicon hay còn gọi là giải trình tự toàn bộ hệ gen trúng đích/có chủ đích vào sản phẩm của quá trình nhân lên/khuếch đại (targeted metagenomic sequencing) -> để phân loài
+ Giải trình tự RNA -> cho nghiên cứu hoạt động chức năng và biểu hiện gen
+ Viral metagenomics giải trình tự dna của virus hiện diện trong môi trường hay vật chủ
– Metagenomic shotgun sequencing: thuật ngữ này trong các trang công nghệ sinh học phân tử cũng không dịch ra tiếng Việt, nhưng bản chất của nó là phương pháp Tin sinh học phân tích giải mã trình tự bộ gen/ vật liệu di truyền DNA đồng loạt của toàn bộ vi sinh vật trong quần thể trên mẫu vật liệu, bằng cách lắp ráp các mảnh nhỏ DNA và phiên giải, giúp xác định các loài vi sinh vật có mặt trong cộng đồng và các gen chúng mang, cung cấp một cái nhìn toàn diện về toàn bộ hệ vi sinh trên mẫu vật.
TÀI LIỆU THAM KHẢO
- Vaidya Vaibhav R, Asirvatham R, Kowlgi Gurukripa N, et al. Trends in cardiovascular implantable electronic device insertion between 1988 and 2018 in Olmsted County. J Am Coll Cardiol EP. 2022; 8:88–100
- Han HC, Hawkins NM, Pearman CM et al. Epidemiology of cardiac implantable electronic device infections: incidence and risk factors. Europace. 2021; 23: iv3–iv10.
- S et al. Infective Endocarditis Involving Implanted Cardiac Electronic Devices. J Am Coll Cardiol 2024; 83:1326–1337
- LM et al. Update on Cardiovascular Implantable Electronic Device Infections and Their Prevention, Diagnosis, and Management: A Scientific Statement From the American Heart Association. Circulation. 2023; 148: e00–e00. DOI: 10.1161/CIR.0000000000001187
- Blomström-Lundqvist C, Traykov V et al. European Heart Rhythm Association (EHRA)
international consensus document on how to prevent, diagnose, and treat cardiac implantable
electronic device infections-endorsed by the Heart Rhythm Society (HRS), the Asia Pacific Heart Rhythm Society (APHRS), the Latin American Heart Rhythm Society (LAHRS), International Society for Cardiovascular Infectious Diseases (ISCVID) and the European Society of Clinical Microbiology and Infectious Diseases (ESCMID) in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS). Europace. 2020; 22:515–549. - Van der Vaart TW, Prins JM, van Werkhoven CH, et al. Positive Impact of [18F] FDGPET/CT on mortality in patients with staphylococcus aureus bacteremia explained by immortal time bias. Clin Infect Dis. 2023; 77:9–15
- Delgado V, Ajmone Marsan N, de Waha S, et al. 2023 ESC guidelines for the management of endocarditis: developed by the Task Force on the Management of Endocarditis of the European Society of Cardiology (ESC) endorsed by the European Association for Cardio-Thoracic Surgery (EACTS) and the European Association of Nuclear Medicine (EANM). Eur Heart J. 2023; 44:3948–4042.
- Mahmood M, Kendi AT, Farid S, et al. Role of 18F-FDG PET/CT in the diagnosis of cardiovascular implantable electronic device infections: a meta-analysis. J Nucl Cardiol. 2019; 26:958–970
- Fowler VG Jr, Durack DT, Selton-Suty C, et al. The 2023 Duke-ISCVID criteria for infective endocarditis: updating the modified Duke Criteria. Clin Infect Dis. 2023; 77:518–526
- Bontempi L, Arabia G, Salghetti F, et al. Lead-related infective endocarditis with vegetations: prevalence and impact of pulmonary embolism in patients undergoing transvenous lead extraction. J Cardiovasc Electrophysiol. 2022; 33:2195–2201.
- Polewczyk A, Jachec W, Tomaszewski A, et al. Lead-related infective endocarditis: factors influencing the formation of large vegetations. Europace. 2016; 19:1022–1030.
- George MP, Esquer Garrigos Z, Vijayvargiya P, et al. Discriminative ability and reliability of transesophageal echocardiography in characterizing cases of cardiac device lead vegetations versus noninfectious echodensities. Clin Infect Dis. 2020; 72:1938–1943.
- Patel NJ, Singleton MJ, Brunetti R et al. Evaluation of leadbased echodensities on transesophageal echocardiogram in patients with cardiac implantable electronic devices. J Cardiovasc Electrophysiol. 2023; 34:7–13.
- Esquer Garrigos Z, George MP, Farid S, et al. Diagnostic evaluation and management of culturenegative cardiovascular implantable electronic device infections. Pacing Clin Electrophysiol. 2018; 41:933–942
- squer Garrigos Z, Sohail MR, Greenwood Quaintance KE, et al. Molecular approach to diagnosis of cardiovascular implantable electronic device infection. Clin Infect Dis. 2020; 70:898–906.
- Olsen T, Justesen US, Nielsen JC, et al. Microbiological diagnosis in cardiac implantable electronic device infections detected by sonication and next-generation sequencing. Heart Rhythm. 2022; 19:901–908
- Wazni O, Epstein LM, Carrillo RG, et al. Lead extraction in the contemporary setting: the LEXICON study: an observational retrospective study of consecutive laser lead extractions. J Am Coll Cardiol. 2010; 55:579–586.
- Sood N, Martin DT, Lampert R et al. Incidence and predictors of perioperative complications with transvenous lead extractions: real-world experience with national cardiovascular data registry. Circ Arrhythm Electrophysiol. 2018; 11: e004768
- Krahn AD, Longtin Y, Philippon F, et al. Prevention of arrhythmia device infection trial: the PADIT trial. J Am Coll Cardiol. 2018; 72: 3098–3109.
- Tarakji KG, Mittal S, Kennergren C, et al. Antibacterial envelope to prevent cardiac implantable device infection. N Engl J Med. 2019; 380: 1895–1905







