BS. NGUYỄN THANH HIỀN
BS. NGUYỄN PHẠM CAO MINH
- Mở đầu
Cứ mỗi 40 giây ở Hoa Kỳ sẽ có một bệnh nhân nhồi máu cơ tim mới, và hơn 1 triệu trường hợp hội chứng mạch vành cấp xảy ra mỗi năm, trong đó 1/3 là các trường hợp tái phát (1). Điều trị kháng kết tập tiểu cầu và những phương pháp để hạ thấp mức low-density lipoprotein là điều trị nền tảng để giảm thiểu nguy cơ tái phát các biến cố huyết khối xơ vữa sau hội chứng vành cấp (2). Từ khi phương pháp dùng kháng kết tập tiểu cầu kép xuất hiện (với clopidogrel ưu thế hơn aspirin trong phòng ngừa nhồi máu tái phát), hàng loạt nghiên cứu ra đã đẩy cao tối đa vai trò của các thuốc kết tập tiểu cầu tác dụng nhanh, hiệu quả và bền vững như ticagrelor và prasugrel. Và trong nghiên cứu đánh giá Cải thiện tiên lượng khi tối ưu hóa liệu pháp kháng kết tập tiểu cầu với Prasugrel – Tiêu sợi huyết ở bệnh nhân Nhồi máu cơ tim [Trial to Assess Improve-ment in Therapeutic Outcomes by Optimizing Platelet Inhibition with Prasugrel–Thrombolysis in Myocardial Infarction (TRITON–TIMI)], Prasugrel được chứng minh ưu thế hơn clopidogrel khi giảm biến cố gộp tim mạch (tử vong do nguyên nhân tim mạch, nhồi máu cơ tim, và đột quị) sau hội chứng vành cấp. Kết quả nghiên cứu này chỉ ra rằng tỉ lệ biến cố nhồi máu cơ tim tái phát giảm, đổi lại làm nguy cơ biến cố xuất huyết nặng tăng lên (3).
Trong nghiên cứu Liệu pháp kháng kết tập tiểu cầu và tiên lượng bệnh nhân [Platelet Inhibition and Patient Outcomes (PLATO)], Ticagrelor ưu thế hơn Clopidogrel trong giảm tỉ lệ biến cố gộp tim mạch (tử vong do nguyên nhân tim mạch, nhồi máu cơ tim, và đột quị) sau hội chứng vành cấp, trong khi không làm tăng biến cố xuất huyết nặng. Dù vậy, tỉ lệ xuất huyết không liên quan thủ thuật lại tăng lên. Các khuyến cáo của AHA-ACC đã cập nhật các thuốc kháng kết tập tiểu cầu này ban đầu với vai trò ngang hàng với Clopidogrel, và sau đó là ưu thế hơn Clopidogrel trong chiến lược điều trị. Dựa vào vai trò giảm đáng kể tỉ lệ nhồi máu cơ tim tái phát và tử vong trong nghiên cứu PLATO, sự áp dụng rộng rãi kết quả nghiên cứu vào điều trị nội khoa và can thiệp, hiệu quả nhanh và cơ chế tác dụng có thể đảo ngược của Ticagrelor so với prasugrel, các nhà lâm sàng đã đẩy mạnh việc sử dụng ticagrelor ở bệnh nhân hội chứng vành cấp (4-7).
Các nghiên cứu ngẫu nhiên đã cho thấy độ ưu thế của Prasugrel và Ticagrelor so với Clopidogrel ở bệnh nhân hội chứng vành cấp, và cả hai thuốc đều đạt mức khuyến cáo loại I sử dụng đối với bệnh nhân hội chứng vành cấp, có hay không ST chênh lên. Dù vậy, vẫn chưa có đầy đủ dữ liệu về hiệu quả tương đối của Ticagrelor so sánh với Prasugrel ở những bệnh nhân hội chứng mạch vành cấp đã được lên kế hoạch can thiệp xâm lấn (8, 9). Một điểm đáng chú ý là, chiến lược khởi trị Ticagrelor và Prasugrel là khác nhau ở bệnh nhân hội chứng vành cấp không ST chênh lên. Ở những bệnh nhân này, Ticagrelor được sử dụng trước khi chụp mạch vành chẩn đoán, trong khi Prasugrel chỉ được chỉ định sau khi đã có giải phẫu mạch vành sau chụp mạch vành, lợi ích của Prasugrel khởi trị trước chụp mạch vành chưa được ghi nhận (10-12).
Chính vì vậy, chúng ta cần thực hiện nghiên cứu lâm sàng ngẫu nhiên, đa trung tâm để so sánh hiệu quả và tính an toàn của hai chiến lược sử dùng từng thuốc này đối với hội chứng vành cấp. Trong hoàn cảnh này, nghiên cứu Liệu pháp chống huyết khối và stent nội mạch vành: tác dụng sớm và nhanh chóng trong điều trị bệnh mạch vành 5 [Intracoronary Stenting and Antithrombotic Regimen: Rapid Early Action for Coronary Treatment (ISAR-REACT)] được thực hiện, báo cáo bởi Schüpke và cộng sự (13). Chúng tôi xin trích dẫn nghiên cứu này và đưa ra các quan niệm hiện nay về vấn đề sử dụng Ticagrelor hay Prasugrel trong hội chứng mạch vành cấp.
- GIỚI THIỆU NGHIÊN CỨU
- THIẾT KẾ NGHIÊN CỨU VÀ GIÁM SÁT
ISAR-REACT 5 là một nghiên cứu nhãn mở, ngẫu nhiên, đa trung tâm, pha 4, không dưới sự hỗ trợ của các công ty dược phẩm. Thiết kế và tính cấp thiết của nghiên cứu đã được thông cáo trước đây. Các tác giả thực hiện nghiên cứu, với sự hỗ trợ từ ban điều hành, đã thiết kế nghiên cứu. Trung tâm nghiên cứu về Stent nội mạch vành và các liệu pháp chống huyết khối, hội viên của Deutsches Herzzentrum München ở Munich, Đức là trung tâm điều phối dữ liệu
Dữ liệu được phân tích bởi các nhà thống kê hợp tác với ban nghiên cứu. Các tác giả cũng cam kết về độ chính xác và toàn vẹn dữ liệu, độ trung thực của nghiên cứu với các phác đồ hiện hành, được thể hiện trên bài báo cáo toàn văn trên NEJM.org. Các viện khoa học tài trợ nghiên cứu không can thiệp vào thiết kế, thực hiện, hay điều chỉnh kết quả nghiên cứu. Thuốc Ticagrelor hoặc Prasugrel sử dụng trong nghiên cứu là sản phẩm thương mại trên thị trường và được tự mua bởi bệnh nhân.
- DÂN SỐ NGHIÊN CỨU
Bệnh nhân được chọn vào mẫu khi nhập viện với hội chứng vành cấp (nhồi máu cơ tim ST chênh lên, nhồi máu cơ tim ST không chênh lên hoặc đau ngực không ổn định) được lên kế hoạch can thiệp xâm lấn (vd: bệnh nhân được lên kế hoạch chụp mạch vành). Tiêu chuẩn loại trừ được xác định chủ yếu dựa vào đặc tính của các thuốc được nghiên cứu:
Những lý do chính để loại trừ bao gồm:
- Không dung nạp hoặc dị ứng với ticagrelor hoặc prasugrel;
- Tiền sử có đột quỵ, cơn thoáng thiếu máu não hoặc chảy máu nội sọ, khối u nội sọ đã được chẩn đoán, dị dạng động tĩnh mạch nội sọ hoặc phình động mạch nội sọ, đang chảy máu; số lượng tiểu cầu <100.000 / μL tại thời điểm sàng lọc; thiếu máu (huyết sắc tố <10 g / dL) tại thời điểm sàng lọc;
- Không thể ngưng sử dụng một cách an toàn thuốc chống đông uống trong thời gian nghiên cứu; INR lớn hơn 1,5 tại thời điểm sàng lọc;
- Điều trị bằng thuốc ức chế CYP3A mạnh uống hoặc truyền tĩnh mạch đồng thời (ví dụ: ketoconazole, itraconazole, voriconazole, telithromycin, voriconazole, telithromycin, clarithromycin, nefazodone, ritonavir, saquinavir, nefazodone, ritonavir, saquinavir, nelfinavir, indinavir, atazanavir, nước nho ép >1 L/ngày) hoặc chất nền CYP3A có chỉ số điều trị hẹp (ví dụ: cyclosporine, quinidine) hoặc thuốc gây sản sinh CYP3A mạnh (ví dụ: rifampin/rifampicin, phenytoin, carbamazepine, dexamethasone, phenobarbital) mà không thể ngưng sử dụng một cách an toàn;
- Đã sử dụng ≥ 1 liều ticagrelor hoặc prasugrel trong vòng 5 ngày trước phân loại ngẫu nhiên.
- NGẪU NHIÊN HÓA
Ở mỗi trung tâm tham gia nghiên cứu, bệnh nhân sẽ nhận được mã nghiên cứu ngẫu nhiên bởi máy tính của trung tâm điều phối, được bảo mật trong phong bì giấy mờ, niêm phong kín. Những bệnh nhân đạt tiêu chuẩn nhận vào nghiên cứu và không có tiêu chuẩn loại trừ, sẽ được phân phối lần lượt vào nhóm sử dụng Ticagrelor hoặc prasugrel, với tỉ lệ phân phối ngẫu nhiên là 1:1. Thời điểm zero được tính từ khi bắt đầu phân phối ngẫu nhiên. Bệnh nhân nghiên cứu được phân nhóm theo khu vực địa lý nghiên cứu và tình trang lâm sàng (vd: hội chứng vành cấp có hay không ST chênh lên). Đảo trật tự đối tượng nghiên cứu (theo từng nhóm 4, 6, 8) được sử dụng ở từng phân nhóm
- QUY TRÌNH (PROTOCOL) SỬ DỤNG TRONG NGHIÊN CỨU
Quy trình điều trị với Ticagrelor khởi trị với liều tải 180 mg và liều duy trì 90 mg 2 lần/ngày. Bệnh nhân ở nhóm dùng Ticagrelor được sử dụng thuốc sớm nhất có thể sau khi phân phối ngẫu nhiên.
Quy trình điều trị với Prasugrel khởi trị với liều tải 60 mg và duy trì ở liều 10 mg 1 lần/ ngày. Ở những bệnh nhân 75 tuổi trở lên hoặc cân nặng dưới 60 kg, liều duy trì Prasugrel sẽ giảm còn 5mg /ngày.
Trong nhóm Prasugrel, thời điểm khởi trị thuốc tùy thuộc vào bệnh cảnh lâm sàng. Nếu bệnh nhân có hội chứng vành cấp với ST chênh lên, Prasugrel được khởi trị sớm nhất có thể sau phân phối ngẫu nhiên. Ở bệnh nhân hội chứng vành cấp không ST chênh lên, liều tải của Prasugrel sẽ được trì hoãn đến khi làm rõ giải phẫu mạch vành và sử dụng trước khi tiến hành can thiệp mạch vành (PCI) (vd: trước khi guidewire mở thông qua tổn thương). Ở bệnh nhân hội chứng vành cấp đã chụp mạch vành nhưng không phù hợp để thực hiện PCI, được điều trị bảo tồn, kháng kết tập tiểu cầu kép (aspirin và một trong hai thuốc trong nghiên cứu) được khuyến cáo.
- ĐỊNH NGHĨA CÁC CHỈ TIÊU LÂM SÀNG
Chỉ tiêu lâm sàng chính của nghiên cứu là tỉ lệ gộp của tỉ lệ tử vong, nhồi máu cơ tim và đột quị ở thời điểm 1 năm sau thời điểm zero.
Chỉ tiêu lâm sàng phụ bao gồm:
- Chỉ tiêu về tính an toàn, cụ thể là tỉ lệ xuất huyết sau 1 năm (xuất huyết type 3,4,5 trên thang điểm xuất huyết Bleeding Academic Research Consortium [BARC], trong đó giới hạn ừ 0 đến 5 điểm, điểm càng cao chỉ điểm mức xuất huyết càng nặng), (11)
- Tỉ lệ từng thành phần trong chỉ tiêu lâm sàng chính sau 1 năm
- Tỉ lệ xác định hay nguy cơ xảy ra huyết khối trong stent sau 1 năm.
Tất cả chỉ tiêu lâm sàng được hiệu chỉnh và bảo mật theo dữ liệu nguồn (vd: giấy ra viện, kết quả xét nghiệm, báo cáo từ đơn vị can thiệp, dữ liệu điện tâm đồ, chụp mạch vành) bởi hai chuyên gia hiệu chỉnh dữ liệu từ ban điều phối nghiên cứu. Dữ liệu ngẫu nhiên hóa được bảo mật khỏi các nhân viên hiệu chỉnh dữ liệu.
- THEO DÕI MẪU NGHIÊN CỨU
Kế hoạch theo dõi được lên ấn định vào ngày 30 (độ lệch ±10 ngày), sau 6 tháng (±1 tháng), và 12 tháng (1 tháng). Khi xảy ra biến cố liên quan chỉ tiêu lâm sàng, truy cập dữ liệu nguồn sẽ được kích hoạt. Tất cả biến cố nghiêm trọng và biến cố liên quan chỉ tiêu lâm sàng chính và phụ sẽ được giám sát tại chỗ. Ngoài ra, 100% dữ liệu nguồn sẽ được tái kiểm tra trong ít nhất 10% bệnh nhân ở tất cả trung tâm.
- PHÂN TÍCH DỮ LIỆU
Cỡ mẫu được tính toán dựa trên giả định tỉ lệ biến cố ở chỉ tiêu lâm sàng chính vào khoảng 10.0% ở nhóm Ticagrelor4 và 12.9% ở nhóm Prasugrel. Với giả định này, chúng tôi tính cỡ mẫu là 1895 bệnh nhân ở mỗi nhóm để nghiên cứu có độ mạnh 80% để xác định tỉ số nguy cơ (relative risk) thấp hơn 22.5% khi so sánh chỉ tiêu lâm sàng chính ở nhóm Ticagrelor với Prasugrel, với two-sided alpha mức 0.05, theo phương trình chi-square. Cần nghiên cứu trên 4000 bệnh nhân để bù đắp khả năng khuyết dữ liệu do mất dấu theo dõi.
Các biến số phân nhóm như đặc điểm nhân khẩu và tiền sử y khoa sẽ được tóm tắt dưới dạng tần số và tỉ lệ, so sánh bằng kiểm định chi-square. Các dữ liệu mang tính tiếp diễn sẽ được báo cáo dưới dạng trung bình với độ lệch chuẩn hoặc trung vị với độ trải giữa (interquartile ranges) và được so sánh sử dụng Student’s t hoặc kiểm định dấu hạng Wilcoxon rank-sum phi tham số.
Kiểm định giả thuyết không của nghiên cứu khẳng định không có sự khác biệt giữa ticagrelor and prasugrel khi điều trị bệnh nhân hội chứng vành cấp có kế hoạch can thiệp xâm (hazard ratio = 1). Kiểm định giả thuyết không ban đầu được thực hiện bởi mô hình Cox proportional-hazards bao gồm các biến số trong nhóm nghiên cứu, các trung tâm tham gia và phân tầng với bệnh cảnh lâm sàng (hội chứng vành cấp có hay không ST chênh lên) làm biến số bên thứ 3. Mức ý nghĩa xác định 2 phía (confirmatory two-sided significance level) được chọn là 5%. Mô hình Cox proportional-hazards cũng được dùng trong các phân tích dưới nhóm theo tuổi (<75 tuổi hoặc ≥75 tuổi), giới (nam hoặc nữ), tình trạng hút thuốc lá, cân nặng (<60 kg hay ≥60 kg), đái tháo đường (mắc đái tháo đường hoặc không), bệnh thận mạn (phân loại theo trung vị nồng độ creatinine), sốc tim (có hay không), bệnh cảnh lâm sàng (đau ngực không ổn định, NSTEMI, hay STEMI), và chiến lược điều trị (PCI, CABG, hay điều trị bảo tồn). Tần suất tích lũy của chỉ tiêu lâm sàng chính được tính toán theo phần mở rộng phương thức ước lượng tỉ lệ sống còn không biến cố Kaplan–Meier. Các chức năng tần suất tích lũy được tính toán theo các kết cục ngoài tử vong để truy tìm nguy cơ cạnh tranh. Ước lượng tác động của các chỉ tiêu lâm sàng phụđược thực hiện với khoảng tin cậy 95%. Một trường hợp ngoại lệ là chỉ tiêu về tính an toàn, đối tượng của kiểm định giả thuyết với mức ý nghĩa truy tìm 2 phía là 5%.
Tất cả phân tích, bao gồm cả chỉ tiêu lâm sàng chính, được thực hiện theo nguyên tắc phân tích theo phân bổ ngẫu nhiên ban đầu (vd: sẽ đưa vào phân tích mọi bệnh nhân được phân phối ngẫu nhiên vào các nhóm nghiên cứu, bất kể thuốc sử dụng thực tế sau đó). Duy nhất chỉ tiêu chí tính an toàn được phân tích trên số phân bổ ngẫu nhiên ban đầu có hiệu chỉnh, bao gồm những bênh nhân đã được sử dụng ít nhất 1 liều các thuốc trong nghiên cứu và được đánh giá biến cố xuất huyết thêm 7 ngày sau ngừng thuốc. Bệnh nhân được phân phối ngẫu nhiên đến khi tử vong, ngưng đồng thuận tiếp tục hợp tác nghiên cứu hoặc đến ngày cuối cùng còn liên lạc được bệnh nhân. Tỉ lệ sống còn không biến cố với thời gian theo dõi dưới 1 năm được tính như dữ liệu khuyết trong các phân tích thời hạn khởi phát biến cố (time-to-event).
- BỆNH NHÂN
Từ tháng 9/2013 đến tháng 2/2018, tổng cộng 4018 bệnh nhân được nhận vào nghiên cứu ở 23 trung tâm (21 trung tâm ở Đức và 2 trung tâm ở Ý); 2012 được phân vào nhóm sử dụng ticagrelor, 2006 bệnh bệnh nhân được phân vào nhóm prasugrel (Hình 1). Các đặc điểm cơ bản dân số nghiên cứu được liệt kê trong Bảng 1. Chẩn đoán nghi ngờ STEMI lúc nhập viện là khoảng 41.1%, NSTEMI là 46.2%, và đau ngực không ổn định là 12.7% bệnh nhân. Trước khi nhập viện, 34.7% và 35.6% ở bệnh nhân ở nhóm prasugrel có sử dụng aspirin, 5.0% bệnh nhân ở nhóm ticagrelor và 4.7% ở bệnh nhân ở nhóm prasugrel sử dụng clopidogrel. Ở nhóm bệnh nhân STEMI, khoảng thời gian từ khi khởi phát triệu chứng đến khi được phân bổ vào nhóm ngẫu nhiên là 3.2 giờ (độ trải giữa 1.8 đến 7.7) ở nhóm ticagrelor và 3.0 giờ (độ trải giữa 1.9 to 8.4) ở nhóm prasugrel.
 Hình 1. Sàng lọc, ngẫu nhiên hóa, điều trị và theo dõi.
Hình 1. Sàng lọc, ngẫu nhiên hóa, điều trị và theo dõi.

Lưu đồ cụ thể thiết kế nghiên cứu
: theo phác đồ ticagrelor được dùng liều sớm ở tất cả bệnh nhân, prasugrel không dùng liều sớm ở những bệnh nhân hội chứng vành cấp không ST chênh lên, vì vậy liều sớm được sử dụng ít hơn ở nhóm prasugrel. Chỉ tiêu lâm sàng chính được đánh giá ở tất cả bệnh nhân theo phân bổ ngẫu (dân số intention-to-treat). Bệnh nhân được đánh giá từ thời điểm bắt đầu phân bổ ngẫu nhiên (thời điểm zero) đến khi tử vong, ngưng đồng thuận tiếp tục hợp tác nghiên cứu hoặc đến ngày cuối cùng còn liên lạc được bệnh nhân. Tiêu chí tính an toàn là xuất huyết type 3, 4, hoặc 5 trên thang điểm xuất huyết Bleeding Academic Research Consortium [BARC], (trong đó giới hạn ừ 0 đến 5 điểm, điểm càng cao chỉ điểm mức xuất huyết càng nặng) được phân tích được phân tích trên số phân bổ ngẫu nhiên ban đầu có hiệu chỉnh bao gồm những bênh nhân đã được sử dụng ít nhất 1 liều các thuốc trong nghiên cứu và được đánh giá biến cố xuất huyết thêm 7 ngày sau ngừng thuốc. CABG: Bắc cầu mạch vành
* Dấu +/- biểu thị độ lệch chuẩn ±SD. Không có sự khác biệt giữa các nhóm về hồ sơ nhân khẩu và đặc điểm lâm sàng ban đầu. CABG -bắc cầu mạch vành, NSTEMI – nhồi máu cơ tim không ST chênh lên, PCI – can thiệp mạch vành qua da, STEMI -nhồi máu cơ tim ST chênh lên
† Huyết áp tâm thu không ghi nhận ở 3 bệnh nhân (1 trong nhóm ticagrelor và 2 trong nhóm prasugrel).
‡ Huyết áp tâm trương không ghi nhận ở 16 bn (7 trong nhóm ticagrelor và 9 trong nhóm prasugrel )
§ Nhịp tim không ghi nhận ở 2 bệnh nhân (1 ở mỗi nhóm).
¶ Chỉ số khối cơ thể (BMI) bằng cân nặng (kg) chia chiều cao (m) bình phương. BMI không ghi nhận ở 31 bệnh nhân (12 trong nhóm ticagrelor và 19 trong nhóm prasugrel).
‖ Creatinine không ghi nhận ở 6 bệnh nhân (5 trong nhóm ticagrelor và 1 trong nhóm prasugrel).
** Chiến lược điều trị không ghi nhận ở 4 bệnh nhân từ chối tiếp tục nghiên cứu
†† Một bệnh nhân nhóm Ticagrelor phải phẫu thuật bóc tách động mạch chủ.
- THỰC HIỆN VÀ THEO DÕI
Tổng cộng 84.1% bệnh nhân được tiến hành PCI, 4% CABG. Thuốc ức chế Glycoprotein IIb/IIIa được sử dụng ở 12.3% bệnh nhân PCI. Hơn 99% bệnh nhân được sử dụng aspirin khi xuất viện, liều dùng hằng ngày không quá 100 mg.
Trong nhóm bệnh nhân PCI đối với hội chứng vành cấp không ST chênh lên, khoảng thời gian từ lúc ngẫu nhiên hóa đến lúc sử dụng liều tải ticagrelor là 6 phút (độ trải giữa 1 đến 25) và 61 phút ở nhóm prasugrel (độ trải giữa 30 đến 142). Vì thiết kế nghiên cứu đặc biệt thực hiện liều sớm ticagrelor ở mọi bệnh nhân nhưng không sử dụng liều sớm prasugrel ở bệnh nhân hội chứng vành cấp không ST chênh lên, liều tải được sử dụng nhiều hơn ở nhóm ticagrelor (1985/ 2012 bệnh nhân [98.7%]) so với nhóm prasugrel (1728/ 2006 patients [86.1%]).
Khi xuất viện, 81.1% bệnh nhân nhóm ticagrelor và 80.7% bệnh nhân prasugrel tiếp tục sử dụng thuốc theo nhóm đã phân bổ ngẫu nhiên trước đó (Bảng S3 trong Phụ lục). Tại thời điểm 1 năm, 243/ 1602 bệnh nhân (15.2%) trong nhóm ticagrelor và 199/ 1596 patients (12.5%) trong nhóm prasugrel ngừng sử dụng thuốc (P = 0.03). Khoảng trung vị thời gian từ khi phân phối ngẫu nhiên đến khi ngừng thuốc là 84 ngày (độ trải giữa 23 đến 181) trong nhóm ticagrelor và 109 ngày (độ trải giữa 35 đến 220) trong nhóm prasugrel (P = 0.01).
Bệnh nhân được liên hệ qua điện thoại (83%), tái khám nội viện hoặc ngoại viện (10%), hoặc qua thư theo dõi theo mẫu thiết kế (7%). Theo dõi 1 năm hoàn tất ở hầu hết bệnh nhân ngoại trừ 90 trường hợp (41 bệnh nhân trong nhóm ticagrelor và 49 bệnh nhân trong nhóm prasugrel). Theo dõi không hoàn tất do ngưng đồng thuận hợp tác nghiên cứu ở 53 bệnh nhân (22 bệnh nhân trong nhóm ticagrelor và 31 bệnh nhân trong nhóm prasugrel). Trong số bệnh nhân không hoàn tất theo dõi, thời gian trung vị theo dõi là 31 ngày (độ trải giữa 3 đến 109) trong nhóm ticagrelor và 32 ngày (độ trải giữa 5 đến 55) trong nhóm prasugrel (P = 0.57). Không có sự khác biệt về đặc điểm lâm sàng ban đầu giữa các bệnh nhân trong nhóm theo dõi hoàn tất và không hoàn tất, ngoại trừ yếu tố chụp mạch vành được thực hiện ít hơn trong nhóm bệnh nhân không theo dõi hoàn tất.
- CÁC CHỈ TIÊU LÂM SÀNG
Các tiêu chí lâm sàng chính — tử vong do mọi nguyên nhân, nhồi máu cơ tim, và đột quị tại thời điểm 1 năm sau phân phối ngẫu nhiên — xảy ra trên 184/2012 bệnh nhân nhóm ticagrelor (9.1%) (Ước lượng Kaplan–Meier lúc 1 năm: 9.3%) và 137/2006 bệnh nhân nhóm prasugrel (6.8%) (Ước lượng Kaplan–Meier lúc 1 năm: 6.9%) (hazard ratio, 1.36; khoảng tin cậy 95% [CI], 1.09 đến 1.70; P = 0.006) (Hình 2 và Bảng 2). Tỉ lệ gộp tử vong do tim mạch, nhồi máu cơ tim và đột quị là 161/2012 bệnh nhân nhóm ticagrelor (8.1%) bệnh nhân nhóm ticagrelor và 124/2006 bệnh nhân nhóm prasugrel (6.3%) (hazard ratio, 1.32; 95% CI, 1.04 đến 1.66).Tỉ lệ từng thành phần trong tiêu chí lâm sàng chính được thể hiện trong Bảng 2. Tỉ lệ tử vong do mọi nguyên nhân tại thời điểm 1 năm là 4.5% trong nhóm ticagrelor và 3.7% trong nhóm prasugrel (hazard ratio, 1.23; 95% CI, 0.91 đến 1.68). Tỉ lệ nhồi máu cơ tim là 4.8% trong nhóm ticagrelor và 3.0% trong nhóm prasugrel (hazard ratio, 1.63; 95% CI, 1.18 đến 2.25). Tỉ lệ đột quị là 1.1% trong nhóm ticagrelor và 1.0% trong nhóm prasugrel (hazard ratio, 1.17; 95% CI, 0.63 đến 2.15).
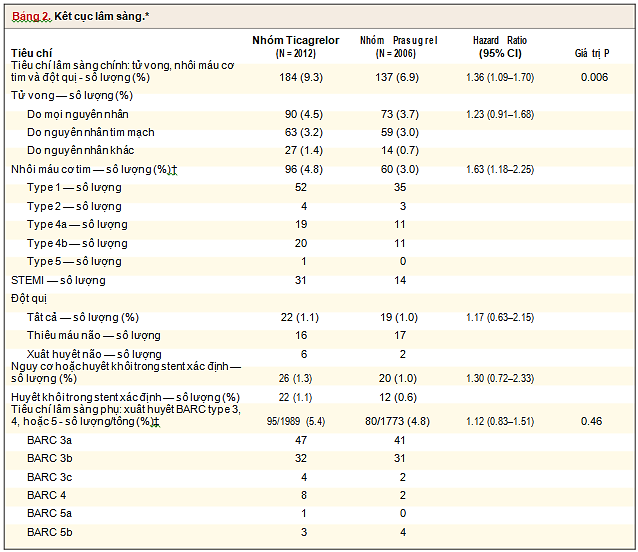
Phần trăm theo ước lượng Kaplan–Meier. Các chức năng tần suất tích lũy được tính toán theo các kết cục ngoài tử vong để truy tìm nguy cơ cạnh tranh.
† Phân loại nhồi máu cơ tim: nhồi máu tự phát (type 1), nhồi máu do mất thăng bằng cung cầu (type 2), nhồi máu liên quan PCI (type 4a), nhồi máu liên quan huyết khối trong stent (type 4b), và nhồi máu liên quan CABG (type 5).
‡ Thang điểm Bleeding Academic Research Consortium (BARC):type 3a – biểu hiện xuất huyết rõ ràng và giảm nồng độ hemoglobin từ 3 đên dưới 5 g/dL hay phải truyền máu; type 3b – biểu hiện xuất huyết rõ ràng và giảm nồng độ hemoglobin 5 g/dL trở lên dẫn đến chèn ép tim, phải can thiệp ngoại khoa hoặc thuốc co mạch; type 3c – xuất huyết nội sọ và xuất huyết nhãn cầu làm mất thị lực; type 4 – xuất huyết liên quan CABG; type 5a – khả năng xuất huyết đe dọa tính mạng; và type 5b – xuất huyết chắc chắn đe dọa tính mạng.
Dữ liệu về xuất huyết được phân tích ở tất cả những bênh nhân đã được sử dụng ít nhất 1 liều các thuốc trong nghiên cứu và được đánh giá biến cố xuất huyết thêm 7 ngày sau ngừng thuốc.
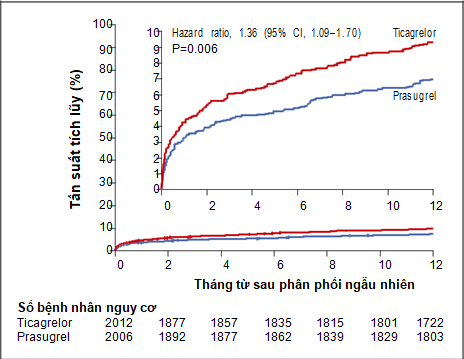
Hình 2.Tần suất tích lũy của tiêu chí lâm sàng chính sau 1 năm. Đường cong Kaplan–Meier cho thấytần suất tích lũy của tiêu chí lâm sàng chính, bao gồm tử vong, nhồi máu cơ tim và đột quị sau 1 năm. Biểu đồ bên trong thể hiện cùng dữ liệu với trục tung Y được phóng to.
Tỉ lệ nguy cơ hoặc xác định huyết khối trong stent là 1.3% trong nhóm ticagrelor và 1.0% trong nhóm prasugrel (hazard ratio, 1.30; 95% CI, 0.72 đến 2.33). Dữ liệu tiêu chí lâm sàng chính trong các phân tích dưới nhóm được thể hiện ở Hình 3.
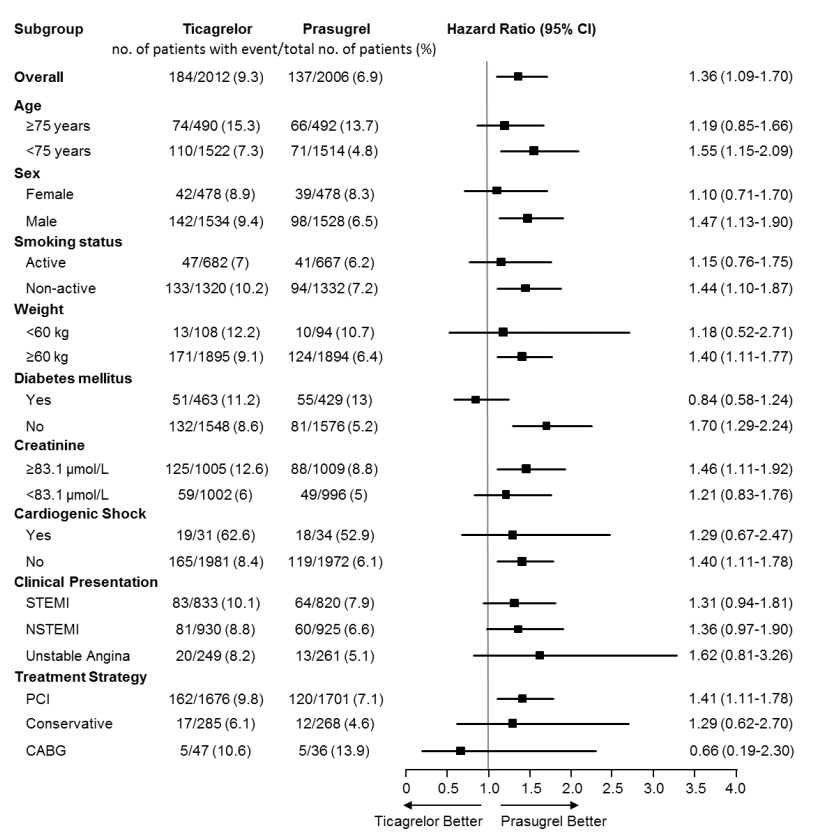
Hình 3. Tỉ lệ biến cố và tỷ lệ rủi ro trong một năm của tiêu chí chính, nhồi máu cơ tim hoặc đột quỵ trong các phân nhóm đã phân chia từ trước
Trong phân tích theo phân bổ ngẫu nhiên ban đầu hiệu chỉnh (bao gồm tất cả bênh nhân đã được sử dụng ít nhất 1 liều các thuốc trong nghiên cứu và được đánh giá biến cố xuất huyết thêm 7 ngày sau ngừng thuốc), biến cố xuất huyết nặng (BARC type 3 đến 5) được ghi nhận ở 5.4% bệnh nhân nhóm ticagrelor và 4.8% bệnh nhân nhóm prasugrel (hazard ratio, 1.12; 95% CI, 0.83 đến 1.51; P = 0.46) (Hình. 4). Trên dân số phân bổ ngẫu nhiên ban đầu, biến cố xuất huyết nặng (BARC type 3 đến 5) được ghi nhận ở 5.8% bệnh nhân nhóm ticagrelor và 5.6% bệnh nhân nhóm prasugrel (hazard ratio, 1.04; 95% CI, 0.80 đến 1.34). Trên dân số phân bổ ngẫu nhiên ban đầu, xuất huyết BARC type 1 hoặc 2 được báo cáoở 13.8% bệnh nhân nhóm ticagrelor và 15.1% bệnh nhân nhóm prasugrel (hazard ratio, 0.90; 95% CI, 0.76 đến 1.06).
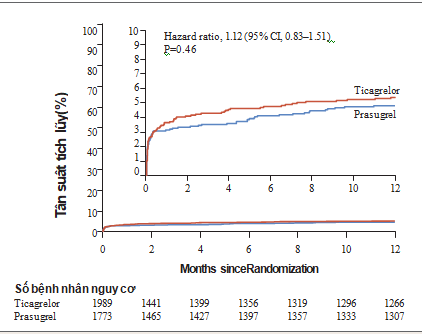
Hình 4. Tần suất tích lũy của tiêu chí tính an toàn sau 1 năm.
Đường cong Kaplan–Meier cho thấytần suất tích lũy của tiêu chí tính an toàn sau 1 năm, cụ thể là tỷ lệ xuất huyết BARC type 3, 4, hoặc 5. Phân tích theo phân bổ ngẫu nhiên ban đầu hiệu chỉnh (bao gồm tất cả bênh nhân đã được sử dụng ít nhất 1 liều các thuốc trong nghiên cứu và được đánh giá biến cố xuất huyết thêm 7 ngày sau ngừng thuốc). Biểu đồ bên trong thể hiện cùng một dữ liệu với trục tung Y được phóng to.
- BÀN LUẬN CÁC CHUYÊN GIA
Trong nghiên cứu ngẫu nhiên, đa trung tâm này, prasugrel tỏ ra ưu thế hơn ticagrelor khi so sánh tỉ lệ gộp tử vong, nhồi máu cơ tim và đột quị sau 1 năm ở bệnh nhân hội chứng vành cấp có kế hoạch can thiệp xâm lấn. Tỉ lệ biến cố thấp hơn chủ yếu do tỉ lệ nhồi máu tái phát thấp hơn ở nhóm prasugrel. Lợi ích về mặt biến cố thiếu máu thấp hơn của prasugrel không phải đổi lại bằng tăng nguy cơ xuất huyết. Kết quả nhất quán ở mọi thể lâm sàng của hội chứng vành cấp.
Một đặc điểm riêng biệt của nghiên cứu này là nghiên cứu không chỉ so sánh hai thuốc kháng kết tập tiểu cầu, mà còn so sánh hai chiến lược điều trị liên quan đến hai thuốc này. Một chiến lược dùng ticagrelor, và chiến lược còn lại dùng prasugrel. Họ cũng lưu ý rằng chiến lược liều tải của ticagrelor và prasugrel là khác nhau trên bệnh nhân hội chứng mạch vành cấp ST không chênh lên. Ở những bệnh nhân này, ticagrelor thường được sử dụng trước khi chụp mạch vành chẩn đoán nhưng prasugrel chỉ sử dụng sau khi giải phẫu mạch vành đã được đánh giá bằng phương pháp chẩn đoán hình ảnh vì không thấy lợi ích nào hơn khi sử dụng prasugrel trước. Do đó, kết quả nghiên cứu cho thấy rằng những bệnh nhân hội chứng mạch vành cấp có kế hoạch đánh giá xâm lấn, prasugrel, được sử dụng như cách kê toa đã phê duyệt, có tỷ lệ tử vong, nhồi máu cơ tim hoặc đột quỵ thấp hơn đáng kể, và không có sự khác biệt về tỉ lệ chảy máu nghiêm trọng so với ticagrelor được sử dụng như cách kê toa đã phê duyệt. Ngoài ra, nghiên cứu hiện tại cũng thấy chiến lược trì hoãn và sử dụng prasugrel sau khi có dữ liệu hình thái mạch vành ưu thế hơn liều tải ticagrelor ở bệnh nhân bệnh nhân hội chứng vành cấp không ST chênh lên (13, 14).
Một cơ chế giải thích ưu thế của prasugrel so với Ticagrelor có thể do liệu pháp điều trị với prasugrel ở bệnh nhân can thiệp mạch vành cho hội chứng vành cấp cho thấy hiệu quả cải thiện chức năng nội mô tốt hơn, kháng tiểu cầu mạnh hơn và giảm nồng độ IL-6, qua đó giúp thay đổi tiên lượng bệnh nhân theo nghiên cứu của Schnorbus. B và cs: “Hiệu quả của clopidogrel so với prasugrel và ticagrelor trên chức năng, thông số phản ứng viêm nội mạc mạch máu và chức năng tiểu cầu ở bệnh nhân hội chứng vành cấp thực hiện can thiệp mạch vành: Một nghiên cứu song song, ngẫu nhiên và mù đơn” (hình 5, 6, 7) (15).
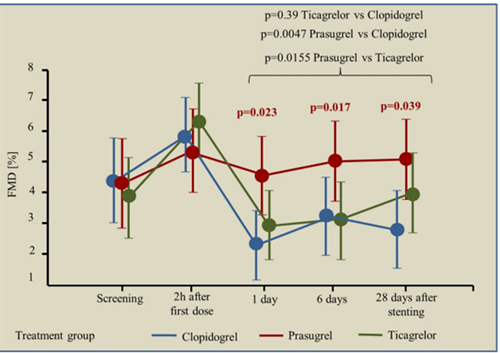
Hình 5. Tác động của 3 nhóm thuốc nghiên cứu trên dãn mạch điều hòa theo lưu lượng. PCI làm bất hoạt khả năng này ở nhóm clopidogrel và ticagrelor, tuy nhiên chức năng này được bảo tồn ở nhóm sử dụng prasugre
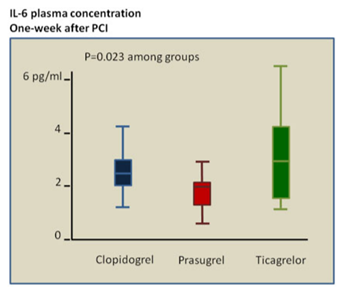
Hình 6. Tác động của 3 nhóm thuốc nghiên cứu trên nồng độ interleu-kin-6 huyết tương sau can thiệp mạch vànhNồng độ trong nhóm prasugrel là thấp nhất.
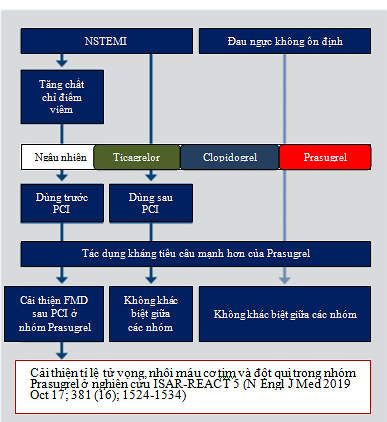
Hình 7. Bệnh nhân NSTEMI hoặc đau ngực không ổn định được phân phối ngẫu nhiên dùng 1 trong 3 kháng tiểu cầu. Prasugrel cho thấy tác dụng kháng tiểu cầu mạnh với hiệu quả cải thiện chức năng nội mạc mạch máu trước và sau đặt stent. Tác dụng này chỉ biểu hiện khi prasugrel được dùng trước PCI. Ghi nhận này đồng thuận với kết quả nghiên cứu ISAR REACT-5.
Dù có nhiều hạn chế, bao gồm không phải nghiên cứu thiết kế mù đôi, xác định biến cố ưu thế thông qua liên lạc điện thoại, và 19% bệnh nhân không tiếp tục dùng thuốc nghiên cứu sau xuất viện, nghiên cứu vẫn mang tính bước ngoặt vì đa trung tâm, và không dưới sự hỗ trợ của công ty dược phẩm. Đây là nghiên cứu đối đầu trực diện giữa các thuốc ức chế thụ thể P2Y12 mới, là nghiên cứu trung thực gợi nhắc tầm quan trọng của nghiên cứu lâm sàng đưa ra bằng chứng khoa học, thay vì ngoại suy từ các so sánh gián tiếp và các nghiên cứu thay thế. Các nhà nghiên cứu đã giảm liều duy trì Prasugrel phù hợp với những bệnh nhân 75 tuổi trở lên hoặc có cân nặng dưới 60 kg (khoảng 30% dân số nghiên cứu) và loại bỏ mẫu đối với những bệnh nhân có tiền căn bệnh lý mạch máu não (nhóm đã được đánh giá có nguy cơ nguy hại lâm sàng thực tế trong nghiên cứu TRITON–TIMI). Những phương pháp trên có thể giúp làm rõ hiệu quả của Prasugrel trong nghiên cứu ISAR-REACT 5.
Nghiên cứu này cũng dẫn đến nhiều ghi nhận đáng chú ý và nhấn mạnh tính phức tạp cũng như thử thách khi sử dụng ức chế thụ thể P2Y12 mới. Gần 3% bệnh nhân xuất viện với Ticagrelor ngưng sử dụng thuốc do triệu chứng khó thở. Đây là tác dụng phụ chủ quan của Ticargrelor đã được ghi nhận, dù tỉ lệ xảy ra vẫn chưa được chứng thực trên các nghiên cứu nhãn mở. Trong nghiên cứu này, những bệnh nhân điều trị với Ticagrelor bỏ thuốc sau xuất viện sớm hơn và nhiều hơn ở nhóm dùng Prasugrel (15.2% so với 12.5%, P = 0.03). Vì vậy, Prasugrel tỏ ra ưu thế hơn Ticagrelor khi so sánh về phương diện tác dụng phụ. Cũng cần lưu ý, số lượng bệnh nhân được loại khỏi phân tích tính an toàn ở nhóm dùng Prasugrel nhiều hơn gấp 10 lần so với Ticagrelor, điều này có thể ảnh hưởng đến kết quả tỉ lệ xuất huyết ở pha 4 của nghiên cứu.
Tóm lại, mặc dù dữ liệu nghiên cứu dài hạn và dữ liệu bổ sung so sánh hiệu quả còn chưa đầy đủ, Prasugrel đã trở thành lựa chọn ức chế thụ thể P2Y12 phù hợp đối với bệnh nhân hội chứng vành cấp. Prasugrel nên được sử dụng thay thế Ticagrelor ở những bệnh nhân thích hợp (NMCT St chênh, hoặc NMCT không ST chênh lên có chỉ định can thiệp (Hình 8) (14).
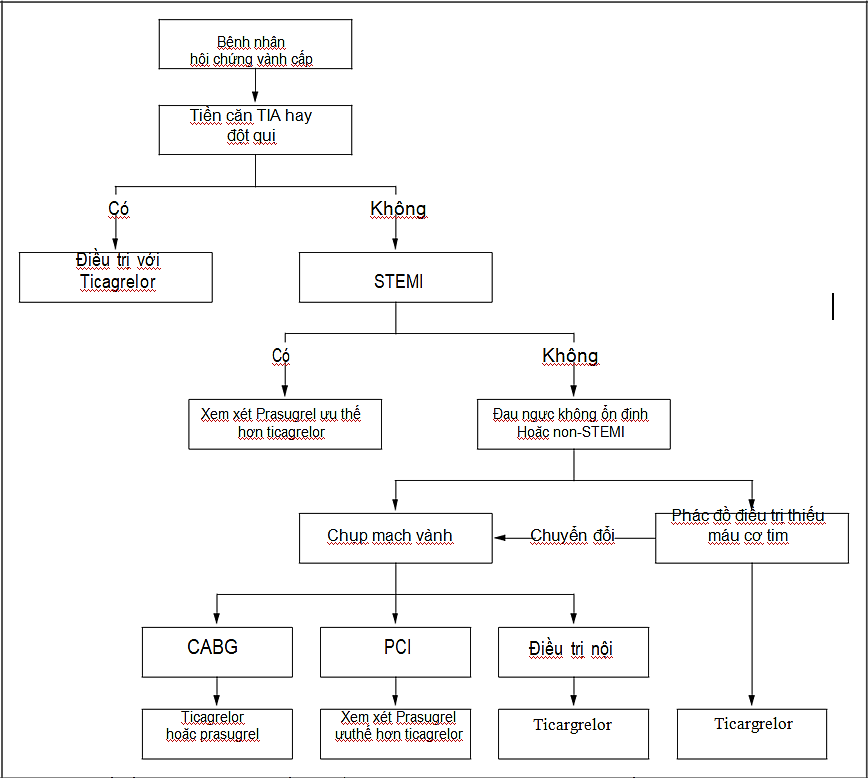
Hình 8. Lưu đồ đề nghị lựa chọn ức chế thụ thể P2Y12 cho bện nhân Hội chứng vành cấp.
Phác đồ điều trị thiếu máu cơ tim đề nghị khởi trị với điều trị nội khoa và chỉ định chụp mạch vành khi bệnh nhân có triệu chứng thiếu máu cơ tim tái phát hoặc khi điều trị nội khoa thất bại, các dấu chỉ lâm sàng tình trạng nguy cơ cao, hoặc có bằng chứng khách quan tình trạng thiếu máu cơ tim rất nặng. CABG: bắc cầu mạch vành, PCI: can thiệp mạch vành qua da, STEMI: nhồi máu cơ tim ST chênh lên, TIA: cơn thiếu máu não thoáng qua.
Tài liệu tham khảo
- Benjamin EJ, Muntner P, Alonso A, et al. Heart disease and stroke statistics —2019 update: a report from the American Heart Association. Circulation 2019; 139(10):e56-e528
- Brandt JT, Payne CD, Wiviott SD, et al. A comparison of prasugrel and clopidogrel loading doses on platelet function: magnitude of platelet inhibition is related to active metabolite formation. Am Heart J 2007;153(1):66.e9-66.e16.
- Gurbel PA, Bliden KP, Butler K, et al. Randomized double-blind assessment of the ONSET and OFFSET of the antiplatelet effects of ticagrelor versus clopidogrel in patients with stable coronary artery disease: the ONSET/OFFSET study. Circulation 2009;120:2577-85.
- Wallentin L, Becker RC, Budaj A, et al. Ticagrelor versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2009;361:1045-57.
- Wiviott SD, Braunwald E, McCabe CH, et al. Prasugrel versus clopidogrel in patients with acute coronary syndromes. N Engl J Med 2007;357:2001-15.
- Amsterdam EA, Wenger NK, Brindis RG, et al. 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes: a report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines. J Am Coll Cardiol 2014;64(24):e139-e228.
- Neumann FJ, Sousa-Uva M, Ahlsson A, et al. 2018 ESC/EACTS guidelines on myocardial revascularization. Eur Heart J 2019;40:87-165.
- Z et al: Prasugrel Versus ticagrelor in Patients With acute Myocardial infarction treated With Primary Percutaneous coronary intervention: Multicenter randomized PragUe-18 study. Circulation. 016;134:1603–1612.
- Z et al: 1-Year Outcomes of Patients Undergoing Primary Angioplasty for Myocardial Infarction Treated With Prasugrel Versus Ticagrelor. J Am Coll Cardiol 2018;71:371–81.
- O’Gara PT, Kushner FG, Ascheim DD, et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines. Circulation 2013;127(4):e362-e425.
- Montalescot G, Bolognese L, Dudek D, et al. Pretreatment with prasugrel in non–ST-segment elevation acute coronary syndromes. N Engl J Med 2013;369:999-1010.
- Levine GN, Bates ER, Bittl JA, et al. 2016 ACC/AHA guideline focused update on duration of dual antiplatelet therapy in patients with coronary artery disease: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines: an update of the 2011 ACCF/ AHA/SCAI guideline for percutaneous coronary intervention, 2011 ACCF/AHA guideline for coronary artery bypass graft surgery, 2012 ACC/AHA/ACP/AATS/PCNA/SCAI/STS guideline for the diagnosis and management of patients with stable ischemic heart disease, 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction, 2014 AHA/ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes, and 2014 ACC/AHA guideline on perioperative cardiovascular evaluation and management of patients undergoing noncardiac surgery. Circulation 2016;134(10): e123-e155.
- Schüpke S, Neumann F-J, Menichelli M, et al. Ticagrelor or prasugrel in patients with acute coronary syndromes. N Engl J Med 2019;381:1524-34.
- H: Ticagrelor or Prasugrel in Acute Coronary Syndromes — The Winner Takes It All?
- B et al: Effects of clopidogrel vs. prasugrel vs. ticagrelor on endothelial function, inflammatory parameters, and platelet function in patients with acute coronary syndrome undergoing coronary artery stenting: a randomized, blinded, parallel study. European Heart Journal (2020) 0, 1–10. doi:10.1093/eurheartj/ehz917.







