“Rationale and protocol of the Dapagliflozin And Prevention of Adverse outcomes in Chronic Kidney Disease (DAPA-CKD) randomized controlled trial”, Nephrol Dial Transplant (2020) 35: 274–282 doi:10.1093/ndt/gfz290
Hiddo J.L. Heerspink 1,2, Bergur V. Stefansson3, Glenn M. Chertow4, Ricardo Correa-Rotter5, Tom Greene6, Fan-Fan Hou7, Magnus Lindberg3, John McMurray8, Peter Rossing9,10, Roberto Toto11,Anna Maria Langkilde3 and David C. Wheeler2,12
1Department of Clinical Pharmacy and Pharmacology, University Medical Center Groningen, University of Groningen, Groningen, The Netherlands, 2George Institute for Global Health, George Institute, Camperdown, Sydney, NSW, Australia, 3Late Stage Development, Cardiovascular, Renal and Metabolism, BioPharmaceuticals R&D, AstraZeneca, Gothenburg, Sweden, 4Division of Nephrology, Department of Medicine, Stanford University School of Medicine, Stanford, CA, USA, 5National Institute of Medical Science and Nutrition Salvador Zubira´n, Tlalpan, Mexico City, Mexico, 6Department of Internal Medicine, University of Utah, Salt Lake City, UT, USA, 7Division of Nephrology, National Clinical Research Center for Kidney Disease, Nanfang Hospital, Southern Medical University, Guangzhou, China, 8British Heart Foundation, Cardiovascular Research Centre, University of Glasgow, Glasgow, UK, 9Steno Diabetes Center Copenhagen, Gentofte, Denmark, 10Department of Clinical Medicine, University of Copenhagen, Copenhagen, Denmark, 11Department of Internal Medicine, University of Texas Southwestern Medical Center, Dallas, TX, USA and 12Department of Renal Medicine, University College London, London, UK
LƯỢC DỊCH VÀ HIỆU ĐÍNH: ThS.BS. NGUYỄN THỊ THU HƯƠNG
BV Nội tiết TW
TÓM TẮT
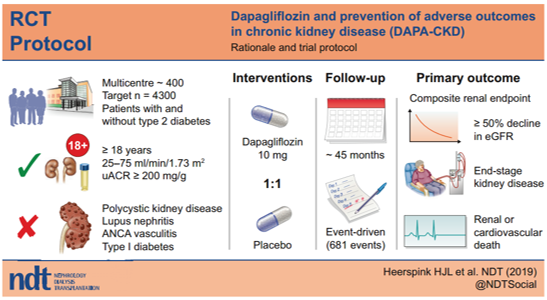
Tổng quan: Các thử nghiệm lâm sàng về kết cục tim mạch gần đây cho thấy thuốc ức chế chọn lọc kênh đồng vận chuyển Natri – glucose (SGLT2) làm chậm tiến triển của bệnh thận mạn (BTM) ở bệnh nhân đái tháo đường (ĐTĐ) typ 2 có nguy cơ tim mạch cao. Liệu những lợi ích đó có được mở rộng trên đối tượng BTM không có ĐTĐ hoặc bệnh tim mạch hay không là chưa được biết. Vì vậy, chúng tôi tiến hành thử nghiệm này nhằm đánh giá ảnh hưởng của thuốc ức chế SGLT2 trên tim mạch và thận ở những bệnh nhân BTM có và không có ĐTĐ.
Phương pháp: Đây là nghiên cứu ngẫu nhiên, mù đôi, đối chứng với giả dược trên 4300 bệnh nhân mắc BTM giai đoạn 2-4 và có albumin niệu, đại đa số bệnh nhân đang dùng thuốc ức chế hệ renin angiotensin liều tối ưu tại thời điểm tuyển chọn .
Kết quả: Sau khi sàng lọc, bệnh nhân có tỉ lệ albumin/ creatinin niệu (UACR) ≥ 200 mg/g và mức lọc cầu thận (eGFR) từ 25 – 75 ml/phút/1.73 m2 được phân ngẫu nhiên một nhóm sử dụng dapagliflozin 10 mg, 1 nhóm sử dụng giả dược. Trong số những bệnh nhân này,đảm bảo có ít nhất 30% không mắc ĐTĐ và không quá 10% có eGFR > 60 ml/ phút/ 1.73 m2. Tiêu chí chính của nghiên cứu là tổ hợp của tiêu chí giảm eGFR ≥ 50%, bệnh thận giai đoạn cuối, tử vong do tim mạch hoặc thận. Nghiên cứu sẽ kết thúc khi xảy ra 681các biến cố chính trên thận, cho phép phát hiện mức giảm nguy cơ tương đối 22% (với β=90% và α =0.05).
Kết luận: Nghiên cứu DAPA-CKD sẽ xác định liệu thuốc ức chế SGLT2 là dapagliflozin có được thêm vào hướng dẫn điều trị như là một liệu pháp giúp làm giảm tỷ lệ các biến cố trên tim mạch và thận ở bệnh nhân BTM các giai đoạn có và không có ĐTĐ.
- GIỚI THIỆU
Thuốc ức chế SGLT2 có tác dụng tăng thải glucose qua nước tiểu nhờ vậy làm giảm glucose máu và HbA1C độc lập với insulin ở bệnh nhân ĐTĐ typ 2[1]. Cho đến nay, ba thử nghiệm an toàn tim mạch lớn đã chứng minh lợi ích tim mạch và thận của các thuốc này không chỉ nhờ tác dụng kiểm soát đường máu. Đối tượng của các nghiên cứu này tập trung chủ yếu trên bệnh nhân ĐTĐ typ 2 có bệnh tim mạch hoặc yếu tố nguy cơ tim mạch, có chức năng thận bảo tồn, còn các bệnh nhân đã có BTM hoặc bệnh thận giai đoạn cuối thì chưa được quan tâm nhiều [2 -4]. Do đó, cần phải tiến hành thêm các thử nghiệm để xác định hiệu quả và tính an toàn của thuốc ức chế SGLT2 ở bệnh nhân có bệnh thận mạn. Thử nghiệm đầu tiên của thuốc ức chế SGLT2 trên bệnh nhân ĐTĐ typ 2 có bệnh thận mạn đã chứng minh sử dụng canagliflozin 100 mg/ ngày làm giảm 30% nguy cơ biến cố gộp trên thận (tăng gấp đôi creatinin, bệnh thận giai đoạn cuối hoặc tử vong do thận hoặc tim mạch) so với giả dược [5].
Trong các thử nghiệm trước đó, lợi ích bảo vệ thận của thuốc ức chế SGLT2 dường như không dựa vào tác dụng giảm nhẹ HbA1C (đặc biệt trên những bệnh nhân có mức lọc cầu thận thấp) mà còn nhờ một số cơ chế khác như kích hoạt phản hồi ống cầu thận, giảm tình trạng thiếu oxy trong thận. Do đó, thuốc ức chế SGLT2 có thể giúp bảo vệ thận trên bệnh nhân BTM không có ĐTĐ [6,7].
Vì vậy, chúng tôi tiến hành nghiên cứu này nhằm đánh giá hiệu quả làm giảm nguy cơ tim mạch và thận của thuốc dapagliflozin so với giả dược trên những bệnh nhân BTM có hoặc không có ĐTĐ typ 2 đã dùng thuốc ức chế men chuyển hoặc thuốc ức chế thụ thể liều tối ưu.
- PHƯƠNG PHÁP
- Tiêu chí nghiên cứu
Tiêu chí chính nhằm đánh giá hiệu quả của dapagliflozin so với giả dược giúp làm giảm các biến cố gộp trên thận (bao gồm giảm eGFR > 50%, bệnh thận giai đoạn cuối hoặc tử vong do bệnh thận) hoặc tử vong do tim mạch trên bệnh nhân BTM. Đồng thời, nghiên cứu cũng giúp đánh giá lợi ích của thuốc dapagliflozin so với giả dược trên tiêu chí gộp làm xấu đi chức năng thận, tiêu chí gộp về tỉ lệ nhập viện do suy tim hoặc tử vong do bệnh tim mạch và tử vong do mọi nguyên nhân. Các tiêu chí khám phá bao gồm sự thay đổi eGFR và UACR cũng như chất lượng cuộc sống liên quan đến sức khỏe.
- Thiết kế nghiên cứu
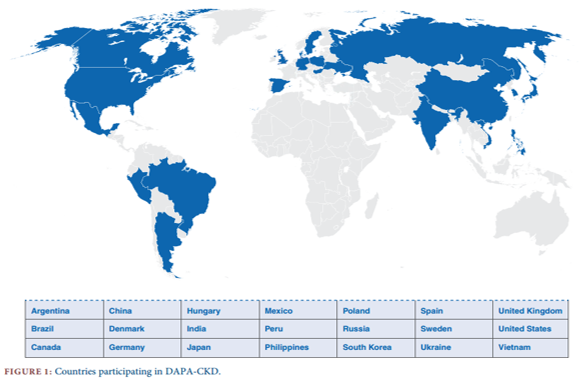
Đây là nghiên cứu đa quốc gia, đa trung tâm, ngẫu nhiên, mù đôi, 2 nhóm nghiên cứu song song có kiểm chứng giả dược. Nghiên cứu được tiến hành trên 4300 bệnh nhân tại gần 400 trung tâm trên 21 quốc gia (Biểu đồ 1).
- Đối tượng nghiên cứu
Nghiên cứu được tiến hành trên bệnh nhân trưởng thành BTM có eGFR từ 25 – 75 ml/ phút/ 1.73 m2 và có UACR từ 200 – 5000 mg/g (22.6 – 565 mg/mmol). Tiêu chuẩn loại trừ bao gồm những bệnh nhân mắc bệnh thận đa nang di truyền gen trội hoặc lặn trên nhiễm sắc thể thường, viêm thận lupus, viêm mạch ANCA và ĐTĐ typ 1.
Bảng 1. Tiêu chuẩn lựa chọn và loại trừ trong thử nghiệm DAPA-CKD
| Tiêu chuẩn lựa chọn |
| · Tuổi ≥ 18
· Mức lọc cầu thận từ 25 – 75 ml/phút/1.73 m2 · Tỉ số A/C niệu từ 200 – 5000 mg/g · Tình trạng bệnh nhân ổn định, có sử dụng ức chế men chuyển hoặc ức chế thụ thể liều tối ưu trong ít nhất 4 tuần trước khi tiến hành sàng lọc nếu không có chống chỉ định. |
| Tiêu chuẩn loại trừ |
| · Đái tháo đường typ 1
· Bệnh thận đa nang di truyền gen trội hoặc lặn trên nhiễm sắc thể thường, viêm thận lupus hoặc viêm mạch ANCA · Bệnh thận nguyên phát hoặc thứ phát điều trị bằng các thuốc gây độc tế bào hoặc ức chế miễn dịch trong vòng 6 tháng trước khi tuyển chọn. · Suy tim sung huyết NYHA IV · Nhồi máu cơ tim, đau thắt ngực không ổn định, đột quị hoặc tai biến mạch não thoáng qua trong vòng 8 tuần trước khi tuyển chọn. · Tái thông mạch vành (can thiệp mạch vành qua da hoặc phẫu thuật bắc cầu nối chủ vành) hoặc sửa/ thay thế van tim trong vòng 8 tuần trước khi tuyển chọn. · Bất kì tình trạng nào ngoài các nghiên cứu tim mạch và thận có kỳ vọng sống < 2 năm trong đánh giá điều tra lâm sàng. · Suy gan (AST hoặc ALT > 3 lần giới hạn trên bình thường hoặc Bilirubin toàn phần >2 lần giới hạn trên bình thường trong thời gian tuyển chọn) |
- Can thiệp
Sàng lọc bệnh nhân: Những bệnh nhân thỏa mãn tất cả các tiêu chuẩn lựa chọn gồm eGFR từ 25 – 75 ml/phút/ 1.73 m2 và UACR từ 200 – 5000 mg/g thực hiện tại phòng thí nghiệm trung tâm và các tiêu chuẩn loại trừ được lựa chọn tại các trung tâm nghiên cứu. Sau đó, những bệnh nhân này được phân ngẫu nhiên trong 14 (± 7) ngày. Tiêu chuẩn loại trừ bao gồm bệnh thận đa nang di truyền gen trội hoặc lặn trên nhiễm sắc thể thường, viêm thận lupus hoặc viêm mạch ANCA và bệnh thận nguyên phát hoặc thứ phát đã điều trị bằng các thuốc ức chế miễn dịch trong vòng 6 tháng trước.
Do sự thay đổi lớn của creatinin huyết thanh (eGFR) và UACR giữa các ngày nên có thể sàng lọc lần 2 cho những bệnh nhân không đủ tiêu chuẩn ở lần đầu tiên tùy thuộc vào quyết định của điều tra viên.
Phân ngẫu nhiên: 4300 bệnh nhân được phân nhóm ngẫu nhiên (1:1) nhận dapagliflozin 10 mg hoặc giả dược, uống cố định vào buổi sáng hàng ngày cùng với các điều trị thông thường bao gồm thuốc ức chế thụ thể hoặc ức chế men chuyển liều tối ưu. Phân bố đối tượng nghiên cứu đảm bảo có ít nhất 30% số bệnh nhân của cả nhóm đái tháo đường và không đái tháo đường được phân bố ở tất cả các trung tâm trên thế giới và không quá 10% số bệnh nhân có eGFR từ 60 -75 ml/phút/ 1.73 m2.
Điều trị mù đôi và quản lí bệnh nhân: Sau khi phân ngẫu nhiên, các lần thăm khám bao gồm: sau 2 tuần, sau 2, 4, 8 tháng và sau mỗi 4 tháng cho đến khi 681 bệnh nhân xảy ra biến cố chính. Lần thăm khám cuối cùng là 6 tuần sau khi đạt đủ biến cố chính. Các biến số cần theo dõi bao gồm các thông tin về tiêu chí nghiên cứu, biến cố ngoại ý, biện pháp điều trị, sự tuân thủ thuốc của bệnh nhân, dấu hiệu sinh tồn và các xét nghiệm máu và nước tiểu.
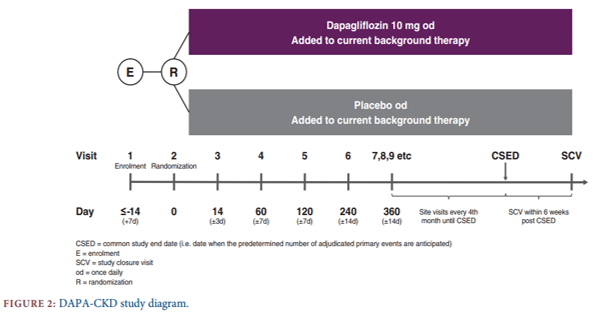
Những bệnh nhân gặp biến cố thận hoặc tim mạch vẫn được khuyên tiếp tục dùng thuốc nghiên cứu. Đối với bệnh nhân giảm thể tích dịch ngoại bào, hạ huyết áp hoặc suy giảm chức năng thận đột ngột cần giảm liều dapagliflozin 5mg hoặc dừng thuốc. Đối với bệnh nhân nhiễm toan đái tháo đường hoặc có thai cần dừng thuốc. Bệnh nhân có thể quyết định ngừng thuốc bất cứ thời gian nào. Những bệnh nhân dừng thuốc sớm được khuyến khích tiếp tục theo dõi theo lịch tại trung tâm nghiên cứu. Nếu không thể đến được, có thể lựa chọn theo dõi qua điện thoại hoặc thông qua các bác sĩ điều trị.
- Tiêu chí nghiên cứu và các biến cố ngoại ý
Tiêu chí nghiên cứu
Tiêu chí chính đánh giá hiệu quả của thuốc dapagliflozin giúp làm giảm tiến triển bệnh thận được xác định là thời điểm đầu tiên xuất hiện bất kì biến cố thận nào trong các biến cố như: giảm eGFR ≥ 50% (xác định bằng xét nghiệm creatinin máu 2 lần, cách nhau ít nhất 28 ngày), xuất hiện bệnh thận giai đoạn cuối hoặc tử vong do thận hoặc tử vong do tim mạch. Tiêu chí phụ và tiêu chí khám phá được trình bày trong bảng 2. Các tiêu chí giảm eGFR ≥ 50%, bệnh thận giai đoạn cuối dựa vào xét nghiệm máu tại phòng thí nghiệm trung tâm, còn các tiêu chí khác được đánh giá nhờ hội đồng chuyên môn gồm các chuyên gia về thận, tim mạch và thần kinh.
Bệnh thận giai đoạn cuối được định nghĩa là cần duy trì lọc máu hoặc lọc màng bụng ít nhất 28 ngày hoặc ghép thận hoặc mức lọc cầu thận <15 ml/phút/1.73 m2 ít nhất 28 ngày. Tử vong do thận được định nghĩa là chết do bệnh thận giai đoạn cuối mà không được lọc máu. Lựa chọn thời điểm 28 ngày trong định nghĩa bệnh thận giai đoạn cuối nhằm loại trừ tổn thương thận cấp tính. Trường hợp bệnh nhân lọc máu tử vong trước ngày 28, lọc máu không hiệu quả hoặc bệnh nhân lựa chọn ngừng lọc máu, hội đồng chuyên môn sẽ quyết định xem có cần lọc máu kéo dài không, nếu có sẽ được đưa và tiêu chuẩn chẩn đoán bệnh thận giai đoạn cuối.
Hội đồng chuyên môn cũng chịu trách nhiệm xác định các trường hợp nhồi máu cơ tim, đau thắt ngực không ổn định, đột quỵ và cơn thiếu máu não thoáng qua.
Tính an toàn
Dữ liệu về các biến cố bất lợi được thu thập bởi các điều tra viên có kinh nghiệm với dapagliflozin. Chỉ các biến cố bất lợi nghiêm trọng, biến cố bất lợi quan tâm và biến cố dẫn đến phải dừng thuốc sớm hoặc dừng thuốc một thời gian hoặc giảm liều được báo cáo. Các biến cố bất lợi quan tâm bao gồm giảm thể tích tuần hoàn, biến cố thận, hạ đường huyết nặng, gãy xương, nhiễm toan đái tháo đường, biến cố bất lợi dẫn đến cắt cụt chi hoặc tăng nguy cơ cắt cụt chi dưới.
Bảng 2. Tiêu chí chính, tiêu chí phụ, tiêu chí khám phá và tính an toàn của thử nghiệm DAPA-CKD
| Tiêu chí chính |
| 1. Thời điểm giảm eGFR ≥ 50% so với thời điểm bắt đầu nghiên cứu (xác nhận bởi creatinin máu trong ≥ 28 ngày)
2. Thời điểm mắc bệnh thận giai đoạn cuối được định nghĩa bằng mức lọc cầu thận < 15 ml/phút/1.73m2, cần phải lọc máu chu kì ít nhất 28 ngày hoặc ghép thận 3. Thời điểm tử vong do thận hoặc tim mạch. |
| Tiêu chí phụ |
| 1. Thời điểm xuất hiện tiêu chí gộp trên thận
a. Giảm eGFR ≥ 50% so với thời điểm bắt đầu nghiên cứu (dựa vào creatinin máu trong ≥ 28 ngày) b. Bệnh thận giai đoạn cuối được định nghĩa bằng mức lọc cầu thận < 15 ml/phút/1.73m2, cần phải lọc máu chu kì ít nhất 28 ngày hoặc ghép thận c. Tử vong do thận 2. Thời điểm đầu tiên xảy ra hoặc tử vong do tim mạch hoặc nhập viện vì suy tim 3. Thời điểm tử vong do mọi nguyên nhân |
| Tiêu chí khám phá bao gồm (nhưng không giới hạn) |
| 1. Thời điểm mắc một trong các tiêu chí chính trên thận
2. Thời điểm mắc tiêu chí gộp về lọc máu chu kì, ghép thận hoặc tử vong do thận 3. Thời điểm xuất hiện giảm eGFR duy trì ≥ 40% so với thời điểm nghiên cứu 4. Thời điểm đầu tiên giảm eGFR duy trì ≥ 30% so với thời điểm nghiên cứu 5. Thay đổi mức lọc cầu thận theo thời gian a. Từ thời điểm bắt đầu nghiên cứu cho đến khi kết thúc điều trị b. Từ thời điểm bắt đầu điều trị cho đến khi kết thúc điều trị 6. Tỉ lệ bệnh nhân có mức lọc cầu thận > 40 ml/ phút/ 1.73 m2 tại thời điểm nghiên cứu tiến triển thành bệnh thận mạn giai đoạn 4 7. Thay đổi tỉ số A/C niệu từ thời điểm nghiên cứu 8. Thời điểm đầu tiên xuất hiện nồng độ kali máu: a. >6 mmol/l b. >5.5 mmol/l c. <3.5 mmol/l d. <3 mmol/l 9. Thời điểm đầu tiên tăng gấp đôi creatinin 10. Thời điểm bệnh nhân chẩn đoán đái tháo đường typ 2 mới trên những bệnh nhân không mắc đái tháo đường từ thời điểm nghiên cứu 11. Thay đổi HbA1C từ thời điểm nghiên cứu 12. Thời điểm mắc tiêu chí tim mạch gộp gồm nhồi máu cơ tim, đột quỵ hoặc tử vong do tim mạch 13. Thời điểm đầu tiên nhập viện do suy tim 14. Thời điểm đầu tiên tử vong do nhồi máu cơ tim hoặc nhồi máu cơ tim không tử vong 15. Thời điểm đầu tiên chết do đột quỵ hoặc đột quỵ không tử vong vì bất cứ nguyên nhân nào 16. Thay đổi điểm số trong 36 mục về chất lượng cuộc sống của bệnh thận và EQ-5D-5L |
| Tiêu chí an toàn |
| 1. Biến cố ngoại ý nghiêm trọng
2. Dừng nghiên cứu do các biến cố ngoại ý 3. Thay đổi các chỉ số sinh hóa và huyết học trên lâm sàng 4. Các tác dụng phụ thường gặp (giảm thể tích, biến cố trên thận, hạ đường huyết nghiêm trọng, gãy xương, nhiễm toan ceton hoặc nguy cơ cắt cụt chi dưới) |
Điều trị nền: Bệnh nhân tham gia nghiên cứu sẽ được duy trì liều điều trị chuẩn tối ưu thuốc ức chế men chuyển hoặc ức chế thụ thể trong suốt thời gian tham gia nghiên cứu. Quản lý HA, Lipid máu và đường huyết cũng như các điều trị thiết yếu khác cũng được để lại tùy thuộc vào ý muốn của nghiên cứu viên, phù hợp với hướng dẫn và thực hành tại địa phương
Cỡ mẫu: DAPA-CKD là một nghiên cứu đếm số biến cố. Cỡ mẫu được tính toán dựa trên tỷ lệ ước tính xuất hiện của tiêu chí chính và tiềm năng hiệu quả dự tính của dapagliflozin. Nếu tuyển ít nhất 4000 bệnh nhân, nghiên cứu sẽ có mức β (power) 90% để phát hiện được nguy cơ giảm tương đối 22% tiêu chí chính dựa trên các biến cố chính sẽ được phát hiện trên 681 bệnh nhân và giá trị P hai chiều là 0,05.
Phân tích hiệu quả: Phân tích đánh giá tiêu chí chính sẽ dựa trên dân số dự định điều trị (intention to treat), tức là toàn bộ những bệnh nhân đã được phân ngẫu nhiên hợp lệ.
Dữ liệu ghi nhận bởi bệnh nhân: Các chỉ số đánh giá chất lượng cuộc sống liên quan đến sức khỏe sẽ được ghi nhận thông qua bộ chỉ số EuroQol 5 Dimensions 5 Levels (EQ-5D-5L) và bộ câu hỏi đánh giá chất lượng cuộc sống liên quan đến bệnh thận được đánh giá tại thời điểm ban đầu và mỗi 4 tháng trong suốt thời gian nghiên cứu.
- THẢO LUẬN
Thuốc ức chế SGLT2 là nhóm thuốc có nhiều bằng chứng mạnh mẽ chứng minh giảm tỉ lệ mắc các biến cố thận cũng như các biến cố tim mạch ở bệnh nhân ĐTĐ typ 2. Khả năng làm giảm tiến triển suy giảm chức năng thận theo thời gian của thuốc này không hoàn toàn giải thích được bởi cơ chế cải thiện kiểm soát đường máu mà có thể liên quan đến các cơ chế khác không phụ thuộc đường máu; bao gồm lợi niệu thẩm thấu, khôi phục phản hồi ống cầu thận dẫn đến co tiểu động mạch đến, làm giảm áp lực lọc ở các nephron, cải thiện tình trạng thiếu oxy của thận và giảm quá trình viêm và xơ hóa thận [1,7]. Vì vậy, nếu một hoặc nhiều cơ chế này hoạt động thì thuốc ức chế SGLT2 cũng có thể đem lại lợi ích ở bệnh nhân BTM không có ĐTĐ. Do đó, thử nghiệm DAPA-CKD ra đời nhằm đánh giá liệu dapagliflozin có làm giảm một cách an toàn nguy cơ của tiêu chí gộp trên thận và tử vong do tim mạch trên phổ rộng bệnh nhân BTM có ĐTĐ hoặc không, đã được điều trị các liệu pháp bảo vệ thận tối ưu.
Thiết kế nghiên cứu trong thử nghiệm DAPA-CKD quan tâm đặc biệt đến hiệu quả và tính an toàn của dapagliflozin trên bệnh nhân BTM không mắc ĐTĐ. Một số nghiên cứu trước đây đã báo cáo về một số trường hợp bệnh nhân sử dụng thuốc ức chế SGLT2 mà không có ĐTĐ. Những nghiên cứu này cho thấy thuốc ức chế SGLT2 có tác dụng tăng thải đường qua nước tiểu dẫn đến giảm huyết áp, cân nặng và nồng độ acid uric máu [8, 9]. Với hầu hết các thuốc làm giảm đường máu, hạ đường huyết đặc biệt được quan tâm. Tuy nhiên, với nhóm thuốc này, tác dụng tăng thải đường qua nước tiểu tỉ lệ thuận với nồng độ glucose máu và khả năng lọc glucose qua thận. Vì vậy, thuốc ức chế SGLT2 thường không gây hạ đường huyết. Đồng thời, cơ chế tăng sản xuất glucose ở gan bù trừ cho việc mất glucose qua đường tiểu cũng giúp duy trì glucose máu lúc đói ở mức bình thường trên bệnh nhân không mắc ĐTĐ [10]. Ngoài ra, ở những bệnh nhân BTM, do khả năng lọc glucose ở cầu thận giảm nên lượng glucose thải ra nước tiểu cũng giảm. Vì lẽ đó nên không có gì đáng ngạc nhiên khi một phân tích tổng hợp các thử nghiệm ngẫu nhiên có đối chứng trên bệnh nhân ĐTĐ typ 2 có eGFR từ 15 – 45 ml/phút/1.73 m2, tỉ lệ hạ đường huyết của nhóm dapagliflozin tương tự giả dược [11].
Chúng tôi đã thu thập các dữ liệu về tính an toàn của các thuốc hạ đường máu nói chung và các thuốc ức chế SGLT2 nói riêng bao gồm các thông tin về gãy xương, nhiễm toan ceton, đoạn chi và tổn thương thận cấp. Trong thử nghiệm DAPA-CKD, tổn thương thận cấp được đặc biệt quan tâm do sự thay đổi huyết động của thuốc ức chế SGLT2 có thể dẫn đến giảm eGFR trong giai đoạn đầu, tương tự như các thuốc ức chế men chuyển hoặc thuốc ức chế thụ thể mặc dù các thuốc này có cơ chế huyết động khác (thuốc ức chế SGLT2 gây co tiểu động mạch đến trong khi các thuốc ức chế hệ renin angiotensin gây giãn tiểu động mạch đi) [12]. Tuy có những điểm tương đồng, nhưng tổn thương thận cấp do thuốc ức chế SGLT2 được báo cáo ít hơn trong các nghiên cứu DECLARE-TIMI 58, EMPAREG-OUTCOME, CANVAS, CREDENCE, cho dù biến cố ngoại ý này không được định nghĩa cụ thể [2-5]. Để xác định chính xác tác động của dapagliflozin trên tổn thương thận cấp ở bệnh nhân BTM, hội đồng chuyên môn đã đưa ra định nghĩa về tổn thương thận cấp nghiêm trọng là sự tăng gấp đôi creatinin huyết thanh ở lần xét nghiệm cuối cùng so với thời điểm nghiên cứu. Trong nghiên cứu CANVAS, tỉ lệ cắt cụt chi tăng lên khi dùng canagliflozin nhưng biến cố này lại không thấy báo cáo trong thử nghiệm CREDENCE [3, 5]. Biến cố ngoại ý này cũng không quan sát thấy trong các nghiên cứu với dapagliflozin gồm DECLARE-TIMI 58, DAPA-HF, với empagliflozin trong EMPAREG-OUTCOME [2, 4, 13]. Tuy nhiên, tất cả các trường hợp cắt cụt chi và các biến cố làm tăng nguy cơ cắt cụt chi phải được thu thập trong tất cả các thử nghiệm của thuốc ức chế SGLT2 trong đó có thử nghiệm DAPA-CKD.
Từ góc độ hiệu quả điều trị, thử nghiệm DAPA-CKD sẽ xác định hiệu quả của dapagliflozin trên tiêu chí thận gộp, đã được sử dụng trong các thử nghiệm về BTM trước đó. Tiêu chí có ý nghĩa lâm sàng nhất là bệnh thận giai đoạn cuối, được định nghĩa là bắt đầu lọc máu > 28 ngày hoặc ghép thận hoặc eGFR duy trì < 15 ml/phút/ 1.73 m2. Vì, khi eGFR giảm ở mức này sẽ làm tăng nguy cơ tử vong và giảm chất lượng cuộc sống của bệnh nhân BTM. Một tiêu chí trên thận khác là giảm 50% eGFR tương đương với tăng 80% creatinin máu , tiêu chí này trái ngược với tiêu chí tăng gấp đôi creatinin hoặc giảm 40% eGFR trong một số thử nghiệm khác. Chúng tôi không sử dụng tiêu chí giảm 40% eGFR bởi vì thuốc dapagliflozin có thể gây giảm eGFR cấp tính do thay đổi huyết động tại thận. Vì vậy, giảm 40% eGFR chưa chắc phản ánh đúng tiến triển BTM, làm giảm khả năng đánh giá sự khác biệt của thuốc dapagliflozin so với giả dược, làm tăng nguy cơ dẫn đến sai lầm loại 1. Tăng gấp đôi creatinin máu không được lựa chọn trong tiêu chí gộp trên thận vì giảm 50% eGFR cũng đã phản ánh được sự giảm đáng kể chức năng thận, nhờ vậy, có thể làm giảm cỡ mẫu và sự phức tạp khi thu thập số liệu của thử nghiệm. Tiêu chí chính cũng bao gồm tử vong do thận hoặc do nguyên nhân tim mạch. Tử vong do mọi nguyên nhân không được đưa vào tiêu chí chính do dapagliflozin không ảnh hưởng đến biến cố tử vong không liên quan đến nguyên nhân thận hoặc tim mạch.
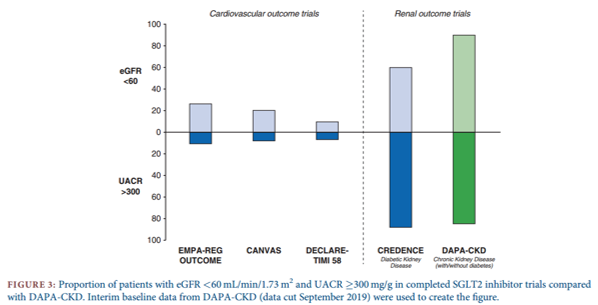
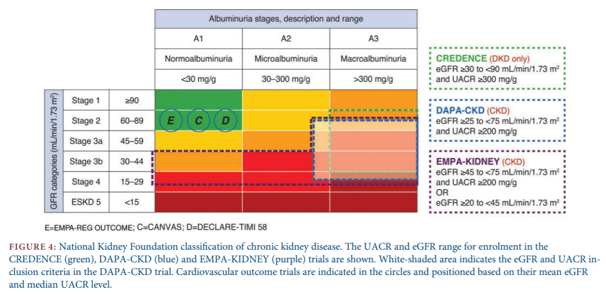
Một câu hỏi được đặt ra là dân số trong thử nghiệm DAPA-CKD có khác biệt gì so với dân số trong các thử nghiệm thuốc ức chế SGLT2 trước đó? Một số lượng nhỏ dân số tham gia thử nghiệm về an toàn tim mạch của thuốc ức chế SGLT2 có BTM (chẩn đoán dựa vào mức lọc cầu thận hoặc tỉ số albumin/creatinin niệu). Cho đến nay, CREDENCE là thử nghiệm duy nhất tuyển chọn các bệnh nhân mắc cả ĐTĐ typ 2 và BTM. Trong thử nghiệm DAPA-CKD, 90% dân số có mức lọc cầu thận < 60 ml/phút/1.73 m2 và ít nhất 80% dân số có UACR > 300 mg/g (Hình 3). Giảm eGFR và tăng UACR là những dấu ấn nguy cơ mạnh mẽ trên thận và tim mạch, giả định tỉ lệ các biến cố tim mạch trong nghiên cứu DAPA-CKD ít nhất tương đương với các nghiên cứu về an toàn tim mạch của các thuốc ức chế SGLT2 trước đó. Khi so sánh thử nghiệm DAPA-CKD với 2 thử nghiệm an toàn trên thận của 2 thuốc ức chế SGLT2 khác (CREDENCE và EMPA-KIDNEY), dân số trong thử nghiệm DAPA-CKD rộng hơn so với CREDENCE (chỉ bao gồm bệnh nhân ĐTĐ typ 2) (Hình 4). Còn trong thử nghiệm EMPA-KIDNEY, nhằm đánh giá hiệu quả của empagliflozin so với giả dược, tiêu chí tuyển chọn được mở rộng hơn bao gồm cả các bệnh nhân đái tháo đường typ 1 và bệnh nhân có UACR < 200 mg/g với eGFR từ 20-45 ml/phút/1.73 m2 (Hình 4). Nhìn chung, 3 thử nghiệm này sẽ giúp xác định lợi ích tối ưu của thuốc ức chế SGLT2 trong quản lý bệnh thận mạn.
Trong quá trình tiến hành thử nghiệm DAPA-CKD, 2 thử nghiệm về hiệu quả an toàn tim mạch lớn của thuốc dapagliflozin là DECLARE-TIMI 58 và DAPA-HF đã được báo cáo. Thử nghiệm DECLARE-TIMI 58 cho thấy dapagliflozin giảm đáng kể tỉ lệ biến cố gộp suy tim và tử vong do tim mạch 17%, giảm 47% nguy cơ tiêu chí gộp trên thận gồm giảm 40% eGFR, bệnh thận giai đoạn cuối và tử vong do thận trên bệnh nhân ĐTĐ typ 2 có chức năng thận bảo tồn, đã hoặc đang có nguy cơ mắc bệnh tim mạch [4]. Thử nghiệm DAPA-HF cũng chứng minh dapagliflozin giảm đáng kể nguy cơ tiêu chí gộp về suy tim và tử vong do tim mạch trên bệnh nhân suy tim phân số tống máu giảm có hoặc không mắc ĐTĐ typ 2 [13]. Những lợi ích này nhất quán ở cả đối tượng có hoặc không mắc đái tháo đường cũng như có hoặc không mắc bệnh thận mạn. Hơn nữa, các thử nghiệm này cũng báo cáo về tỉ lệ các biến cố ngoại ý liên quan đến thận của dapagliflozin (1.6%) thấp hơn đáng kể so với giả dược (2.7%, P=0.09). Mặc dù, các kết quả này được kì vọng ở bệnh nhân BTM, nhưng chúng phải được xác nhận trong nghiên cứu DAPA-CKD.
Tóm lại, DAPA-CKD là thử nghiệm lâm sàng đầu tiên nhằm khám phá những lợi ích và nguy cơ tiềm tàng của thuốc ức chế SGLT2 ở bệnh nhân bệnh thận mạn các giai đoạn trên cả nhóm đái tháo đường và không đái tháo đường, được điều trị bằng các liệu pháp bảo vệ thận dựa trên bằng chứng.
“Cảm ơn AstraZeneca hỗ trợ vì mục đích cập nhật và giáo dục y khoa”
TÀI LIỆU THAM KHẢO
- Heerspink HJ, Perkins BA, Fitchett D et al. Sodium glucose cotransporter 2 inhibitors in the treatment of diabetes: cardiovascular and kidney effects, potential mechanisms and clinical applications. Circulation 2016; 134: 752–772
- Zinman B, Wanner C, Lachin JM et al. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med 2015; 373: 2117–2128
- Neal B, Perkovic V, Mahaffey KW et al. Canagliflozin and cardiovascular and renal events in type 2 diabetes. N Engl J Med 2017; 377: 644–657
- Wiviott SD, Raz I, Bonaca MP et al. Dapagliflozin and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2019; 380: 347–357
- Perkovic V, Jardine MJ, Neal B et al. Canagliflozin and renal outcomes in type 2 diabetes and nephropathy. N Engl J Med 2019; 380: 2295–2306
- Dekkers CCJ, Gansevoort RT, Heerspink HJL. New diabetes therapies and diabetic kidney disease progression: the role of SGLT-2 inhibitors. Curr Diab Rep 2018; 18: 27
- Rajasekeran H, Cherney DZ, Lovshin JA. Do effects of sodium-glucose cotransporter-2 inhibitors in patients with diabetes give insight into potential use in non-diabetic kidney disease? Curr Opin Nephrol Hypertens 2017; 26: 358–367
- Komoroski B, Vachharajani N, Boulton D et al. Dapagliflozin, a novel SGLT2 inhibitor, induces dose-dependent glucosuria in healthy subjects. Clin Pharmacol Ther 2009; 85: 520–526
- Lundkvist P, Sjostrom CD, Amini S et al. Dapagliflozin once-daily and exenatide once-weekly dual therapy: a 24-week randomized, placebocontrolled, phase II study examining effects on body weight and prediabetes in obese adults without diabetes. Diabetes Obes Metab 2017; 19: 49–60
- Al Jobori H, Daniele G, Adams J et al. Determinants of the increase in ketone concentration during SGLT2 inhibition in NGT, IFG and T2DM patients. Diabetes Obes Metab 2017; 19: 809–813
- Dekkers CCJ, Wheeler DC, Sjostrom CD et al. Effects of the sodiumglucose co-transporter 2 inhibitor dapagliflozin in patients with type 2 diabetes and stages 3b–4 chronic kidney disease. Nephrol Dial Transplant 2018; 33: 2005–2011
- Pleros C, Stamataki E, Papadaki A et al. Dapagliflozin as a cause of acute tubular necrosis with heavy consequences: a case report. CEN Case Rep 2018; 7: 17–20
- McMurray J. Dapagliflozin in patients with heart failure and reduced ejection fraction (DAPA-HF). Presented at the European Society for Cardiology Congress 2019, 1 September 2019, Paris, France
- Perkovic V, de Zeeuw D, Mahaffey KW et al. Canagliflozin and renal outcomes in type 2 diabetes: results from the CANVAS program randomised clinical trials. Lancet Diabetes Endocrinol 2018; 6: 691–704







