I. MỞ ĐẦU
Các thử nghiệm lâm sàng (TNLS) ngẫu nhiên đã chứng minh rằng các thuốc chẹn beta giúp cải thiện triệu chứng, giảm nhập viện và tăng sống còn ở bệnh nhân (BN) suy tim (ST) với EF giảm. Do vậy các thuốc chẹn bêta là điều trị nền tảng cho nhóm BN này (1-5).
Bs Nguyễn Thanh Hiền
Bs Ngô Nguyễn Kim Hường
Bs Phạm Tú Quỳnh
Gần đây Ivabradine, thuốc ức chế kênh If chuyên biệt cũng được chứng minh làm giảm tỷ lệ nhập viên và tử vong do ST trênBN ST EF giảm có nhịp xoang >70 lần/phút dù đang điều trị chẹn β liều tối ưu dung nạp được (6,7).
Vậy vấn đề sử dụng các thuốc này trong điều trị ST EF giảm như thế nào hiện nay, đặc biệt khi dùng phối hợp? Bài viết này nhằm thảo luận các vấn đề dùng chẹn β và Ivabradine trong điều trị ST EF giảm hiện nay sau khi cập nhật các hướng dẫn mới nhất về ST của Hội tim mạch Mỹ và châu Âu.
II. LÝ DO SỬ DỤNG
1. Tần số tim như là mục đích điều trị
Tần số tim tăng kết hợp với tiên lượng tim mạch xấu. Tần số tim tăng một phần phản ánh tăng hoạt tính hệ thần kinh giao cảm và giảm hoạt tính phó giao cảm. Đó là cơ chế tự bù trừ hormone trong ST. Tăng nồng độ norepinephine là dấu ấn chứng tỏ khả năng sống sót kém ở những BN này. Hiệu quả của thuốc ivabradine, thuốc tác động đơn thuần giảm tần số tim, làm giảm biến cố tim mạch ở BN chứng tỏ rằng tần số tăng là yếu tố tiên lượng xấu ở BN STEF giảm. Tăng tần số tim làm tăng nhu cầu oxy cơ tim và tăng lực xé, cũng như làm giảm tưới máu cơ tim. Chính vì vậy trong điều trị ST làm giảm tần số tim tới mức thích hợp là mục đích của điều trị (hình 1) (6-8).
2. Hiệu quả của các thuốc làm giảm tần số tim:
Các thuốc làm giảm tần số tim có hiệu quả khác nhau lên ST. Trong khi một số thuốc làm giảm tần số tim là có lợi ở BN ST EF giảm, một số thuốc khác lại cho hiệu quả khác nhau lên tiên lượng BN ST EF giảm (bảng 1).
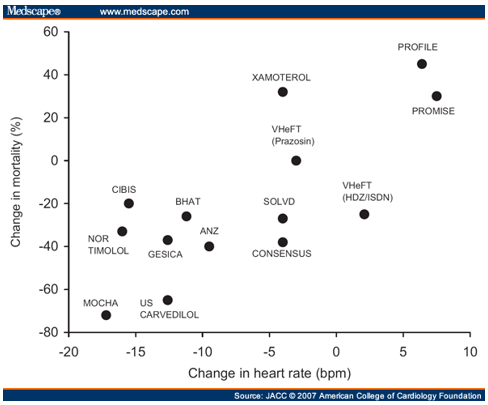
Hình 1. Liên quan giữa TS tim và TV ở BN ST
Bảng 1. Cơ chế tác động và chỉ định các thuốc làm chậm nhịp tim trong ST mạn (7)
|
Thuốc |
Cơ chế tác dụng |
Chỉ định |
|
Chẹn beta
Ivabradine
Digoxin
Verapamil
Amiodarone |
– Block hoạt tính giao cảm: Chậm nhịp xoang và kéo daì thời gian dẫn truyền AV. – Ức chế chọn lọc kênh If của nút xoang: làm chậm tần số xoang. Không tác dụng lên nút AV – Tăng trương lực phó giao cảm: ức chế hoạt tính Tk giao cảm, làm chậm nhịp xoang và kéo dài dẫn truyền AV – Block kênh calcium điện thế cao: làm chậm nhịp xoang và kéo dài dẫn truyền AV – Block kênh kali: hiệu quả chống giao cảm, làm chậm nhịp xoang và kéo dài thời gian dẫn truyền AV.
|
– ST EF giảm với nhịp xoang hay rung nhĩ – ST với EF bảo tồn – ST EF giảm với nhịp xoang
– ST EF giảm với nhịp xoang hay rung nhĩ – ST với EF bảo tồn – ST với EF bảo tồn với nhịp xoang hay RN
– ST EF giảm với rung nhĩ
|
Chẹn β và ivabradine đều làm giảm tần số tim và cải thiện tiên lượng BN ST và EF giảm nhưng 2 thuốc này có cơ chế tác dụng khác nhau. Cả hai thuốc đều có bằng chứng lợi ích lâm sàng liên quan với giảm tần số tim, dù chẹn β có thể có thêm nhiều hiệu quả khác (phần dưới) (3-6,9)
Digoxin, thuốc có tác động chống giao cảm và hoạt hoá phó giao cảm dẫn tới có thể giảm tần số tim ở BN ST và EF giảm nhịp xoang, tuy nhiên chưa có bằng chứng chứng tỏ thay đổi tần số tim mang lại lợi ích lâm sàng. Ở BN ST và EF giảm, digoxin giảm nguy cơ nhập viện doST. Vì digoxin có nhiều tác động lên chức năng tim mạch và hoạt tính thần kinh, nên còn chưa chắc hiệu quả lâm sàng của thuốc có liên quan đến giảm tần số tim hay không (1-5,10).
Thuốc ức chế kênh calci nondihydropyridine (diltiazem và verapamil) có hiệu quả ức chế co bóp cơ tim và giảm tầnsố tim ở BN nhịp xoang hay rung nhĩ nhưng không có lợi ích ở BN ST và EF giảm. Vì vậy các thuốc này không được sử dụng ở BN ST và EF giảm (1-4,10).
III. Điều trị với chẹn β
1. Cơ chế tác dụng của chẹn β
Thuốc làm giảm nhịp xoang do ngăn chặn hoạt tính catecholamin ở thụ thể β1 tại nút xoang. Ở BN rung nhĩ, chẹn β làm giảm đáp ứng thất thông qua làm chậm dẫn truyền nút nhĩ thất. Ngoài ra, block thụ thể β1 ở cơ tim dẫn tới làm giảm co bóp. Cơ chế lợi ích của chẹn β ở BN ST và EF giảm có thể liên quan với giảm tần số tim cũng như giảm các hiệu quả khác như giảm nhu cầu oxi cơ tim, giảm sản xuất cytokine viêm, tăng quá trình tái cấu trúc, tăng mật độ thụ thể β1 cơ tim (tránh được hiện tượng giảm thụ thể β1 do bị kích thích giao cảm quá mức), chống loạn nhịp, giảm chết theo chương trình (hình 2) (5,6).
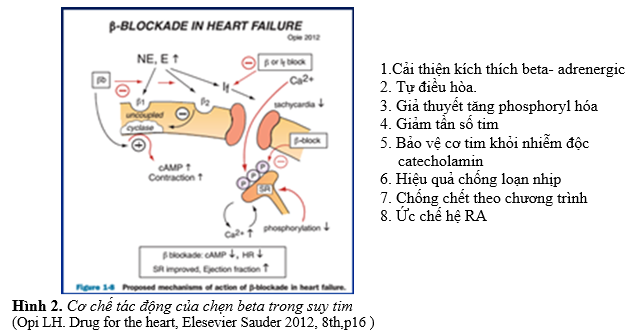
2. Chỉ định và chống chỉ định (1-5,10)
2.1. Chỉ định:Dùng cho mọi BN ST và EF giảm nếu không có chống chỉ định.
2.2. Chống chỉ định:
– Tuyệt đối: hen phế quản, COPD mức độ nặng, block nhĩ thất độ II trở lên
– Tương đối: tần số tim dưới 60l/ph, huyết áp thấp có triệu chứng, dấu hiệu giảm tưới máu ngoại vi, bằng chứng còn ứ dịch, giảm tưới máu ngoại biên, PR>0.24s, bệnh mạch máu ngoại biên và thiếu máu chi khi nghỉ.
3. Hiệu quả điều trị chẹn β (hình 3) [3,9,11]
3.1. Hiệu quả chung:Thuốc đã được chứng minh giảm tỷ lệ tử vong, giảm tỷ lệ nhập viện và cải thiện triệu chứng. Qua phân tích gộp 22 TNLS hơn 10000 BN ST và EF giảm <35-45%, NYHA II-IV và điều trị cùng với ƯCMC cho thấy:
Giảm tỷ lệ tử vong 1 năm (tỷ số chênh 0,65; khoảng tin cậy 95% (CI) 0,53-0,8), và 2 năm (tỷ số chênh 0,72; khoảng tin cậy 95% (CI); 0,61-0,84).
Giảm tỷ lệ nhập viện do ST (tỷ số chênh 0.64, khoảng tin cậy 95% (CI) 0,53-0,79) với lợi ích tuyệt đối nhỏ hơn 4 lần nhập viện trong năm đầu trên 100 BN điều trị.
3.2. Các nhóm BN đặc biệt (6):
– Phụ nữ: có hiệu quả tương đương như nam.
– Bệnh cơ tim thiếu máu cục bộ và bệnh cơ tim không thiếu máu cục bộ: cải thiện khả năng gắng sức, ổn định chức năng thất, và tử vong là tương tự ở hai nhóm bệnh.
– NYHA IV ổn định: lợi ích tử vong vẫn có được ở BN ST NYHA III nặng và IV.
– BN ĐTĐ: lợi ích sống còn là tương đương giữa BN có ĐTĐ và không ĐTĐ.
– BN lọc thận: dựa trên số liệu có sẵn, gồm các TNLS nhỏ của carvedilol, cho thấy điều trị chẹn β có lợi ở BN lọc thận.
– BN lớn tuổi: tất cả các (TNLS chủ yếu gồm nhiều BN lớn tuổi cho thấy hiệu quả tương đương với người trẻ. Lợi ích trên người lớn tuổi được đánh giá trực tiếp trong thử nghiệm SENIOR. Thử nghiệm này đánh giá hiệu quả của nebivolol, ức chế β1 chọn lọc (và đồng vận β3) với hoạt tính giãn mạch ở BN ≥ 70 tuổi có tiền sử nhập viện vì ST hay biết ST EF giảm (≤ 35%). Kết quả cho thấy nebivolol làm giảm tiêu chí tiên phát gồm giảm tử vong do mọi nguyên nhân hay nhập viện vì nguyên nhân tim mạch và có xu hướng giảm tử vong do mọi nguyên nhân.
|
Thử nghiệm |
N |
Hoạt chất |
Tiêu chuẩn nhận |
Thời gian theo dõi |
Tiêu chí đánh giá |
Kết quả |
|
CIBIS I |
641 |
Biscoprolol và gd |
LVEF <40% |
23 tháng |
Tử vong |
Gd 21% (20% â, P= 0,22) |
|
U.S. Carvedilol heart failure trials |
1094 |
Carvedilol và giả dược |
LVEF ≤35% |
6 tháng |
Tử vong |
Gd 7.8% |
|
CIBIS II |
2647 |
Biscoprolol và giả dược |
LVEF ≤35% |
16 tháng |
Tử vong |
Gd 17% (34%â) |
|
MERIT- HF |
3991 |
Metoprolol CR/XL và giả dược |
LVEF ≤40% |
12 tháng |
Tử vong |
Gd 11% (34%â) |
|
BEST |
2708 |
Bucindolol và giả dược |
LVEF ≤35% |
2 tháng |
Tử vong |
Gd 33% (10%âP= 0,10) |
|
COPERNICUS |
2289 |
Carvedilol và giả dược |
LVEF ≤25% |
10 tháng |
Tử vong |
Gd 17% |
|
CAPRICORN |
1959 |
Carvedilol và giả dược |
LVEF ≤40% 3-21 ngày sau NMCT |
1,3 năm |
Tử vong hoặc CV nhập viện |
Gd 37% |
|
COMET |
3029 |
Carvedilol và metoprolol tartrate |
LVEF ≤35% |
58 tháng |
Tử vong |
Metoprolol 40% |
|
SENIORS |
2128 |
Nebivolol và giả dược |
Tuổi ≥70 |
21 tháng |
Tử vong hoặc CV nhập viện |
Gd 35% |
Hình 3.Vai trò beta-blockers trong điều trị ST qua các TNLS (CV: do tim mạch)(Anmant.EM & Sabatine.MS: Cardiovascular Therapeutics.A Companion to Braunwald’s Heart Disease. 4th 2013:251).
– BN COPD (12-18):
+ Hiện nay, sử dụng chẹn β vẫn ở dưới mức yêu cầu ở BN ST mạn (CHF) và COPD kết hợp bất chấp nhiều số liệu an toàn ở BN CHF vừa tới nặng. Chỉ 36,9% trong số 11.016 BN CHF trong nghiên cứu CHF của Hội tim mạch châu Âu là dùng BB. Nhiều BN không dùng đạt được tới liều đích và tỉ lệ ngưng thuốc từ 13,9% tới 32%. Có nhiều lí do để BN phải ngưng thuốc (hình 4). Nhiều báo cáo cho thấy tình trạng co thắt phế quản cấp sau khi bắt đầu điều trị chẹn β dẫn tới loại bỏ BN COPD và CHF kết hợp ra khỏi các nghiên cứu dùng chẹn β.
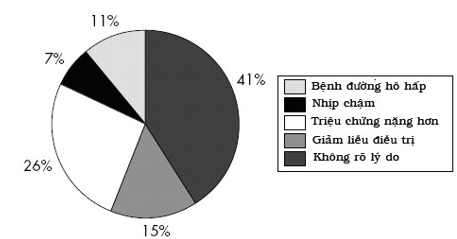
Hình 4. Lý do ngưng hay giảm liều chẹn β(17).
+ Lựa chọn BB trên BN COPD và ST.
Các thuốc chẹn β cũng đuợc nghiên cứu sử dụng trên các BN có kết hợp COPD với các mức độ ảnh huởng lên FEV1 và tăng đáp ứng đường thở (airway hyperresponsiveness – AHR) khác nhau. Trong thực hành điều trị CHF, chỉ có bốn thuốc chẹn β đuợc chấp nhận sử dụng trong ST là bisoprolol, carvedilol, metoprolol, nebivolol và việc sử dụng các thuốc này không làm xấu đi tình trạng lâm sàng một cách có ý nghĩa ở BN COPD nhẹ và trung bình (14,18).
+ Chỉ định lâm sàng.
Hướng dẫn gần đây của Hội ST Mỹ đề nghị sử dụng chẹn β ở tất cả BN CHF kèm COPD. Tuy nhiên lưu ý trong thực hành là chỉ nên dùng ở BN COPD từ giai đoạn C trở lên (không nên dùng cho BN COPD giai đoạn D) và bắt đầu liều thấp hơn và khoảng cách tăng liều dài hơn. Đôi khi phải giảm liều tạm thời khi triệu chứng xấu đi và ngưng hẳn nếu BN không dung nạp đuợc.
+ Sử dụng phối hợp chẹn β và thuốc hít đồng vận beta (IBA).
Các thuốc IBA là thuốc thường dùng trong điều trị tình trạng co thắt phế quản cả cấp tính và dài hạn. Tuy nhiên sử dụng thuốc này làm tăng nguy cơ tim mạch và các thuốc chẹn β có thể có lợi. Một phân tích gộp các thử nghiệm so sánh ngẫu nhiên sử dụng IBA so với chứng cho thấy thuốc làm tăng nhịp tim lên 9,12 l/ph (khoảng tin cậy – CI 95% là 5,32 – 12,9) và nguy cơ tương đối nhịp xoang nhanh là 3,06 lần (95% CI là 1,7 – 5,5), giảm kali máu 0,36mmol/l (95% CI 0,18 – 0,54), tăng nguy cơ các biến cố tim mạch (RR, 2,54; 95% CI 1,59 – 4,05), tính chung các biến cố chủ yếu là 1,66 (95% CI 0,769 – 3,42). Vì vậy việc điều trị kết hợp chẹn β với IBA có thể là cần thiết. Tuy nhiên hiệu quả điều trị kết hợp chẹn β với IBA trong ngăn chặn biến chứng tim mạch còn chưa được đánh giá qua các TNLS. Trong thực hành khi BN đang phải dùng dạng phun khí dung để điều trị tình trạng co thắt phế quản, ngưng dùng chẹn β. Khi tình trạng COPD ổn định và BN chỉ dùng dạng MDI để điều trị duy trì thì lúc đó chúng ta có thể bắt đầu cho chẹn β (thường sau đợt cấp COPD 4 tuần).
4. Chiến lược sử dụng:
4.1. Thời điểm:
BN đã ĐT nội tối đa (lợi tiểu, UCMC, digoxin…) và tình trạng ổn định (3,4,10,19):
– Không có dấu hiệu ứ dịch (phù, gan to, TDMP, MB…),
– Không dùng thuốc đường tĩnh mạch: vận mạch, không truyền lasix…
4.2. Cách dùng (3,4,10,19):
+ Cần lưu ý 5 điểm sau trước khi dùng:
– ĐT lợi tiểu để không còn quá tải dịch.
– Dùng ACEIs trước (thường khoảng 1 tuần).
– Bắt đầu liều rất thấp và tăng dần (sau 2-4 tuần).
– Điều chỉnh liều ACEIs và lợi tiểu cho phù hợp.
– Theo dõi tình trạng quá tải dịch.
+ Liều: Phải bắt đầu từ những liều rất nhỏ sau đó mới từ từ tăng dần liều lượng ( bảng 2) mỗi 2 – 4 tuần nếu BN dung nạp (3,4,10,19,20).
Bảng 2. Các thuốc chẹn β có chỉ định trong điều trị ST và cách chỉnh liều
|
β-Blocker |
Liều đầu |
Tuần thứ 3 |
Tuần thứ 56 |
Liều cuối |
|
Carvedilol |
3,125 |
6,25×2 |
12,5×2 |
25×2 |
|
Metoprolol SR |
25 |
50 |
100 |
200 |
|
Bisoprolol |
1,25 |
3,75 |
5 |
10 |
|
Nebivolol |
1,25 |
2,5 |
5 |
10 |
4.3. Chọn chẹn β:
Chỉ sử dụng 4 lọai chẹn beta là Carvedilol, bisoprolol, nebivolol và metoprolol succinate phóng thích chậm vì đã được chứng minh làm giảm tỉ lệ tử vong do mọi nguyên nhân và giảm tỉ lệ nhập viện do ST ở Bn phân suất tống máu giảm. Hiện còn ít số liệu so sánh 4 loại chẹn beta này. Các bằng chứng gián tiếp cho thấy carvedilol cải thiện EF tốt hơn metoprolol. BN có HA thấp ít dung nạp với carvedilol do tác dụng dãn mạch của thuốc. ngược lại thuốc lại phù hợp cho BN HA cao. Không khuyến cáo sử dụng loại chẹn beta không có được chứng minh lợi ích trong các TNLS (6).
4.4 Một số lưu ý:
– 4.4.1.BN ngưng thuốc và cần dùng lại:
< 72h, không dấu hiệu ST dùng lại với liều như trước khi ngưng.
>72h và < 7 ngày, không dấu hiệu STdùng lại nửa liều trước khi ngưng.
> 7 ngày, không có dấu hiệu STdùng lại bắt đầu từ liều thấp nhất (21).
– 4.4.2. Chuyển thuốc:
Hiện chưa có nghiên cứu, do vậy nên thận trọng chuyển khi cần. Nếu cần chuyển, dùng liều chẹn beta tương đương hoặc thấp hơn. Thời điểm dùng sau liều cuối cùng hết tác dụng (12h sau carvedilol, 24h sau bisoprolol và metoprolol succinat) (6).
– 4.4.3. Sử dụng với thuốc khác:
Với các thuốc điều trị dài hạn cho ST như các thuốc ƯCMC, ƯCTT và kháng Aldosteron cũng như với phối hợp hydralazine và nitrate đều cải thiện sống còn ở BNST EF giảm.
Điều trị ST với ƯCMC/ƯCTT và chẹn β hiệu quả hơn khi dùng đơn độc. Chẹn β và ƯCMC/ƯCTT phối hợp với kháng thụ thể mineralocorticoid (MRA) cũng hiệu quả ở BNST có triệu chứng EF<35% với điều kiện theo dõi được Kali máu và chức năng thận. Phối hợp MRA với chẹn β và ƯCMC/ƯCTT cũng nên cho ở BN sau nhồi máu cơ tim, EF<40% và hoặc có dấu hiệu ST, ĐTĐ (3-6).
Chẹn β với aspirin: một số tài liệu cho thấy aspirin có thể tương tác với thuốc điều trị ST, tuy nhiên bằng chứng còn thiếu. Hiện nay thuốc chỉ nên sử dụng khi có bệnh lý ST kèm bệnh mạch vành và liều thấp (22).
4.5. Tác dụng phụ:
4.5.1.Trong quá trình bắt đầu điều trị:
BN phải đối mặt với 4 vấn đề là: tụt HA, ST nặng hơn, nhịp chậm, cảm giác mệt hơn /hoặc không dung nạp. Tình trạng ST có thể xấu đi trong 2-3 tuần đầu sử dụng chẹn β. Hạn chế điềunày bằng điều trị ST thật ổn trước khi bắt đầu, bắt đầu liều thật thấp và tăng liều chậm. Có thể cần giảm liều ƯCMC/ƯCTT hoặc lợi tiểu để hạn chế tình trạng giảm huyết áp. Điều chỉnh những thay đổi này khi dùng BB nêu ở hình 5 (1-5).
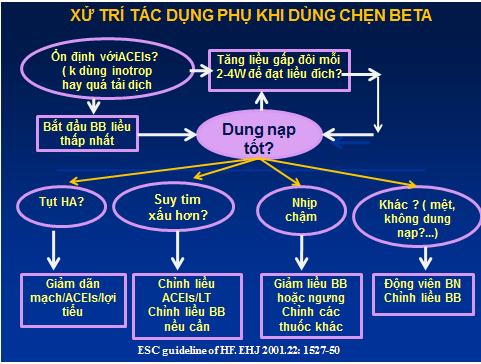
Hình 5. Xử trí tác dụng phụ khi dùng chẹn beta
(ESC guideline of HF. EHJ 2001,22,1527-50)
4.5.2. Trong quá trình điều trị duy trì (23-26):
Mục đích của phần này là thảo luận về vai trò chẹn beta trong ST mạn mất bù mạn cấp. Đã có những quan điểm cho rằng chúng ta vẫn có thể sử dụng chẹn beta khi BN nhập viện vìST mạn mất bù mạn cấp. Qua tìm hiểu tài liệu, chúng tôi nhận thấy, thuốc BB được phép sử dụng nếu có thể được chỉ cho BN với kiểu rối loạn huyết động A or B mức độ nhẹ (hình 6). Thuốc nên ngưng hoặc ở BN có bằng chứng giảm tưới máu, đặc biệt nếu sử dụng thuốc tăng sức co bóp. Khi dùng, cần cụ thể các vấn đề sau:
o Nếu BN đang dùng thuốc chẹn beta:
– Nếu đã dùng lâu (> 3 tháng) và liều ổn định, nên tiếp tục với liều dung nạp cho BN nhập viện vì ST cấp với ứ dịch nhưng không có giảm tưới máu, không có HA thấp, không dùng thuốc vận mạch.
– Nếu thuốc mới dùng hay mới tăng liều gần đây ( <4 tuần ), nên ngưng hoặc giảm liều cho đến khi tình trạng ứ dịch được giải quyết hiệu quả.
o Nếu BN chưa dùng:
– Có thể dùng khi còn nằm viện với điều kiện không có HA thấp, không dùng thuốc vận mạch. Thông thường vào ngày thứ 7chúng ta nên đánh giá lại tình trạng BN, đo ECG, làm lại siêu âm tim, chụp lại tim phổi thẳng để quyết định đã dùng được hay chưa. Những BN ST do nhiễm độc, thời gian dùng BB sẽ muộn hơn. BN phù phổi nhẹ sau NMCT ( KILLIP II ) không có ST tâm thu và biến chứng cơ học có thể dùng chẹn beta sau 48 giờ.
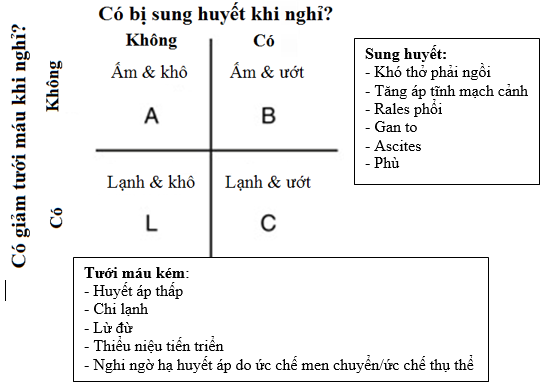
Hình 6.Các kiểu rối loạn huyết động trong ST mất bù cấp(BN rối loạn type A và B nhẹ có thể dùng tiếp chẹn betanếu đã dùng lâu (> 3 tháng) và liều ổn định) (23).
IV. Điều trị với ivabradine
IV.1. Cơ chế tác dụng
Nút xoang là chủ nhịp của tim. Tại nút xoang có nhiều kênh ion khác nhau như kênh Ca, kênh K & kênh f (If) (hình 7).
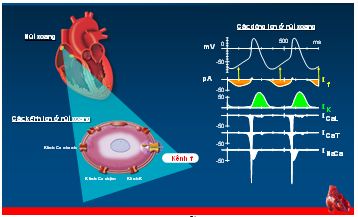
Hình 7. Các kênh ion của nút xoang, mỗi kênh cho 1 dòng ion đi qua và ảnh hưởng đến hình dạng điện thế hoạt động tại những giai đoạn khác nhau (27).
Gọi là tác động chuyên biệt vì Ivabradine chỉ ức chế dòng ion qua kênh f (If), kênh ion chịu trách nhiệm chính cho tính tự động của nút xoang và không gây bất kỳ một ảnh hưởng nào đến các kênh ion khác có ở nút xoang (hình 8). Thuốc cũng duy trì đặc tính dãn mạch vành khi gắng sức (GS), điều này đặc biệt có lợi cho BN ĐTNÔĐ khi TMCB cơ tim thường xảy ra sau GS. Bên cạnh đó thuốc cũng không có tác động ức chế co bóp cơ tim. Đó là lý do vì sao với cùng một mức giảm nhịp tim, nhưng chỉ có Ivabradine cải thiện được cung lượng tim một cách có ý nghĩa khi so với chẹn beta. Như vậy giữa Ivabradine & chẹn betacó nhiều sự khác biệt (bảng 3) (27-29).
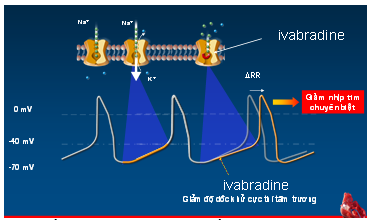
Hình 8.Cơ chế hoạt động kênh Ifvà thuốc Ivabradine (28)
Bảng 3:Sự khác biệt giữa chẹn β và Ivabradine (27,28)
|
Hiệu quả TM |
Chẹn β |
Ivabradine |
|
Tính dẫn truyền |
Ức chế |
Ức chế |
|
Sức co bóp |
Ức chế |
Không |
|
Tính thư giãn |
Ức chế |
Không |
|
Dẫn truyền trong tim |
Ức chế |
Không |
|
Kích thích cơ tim |
Ức chế |
Không |
IV.2. Ứng dụng lâm sàng (3-6)
2.1. Chỉ định:
BNST EF ≤ 35%, và nhịp xoang ≥ 70l/ph đã điều trị tối đa liều chẹn beta dung nạp hoặc chống chỉ định. Điều trị đồng thời phải bao gồm ức chế hệ RAA và kháng thụ thể mineralocorticoid (nếu theo dõi được kali máu). Ngưỡng nhịp tim trên 70l/ph và dựa vào các tiêu chuẩn của TNLS. Các hướng dẫn của hiệp hội tim mạch Mỹ và châu Âu năm 2016 đã nâng mức khuyến cáo lên IIA (bảng 4).
Bảng 4. Hướng dẫn của hiệp hội tim mạch Mỹ và châu Âu năm 2016 về sử dụng ivabradine trong ST EF giảm(3,4)
|
Khuyến cáo cho Ivabradine (ACC/AHA) |
|||||
|
COR |
LOE |
Khuyến cáo |
|||
|
IIa |
B-R |
Ivabradine làm giảm nhập viện do ST cho BN ST mạn ổn định có triệu chứng (NYHA độ II-III, LVEF ≤35%), đang điều trị theo phác đồ chuẩn bao gồm chẹn beta ở liều tối đa dung nạp được và nhịp xoang tần số 70l/ph hoặc cao hơn lúc nghỉ. |
|||
|
ESC 2016: Ức chế kênh If |
|||||
|
Ivabradin được xem xét để giảm nguy cơ nhập viện do ST và tử vong do tim mạch ở những BN ST có triệu chứng với LVEF≤35%, nhịp xoang và tần số tim ≥70 l/ph mặc dù điều trị với liều tối ưu của chẹn beta (hoặc liều tối đa dung nạp được), ƯCMC (hoặc ƯCTT) và một MRA (hoặc ARB) |
IIa |
B |
180 |
||
|
Ivabradin nên được xem xét để giảm nguy cơ nhập viện do ST và tử vong do tim mạch ở những bệnh nhân ST có triệu chứng với LVEF≤35%, nhịp xoang và tần số tim ≥70 l/ph và không thể dung nạp hoặc chống chỉ định của chẹn beta. BN nên được điều trị với ƯCMC (hoặc ƯCTT) và một MRA (hoặc ƯCTT) |
IIa |
C |
181 |
||
2.2. Chống chỉ định:
+ Suy tim mất bù cấp.
+ HA< 90/50.
+ Hội chứng suy nút xoang, block xoang nhĩ hoặc AV, trừ khi đã được đặt máy tạo nhịp.
+ Suy gan nặng.
+ Dùng phối hợp với uống ức chế CYP3A cytochrome mạnh như: thuốc chống virus (Ritonavir, Indinavir…), thuốc chống nấm (Ketoconazole,Itraconazole…), thuốc kháng sinh (Claritromycin, Telithromycin…).
2.3. Hiệu quả lâm sàng:
Thử nghiệm SHIFT cho thấy Ivabradin làm giảm tiêu chí gộp tử vong tim mạch hoặc nhập viện vì ST xấu đi ở BNST EF giảm và lợi ích lâm sàng kết hợp với giảm tần số tim.Thử nghiệm SHIFT gồm 6558 BNST EF≤35%, và nhịp xoang ≥70l/ph. BN được phân ngẫu nhiên hoặc là dùng Ivabradin hoặc dùng placebo, theo dõi 23 tháng. Tiêu chí chính gồm tử vong tim mạch hoặc nhập viện và ST xấu đi. BN ở nhóm dùng Ivabradin có tiêu chí chính thấp hơn nhóm chứng (24% so với 29%) do chủ yếu giảm nhập viện do ST (tỷ số chênh (HR) 0.74%, CI 95% 0.66-0.83%) và giảm tử vong do ST (HR 0.74, 95% CI 0.58-0.94). Sau 28 ngày tần số tim nhóm Ivabradin giảm trung bình là 15,4 nhịp/phút,BN có giảm nhịp tim sau 28 ngày còn 60l/ph có ít biến cố theo tiêu chí chính hơn trên BN có tần số tim cao hơn.
Phân tích sau này của thử nghiệm SHIFT cho thấy tử vong do mọi nguyên nhân (HR 0.83, 95% CI 0.72-0.96%) và nhập viện vì ST (HR 0.70, 95% CI, 0.61-0.80) giảm có ý nghĩa ở BN với tần số tim ban đầu ≥75l/ph, nhưng không có ý nghĩa ở BN với tần số tim ban đầu ≤75 l/ph. Thử nghiệm SHIFT chứng tỏ kiểm soát tần số tim là quan trọng ở BNST.
2.4. Cách sử dụng:
Bắt đầu điều trị: trước khi bắt đàu cần hướng dẫn kỹ cho BN hết nguy cơ các tác dụng phụ của thuốc (làm chậm nhịp tim). Cũng giống như bắt đầu điều trị chẹn β, BN không còn quá tải dịch. Điều trị đầy đủ các thuốc điều trị ST nền tảng. Nếu còn nhịp xoang và tần số ≥70l/ph mới được cho. BN có chống chỉ định với chẹn β, có thể cho luôn Ivabradin sau ức chế hệ RAA và lợi tiểu (nếu có). Nên khởi đầu với liều 2,5mg x 2 lần/ngày trong 2 tuần. Nếu không đạt hiệu quả mới tăng liều lên 5mg x 2 lần/ngày. Sau 2 tuần, nếu không đạt mục tiêu điều trị mới tăng lên 7,5mg x 2 lần/ngày. Nếu nhịp tim 55-60 l/ph, duy trì liều đó. Nếu <55 l/ph hoặc nếu BN có triệu chứng chóng mặt thì giảm liều. Ngưng nếu tần số tim <50 l/ph. Cũng cần biết khi dùng với liều điều trị tối thiểu (5mg x 2 lần/ngày) nhịp tim giảm ít nhất là 10 à12 nhịp/ phút. Chúng ta có thể căn cứ vào mức này để tiên đoán khả năng đạt hiệu quả điều trị của BN, qua đó chỉnh liều cho phù hợp. Ơ người lớn tuổi ( > 75 tuổi) chỉ nên bắt đầu bằng liều 2,5mg/ngày. Mục tiêu nhịp tim cần đạt là khoảng 60 à65 lần/phút. Ơ BNkèm COPD hay các bệnh phổi mạn tính khác, nhịp tim đích có thể cao hơn (khoảng 70 lần/phút), tuy nhiên cũng còn phụ thuộc từng người bệnh.
Thuốc có thể dùng chung với các thuốc TM khác: kháng tiểu cầu, statin, ức chế men chuyển hay thụ thể, chẹn kênh Calcium Dihydropyridine, Fibrate, Nitrate, Warfarin, Digoxin. Không nên phối hợp với các thuốc chẹn trên Calcium nhóm Non Dihydropyridine, các thuốc chống loạn nhịp khác, cũng như các thuốc chủ yếu chuyển hóa qua men CYP3A4 ở gan, kháng sinh nhóm Macrolid, thuốc ức chế men protein HIV,…
2.5. Phối hợp Ivabradin và liều chẹn β tối đa dung nạp (6,8, 30-33):
Trong nghiên cứu SHIFT 56% BN dùng liều chẹn β≥ 50% liều đích: liều này thấp hơn liều chẹn β trong các TNLS ST khác như CIBIS-II và MERIT với 67% BN dùng > 50% liều đích chẹn β. Lý do BN trong nghiên cứu SHIFT, BN huyết áp thấp hơn vì có phối hợp với lợi tiểu kháng aldosterone, nên chiến lược dùng liều chẹn β có thể khác liều chẹn β đạt được trong các nghiên cứu trước đây. Tuy nhiên, điều này lại tương đương trong thế giới thực. Trong thực hành, chúng tôi cũng it khi dùng tới liều đích chẹn β (thường cũng là 50% liều đích). Tương tự, tại châu Âu, nghiên cứu ESC-HF Pilot, HF-ACTION cũng cho thấy đa số chỉ dùng 50% liều chẹn beta đích. Mặt khác, hậu phân tích sau nghiên cứu MERIT-HF, CIBIS-II, SENIOR cũng không cho thấy cải thiện tiên lượng liên quan đến liều chẹn β. Một số phân tích gộp cho thấy giảm tần số tim không do chẹn β cũng có tiên lượng tốt hơn. Chính vì vậy chúng ta có thể áp dụng phối hợp Ivabradin và chẹn β liều tối đa dung nạp cho BN ST EF giảm, nhịp xoang, tần số ≥ 70 lần/ph.
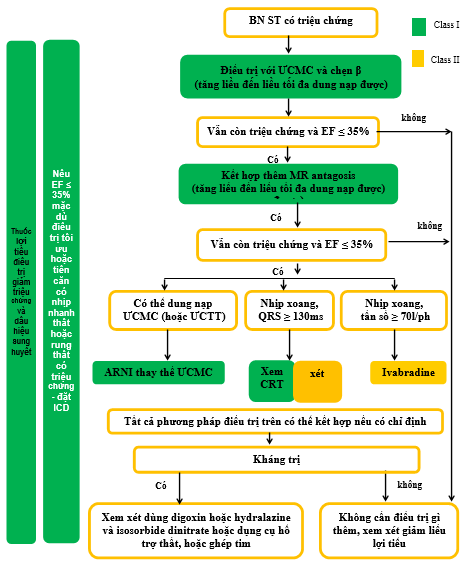
V. Tóm tắt và đề nghị (Hình 9)
1. Chẹn beta chắc chắn làm giảm nhập viện do ST và cải thiện sống còn ở BN ST EF giảm. Chúng ta cần chọn một trong 4 loại chẹn beta đã được chứng minh qua các TNLS (carvedilol, bisoprolol, nebivolol, metoprolol succinate).
2. Cần tuân thủ các nguyên tắc dùng chẹn beta trong lâm sàng.
3. Bằng chứng hiện tại cho phép sự dụng cho nhiều phân nhóm BN ST (bệnh tim thiếu máu cục bộ hoặc không do bệnh tim thiếu máu cục bộ, giới, lớn tuổi, ĐTĐ hoặc không,…) và thận trọng ở BN kèm COPD.
4. Khi dùng chẹn beta, cố gắng tăng dần liều đến liều đích. Tuy nhiên, nhiều BN không dung nạp với liều đích và chúng ta duy trì cho BN liều tối đa dung nạp được.
5. Ivabradine nên sử dụng ở BN ST EF ≤ 35%, và nhịp xoang ≥ 70l/ph dù đã điều trị tối đa liều chẹn beta dung nạp hoặc có chống chỉ định. Trước khi bắt đàu điều trị, cần hướng dẫn kỹ cho BN hết nguy cơ các tác dụng phụ của thuốc (làm chậm nhịp tim). Cũng giống như bắt đầu điều trị chẹn β, BN không còn quá tải dịch. Điều trị đầy đủ các thuốc điều trị ST nền tảng. Nên khởi đầu với liều 2,5mg x 2 lần/ngày trong 2 tuần; và điều chỉnh liều theo đáp ứng của BN.
Hình 9. Tóm tắt chiến lược điều trị ST, chỉ định dùng chẹn beta và ivabradine
Tài liệu tham khảo
1. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012.
2. 2013 ACCF/AHA Guideline for the Management of Heart Failure.
3. 2016 ACC/AHA/HFSA Focused Update on New Pharmacological Therapy for Heart Failure: An Update of the 2013 ACCF/AHA.
4. 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure.
5. Colucci. WS: Rationale for and clinical trials of beta blockers in heart failure due to systolic dysfunction. Uptodate 2016.
6. Colucci. WS: Use of beta blockers and ivabradine in heart failure with reduced ejection fraction. Uptodate 2016.
7. Dobre.D et al: Heart rate: a prognostic factor and therapeutic target in chronic heart failure. The distinct roles of drugs with heart rate-lowering properties. European Journal of Heart Failure (2014) 16, 76–85.
8. Bohm. M et al: Heart rate as a risk factor in chronic heart failure (SHIFT): the association between heart rate and outcomes in a randomised placebo-controlled trial. Lancet 2010; 376: 886–94.
9. Chatterjee. S et al:Benefits of â blockers in patients with heart failure andreduced ejection fraction: network meta-analysis. BMJ 2013;346: 1-10.
10. Mann.Dl: Management of heart failure patient with reduced ejection fraction. In Boow.RO et al: Braunwalds heart disease. 10th 2015: 512-540.
11. Wikstrand. J, Wedel. H, Castagno. D & McMurray JJV: The large-scale placebo-controlled beta-blocker studies in systolic heart failure revisited: results from CIBIS-II, COPERNICUS and SENIORS-SHF compared with stratified subsets from MERIT-HF.
12. Le Jemtel.T.H: Diagnostic and therapeutic challenges in Patients With Coexistent Chronic Obstructive Pulmonary Disease and Chronic Heart Failure. JACC 2007; 49: 171-180.
13. Nguyễn Thanh Hiền, Phạm Nguyễn Vinh: Những thay đổi về chẩn đoán và điều trị BN COPD và ST mạn tính kết hợp. Thời sự Tim mạch học 2007; số 111: 2-10.
14. Minor.DS et al: beta-blocker and COPD: Inappropriadte Avoidance? The Journal of Clinical Hypertension Vol 15 | No 12 | December 2013: 925-930.
15. van der Woude.H.J et al: Detrimental effects of beta-blockers in COPD. Chest 2005; 127: 818-824.
16. Salpeter SR, Ormiston TM, Salpeter EE, Wood-Baker R.Cardioselective beta-blockers for reversible airway disease (Review). Cochrane Database of Systematic Reviews 2002, Issue 4. Art. No.: CD002992.
17. Shelton.R.J et al: Effect of a community heart failure clinic on uptake of beta blockers by patients with obstructive airways disease and heart failure. Heart 2006; 92: 331-336.
18. GOLD 2016.
19. Colucci.WS: Pharmacologic therapy of heart failure with reduced ejection fraction. Uptodate 2016.
20. McAlister.FA et al:Meta-analysis: Blocker Dose, Heart Rate Reduction, and Death in Patients With Heart Failure. Ann Intern Med. 2009;150:784-794.
21. Mann.DL: Heart failure. A companion to Braunwalds Heart disease. 2004; p: 629.
22. Lindenfeld.J et al: Aspirin Impairs Reverse Myocardial Remodeling in Patients With Heart Failure Treated With Beta-Blockers. J Am Coll Cardiol 2001;38:1950–6.
23. Stevenson.LW: Management of acute decompensated heart failure. In Mann.DL: Heart failure. 3th 2016: 634-647.
24. Colucci. WS: Treatment of Acute decompensated heart failure: Components of therapy. Uptadate 2016.
25. Prins. KW ET AL:Effects of Beta-Blocker Withdrawal in Acute Decompensated Heart Failure: A Systematic Review and Meta-Analysis. J Am Coll Cardiol HF 2015;3:647–53.
26. Nguyễn Thanh Hiền: Cập nhật chẩn đoán, điều trị ST và vai trò của ức chế thụ thể beta trong ST. Chuyên đề Tim mạch học. tháng 6. 2012.
27. Thollon C et al: Electrophysiological effects of S 16257, a novel sinoatrial node modulator, on rabbit and guinea-pig cardiac preparation: comparision with UL-FS 49 . Br J Pharmacol. 1994;112:37-42.
28. Bois P et a: Mode of action of bradycardic agent, S 16257, on ionic currentof rabbit sinoatrial node cells. Br J Pharmacol. 1996;118:1051-1057.
29. DiFrancesco A, et al: Heart rate lowering by specific and selective If current inhibition with ivabradine. Drugs. 2004;64:1757-1765.
30. Bohm. M et al: Heart rate at baseline influences the effect of ivabradineon cardiovascular outcomes in chronic heart failure: analysis from the SHIFT study. Clin Res Cardiol (2013) 102:11–22.
31. Maggioni.AP et al: EURObservational Research Programme: The Heart Failure Pilot Survey (ESC-HF Pilot). European Journal of Heart Failure (2010) 12, 1076–1084.
32. Cullingtin.D, Goode. KM, Clark. Al, Cleland. JGF: Heart rate achieved or beta-blocker dose in patients with chronic heart failure: which is the better target? European Journal of Heart Failure (2012) 14, 737–747.
33. PharmD.MF et al: Relationship of Beta-Blocker Dose With Outcomes in Ambulatory Heart Failure Patients With Systolic Dysfunction :Results From the HF-ACTION (Heart Failure: A Controlled Trial Investigating Outcomes of Exercise Training) Trial. J Am Coll Cardiol 2012;60:208–15.







