TS. PHẠM HỮU VĂN
BS CKI. NGUYỄN ANH THƯ
Mở đầu
Viêm cơ tim do virus cấp tính và viêm màng ngoài tim cấp tính thường là tình trạng tự giới hạn, diễn ra lành tính và có thể thậm chí không có triệu chứng để đưa đến sự quan tâm về y tế. Tuy nhiên, rối loạn nhịp thất là tình trạng thường xuyên xảy ra trong viêm cơ tim do virus; điều này có thể chỉ ở dạng các ngoại tâm thu thất hay còn gọi là phức hợp thất sớm (PVC) nhưng cũng có thể ác tính hơn nhiều như nhịp nhanh thất dai dẳng (VT) hoặc VF không kịp phát hiện và được điều trị. Do đó, viêm cơ tim được cho là chiếm tỷ lệ lớn trong các trường hợp đột tử tim ở những người trẻ tuổi không mắc bệnh tim cấu trúc trước đó. [1.3] Xác định viêm cơ tim cấp có hoặc không có viêm màng ngoài tim là rất quan trọng. Tuy nhiên, có nhiều cản trở tiềm ẩn cho việc này. Hơn nữa, ngay cả khi chẩn đoán được thực hiện, các can thiệp điều trị vẫn còn hạn chế và không đặc hiệu. Xác định những người có nguy cơ rối loạn nhịp tim đe dọa tính mạng cao nhất là rất quan trọng để giảm tỷ lệ tử vong do tình trạng này. [4] Trong những năm qua, trong thực hành lâm sàng, nhiều trường hợp viêm cơ tim cấp có biến chứng rối loạn nhịp, suy tim cấp đã được chẩn đoán và điều trị, thậm chí tiên lượng rất nặng phải nhờ những can thiệp hiện đại mới có thể cứu sống như máy hỗ trợ thất trái. Tuy nhiêu đôi khi vẫn gặp những nhầm lẫn trong chẩn đoán nguyên nhân. Với hy vọng giúp các đồng nghiệp quan tâm hơn về bệnh lý này, chúng tôi giời thiệu một cách tóm tắt những hiểu biết hiện tại về lĩnh vực đầy thách thức này.
Viêm cơ tim do virus
Mặc dù có nhiều khởi kích tiềm tang, ở các nước kinh tế đã phát triển, virus là nguyên nhân thông thường nhất của viêm cơ tim (viêm các cơ của tim). [5] Virus được nhận biết phổ biến nhất trong trạng thái này là adenovirus, [6] parvovirus B19, [7] herpes virus [6] và enterovirus.
Tỷ lệ thực sự của viêm cơ tim do virus vẫn chưa chắc chắn, phần lớn là kết quả của quá trình thường không có triệu chứng. Ngay cả khi có triệu chứng, viêm cơ tim do virus thường vẫn không được nhận biết hoặc không được khẳng định. Viêm cơ tim đã được đưa ra ở tỷ lệ 1% đến 40% các trường hợp đột tử, nhưng tỷ lệ thực sự lại biểu hiện thấp. Viêm cơ tim được xác định là nguyên nhân tử vong trong 40% trường hợp trong một nghiên cứu về các tân binh Không quân bị chết tim đột ngột.[8]
Có 3 giai đoạn đối với viêm cơ tim do virus.[9] Giai đoạn đầu tiên bao gồm sự nhân lên của virus hoạt động trong cơ tim gây ra sự phân giải trực tiếp các tế bào cơ tim và kích hoạt phản ứng miễn dịch bẩm sinh. Tổn thương cơ tim tiếp theo có thể không có triệu chứng hoặc có thể bao gồm các triệu chứng ở bất cứ mức độ nào đến mức độ sốc tim. Hầu hết bệnh nhân hồi phục hoàn toàn từ giai đoạn cấp tính ban đầu này. Ở một số người, hoạt động bệnh dai dẳng được cho là kích hoạt phản ứng tự miễn dịch thích ứng với protein của virus và cơ tim. Một lần nữa, ở phần lớn các trường hợp, các kích thích gây bệnh được tiêu biến và đáp ứng miễn dịch giảm dần. Nhưng ở một số người, do hậu quả của tác động viêm có hại của phản ứng này đối với cơ tim, trong giai đoạn thứ hai của quá trình bệnh, thường có biểu hiện suy tim. Hơn nữa, phản ứng tự miễn dịch này dường như là nguyên nhân chính gây tổn thương tế bào, sau đó có thể dẫn đến rối loạn nhịp thất. Vai trò then chốt của thành phần tự miễn được làm nổi bật bằng dữ liệu thực nghiệm cho thấy mức độ nghiêm trọng của bệnh được điều chỉnh bằng 2 gene mức độ phức hợp tương hợp mô học chính bằng cách điều chỉnh yếu tố tự miễn của viêm cơ tim. [10]
Mặc dù kích thước và phân suất tống máu thất trái (LV) thường vẫn bình thường trong viêm cơ tim do virus cấp tính, một kiểu hình bệnh cơ tim giãn có thể phát triển do viêm cơ tim dai dẳng, [11,12] và điều này thể hiện giai đoạn thứ ba của quá trình bệnh. Chiến lược chẩn đoán và điều trị được định hướng tốt nhất theo giai đoạn cụ thể của quá trình bệnh. Rối loạn nhịp tim trong bệnh cơ tim giãn đã được John và các đồng nghiệp xem xét một cách chuyên biệt trong vấn đề này.
Sự đóng góp của viêm cơ tim do virus vào sự phát triển của bệnh cơ tim giãn đã được suy ra bằng sự phân lập phổ biến tư liệu gen của virus trong cơ tim của các cá thể bị ảnh hưởng.[6,13] Ngoài ra, rối loạn chức năng cơ tim tiến triển có liên quan đến sự tồn tại của virus, ngược lại chức năng tâm thất được cải thiện khi virus được loại bỏ.[14] Vai trò nguyên nhân của virus được hỗ trợ thêm bằng cách cải thiện chức năng tâm thất sau khi điều trị bằng điều biến miễn dịch. Tuy nhiên, với sự đánh giá cao và sự hiểu biết về cơ sở di truyền của bệnh cơ tim giãn, [15,16] cơ chế nguyên nhân có thể trong trường hợp phức tạp hơn. Người ta nhận ra phần lớn dân số bị nhiễm virut tim mạch hết lần này đến lần khác, nhưng chỉ một số ít người bị nhiễm bệnh (1% – 5%) tiếp tục phát triển được chứng minh về tổ chức học là viêm cơ tim.[17] Có thể trong một số trường hợp, một đợt viêm cơ tim do virus là yếu tố khởi phát một khuynh hướng di truyền đối với bệnh cơ tim giãn. Tuy nhiên, hầu hết những người bị nhiễm vi-rút có thể gây viêm cơ tim không tiếp tục phát triển bệnh lâm sàng và những người mắc bệnh này, chỉ một số ít người chuyển sang bệnh cơ tim. Trong một nghiên cứu kết hợp trên toàn bộ bộ gen, Bezzina và cộng sự [18] đã xác định một đa hình liền kề với gen mã hóa một thụ thể virus liên quan đến cả bệnh cơ tim giãn và điều biến hệ thống dẫn truyền tim mà họ thấy thường gặp ở bệnh nhân bị VF hơn là đối chứng .
Điều tra nghiên cứu viêm cơ tim do virus
Các nhận định điện tâm đồ (ECG) trong viêm cơ tim cấp tính phần lớn thường không đặc hiệu. [19] Nhịp xoang nhanh là một phát hiện điển hình. Chênh lên của đoạn ST có khả năng giả nhồi máu cơ tim cấp tính thường xuyên xuất hiện. Chứng loạn nhịp tim hoặc block nhánh bó có thể thấy rõ trên ECG. Liên quan đến các enzyme của tim, độ nhạy vượt trội của các troponin tim so với creatine kinase MB đã được thiết lập, [20] và điều này thậm chí còn rõ rệt hơn với các xét nghiệm có độ nhạy cao. Tương tự, các xét nghiệm protein phản ứng C (CRP) có độ nhạy cao cũng có khả năng tốt để phát hiện viêm cơ tim do virus cấp tính. [21]
Khẳng định nguyên nhân virus gây bệnh vượt quá tiền sử các tiền triệu của virus đòi hỏi phải phát hiện một loại virus phù hợp, bộ gen virus hoặc kháng thể thích hợp trên huyết thanh học hoặc trong mô hoặc chất lỏng có liên quan. Huyết thanh cập đôi được thu thập cách nhau ít nhất hai tuần có thể tạo ra cơ chất virus, nhưng bằng chứng rõ ràng hơn bằng cách xác định trực tiếp virus từ mô sinh thiết bằng phản ứng chuỗi polymerase (PCR) hoặc ở sản xuất lai tại chỗ là mong muốn, nhưng không được thực hiện thông thường.
Vai trò hình ảnh học
Siêu âm tim vẫn là nền tảng của hình ảnh tim. Tuy nhiên, CMR có khả năng đặc biệt làm cho nó trở thành một nghiên cứu đầu tiên mạnh mẽ tăng lên trong chẩn đoán và đánh giá viêm cơ tim. CMR sử dụng phản ứng của các proton hydro để kích thích tần số radio và do đó rất nhạy cảm với các vùng có hàm lượng nước tăng. Các trình tự cụ thể, đáng chú ý là các chuỗi T2 phục hồi đảo ngược ngắn (Short-TI Inversion Recovery: STIR), đã được phát triển để xác định các vùng của cơ tim (Hình 1) và viêm màng ngoài tim hoặc phù. Trong viêm cơ tim cấp tính, trong đó có ly giải tế bào và hoại tử ngoài viêm, các vùng tổn thương cơ tim được xác định thêm bằng cách sử dụng các chất tương phản ngoại bào dựa trên gadolinium, trong trạng thái này có thể tích tụ ở nơi màng tế bào bị tổn thương. Trong trường hợp xơ hóa thay thế đã xảy ra sau viêm cơ tim cấp tính, không gian ngoại bào tăng lên được xác định trên hình ảnh gadolinium muộn. Những vùng sẹo này được làm nổi bật bởi sự tăng cường độ tương phản dựa trên gadolinium trên hình ảnh muộn thường được coi là chất nền cho các vòng vào lại đóng vai trò là chất nền cho rối loạn nhịp tim. [22] Điển hình là mô hình tăng cường gadolinium muộn trong viêm cơ tim liên quan đến viêm cơ tim. Thông thường, điều này chủ yếu là thành bên tự do thất trái (LV). [23]
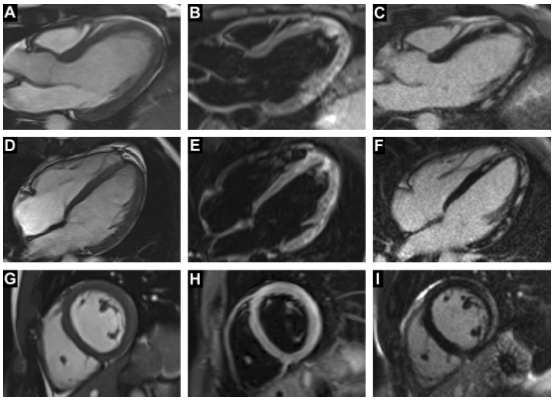
Hình 1. Hình ảnh CMR chẩn đoán viêm cơ tim cấp. Hàng trên (A- C) là góc nhìn LVOT (đường ra của tâm thất trái); hàng giữa (D – F), góc nhìn HLA (trục ngang dài; tương đương 4 buồng); và hàng dưới (G – I) một lát trục ngắn nền. Trong mỗi loạt, cột đầu tiên là hình ảnh SSFP (diễn biến tự nhiên trạng thái ổn định) (đối với hình ảnh cine). Ngay cả trong những hình ảnh này, có các tín hiệu cao hơn một chút ở các vùng cơ tim, đó là phù nề. Cột giữa là hình ảnh STIR để phát hiện viêm cơ tim hoặc phù. Các khu vực có tín hiệu cao được xác định rõ ràng là viêm cơ tim hoặc phù ở các khu vực tương tự như tăng cường gadolinium muộn (LGE) được thấy trong cột thứ ba. LGE này điển hình trong phân tán dưới thượng tâm mạc / giữa thành, ngược lại với nguồn gốc dưới nội tâm mạch của LGE được nhìn thấy trong nhồi máu cơ tim.
Lợi ích bổ sung là khả năng CMR phân biệt viêm cơ tim với nhồi máu cơ tim chủ yếu dựa trên mô hình tăng cường gadolinium muộn. Nhồi máu cơ tim thường có nguồn gốc từ dưới nội tâm mạc. Với khả năng của CMR để dễ dàng xác định các vùng viêm cơ tim, sinh thiết nội mô không còn cần thiết cho chẩn đoán viêm cơ tim trong hầu hết các trường hợp. Mặc dù chẩn đoán này có thể rõ ràng từ tiền sử khỏe mạnh, kết quả ECG bất thường và nồng độ men tim tăng cao, CMR có thể xác nhận một cách dứt khoát điều này cũng như đánh giá phạm vi viêm cơ tim và tác động của nó đối với kích thước và chức năng của tâm thất. Viêm lan rộng và / hoặc tăng cường gadolinium muộn có thể cho thấy khả năng tái cấu trúc bất lợi cao hơn và làm rõ giá trị của một nghiên cứu tiếp theo hoặc siêu âm tim hoặc CMR để đánh giá điều này. CMR cũng hữu ích trong việc chỉ ra khu vực đích để sinh thiết cơ tim nội tâm mạch. [22] Tuy nhiên, trên lâm sàng, sinh thiết nội mô hiện nay thường dành cho những người nghi ngờ bị viêm cơ tim tế bào khổng lồ hoặc những người đã được điều trị hỗ trợ thông thường nhưng bệnh vẫn suy thoái tiến triển.
Cơ chế điện học của rối loạn nhịp
Một số cơ chế phân tử và miễn dịch có khả năng liên quan đến quá trình bệnh (khung 1). Cơ chế chính xác hoặc nhiều cơ chế có khả năng gây rối loạn nhịp thất do viêm cơ tim cấp không rõ ràng, mặc dù một số giả thuyết đã được đưa ra. Sự hình thành các vòng vào lại do sự chậm lại của điện thế hoạt động vì xơ hóa cơ tim do virus và phì đại thứ phát đã được đề xuất. [22] Sự phát triển của các khu vực viêm khu trú ở khu vực nhạy cảm về điện của cơ tim cũng có thể gây ra rối loạn nhịp thất. Cũng có khả năng bị rối loạn chức năng kênh ion cơ tim, như đã thấy trong các mô hình động vật, [25] cũng như thiếu máu cơ tim góp phần hoặc cơ chế gây rối loạn nhịp thất trong viêm cơ tim do virus. Bản thân quá trình viêm dường như thúc đẩy loạn nhịp, và việc giải quyết điều này cũng có thể làm giảm đi nền thúc đẩy rối loạn nhịp.
Có tư liệu từ động vật để ủng hộ sự thay đổi trong biểu hiện của connexin cơ tim, các protein quan trọng liên quan đến chức năng tiếp giáp khoảng cách và do đó liên hệ giữa các cơ tim, trong quá trình viêm cơ tim được tạo ra do coxsackievirus B3 (CVB3). [26] Điều đáng quan tâm, atorvastatin có thể điều chỉnh sự điều hòa giảm biểu hiện của connexin, khôi phục chức năng kênh tiếp giáp khoảng cách và hậu quả trong viêm cơ tim do virus ở chuột sau khi tiêm CVB3. Điều hòa canxi bị thay đổi cũng có khả năng là một thành phần quan trọng của sự nhiễu loạn chức năng cơ tim bình thường trong viêm cơ tim cấp tính. [27] Vùng nhồi máu cơ tim có thể là kết quả của co thắt mạch máu kéo dài. Thiếu máu cục bộ vi mạch cũng có thể là một điểm thúc đẩy rối loạn nhịp tim.
Một số nền rối loạn nhịp tim của viêm cơ tim dường như nằm trong bệnh lý – bệnh cơ tim được bộc lộ hoặc bệnh lý kênh. Một thành phần viêm thường được xác định trong cơ tim của các cá nhân với bệnh cơ tim thất phải gây rối loạn nhịp (ARVC) tại sau tử vong và có khả năng thúc đẩy rối loạn nhịp thất.[28] ARVC có thể bị thúc đẩy hay bộc lộ của viêm cơ tim, nhưng dữ liệu cho thấy viêm cơ tim thường xuyên có thể dẫn đến thay đổi cấu trúc bắt chước ARVC. [29] Trong một nhóm 30 bệnh nhân đáp ứng các tiêu chí không xâm lấn đối với ARVC, một nửa có bằng chứng mô học và hóa mô miễn dịch của ARVC, trong khi viêm cơ tim hoạt động được xác định ở nửa còn lại. Sinh thiết nội tâm mạc được yêu cầu để xác định xem ai trong số họ có ARVC và bệnh nào bị viêm cơ tim. Những người bị ARVC có rối loạn nhịp tim ác tính tái phát, trong khi những người bị viêm cơ tim vẫn không có triệu chứng và không bị rối loạn nhịp tim.
Viêm cơ tim do virus và bệnh kênh
Một số bài báo trong y văn báo cáo về mối liên quan của viêm cơ tim cấp và rối loạn nhịp thất với các bệnh lý cơ tim, đáng chú ý là hội chứng Brugada, hội chứng QT ngắn và tái cực sớm. [30,31] Viêm cơ tim thất phải (RV) thường được xác định ở bệnh nhân có kiểu hình giống Brugada; trong một nghiên cứu, nó được xác định trên 77% bệnh nhân. [32]
| Khung 1
Các cơ chế rối loạn nhịp trong viêm cơ tim Cơ chế tổn thương cơ tim – Ly giải các tế bào cơ tim được tạo ra trực tiếp do virus khởi kích đáp ứng miễn địch khở đầu – Đáp ứng tự miễn dịch tương ứng – Sự dai dẳng của virus – Chết tế bào theo chương trình (apoptotic) – Cơ chế điện học gây rối loạn nhịp và được bổ xung – Xơ hóa thay thế cơ tim, ủng hộ cơ chế vào lại – Hoại tử tế bào cơ – Tác dụng thúc đẩy loạn nhịp của cytokine – Chức năng thay đổi tại các điểm nối khoảng cách cơ tim – Điều chỉnh canxi bị thay đổi – Nhồi máu, tổn thương thiếu máu cục bộ vi mạch – Giải phóng protease dẫn đến sự phân cắt của dystrophin với hậu quả bất thường về tế bào học – Bệnh cơ tim được bộc lộ, bệnh cơ tim giãn (DCM) / bệnh cơ tim thất phải gây loạn nhịp tim (ARVC) – Bệnh kênh đồng thời |
Điều trị
Trong hầu hết các trường hợp, không cần điều trị. Như đã được mô tả, viêm cơ tim cấp tính có thể không có triệu chứng hoặc thường chỉ gây ra các triệu chứng siêu vi không đặc hiệu tự giới hạn ở các cá nhân bị ảnh hưởng có thể tìm kiếm nhiều loại thuốc không cần kê đơn. Hiện tại có bằng chứng khá ít và yếu để chứng minh việc sử dụng bất kỳ liệu pháp điều trị bệnh cụ thể nào đối với viêm cơ tim do virus cấp tính, mặc dù đã được sử dụng các globulin miễn dịch (immunoglobulin), ức chế miễn dịch, interferon (IFN) và liệu pháp hấp phụ miễn dịch. Những liệu pháp này không có hiệu quả nhất trong giai đoạn 2 của quá trình bệnh, đó là giai đoạn đáp ứng tự miễn dịch. Tương tự, thiếu bằng chứng để hỗ trợ việc sử dụng các thuốc chống loạn nhịp cụ thể ngoài các chiến lược thông thường. Điều trị suy tim tuân theo các hướng dẫn hiện hành. [33] Bản chất thường tự giới hạn của viêm cơ tim làm cho điều này trở thành một điều kiện hấp dẫn để hỗ trợ tuần hoàn như một cầu nối để phục hồi ở những bệnh nhân cần điều trị này. Các chiến lược dài hạn hơn để tác động đến bệnh có thể nằm trong việc phòng ngừa bằng cách tiêm chủng hoặc phát triển các phân tử để ngăn chặn các thụ thể của virus. Về cơ bản, điều trị là hỗ trợ, trong đó bất kỳ điều gì cần thiết. Theo truyền thống, các cá nhân bị ảnh hưởng nên tránh hoạt động gắng sức trong vài tháng.[34] Bằng chứng hỗ trợ cho khuyến nghị để tránh tình trạng làm việc không ngừng trong bệnh do virus gây ra là không tương ứng.
Tiên lượng
Có tư liệu hạn chế về tiên lượng dài hạn sau viêm cơ tim do virus. Một nghiên cứu cho thấy tỷ lệ tử vong 20% trong 5 năm sau viêm cơ tim do virus.[4] Nhiều nghiên cứu lớn về bệnh cơ tim giãn đặc biệt loại trừ các trường hợp được coi là do viêm cơ tim quá mức, mặc dù rất có thể ngay cả khi đây là tiêu chí loại trừ rõ ràng, Nguyên nhân trong một số trường hợp vẫn là viêm cơ tim do virus. Trong trường hợp không có kiểu hình bệnh cơ tim giãn, tiên lượng cho các cá nhân sống sót sau ngừng tim do rối loạn nhịp thất trong bối cảnh viêm cơ tim cấp có vẻ thuận lợi nếu hồi sức nhanh chóng và hiệu quả vì rối loạn nhịp tim như vậy có xu hướng tự giới hạn. Tuy nhiên nghiên cứu lớn dài hạn được đòi hỏi.
Phân tầng nguy cơ cho bệnh nhân bị viêm cơ tim cho đến gần đây rất khó khăn vì dữ liệu tiên lượng và các dấu ấn sinh học nguy cơ bị hạn chế. Một trong những hạn chế chính là khó khăn trong việc thiết lập chẩn đoán vì phổ các biểu hiện có thể rộng và các khoảng thời gian bệnh thường không triệu chứng. Tuy nhiên, nơi có nghi ngờ chẩn đoán, CMR đã nổi lên như một công cụ chẩn đoán mạnh mẽ. Hơn nữa, ngày càng có nhiều dữ liệu cho thấy sự xuất hiện của CMR mang thông tin tiên lượng có giá trị. Tăng cường muộn gadolinium biểu lộ xơ hóa thay thế đã được chứng minh là một yếu tố dự báo độc lập về kết quả bất lợi trong bệnh cơ tim giãn. [36] Schumm và đồng nghiệp [37] theo dõi 405 bệnh nhân liên tiếp được thực hiện CMR để đánh giá nghi ngờ viêm cơ tim. Ở 55,6% bệnh nhân, CMR ban đầu đã xác nhận khối lượng LV và phân suất tống máu bình thường không có gia tăng gadolinium muộn. Trình tự STIR T2 đã không được thực hiện. CMR được xem xét để xác nhận chẩn đoán viêm cơ tim ở 28,8% bệnh nhân. Các bệnh nhân được theo dõi trong thời gian trung bình là 1591 ngày. Một kết quả bình thường trên CMR đã cho thấy tiên lượng tốt bất kể triệu chứng hay các phát hiện khác. Tất cả 10 biến cố tim bất lợi lớn (7 trường hợp tử vong do tim, 1 trường hợp đột tử do tim được cứu sống và 2 trường hợp sốc khử rung tim do (ICD) phù hợp đã xảy ra ở những bệnh nhân có kết quả bất thường về CMR. Tuy nhiên, chính xác những bệnh nhân nào nên được đề nghị phòng ngừa tiên phát chống lại chứng loạn nhịp thất bằng ICD vẫn còn không có kết luận gì ngoài các khuyến nghị hiện tại đối với bệnh cơ tim giãn; đây là một lĩnh vực quan trọng khi dữ liệu đang còn thiếu.
Viêm màng ngoài tim
Viêm màng ngoài tim cấp tính là một chẩn đoán lâm sàng được thực hiện bằng sự hiện diện của ít nhất 2 trong 3 tình trạng sau: đau ngực điển hình, tiếng cọ màng ngoài tim và ST chênh lên lan rộng; tỷ lệ mắc ước tính là 27,7 trên 100.000 ở châu Âu. [38] Mức độ cao của các dấu hiệu viêm được tìm thấy trong phần lớn [39] kèm theo các dấu hiệu bình thường của tổn thương cơ tim. Một trường hợp mẫu bao gồm tiền triệu nhiễm siêu vi gần đây; đau ngực dữ dội nặng hơn khi hít thở sâu, ho, hoặc khi nằm thẳng; và một ECG với chênh lên của ST hình yên ngựa toàn bộ cũng như đoạn PR chênh xuống (một phát hiện đặc hiệu trong viêm màng ngoài tim). Sự khác biệt với viêm cơ tim nằm ở chẩn đoán viêm màng ngoài tim cùng với việc chứng minh tổn thương cơ tim bằng cách sử dụng các dấu hiệu đặc biệt của tổn thương cơ tim mà không có chức năng thất trái suy giảm khu trú. Trong trường hợp này, viêm màng ngoài tim được cho là dẫn đến tham gia của cơ tim thứ phát bị hạn chế (được tìm thấy trong khoảng 15% trong một đoàn hệ quan sát bao gồm 274 trường hợp viêm màng ngoài tim nguyên phát hoặc virus, và 32% trong một đoàn hệ nhỏ hơn) .[38, 40] Viêm cơ tim được phân biệt với viêm màng ngoài tim do rối loạn chức năng cơ tim khu trú trong viêm màng ngoài tim là một hội chứng cơ tim chiếm ưu thế. [41]
Bệnh căn
Viêm màng ngoài tim do virus là nguyên nhân phổ biến nhất trong nhiều nguyên nhân, [42] nhưng thật không may, nó có thể là một chẩn đoán khó thực hiện, với rất nhiều trường hợp được đặt trong một thể loại nguyên phát hoặc virus, bao gồm cả trong y văn. Một nghiên cứu đã sử dụng điều tra huyết thanh học rộng rãi trong nhóm này và thấy rằng nó không chỉ vô ích về mặt chẩn đoán mà còn vô ích về mặt điều trị. [43] Một nhóm virus tương tự, đặc biệt là coxsackieviruses, bệnh căn trong viêm cơ tim xuất hiện trở lại là thủ phạm trong các trường hợp viêm màng ngoài tim; điều này bao gồm các virus torque teno và virut papilloma được xác định gần đây thông qua phân tích metagenome của dịch màng ngoài tim từ các bệnh nhân bị ảnh hưởng. [44] Viêm cơ tim do virus tái phát được cho là có cơ sở chủ yếu tự miễn dịch, thông qua kích hoạt cả hệ thống miễn dịch bẩm sinh và thích nghi và thông qua việc giải phóng cytokine sau đó. Tăng nồng độ interleukin-6 và yếu tố hoại tử khối u (tumor necrosis factor: TNF) -a với nồng độ IFN-g thấp phân tích dịch màng ngoài tim so với giá trị huyết thanh đã được tìm thấy trong một nghiên cứu trên bệnh nhân có quá trình viêm màng ngoài tim. Mẫu cytokine có nồng độ TNF-a cao và mức độ biến đổi yếu tố tăng trưởng thấp b1 là dấu hiệu cho bệnh nhân viêm màng ngoài tim do virus cho thấy một cơ chế viêm duy nhất. [46]
Vai trò của hình ảnh học (cộng hưởng từ tim và chụp cắt lớp vi tính)
Hình ảnh trong viêm màng ngoài tim có thể mang lại kết quả khác nhau, không có bất thường đáng kể nào có thể tìm thấy bất kể phương thức được sử dụng; do đó viêm màng ngoài tim vẫn là một chẩn đoán lâm sàng. Tuy nhiên, siêu âm tim là một hình ảnh ban đầu hữu ích cho tràn dịch và sinh lý liên quan thông qua đánh giá RV tâm trương và Doppler qua van hai lá và ba lá cộng với đánh giá các biến chứng hiếm gặp của co thắt hạn chế. Tuy nhiên, độ sáng của màng ngoài tim vẫn chủ quan và là một công cụ không chính xác để xác định viêm màng ngoài tim và đánh giá chính xác độ dày màng ngoài tim là không đáng tin cậy. Do đó trong viêm màng ngoài tim không biến chứng có hoặc không có tràn dịch, siêu âm tim là thích hợp. Hình ảnh chuyên dụng với CMR cho phép đặc tính màng ngoài tim với các chuỗi viêm (như chuỗi STIR T2 có trọng lượng) và hình ảnh gadolinium muộn để gia tăng màng ngoài tim (Hình 2) cũng như đánh giá độ dày và tràn dịch màng ngoài tim (sử dụng các chuỗi cơ bản như trạng thái ổn định tiến triển tự do) và tác dụng huyết động của co thắt màng ngoài tim có thể (chuỗi thở tự do). Chụp cắt lớp vi tính tim (CT) cũng là một công cụ hình ảnh có giá trị trong đánh giá bệnh màng ngoài tim với đánh giá chính xác về độ dày màng ngoài tim, vôi hóa và tràn dịch và lợi ích bổ sung của kế hoạch trước phẫu thuật cộng với phân định giải phẫu mạch vành.[47] CT tim hồi cứu có thể cũng được sử dụng cho sự mở rộng trong đánh giá ảnh hưởng lý học của huyết động học bất lợi. Những nhược điểm rõ ràng là liều bức xạ ion hóa và thiếu hình ảnh viêm chuyên dụng. [48]
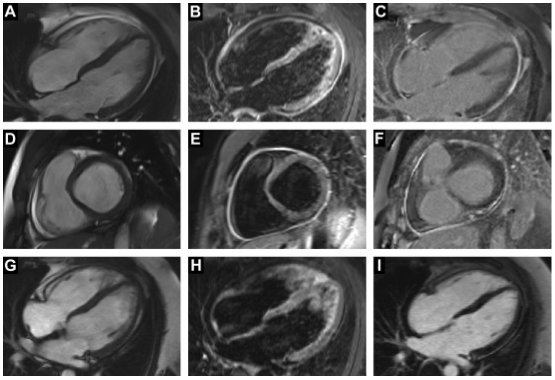
Hình 2. Chẩn đoán hình ảnh CMR từ bệnh nhân trong giai đoạn viêm màng ngoài tim cấp tính và hình ảnh tiếp theo sau khi các đợt được giải quyết. Hai hàng trên cùng (A-F) hiển thị hình ảnh CMR chẩn đoán viêm màng ngoài tim cấp tính (không có sự tham gia của cơ tim). Hàng dưới cùng (G – I) hiển thị hình ảnh CMR từ cùng một bệnh nhân sau khi các đợt được giải quyết. Các hàng trên cùng và dưới cùng thể hiện chế độ xem HLA (tương đương 4 buồng) và hàng giữa là một lát trục ngắn ở nền. Trong mỗi loạt, cột đầu tiên là hình ảnh SSFP (đối với hình ảnh cine). Màng ngoài tim có màu sẫm và có thể nhìn thấy một vành nhỏ của dịch màng tim sáng. Cột giữa là hình ảnh STIR để phát hiện viêm hoặc phù. Toàn bộ màng ngoài tim sáng trong các hình ảnh trong giai đoạn cấp tính cho thấy viêm. Tín hiệu này đã được bình thường hóa trong các hình ảnh thấp hơn xác nhận giải quyết tình trạng viêm. Tăng cường gadolinium muộn (LGE) của màng ngoài tim rõ ràng trong cột thứ ba trong giai đoạn cấp tính (2 hình ảnh trên cùng), nhưng không phải sau khi giải quyết viêm (hình ảnh dưới cùng). Độ dày của màng ngoài tim có vẻ lớn hơn một chút trong giai đoạn cấp tính so với theo dõi khi tình trạng viêm đã được giải quyết.
Khi có triệu chứng cấp và bán cấp của suy tim trơ với điều trị thuốc, phát triển rối loạn nhịp được cấu thành, suy tim với viêm cơ tim bạch cầu ai toan, nghi ngờ tế bào lớn, hoặc bệnh sử bệnh mạch máu liên kết collagen sinh thiết nội cơ tim nên được xem xét.[38]
Điều chỉnh viêm màng ngoài và các biến chứng
Tóm lại, việc điều trị lâm sàng viêm màng ngoài tim có thể gặp khó khăn với viêm màng ngoài tim tái phát, một đặc điểm ở gần một phần ba số bệnh nhân. [49,50] Những người bị viêm màng ngoài tim tái phát có xu hướng lành tính hơn với ít biến chứng khi tái phát. [51] Điều trị tối ưu bằng thuốc chống viêm không steroid liều đầy đủ trong khoảng 7 ngày (tối đa 6 tuần) hoặc cho đến khi giải quyết triệu chứng với liều giảm dần sau đó (khung 2). Việc bổ sung colchicine đã được tìm thấy để làm giảm đáng kể tỷ lệ tái phát viêm màng ngoài tim từ 32,3% xuống còn 10,7% trong một thử nghiệm ngẫu nhiên có triển vọng lớn, mặc dù đã ngừng 8% vì tiêu chảy. [50] Steroid có liên quan đến tái phát [50] và thường được bảo lưu để kháng và các trường hợp tái phát hoặc trong một số trường hợp bệnh lao có tràn dịch liên quan. [52,53] Cũng như viêm cơ tim, việc ngừng hoạt động thể lực cũng được khuyên ngừng trong 6 tháng. [54]
Hai thử nghiệm Colchicine trong dự phòng Hội chứng lấy bỏ màng ngoài tim sau phẫu thuật (The Colchicine for the Prevention of the Postpericardiotomy Syndrome: COPPS) của Imazio và cộng sự [55] đã điều tra việc giảm rung nhĩ sau phẫu thuật (AF) cũng như hội chứng sau phẫu thuật cắt bỏ màng ngoài tim và tràn dịch màng phổi và tràn dịch màng tim. Các nhà điều tra không tìm thấy giảm AF sau phẫu thuật hoặc tràn dịch nhưng giảm có ý nghĩa hội chứng cắt bỏ màng ngoài tim sau phẫu thuật trong một phân tích điều trị tích cực. Đáng chú ý, có nhóm tác dụng phụ đường tiêu hóa đáng kể trong nhóm điều trị (20% bệnh nhân) và khi phân tích điều trị được thực hiện, thực sự đã giảm AF. [55]
Viêm màng ngoài tim hạn chế là một biến chứng hiếm gặp của viêm màng ngoài tim do virus hoặc nguyên phát. Các nguyên nhân khác gây ra viêm màng ngoài tim như bệnh lao, tân sinh và nguyên nhân có liên quan đến nguy cơ co thắt tăng đáng kể (được phát hiện là 0,76 trường hợp trong 1000 năm đối với viêm màng ngoài tim do virus vô căn so với 52,74 trường hợp trên 1000 năm đối với viêm màng ngoài tim theo dõi 72 tháng của 500 bệnh nhân). [56]
Điện tâm đồ trong viêm màng ngoài tim và viêm cơ tim màng ngoài tim
Kết quả điện tâm đồ ở bệnh nhân viêm cơ tim màng ngoài tim (perimyocarditis) có xu hướng rõ ràng hơn so với bệnh nhân chỉ bị viêm màng ngoài tim cơ tim (myopericarditis) và phát triển như tiến triển của bệnh. Các giai đoạn tiến triển được mô tả như sau: giai đoạn 1 liên quan đến ST chênh lên và sóng T thẳng đứng thường thoái lui về bình thường (giai đoạn II) trong vài ngày hoặc phát triển thêm thành đảo ngược sóng T (giai đoạn III) và cuối cùng là bình thường hoặc có khả năng sóng T đảo ngược cố định (giai đoạn IV). [57] Cũng có thể có chênh lên của đoạn PR ở aVR cho thấy dòng tổn thương tâm nhĩ. [58,59] Viêm cơ tim có thể dẫn đến thay đổi phân đoạn ST khu vực giả nhồi máu cấp tính trước khi bình thường hóa. [38] ECG biểu hiện khởi đầu ST chênh lên hình dép sang dan đảo ngược (sandal back) có thể bị nhầm lẫn với tái cực sớm và phì đại LV với tái cực sớm. Tỷ lệ chiều cao của điểm nối đoạn ST so với chiều cao của đỉnh sóng T hơn 0,25 cho thấy viêm màng ngoài tim, [60] một cách đặc biệt ở chuyển đạo I, V4, V5 và V6, với chuyển đạo I cung cấp giá trị tiên đoán tối ưu trong một loạt 80 bệnh nhân. [61]
| Khung 2
Chẩn đoán và xử trí viêm màng ngoài tim – Chẩn đoán dựa trên sự hiện diện của 2 trong số những điều sau đây: đau ngực điển hình, tiếng cọ màng ngoài tim và ST chênh lên lan rộng. – Làm sáng tỏ nguyên nhân cơ bản có thể là vô ích và không cần thiết trong các trường hợp không biến chứng. – Viêm màng ngoài tim là một chẩn đoán lâm sàng, nhưng hình ảnh có thể giúp và đặc biệt là đánh giá các biến chứng. CMR cung cấp đặc tính mô vượt trội. – Xử trí dựa trên sự kết hợp của một loại thuốc chống viêm như NSAID và colchicine. Tên viết tắt: NSAID, thuốc chống viêm không steroid. |
Các nghiên cứu bệnh học và sau tử vong trong viêm màng ngoài tim và viêm cơ tim màng ngoài tim
Dữ liệu bệnh lý từ những năm 1960 ban đầu đã chứng minh sự liên quan của nút xoang, vì sự gần gũi của nó với màng ngoài tim, trong các mẫu viêm màng ngoài tim, [62] chỉ sau đó đã trở nên không đúng trong một loạt lớn hơn. [63]
Tại Croatia, trong khoảng thời gian 10 năm kể từ năm 1998, đã có 4 trường hợp đột tử bất ngờ vì viêm cơ tim trong hoặc sau khi gắng sức. Tỷ lệ tử vong ở vận động viên là 0,15 trên 100.000 so với 0,75 trên 100.000 ở tất cả nam giới gắng sức và bị viêm cơ tim màng ngoài tim (P = 0,0014). Thông tin chi tiết về rối loạn nhịp tim còn hạn chế, nhưng 1 bệnh nhân có các nhắt bóp thất sớm trong khi tập luyện. [44]
Rối loạn nhịp trong thông báo trường hợp viêm màng ngoài tim do virus
Tim kiếm trên PubMed về các báo cáo trường hợp viêm màng ngoài tim và rối loạn nhịp tim từ khi bắt đầu sử dụng hồ sơ điện tử đến tháng 1 năm 2015 mang lại rất ít trong cách ghi nhận rối loạn nhịp tim trong viêm màng ngoài tim do virus chuyên biệt. [64 – 67] Một trường hợp viêm cơ tim màng ngoài tim từ 1976 chứng minh ngừng tim do VF ở em bé 12 tuổi đã được khẳng định do coxsackievirus dường như là viêm màng ngoài tim cơ tim chiếm ưu thế, không có tiếng cọ màng ngoài tim nào được nghe thấy nhưng tim to đáng kể trên X – Ray một cách ngắn ngủi sau hồi sức và tràn dịch ít một tháng sau biểu hiện. [68] Trường hợp khác được thông báo bệnh nhân bị nhịp xoang chậm 35 chu kỳ / phút với bệnh nguyên phát, cho rằng do virus, viêm màng ngoài tim được chẩn đoán trên cơ sở đau ngực, tiếng cọ màng ngoài tim, đoạn ST hình vòm. [69] Các khám phá khác ở bệnh nhân này gồm kết quả chụp mạch vành bình thường, nhịp chậm được thoái lui trong vài giờ và được cho do đáp ứng phế vị do đau ngực. Quan sát này thực sự trái ngược với nhịp xoang nhanh chiếm ưu thế được mô có biểu hiện, tại một thời điểm chỉ được điều trị bằng ép xoang cảnh. [70] Gần đây, tầm quan trọng của thuốc giảm đau tim đã được nâng lên mặc dù không có dữ liệu lâm sàng trong viêm màng ngoài tim, nhưng với kết quả bất lợi trong viêm cơ tim được quản lý mà không có thuốc giảm đau. [71] Roubille và cộng sự [72] đưa ra giả thuyết việc nghỉ ngơi do thuốc có thể sẽ làm giảm viêm và do đó hạn chế tác hại trong viêm màng ngoài tim; tuy nhiên, bằng chứng lâm sàng vẫn còn hạn chế chỉ có mối tương quan giữa tần số tim nhập viện và mức CRP xuất viện. [73]
Các nghiên cứu theo dõi gánh nặng rối loạn nhịp trong viêm màng ngoài tim
Dữ liệu Holter năm 1984 ở 49 bệnh nhân được chẩn đoán viêm màng ngoài tim, thông qua tiếng cọ màng ngoài tim và thay đổi điện tâm đồ điển hình, và nhịp xoang tại thời điểm chẩn đoán cho thấy tỷ lệ rối loạn nhịp tim thấp so với nhồi máu cấp tính. [74] Ngoại tâm thu đơn độc là rối loạn nhịp thất duy nhất được công nhận, chỉ có 4 trường hợp rối loạn nhịp trên thất ở bệnh nhân không có tiền sử bệnh tim. Ở những bệnh nhân có tiền sử (n = 29), trong đó có 21 người bị nhồi máu cấp và viêm màng ngoài tim kiểu Dressler, 3 người bị VT tạm thời, 3 người bị rối loạn nhịp nhĩ, 1 người bị rung nhĩ, 1 người bị loạn nhịp nhĩ ngoại vị, 1 người bị loạn nhịp nhanh trên thất (SVT) và 1 có block nhĩ thất không liên tục (AV). [74] Một nghiên cứu tiếp theo vào năm 1986 đã báo cáo trên 31 bệnh nhân bị viêm màng ngoài tim (24 người trong số họ bị viêm màng ngoài tim nguyên phát) và phát hiện 1 bệnh nhân bị rung nhĩ (AF) và 1 SVT theo dõi đến 19 năm. [49]
Bệnh nhân bị viêm cơ tim đã được phát hiện có nhiều rối loạn nhịp tim hơn so với những người bị viêm màng ngoài tim đơn thuần. Trong một nghiên cứu quan sát, trong số những bệnh nhân bị viêm màng ngoài tim cấp tính, 7,7% (n = 234) đã phát triển AF, 9% một rối loạn nhịp thất khác , trong khi ở những bệnh nhân bị viêm cơ tim, 2,5% (n = 40) phát triển AF, 17,5% một rối loạn nhịp trên thất khác, rối loạn nhịp thất 40% và block AV 5%. Nhìn chung, 65% bệnh nhân bị viêm cơ tim phát triển rối loạn nhịp tim. [38]
Theo dõi bệnh nhân hồi cứu 37 tháng trên phổ bệnh viêm màng ngoài tim thuần túy đến viêm cơ tim đơn thuần (với phần lớn bị viêm màng ngoài tim chiếm ưu thế) không xác nhận tử vong. Rối loạn nhịp tim không được báo cáo cụ thể. [75] Imazio và cộng sự [76] đã nghiên cứu 300 trường hợp với thời gian theo dõi tương tự 38 tháng và chia chúng thành một nhóm có nguy cơ thấp và nhóm có nguy cơ cao được bảo đảm điều tra và quản lý tại bệnh viện. Nhóm có nguy cơ cao (trong đó 22% có nguyên nhân do virus / nguyên phát) được cho là khởi phát bán cấp, ức chế miễn dịch, chấn thương, điều trị chống đông máu, tràn dịch màng ngoài tim nặng, tamponade, hoặc bằng chứng viêm màng ngoài tim. Nhóm có nguy cơ thấp (84,7%, trong đó 91% có nguyên nhân do virus / nguyên phát) được cho là có một ngày điều tra cơ bản gồm ECG và siêu âm tim và sau đó được xuất viện để theo dõi tại phòng khám. Một lần nữa, mặc dù rối loạn nhịp tim không được ghi nhận cụ thể, không có trường hợp tử vong ở một trong hai nhóm với tỷ lệ mắc bệnh khách quan là co thắt. [76]
Imazio và cộng sự [77] trong một nghiên cứu đoàn hệ khác với 486 bệnh nhân trong thời gian theo dõi trung bình 36 tháng đã chia bệnh nhân thành những người bị viêm màng ngoài tim cơ tim (23%), viêm cơ tim màng ngoài tim (5%) và viêm màng ngoài tim đơn thuần (71%). Các nhà nghiên cứu đã tìm thấy một sự khác biệt có ý nghĩa thống kê về rối loạn nhịp thất giữa 4,4% và 7,7% những người bị màng ngoài tim cơ tim và viêm cơ tim màng ngoài tim, theo thứ tự, và chỉ 0,3% những người bị viêm màng ngoài tim đơn thuần. Rối loạn nhịp thất được tìm thấy ở 8,8% và 19,2% những người bị viêm màng ngoài tim cơ tim và viêm cơ tim màng ngoài tim, và chỉ 5,8% những người bị viêm màng ngoài tim thuần túy (không có ý nghĩa thống kê). Không có block AV được chứng minh. Trong tổng số đoàn hệ, 84,8% được coi là có nguyên nhân nguyên phát và chỉ 4,5% được coi là có khả năng nhiễm trùng (gồm đánh giá coxsackievirus, virus Epstein Barr, parvovirus, adenovirus, cytomegalovirus và cúm). Bệnh nhân được khuyên chống lại các môn thể thao cạnh tranh, nghiệp dư hoặc giải trí trong 3 tháng với viêm màng ngoài tim và 6 tháng với các tổn thương khác. Không có trường hợp tử vong trong tổng số theo dõi với rối loạn chức năng LV nhẹ tồn dư ở 8% bệnh nhân bị viêm màng ngoài tim cơ tim và 15% trong số những người bị viêm cơ tim màng ngoài tim. Đáng chú ý, nồng độ CRP cao hơn ở những bệnh nhân bị viêm màng ngoài tim đơn thuần, và sự tăng nhiệt độ có liên quan đến mức độ liên quan đến viêm màng ngoài tim cơ tim và viêm cơ tim màng ngoài tim, mặc dù được biết đó không phải là một chỉ số tiên lượng. [40] Quản lý rối loạn nhịp tim không được chỉ định; tuy nhiên, hầu hết bệnh nhân có liên quan đến cơ tim được điều trị bằng thuốc chẹn beta, có thể là do suy LV chứ không phải do kiểm soát nhịp.
Xác định rối loạn nhịp trong viêm màng ngoài tim đối lại với viêm màng ngoài tim cơ tim
Một nghiên cứu tìm cách xác định rối loạn nhịp tim ở bệnh nhân viêm màng ngoài tim cấp tính chia bệnh nhân thành những người có bằng chứng đã được chứng minh bằng sinh thiết nội mạc cơ tim của viêm cơ tim (viêm cơ tim màng ngoài tim và viêm màng ngoài tim cơ tim, n = 10) và những người không có bằng chứng (n = 40) [78]; 6 đến 9 mẫu được lấy từ cả hai tâm thất để giảm thiểu lỗi lấy mẫu, nhưng đây vẫn là một khả năng. Các nhà điều tra phát hiện ra rối loạn nhịp trên thất, VF và AF xảy ra lần lượt ở 40%, 20% và 0% ở những bệnh nhân bị viêm cơ tim và viêm màng ngoài tim so với 5%, 0% và 20% theo thứ tự, ở những người bị viêm màng ngoài tim đơn thuần. Người ta cũng phát hiện ra 1 bệnh nhân đã tử vong do VF và 2 bệnh nhân được cấy ICD trong nhóm viêm cơ tim và viêm cơ tim màng ngoài tim. Không có sự khác biệt được tìm thấy trong block AV giữa các nhóm, với cả hai đều thể hiện mức độ thấp. Trong số 40 bệnh nhân chỉ bị viêm màng ngoài tim, 12,5% đã xác nhận viêm màng ngoài do virus sau khi sinh thiết màng tim và phân tích tràn dịch virus bằng PCR, nhưng không có dữ liệu cụ thể nào được trình bày trong nhóm này. Ngoài ra, dữ liệu hạn chế được trình bày trên nhóm với bằng chứng đã được chứng minh bằng sinh thiết về viêm cơ tim mà không có thêm thông tin chi tiết về các bệnh nhân cấy ICD hoặc VF.
Một nghiên cứu gần đây tập trung vào điều trị VT thượng tâm mạc đã tìm cách giải quyết khó khăn trong việc tiếp cận ở những bệnh nhân bị viêm màng ngoài tim trước đó và phẫu thuật tim không phải mạch vành với VT tái phát. [79]
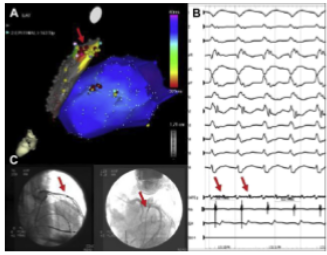
Hình 3. Hình ảnh có thể nhìn thầy việc triệt phá VT thượng tâm mạc. (A) Bản đồ kích hoạt thượng tâm mạc và nội tâm mạc từ một người đàn ông 48 tuổi bị viêm màng ngoài tim. Mũi tên màu đỏ cho thấy kích hoạt VT sớm nhất trên biểu mô LV. (B) Điện đồ giữa tâm trương (mũi tên đỏ) được xác định tại vị trí được thể hiện trong bảng A. Đáp ứng lắp đi lắp lại hoàn hảo với tạo nhịp đã được thể hiện tại vị trí này (không hiển thị). (C) Chụp mạch cine xác nhận vị trí catheter ra khỏi giải phẫu mạch vành (mũi tên đỏ) tại vị trí cho thấy điện thế giữa tâm trương. Triệt phá tại địa điểm này đã chấm dứt thành công VT. (Theo Tschabrun CM, Haggani HM, Cooper JM, và cộng sự. Triệt phá qua da nhịp nhanh thất thượng tâm mạc sau ngoại khoa tim không phải mạch vành hoặc viêm màng ngoài tim. Heart Rhythm 2013; 10:168)
Những bệnh nhân có nền ngoại tâm mạc rõ ràng trên hình ảnh, những người có hình thái VT thượng tâm mạc trên ECG 12 đạo trình của họ, và những người đẫ thất bại trong triệt phá VT nội tâm được đưa vào để thử tiếp cận vùng thượng tâm mạc. Sau đó, chọc qua da được thực hiện từ phương pháp dưới mũi ức (subxiphoid) bằng cách sử dụng một hướng dẫn để theo dõi tim, bằng cách tiêm thuốc cản quang nếu điều này thất bại, để chứng minh sự kết dính. Sau đó, catheter điều chỉnh để phân chia các phần này trước khi lập bản đồ (mapping) giải phẫu điện học (Hình 3). Trong nghiên cứu đơn trung tâm này, trong khoảng thời gian 10 năm, 10 bệnh nhân được phẫu thuật tim không phải mạch vành trước đó hoặc viêm màng ngoài tim (n = 2) và VT tái phát với nhu cầu tiếp cận vùng thượng tâm mạc đã được tuyển chọn. Trong số 2 bệnh nhân bị viêm màng ngoài tim, một người bị bão VT và người kia bị VT, và cả hai đều có khả năng tiếp cận màng ngoài tim thành công nhưng một người bị thủng RV. Bóc tách catheter đầu tù cho phép phá vỡ sự kết dính và lập bản đồ thành công ở vùng mục tiêu ở tất cả trừ 1 bệnh nhân, trong đó độ bám dính tỏ ra quá mạnh mặc dù cửa sổ màng ngoài tim phẫu thuật ngẫu nhiên. Trong số 10 bệnh nhân, 8 bệnh nhân không bị rối loạn nhịp tim khi kết thúc quá trình triệt phá. Trong 1 bệnh nhân không đạt được điều này, có 30 tổn thương triệt phá sau khi lập bản đồ, nhưng rối loạn nhịp tim vẫn không được tạo ra. Sau 13 tháng theo dõi, 50% thoát khỏi VT.
Có bằng chứng rõ ràng viêm màng ngoài tim cơ tim và viêm cơ tim màng ngoài tim mang gánh nặng rối loạn nhịp tim cao hơn so với viêm màng ngoài tim đơn thuần. Về mặt lâm sàng, vẫn có trách nhiệm xác định rối loạn nhịp tim trong đoàn hệ này, [80] đặc biệt nếu VF đã được mô tả tới 20% trong 1 nghiên cứu nhỏ, [78] mặc dù con số ở nơi khác có vẻ thấp hơn nhiều. AF và rối loạn nhịp trên thất dường như là những phát hiện phổ biến nhất trong viêm màng ngoài tim đơn thuần (khung 3), với các trường hợp rối loạn nhịp thất hiếm gặp được mô tả trong y văn. Do sự không thường xuyên của rối loạn nhịp trên thất thường trong nhóm này, không có thử nghiệm nào về quản lý viêm màng ngoài tim do virus, mặc dù ngoại suy từ các nguyên nhân khác của viêm màng ngoài tim có thể được phỏng đoán. [81] Trong một số trường hợp đã được mô tả trong tài liệu, block AV và VT thượng tâm mạc cả hai đặc tính.
Tóm tắt và thảo luận
Các tài liệu liên quan đến cơ chế rối loạn nhịp tim trong viêm cơ tim do virus và viêm màng ngoài tim vẫn còn hạn chế với sự hiểu biết không đầy đủ về các tình trạng này. Cụ thể, các cơ chế chính xác rối loạn nhịp thất xảy ra trong viêm cơ tim và viêm màng ngoài tim chưa được biết. Dường như một số yếu tố di truyền ảnh hưởng và / hoặc xác định di chứng của nhiễm virus cơ tim, bao gồm cả sự phát triển của rối loạn nhịp tim. Các nguyên tắc quản lý rộng vẫn tập trung vào rối loạn nhịp cụ thể và đặc biệt là tác động lâm sàng của nó và tuân theo các hướng dẫn đã được công bố. [82] Sự kết hợp với các bệnh kênh hỗ trợ thăm dò chất nền rối loạn nhịp tim ở bệnh nhân viêm cơ tim cấp có biến chứng VF. Sức mạnh của CMR để xác định viêm cơ tim và xơ hóa cơ tim và cũng cung cấp định lượng chính xác thể tích và chức năng của tâm thất hỗ trợ tăng cường sử dụng kỹ thuật này một cách mạnh mẽ và ngày càng có sẵn trong trạng thái này. Sự kết hợp của hình ảnh như vậy với sự tin cậy sinh học và đặc biệt là phân tích di truyền sẽ tăng cường sự hiểu biết về tình trạng này và đặc biệt là quá trình biến đổi bệnh giữa các cá nhân. Ngoài ra, cần có nhiều nghiên cứu khoa học cơ bản và sinh học phân tử để tăng cường sự hiểu biết cực kỳ hạn chế về cơ sở điện của rối loạn nhịp tim trong tình trạng này. Điều quan trọng nhất của việc này là xác định rõ hơn những người có nguy cơ đột tử do tim do viêm cơ tim cấp tính do virus, cũng như xác định những người có khả năng nhiều nhất bị bệnh cơ tim giãn. Các thử nghiệm bổ sung để đánh giá khả năng can thiệp dược lý để loại bỏ hoặc hạn chế sự phát triển của cả rối loạn nhịp tim và bệnh cơ tim giãn là rất cần thiết.
| Khung 3
Rối loạn nhịp tim trong viêm màng ngoài tim do virus – Có dữ liệu hạn chế về phân nhóm viêm màng ngoài tim do virus – Hầu hết các dữ liệu đến từ việc theo dõi các đoàn hệ lớn của viêm màng ngoài tim căn nguyên hỗn hợp – Có một tỷ lệ thấp của rối loạn nhịp thất đặc biệt ở bệnh nhân viêm màng ngoài tim nói chung – Rối loạn nhịp trên thất là gánh nặng lớn nhất ở bệnh nhân viêm màng ngoài tim đơn thuần. |
Tài liệu tham khảo
- Sagar S, Liu PP, Cooper LT Jr. Myocarditis. Lancet 2012; 379:738–47.
- Fabre A, Sheppard MN. Sudden adult death syndrome and other non-ischaemic causes of sudden cardiac death. Heart 2006;92(3):316–20.
- Doolan A, Semsarian C, Langlois N. Causes of sudden cardiac death in young Australians. Med J Aust 2004;180(3):110–2.
- Gru¨n S, Schumm J, Greulich S, et al. Long-term follow-up of biopsy-proven viral myocarditis: predictors of mortality and incomplete recovery. J Am Coll Cardiol 2012; 59:1604–15.
- Shauer A, Gotsman I, Keren A, et al. Acute viral myocarditis: current concepts in diagnosis and treatment. Isr Med Assoc J 2013; 15:180–5.
- Bowles NE, Ni J, Kearney DL, et al. Detection of viruses in myocardial tissues by polymerase chain reaction. Evidence of adenovirus as a common cause of myocarditis in children and adults. J Am Coll Cardiol 2003; 42:466–72.
- Bock CT, Klingel K, Kandolf R. Human parvovirus B19-associated myocarditis. N Engl J Med 2010; 362:1248–9.
- Phillips MP, Robinowitz M, Higgins JR, et al. Sudden cardiac death in Air Force recruits. JAMA 1986;256: 2696–9.
- Mason JW, Trehan S, Renlund DG. Myocarditis. In: Willerson JT, Cohn JN, Wellens HJ, et al, editors. Cardiovascular medicine. 3rd edition. London: Springer; 2007. p. 1314–47. 1
- Li HS, Ligons DL, Rose NR. Genetic complexity of autoimmune myocarditis. Autoimmun Rev 2008; 7(3):168–73.
- Kawai C. From myocarditis to cardiomyopathy: mechanisms of inflammation and cell death. Learning from the past for the future. Circulation 1999; 99:1091–100.
- D’Ambrosio A, Patti G, Manzoli A, et al. The fate of acute myocarditis between spontaneous improvement and evolution to dilated cardiomyopathy: a review. Heart 2001; 85:499–504.
- Kuhl U, Pauschinger M, Noutsias M, et al. High prevalence of viral genomes and multiple viral infections in the myocardium of adults with “idiopathic” left ventricular dysfunction. Circulation 2005;111:887–93.
- Ku¨hl U, Pauschinger M, Seeberg B, et al. Viral persistence in the myocardium is associated with progressive cardiac dysfunction. Circulation 2005; 112:1965–70.
- Hershberger RE, Hedges DJ, Morales A. Dilated cardiomyopathy: the complexity of a diverse genetic architecture. Nat Rev Cardiol 2013;10(9):531–47.
- Roberts AM, Ware JS, Herman DS, et al. Integrated allelic, transcriptional, and phenotypic dissection of the cardiac effects of titin truncations in health and disease. Sci Transl Med 2015;7(270):270.
- Andreoletti L, Leveque N, Boulagnon C, et al. Viral causes of human myocarditis. Arch Cardiovasc Dis 2009;102(6–7):559–68.
- Bezzina CR, Pazoki R, Bardai A, et al. Genome-wide association study identifies a susceptibility locus at 21q21 for ventricular fibrillation in acute myocardial infarction. Nat Genet 2010;42(8):688–91.
- Punja M, Mark DG, McCoy JV, et al. Electrocardiographic manifestations of cardiac infectiousinflammatory disorders. Am J Emerg Med 2010;28: 364–77.
- Smith SC, Ladenson JH, Mason JW, et al. Elevations of cardiac troponin I associated with myocarditis. Experimental and clinical correlates. Circulation 1997;95:163–8.
- Guo JG. Detection of cardiac troponin and highsensitivity C reactive protein in children with viral myocarditis. Na Fang Yi ke Da Xue Xue Bao 2008; 28(6):1076–7.
- Pieroni M, Smaldone C, Bellocci F. Myocarditis presenting with ventricular arrhythmias: role of electroanatomical mapping-guided endomyocardial biopsy in differential diagnosis. In: Cihakova D, editor. Myocarditis. InTech; 2011. p. 365–86. http://dx.doi.org/10. 5772/22123. ISBN: 978-953-307-289-0. Available at: http://www.intechopen.com/books/myocarditis/myo carditis-presenting-with-ventricular-arrhythmias-roleof-electroanatomical-mapping-guided-endomyo. Accessed March 04, 2015.
- Mahrholdt H, Goedecke C, Wagner A, et al. Cardiovascular magnetic resonance assessment of human myocarditis: a comparison to histology and molecular pathology. Circulation 2004;109:1250–8.
- De Cobelli F, Pieroni M, Esposito A, et al. Delayed gadolinium-enhanced cardiac magnetic resonance in patients with chronic myocarditis presenting with heart failure or recurrent arrhythmias. J Am Coll Cardiol 2006;47:1649–54.
- Saito J, Niwano S, Niwano H, et al. Electrical remodeling of the ventricular myocardium in myocarditis: studies of rat experimental autoimmune myocarditis. Circ J 2002;66:97–103.
- Zhang A, Zhang H, Wu S. Immunomodulation by atorvastatin upregulates expression of gap junction proteins in coxsackievirus B3 (CVB3)-induced myocarditis. Inflamm Res 2010;59(4):255–62.
- Li Y, Ge S, Peng Y, et al. Inflammation and cardiac dysfunction during sepsis, muscular dystrophy, and myocarditis. Burns Trauma 2013;1(3):109–21.
- Thiene G, Basso C. Arrhythmogenic right ventricular cardiomyopathy: an update. Cardiovasc Pathol 2001; 10:109–17.
- Pieroni M, Dello Russo A, Marzo F, et al. High prevalence of myocarditis mimicking arrhythmogenic right ventricular cardiomyopathy differential diagnosis by electroanatomic mapping-guided endomyocardial biopsy. J Am Coll Cardiol 2009;53(8):681–9.
- Salerno F, Girerd N, Chalabreysse L, et al. Myocarditis and cardiac channelopathies: a deadly association? Int J Cardiol 2011;147(3):468–70.
- Buob A, Siaplaouras S, Janzen I, et al. Focal parvovirus B19 myocarditis in a patient with Brugada syndrome. Cardiol Rev 2003;11(1):45–9.
- Frustaci A, Priori SG, Pieroni M, et al. Cardiac histological substrate in patients with clinical phenotype of Brugada syndrome. Circulation 2005; 112:3680 –7.
- McMurray JJ, Adamopoulos S, Anker SD, et al. ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012. Eur Heart J 2012;33: 1787–847.
- Pelliccia A, Corrado D, Bjornstad HH, et al. Recommendations for participation in competitive sport and leisure-time physical activity in individuals with cardiomyopathies, myocarditis and pericarditis. Eur J Cardiovasc Prev Rehabil 2006;13: 876–85.
- Chau EM, Chow WH, Chiu C, et al. Treatment and outcome in biopsy proven fulminant myocarditis in adults. Int J Cardiol 2006;110(3):405–6.
- Gulati A, Jabbour A, Ismail TF, et al. Association of fibrosis with mortality and sudden cardiac death in patients with nonischemic dilated cardiomyopathy. JAMA 2013; 309:896–908.
- Schumm J, Greulich S, Wagner A, et al. Cardiovascular magnetic resonance risk stratification in patients with clinically suspected myocarditis. J Cardiovasc Magn Reson 2014; 16:14.
- Imazio M, Cecchi E, Demichelis B, et al. Myopericarditis versus viral or idiopathic acute pericarditis. Heart 2008; 94:498–501.
- Imazio M, Brucato A, Maestroni S, et al. Prevalence of C-reactive protein elevation and time course of normalisation in acute pericarditis: implications for the diagnosis, therapy, and prognosis of pericarditis. Circulation 2011; 123:1092–7.
- Imazio M, Demichelis B, Cecchi E, et al. Cardiac troponin I in acute pericarditis. J Am Coll Cardiol 2003; 42:2144–8.
- Imazio M, Cooper LT. Management of myopericarditis. Expert Rev Cardiovasc Ther 2013; 11:193–201.
- Oakley CM. Myocarditis, pericarditis and other pericardial diseases. Heart 2000; 84:449–54.
- Abu Fanne R, Banai S, Chorin U, et al. Diagnostic yield of extensive infectious panel testing in acute pericarditis. Cardiology 2011; 119:134–9.
- Fancello L, Monteil S, Popgeorgiev N, et al. Viral communities associated with human pericardial fluids in idiopathic pericarditis. PLoS One 2014;9: e93367.
- Cantarini L, Lopalco G, Selmi C, et al. Autoimmunity and autoinflammation as the yin and yang of idiopathic recurrent acute pericarditis. Autoimmun Rev 2015; 14:90–7.
- Ristic AD, Pankuweit S, Maksimovic R, et al. Pericardial cytokines in neoplastic, autoreactive and viral pericarditis. Heart Fail Rev 2013; 18:345–53.
- Kanaganayagam GS, Ngo AT, Alsafi A, et al. CT coronary angiography in the investigation of chest pain—beyond coronary artery atherosclerosis: a pictorial review. Int J Cardiol 2014; 176:618–29.
- Verhaert D, Gabriel RS, Johnston D, et al. The role of multimodality imaging in the management of pericardial disease. Circ Cardiovasc Imaging 2010;3: 333–43.
- Fowler NO, Harbin AD 3rd. Recurrent acute pericarditis: follow-up study of 31 patients. J Am Coll Cardiol 1986; 7:300–5.
- Imazio M, Bobbio M, Cecchi E, et al. Colchicine in addition to conventional therapy for acute pericarditis: results of the Colchicine for Acute Pericarditis (COPE) trial. Circulation 2005; 112:2012–6.
- Soler-soler J, Sagrista-Sauleda J, PermanyerMiralda G. Relapsing pericarditis. Heart 2004;90: 1364–8.
- Troughton RW, Asher CR, Klein AL. Pericarditis. Lancet 2004; 363:717–27.
- Hakim JG, Ternouth I, Mushangi E, et al. Double blind randomised placebo controlled trial of adjunctive prednisolone in the treatment of effusive tuberculous pericarditis in HIV seropositive patients. Heart 2000; 84:183–8.
- Durakovic Z, Misigoj Durakovic M, Skavic J, et al. Myopericarditis and sudden cardiac death due to physical exercise in male athletes. Coll Anthropol 2008; 32:399–401.
- Imazio M, Brucato A, Ferrazzi P, et al. Colchicine for prevention of postpericardiotomy syndrome and postoperative atrial fibrillation: the COPPS-2 randomised clinical trial. JAMA 2014; 312:1016–23.
- Imazio M, Brucato A, Mestroni S, et al. Risk of constrictive pericarditis after acute pericarditis. Circulation 2011; 124:1270–5.
- Braunwald E, Zipes DP, Libby P, et al. Pericardial diseases. In: Khan MG, editor. Heart disease: a textbook of cardiovascular medicine. 6th edition. Philadelphia: Saunders; 2001. p. 1823–76.
- Spodick DH. Diagnostic electrocardiographic sequences in acute pericarditis. Significance of PR segment and PR vector changes. Circulation 1973; 48:575–80.
- Khandaker MH, Espinosa RE, Nishimura RA, et al. Pericardial disease: diagnosis and management. Mayo Clin Proc 2010; 85:572–93.
- Ginzton LE, Laks MM. The differential diagnosis of acute pericarditis from the normal variant: new electrocardiographic criteria. Circulation 1982; 65:1004–9.
- Bhardwaj R, Berzingi C, Miller C, et al. Differential diagnosis of acute pericarditis from normal variant early repolarisation and left ventricular hypertrophy with early repolarisation: an electrocardiographic study. Am J Med Sci 2013; 345:28–32.
- James TN. Pericarditis and the sinus node. Arch Intern Med 1962; 110:305–11.
- Le Kieffre J, Medvedowsky JL, Thery C. Le node sinusale normale et pathologie. Rueil-Malmaison (France): Sandoz ed; 1979. p. 162.
- Lee WS, Lee KJ, Kwon JE, et al. Acute viral myopericarditis presenting as a transient effusive constrictive pericarditis caused by coinfection with coxsackieviruses A4 and B3. Korean J Intern Med 2012; 27:216–20.
- De A, Myridakis D, Kerrigan M, et al. Varicella myopericaeditis mimicking myocardial infarction in a 17 year old boy. Tex Heart Inst J 2011; 38:288–90
- Morita H, Kitaura Y, Deguchi H, et al. Coxsackie B5 myopericarditis in a young adult—clinical course and endomyocardial biopsy findings. Jpn Circ J 1983; 47:1077–83.
- Biton A, Herman J. Perimyocarditis. Report on an unusual case. Postgrad Med 1989; 85:77–80.
- Ward C. Severe arrhythmias in coxsackievirus B3 myopericarditis. Arch Dis Child 1978; 53:174–6.
- Gosselink AT, Van den Berg MP, Crijns HJ. Acute pericarditis presenting with sinus bradycardia. Int J Cardiol 1997; 60:307–10.
- Dressler W. Sinus tachycardia complicating and outlasting pericarditis. Am Heart J 1966; 72:422–3.
- Kindermann I, Kindermann M, Kandolf R, et al. Predictors of outcome in patients with suspected myocarditis. Circulation 2008; 118:639–48.
- Roubille F, Tournoux F, Roubille C, et al. Management of pericarditis and myocarditis: could heart rate reducing drugs hold a promise? Arch Cardiovasc Dis 2013; 106:672–9.
- Khoueiry Z, Roubille C, Nagot N, et al. Could heart rate play a role in pericardial inflammation? Med Hypotheses 2012; 79:512–5.
- Spodick DH. Frequency of arrhythmias in acute pericarditis determined by Holter monitoring. Am J Cardiol 1984; 53:842–5.
- Leitman M, Tyomkin V, Peleg E, et al. Left ventricular function in acute inflammatory peri-myocardial diseases – new insights and long term follow up. Cardiovasc Ultrasound 2012; 10:42.
- Imazio M, Demichelis B, Parrini I, et al. Day hospital treatment of acute pericarditis: a management program for outpatient therapy. J Am Coll Cardiol 2004; 43:1042–6.
- Imazio M, Brucato A, Barbieri A, et al. Good prognosis for pericarditis with and without myocardial involvement: results from a multicentre, prospective cohort study. Circulation 2013; 128:42–9.
- Ristic AD, Maisch B, Hufnagel G, et al. Arrhythmias in acute pericarditis. An endomyocardial biopsy study. Herz 2000; 25:729–33.
- Tschabrun CM, Haggani HM, Cooper JM, et al. Percutaneous epicardial ventricular tachycardia ablation after non-coronary cardiac surgery or pericarditis. Heart Rhythm 2013; 10:165–9.
- Chevalier P, Scridon A. Ventricular arrhythmias complicating acute myocarditis. E-Journal of the ESC Council for Cardiology Practice 2011;9(26). Available at. http://www.escardio.org/communities/ councils/ccp/e-journal/volume9/Pages/Ventriculararrhythmias-complicating-acute-myocarditis-ChevalierScridon.aspx#. VQ 8lnOFvLr4. Accessed March 04, 2015.
- Imazio M, Brucato A, Ferrazzi P, et al. Colchicine reduced postoperative atrial fibrillation: results of the Colchicine for the Prevention of the Postpericardiotomy Syndrome (COPPS) atrial fibrillation substudy. Circulation 2011; 124:2290–5.
- Caforio AL, Pankuweit S, Arbustini E, et al. Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. Eur Heart J 2013; 34:2636–48.







