1. ĐẠI CƯƠNG
Tỉ lệ hiện mắc tăng huyết áp (THA) đang tăng lên trên thế giới với ước đoán 972 triệu người trưởng thành mắc THA vào năm 2000 và dự đoán tăng lên đến 1,56 tỉ người vào năm 2025.
Mặc dù có nhiều thuốc hạ áp hiệu quả nhưng nhiều bệnh nhân THA vẫn không được kiểm soát huyết áp vì nhiều lý do bao gồm cả điều trị không đầy đủ. Trong số các bệnh nhân THA đang điều trị, tỉ lệ ước đoán bệnh nhân có huyết áp đạt mục tiêu < 140/90 mmHg thay đổi từ 47% đến 84% ở châu Âu và Bắc Mỹ [1]. Hơn nữa, nhiều bệnh nhân tuân thủ điều trị với 3 thuốc hạ áp bao gồm thuốc lợi tiểu với liều tối ưu vẫn không kiểm soát huyết áp gọi là tăng huyết áp kháng trị [2]. Ở Hoa Kỳ, ước đoán tỉ lệ hiện mắc của THA kháng trị thay đổi từ 13% đến 30% bệnh nhân đang điều trị [3],[4]. Các con số này phản ánh một sự thử thách sức khỏe toàn cầu vì huyết áp tăng mỗi 20/10 mmHg thì nguy cơ tử vong tim mạch tăng gấp đôi [5].
Hệ thần kinh giao cảm đóng vai trò quan trọng trong cơ chế bệnh sinh của THA. Các nghiên cứu trước đây đã chứng minh sự hoạt hóa hệ thần kinh giao cảm ở các bệnh nhân THA nguyên phát làm tăng tỉ lệ norepinephrine từ các dây thần kinh giao cảm của thận vào huyết tương [6]-[8]. Tăng dòng giao cảm ly tâm đến thận gây ra sự tăng huyết áp thông qua phóng thích renin, với sự hoạt hóa kế tiếp hệ thống renin-angiotensin-aldosterone, tăng ứ natri ở ống thận và giảm dòng máu thận [9],[10]. Tín hiệu thần kinh hướng tâm từ thận với các kích thích tổn thương thận sẽ kích thích dòng giao cảm từ hệ thần kinh trung ương [11]-[13]. Phẫu thuật cắt giao cảm ngực lưng cho thấy giảm huyết áp ở các bệnh nhân THA trước khi có nhiều điều trị dược lý hiệu quả nhưng liên quan với tỉ lệ tử vong đáng kể [14]. Giả thuyết được đặt ra rằng loại bỏ sự co mạch hệ thống bằng phẫu thuật mở rộng cắt các dây thần kinh giao cảm “áp lực” sẽ làm giảm huyết áp. Các nghiên cứu tiền lâm sàng của hủy thần kinh thận chọn lọc ở các mô hình động vật THA cung cấp các chứng cớ trực tiếp của việc giảm huyết áp, cho thấy tính quan trọng của thần kinh giao cảm động mạch thận trong cơ chế bệnh sinh của THA.
Hủy thần kinh giao cảm động mạch thận qua catheter là một thủ thuật xâm lấn tối thiểu bao gồm sự ứng dụng năng lượng tần số radio lan dọc theo chiều dài động mạch thận để hủy các dây thần kinh nằm bên trong và ở lớp áo ngoài của động mạch thận khi chúng phân bố đến thận. Các kết quả hai năm từ một nghiên cứu đoàn hệ không ngẫu nhiên (Symplicity HTN-1) và một nhóm lớn hơn các bệnh nhân THA kháng trị được điều trị bằng hủy thần kinh giao cảm động mạch thận đã chứng minh làm giảm đáng kể huyết áp tại phòng khám mà không gây ra các biến cố nặng [15],[16]. Các bệnh nhân THA kháng trị trong nghiên cứu Simplicity HTN-2 đáp ứng tất cả các tiêu chuẩn nhận vào về mặt lâm sàng và giải phẫu, được phân ngẫu nhiên vào nhóm hủy thần kinh giao cảm hoặc không hủy thần kinh giao cảm, cả hai nhóm duy trì thuốc hạ áp trong 6 tháng. Kết cục chính, sự thay đổi huyết áp tâm thu (HATT) tại phòng khám sau 6 tháng theo dõi, chứng tỏ sự giảm HATT có ý nghĩa giữa nhóm điều trị và nhóm chứng (33/11 mmHg; p<0,0001) [17]. Sau khi đánh giá kết cục chính, các bệnh nhân trong nhóm chứng được lựa chọn thủ thuật hủy thần kinh giao cảm. Bài báo này trình bày các kết quả 1 năm từ thử nghiệm Simplicity HTN-2 trong đó bao gồm kết quả của các bệnh nhân trong nhóm chứng đổi chéo sang điều trị bằng hủy thần kinh giao cảm sau khi đánh giá kết cục chính.
2. NGHIÊN CỨU SIMPLICITY HTN-2
2.1. PHƯƠNG PHÁP
Simplicity HTN-2 là một thử nghiệm ngẫu nhiên, đa trung tâm được thực hiện tại 24 trung tâm ở châu Âu, Úc và New Zealand. Mục tiêu chính của thử nghiệm là đánh giá hiệu quả và tính an toàn của hủy thần kinh giao cảm động mạch thận qua catheter trong điều trị THA kháng trị. Thử nghiệm được chấp thuận bởi hội đồng y đức tại mỗi trung tâm, tuân theo Tuyên ngôn Helsinki. Tất cả bệnh nhân đều kí vào bản đồng thuận tham gia nghiên cứu.
Các bệnh nhân trưởng thành (18-85 tuổi) THA nguyên phát với HATT ≥ 160 mmHg (≥ 150 mmHg nếu có đái tháo đường típ 2) đủ tiêu chuẩn nhận vào. Các bệnh nhân phải đang điều trị ổn định bằng ít nhất 3 thuốc hạ áp mà không thay đổi trong 2 tuần trước khi tham gia nghiên cứu. Các bệnh nhân bị loại nếu đã can thiệp động mạch thận trước đây, động mạch thận chính có đường kính <4 mm hoặc chiều dài < 20 mm, hoặc bất thường đáng kể về huyết động hoặc giải phẫu động mạch thận. Các tiêu chuẩn loại trừ khác bao gồm suy thận với độ lọc cầu thận ước đoán <45 mL/ph/1,73 m2 da theo công thức MDRD (Modification of Diet in Renal Disease) [18], đái tháo đường típ 1, hẹp van tim, nhồi máu cơ tim, đau thắt ngực không ổn định, hoặc tai biến mạch máu não trong vòng 6 tháng trước.
Tất cả bệnh nhân trải qua thời gian tầm soát 2 tuần trước khi phân nhóm ngẫu nhiên và một lần nữa trước khi theo dõi 6 tháng. Trong thời gian tầm soát, các bệnh nhân được yêu cầu báo cáo việc sử dụng thuốc và ghi chép các trị số huyết áp tại nhà hai lần mỗi ngày. Đo huyết áp ban đầu tại phòng khám và theo dõi bằng máy đo huyết áp tự động Omron HEM-705, và báo cáo trị số trung bình của 3 lần đo. Trước khi phân nhóm ngẫu nhiên, tất cả bệnh nhân được chụp động mạch thận (siêu âm duplex động mạch thận, chụp cắt lớp điện toán, cộng hưởng từ, hoặc chụp mạch máu) để xác định tiêu chuẩn nhận vào về mặt giải phẫu. Các bệnh nhân đủ tiêu chuẩn được phân nhóm ngẫu nhiên 1:1 vào nhóm hủy thần giao cảm động mạch thận ngay lập tức bằng hệ thống Simplicity hoặc nhóm chứng (Hình 1). Nhân viên nghiên cứu và các bệnh nhân không bị làm mù về vị trí tham gia nhóm nghiên cứu. Cả hai nhóm duy trì chế độ thuốc hạ áp ban đầu trong 6 tháng đầu của thử nghiệm.
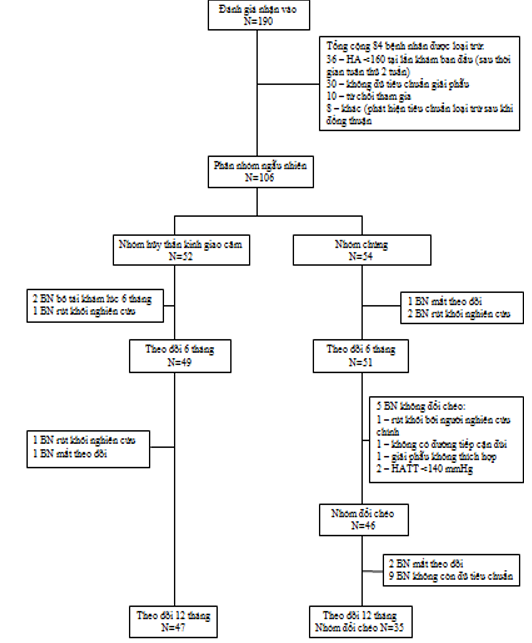
Hình 1. Phân bố bệnh nhân
Kết cục chính là sự thay đổi HATT tại phòng khám sau theo dõi 6 tháng. Tại lần khám lúc 6 tháng, các bệnh nhân nhóm chứng có thể nhận điều trị hủy thần kinh giao cảm động mạch thận; các bệnh nhân tạo thành nhóm đổi chéo. Các bệnh nhân đổi chéo có HATT ≥ 160 mmHg tại lần khám lúc 6 tháng. Các bệnh nhân nhóm chứng chọn hủy thần kinh giao cảm động mạch thận sau 6 tháng nhưng HATT < 160 mmHg (Hình 1) bị loại khỏi phân tích huyết áp, nhưng dữ liệu an toàn đối với các bệnh nhân này được bao gồm trong phần phân tích.
Sau thử nghiệm 6 tháng, sự điều chỉnh định kỳ thuốc hạ áp được cho phép nếu xảy ra các thay đổi huyết áp quan trọng về mặt lâm sàng hoặc các biến chứng liên quan thuốc.
Các bệnh nhân trong nhóm hủy thần kinh giao cảm ban đầu và nhóm đổi chéo sang thủ thuật hủy thần kinh giao cảm tại thời điểm 6 tháng được theo dõi đến 12 tháng. Sự thay đổi về các trị số huyết áp tại phòng khám, tỉ lệ bệnh nhân giảm HATT ≥ 10 mmHg so với ban đầu, và các kết cục an toàn lâu dài của thủ thuật (bao gồm hẹp động mạch thận mới, nhu cầu lọc máu, các biến cố hạ huyết áp hoặc tăng huyết áp cần nhập viện, các biến cố tim mạch gồm nhồi máu cơ tim, suy tim mới khởi phát, đột quỵ, hoặc tử vong do tim mạch) được phân tích. Sự thay đổi thuốc hạ áp, điện giải huyết thanh, độ lọc cầu thận ước đoán, nồng độ creatinine và cystatin C huyết thanh được thu thập vào mỗi lần khám theo dõi.
2.2. PHÂN TÍCH THỐNG KÊ
Các so sánh giữa hai nhóm chính thức không được thực hiện. Thống kê mô tả được sử dụng để trình bày các kết quả của nhóm điều trị và nhóm đổi chéo. So sánh các trị số huyết áp vào mỗi lần khám theo dõi trước thủ thuật được thực hiện bằng phép kiểm t cặp. Sự thay đổi có ý nghĩa nếu mức α 2 đuôi ≤0,05. Phân tích thống kê bằng phần mềm SAS phiên bản 9.2.
2.3. KẾT QUẢ
106 bệnh nhân được phân nhóm ngẫu nhiên vào nhóm hủy thần kinh giao cảm hoặc nhóm chứng sau khi tầm soát ban đầu để nhận vào. Kết cục hiệu quả chính lúc 6 tháng được báo cáo đối với 49 bệnh nhân trong nhóm hủy thần kinh giao cảm và 51 bệnh nhân trong nhóm chứng. Tại thời điểm khám theo dõi lúc 6 tháng, 46 bệnh nhân nhóm chứng chọn lựa hủy thần kinh giao cảm. HATT của 9 bệnh nhân này <160 mmHg tại thời điểm đổi chéo mặc dù >160 mmHg lúc ban đầu. Các đối tượng này được hủy thần kinh giao cảm nhưng bị loại khỏi phân tích kết quả. Hai đối tượng nhóm chứng bị mất theo dõi, còn lại 35 bệnh nhân đổi chéo thực hiện hủy thần kinh giao cảm động mạch thận theo đề cương (HATT ≥160 mmHg (Hình 1). Kết quả của 47 bệnh nhân trong nhóm hủy thần kinh giao cảm ngay từ đầu và 35 bệnh nhân đổi chéo theo đề cương được báo cáo tại thời điểm theo dõi 1 năm sau phân nhóm. Do đó, các kết quả có được từ nhóm bệnh nhân hủy thần kinh giao cảm ngay từ đầu sau 12 tháng và các bệnh nhân đổi chéo sau 6 tháng.
Đặc điểm dân số bệnh nhân ban đầu tại thời điểm phân nhóm ngẫu nhiên là tương tự giữa 2 nhóm về HATT và huyết áp tâm trương tại phòng khám, chủng tộc, tuổi, chỉ số khối cơ thể, và nhịp tim (Bảng 1). Nhiều bệnh nhân hơn ở nhóm hủy thần kinh giao cảm có tiền sử bệnh mạch vành và đái tháo đường típ 2. Trong nhóm đổi chéo, độ lọc cầu thận ước đoán cao hơn, và nhiều bệnh nhân nữ hơn. Sự phân bố thuốc hạ áp ban đầu giữa 2 nhóm tương đương (Bảng 2). Tại lần khám theo dõi 6 tháng, trước khi hủy thần kinh giao cảm động mạch thận, HATT trung bình của nhóm đổi chéo tăng từ 182,9±16,3 mmHg lúc ban đầu đến 190±19,6 mmHg (+7 mmHg; p=0,026), và huyết áp tâm trương trung bình tăng từ 99,1±17,0 mmHg đến 99,9±15,1 mmHg (p=0,066) (Bảng 3).
Bảng 1. Dân số bệnh nhân ban đầu tại thời điểm phân nhóm
|
|
Nhóm hủy thần kinh giao cảm động mạch thận (n=49) |
Nhóm đổi chéo* (n=35) |
p |
|
HATT tại phòng khám, mmHg |
178,3±18,2 |
182,8±16,3 |
0,250 |
|
HTTTr tại phòng khám, mmHg |
96,1±15,5 |
99,1±17,0 |
0,402 |
|
Tuổi |
59,0±11,5 |
58,1±13,0 |
0,741 |
|
Giới, % nữ |
32,7 |
60,0 |
0,015 |
|
Chủng tộc, % Da trắng |
98 |
97,1 |
1,000 |
|
Chỉ số khối cơ thể |
30,8±5,2 |
31,5±5,3 |
0,559 |
|
Đái tháo đường típ 2 |
42,9 |
28,6 |
0,252 |
|
Bệnh mạch vành, % |
18,4 |
5,7 |
0,111 |
|
Tăng cholesterol máu, % |
53,1 |
45,7 |
0,658 |
|
Nhịp tim, lần/phút |
75±15 |
73±15 |
0,568 |
|
eGFR, mL/ph/1,73 m2 daǂ |
76,9±19,3 |
88,8±20,7 |
0,008 |
|
Creatinine huyết thanh, mg/dL |
1,03±0,29 |
0,84±0,21 |
0,001 |
|
Cystatin C, mg/L |
0,91±0,25 |
0,78±0,17 |
0,026 |
|
Các giá trị là trung bình±độ lệch chuẩn hoặc phần trăm. HTTT: huyết áp tâm thu; HATTt: huyết áp tâm trương *Nhóm đổi chéo không hủy thần kinh giao cảm động mạch thận cho đến 6 tháng sau phân nhóm khi đạt kết cục chính. ǂeGFR: độ lọc cầu thận tính theo công thức MDRD |
|||
Bảng 2. Sử dụng thuốc hạ áp tại thời điểm ban đầu
|
|
% sử dụng |
|
|
|
|
Nhóm hủy thần kinh giao cảm (n=49) |
Nhóm đổi chéo (n=35) |
p |
|
Ức chế men chuyển |
51,0 (25/49) |
48,6 (17/35) |
1,000 |
|
Ức chế thụ thể angiotensin |
67,3 (33/49) |
82,9 (29/35) |
0,136 |
|
Ức chế canxi |
77,6 (38/49) |
77,1 (27/35) |
1,000 |
|
Lợi tiểu |
89,8 (44/49) |
91,4 (32/35) |
1,000 |
|
Kháng aldosterone |
18,4 (9/49) |
22,9 (8/35) |
0,784 |
|
Ức chế giao cảm trung ương |
51,0 (25/49) |
42,9 (15/35) |
0,511 |
|
Ức chế trực tiếp renin |
16,3 (8/49) |
22,9 (8/35) |
0,575 |
|
Ức chế beta |
81,6 (40/49) |
62,9 (22/35) |
0,078 |
|
Ức chế alpha giao cảm |
8,2 (4/49) |
2,9 (1/35) |
0,396 |
|
Dãn mạch trực tiếp |
8,2 (4/49) |
2,9 (1/35) |
0,396 |
Bảng 3. Huyết áp trung bình tại phòng khám trước hủy thần kinh giao cảm, 6 và 12 tháng sau thủ thuật hủy thần kinh giao cảm
|
|
Nhóm hủy thần kinh giao cảm (n=49) |
Nhóm đổi chéo (n=35) |
|
Trước thủ thuật* |
|
|
|
HATT, mmHg |
178,3 ± 18,2 |
190,0 ± 19,6 |
|
HATTr, mmHg |
96,1 ± 15,5 |
99,9 ± 15,1 |
|
6 tháng sau thủ thuật |
|
|
|
HATT, mmHg |
146,7 ± 23,3 |
166,3 ± 24,7 |
|
HATTr, mmHg |
84,4 ± 17,0 |
91,5 ± 14,6 |
|
12 tháng sau thủ thuật |
|
|
|
HATT, mmHg |
150,7 ± 21,9ǂ |
N/A |
|
HATTr, mmHg |
87,0 ± 16,1 |
N/A |
|
Các giá trị là trung bình ± độ lệch chuẩn. HATT: huyết áp tâm thu; HATTr: huyết áp tâm trương; N/A: không có *Huyết áp trước thủ thuật là tại thời điểm phân nhóm đối với nhóm hủy thần kinh giao cảm ngay từ đầu và 6 tháng sau phân nhóm đối với nhóm đổi chéo. |
||
Tại thời điểm 12 tháng sau thủ thuật, HATT trung bình của nhóm hủy thần kinh giao cảm ngay từ đầu tiếp tục thấp hơn có ý nghĩa so với ban đầu; sự thay đổi so với ban đầu (-28,1±25,9 mmHg; p<0,001) không khác biệt so với thay đổi sau 6 tháng thủ thuật là -31,7±21,3 mmHg (p=0,16). HATT trung bình của nhóm đổi chéo 6 tháng sau thủ thuật thấp hơn có ý nghĩa so với trị số trước thủ thuật (190,0±19,6 mmHg so với 166,3±24,7 mmHg; thay đổi 23,7±27,5 mmHg; p<0,001). Sự thay đổi HATT tại thời điểm 6 tháng sau thủ thuật tương tự giữa 2 nhóm (p=0,15). Huyết áp tâm trương tại thời điểm 6 và 12 tháng ở nhóm hủy thần kinh giao cảm động mạch thận và tại thời điểm 6 tháng sau thủ thuật ở nhóm đổi chéo cũng thấp hơn có ý nghĩa so với ban đầu (p<0,001 đối với 2 nhóm) (Hình 2 và Bảng 4).
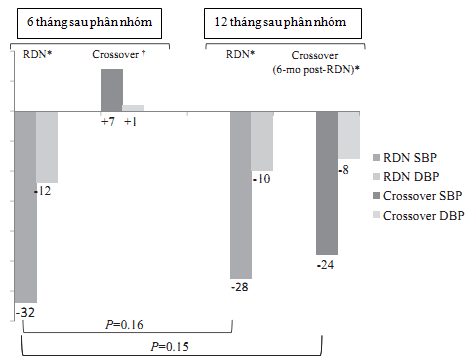
Hình 2.Thay đổi huyết áp tại phòng khám. RDN: nhóm hủy thần kinh giao cảm ngay từ đầu; crossover: nhóm đổi chéo; SBP: huyết áp tâm thu; DBP: huyết áp tâm trương
*p<0,001: thay đổi SBP và DBP sau hủy thần kinh giao cảm động mạch thận
ǂp=0,026: thay đổi SBP so với ban đầu và p=0,066 thay đổi DBP so với ban đầu đối với nhóm đổi chéo trước khi hủy thần kinh giao cảm tại thời điểm 6 tháng
Bảng 4. Thay đổi huyết áp tại phòng khám so với trước thủ thuật tại thời điểm 6 và 12 tháng
|
|
Nhóm hủy thần kinh giao cảm (n=49) |
p |
Nhóm đổi chéo (n=35) |
p |
|
Thay đổi HA 6 tháng |
|
|
|
|
|
HATT |
-31,7 ± 23,1 |
<0,001 |
-23,7 ± 27,5 |
<0,001 |
|
HATTr |
-11,7 ± 11,2 |
<0,001 |
-8,4 ± 12,1 |
<0,001 |
|
Thay đổi HA 12 tháng |
|
|
|
|
|
HATT |
-28,1 ± 24,9 |
<0,001 |
N/A |
|
|
HATTr |
-9,7 ± 10,6 |
<0,001 |
N/A |
|
|
Các giá trị là trung bình ± độ lệch chuẩn. HATT: huyết áp tâm thu; HATTr: huyết áp tâm trương; N/A: không có. Không có khoảng thời gian 2 tuần trước theo dõi 6 tháng sau hủy thần kinh giao cảm thận đối với nhóm đổi chéo. Giá trị p đối với thay đổi huyết áp so với huyết áp trước thủ thuật của mỗi nhóm. |
||||
Phần lớn bệnh nhân ở nhóm hủy thần kinh giao cảm ngay từ đầu giảm HATT tại thời điểm 6 và 12 tháng với HATT giảm ≥10 mmHg (83,7% [41/49] tại thời điểm 6 tháng và 78,7% [37/47] tại thời điểm 12 tháng). Nhóm đổi chéo chứng minh kết quả tương tự với HATT giảm ≥10 mmHg tại thời điểm 6 tháng sau hủy thần kinh giao cảm động mạch thận chiếm 62,9% (22/35).
Sự thay đổi chế độ thuốc hạ áp xảy ra ở cả 2 nhóm điều trị (Bảng 5). Trong nhóm hủy thần kinh giao cảm động mạch thận ngay từ đầu, tỉ lệ nhiều hơn bệnh nhân giảm thuốc sử dụng (ít thuốc hơn và/hoặc giảm liều), nhưng không có sự khác biệt thống kê về thay đổi sử dụng thuốc giữa 2 nhóm.
Bảng 5. Tỉ lệ bệnh nhân thay đổi sử dụng thuốc sau hủy thần kinh giao cảm động mạch thận
|
Thay đổi thuốc, %* |
Nhóm hủy thần kinh giao cảm |
Nhóm đổi chéo |
|
6 tháng sau thủ thuật |
|
|
|
Giảm |
20,9 (9/43) |
18,2 (6/33) |
|
Tăng |
11,6 (5/43) |
15,2 (5/33) |
|
12 tháng sau thủ thuật |
|
|
|
Giảm |
27,9 (12/43) |
N/A |
|
Tăng |
18,6 (8/43) |
N/A |
|
N/A: không có *Thay đổi số lượng thuốc hoặc liều; P khác biệt không ý nghĩa đối với sự thay đổi thuốc giữa 2 nhóm tại thời điểm 6 tháng sau thủ thuật. |
||
Một trường hợp bóc tách động mạch thận xảy ra ở một bệnh nhân đổi chéo trong lúc đưa catheter để chụp mạch máu và trước khi đưa vào catheter Symplicity. Tổn thương này được đặt stent và không có biến cố khác, và bệnh nhân được xuất viện sau thủ thuật hủy thần kinh giao cảm mà không nằm viện kéo dài. Một bệnh nhân đổi chéo khác cần nhập viện sau hủy thần kinh giao cảm động mạch thận vì một đợt hạ huyết áp cần truyền dịch và giảm liều thuốc hạ áp. Bệnh nhân được xuất viện mà không có các vấn đề khác.
Không có sự thay đổi đáng kể về độ lọc cầu thận ước đoán và cystatin C ở 2 nhóm (Bảng 6). Hai bệnh nhân đổi chéo có biến cố tăng huyết áp cần nhập viện. Một biến cố THA xảy ra 106 ngày sau hủy thần kinh giao cảm sau khi dùng thuốc cản quang để chuẩn bị chụp cắt lớp điện toán nhằm chẩn đoán viêm túi thừa. Bệnh nhân được xuất viện sau khi tăng thuốc hạ áp. Bệnh nhân đổi chéo thứ hai có 2 lần THA riêng biệt và cần tăng liều thuốc hạ áp. Chụp cắt lớp điện toán động mạch thận không phát hiện các biến chứng động mạch.
Bảng 6. Chức năng thận tại thời điểm ban đầu, 6 và 12 tháng
|
|
Nhóm hủy thần kinh giao cảm |
Nhóm đổi chéo |
|
eGFR, mL/ph/1,73 m2 |
|
|
|
Ban đầu |
76,9 ± 19,3 (n=49) |
88,8 ± 20,7 (n=35) |
|
6 tháng |
77,1 ± 18,8 (n=49) |
89,3 ± 19,5 (n=35) |
|
12 tháng |
78,2 ± 17,4 (n=45) |
85,2 ± 18,3 (n=35) |
|
Creatinine huyết thanh, mg/dL |
|
|
|
Ban đầu |
1,03 ± 0,29 (n=49) |
0,84 ± 0,21 (n=35) |
|
6 tháng |
1,04 ± 0,32 (n=49) |
0,83 ± 0,18 (n=35) |
|
12 tháng |
1,01 ± 0,28 (n=45) |
0,86 ± 0,20 (n=35) |
|
Cystatin C, mg/L |
|
|
|
Ban đầu |
0,91 ± 0,25 (n=38) |
0,78 ± 0,17 (n=27) |
|
6 tháng |
0,98 ± 0,36 (n=40) |
0,82 ± 0,16 (n=26) |
|
12 tháng |
0,98 ± 0,30 (n=38) |
0,89 ± 0,20 (n=26) |
|
Các giá trị là trung bình ± độ lệch chuẩn. eGFR là độ lọc cầu thân ước đoán |
||
Ngoài ra, không có các lo ngại về tính an toàn dài hạn liên quan thủ thuật hủy thần kinh giao cảm ở 9 bệnh nhân nhóm chứng được điều trị với HATT <160 mmHg.
2.4. BÀN LUẬN
Ngày càng có nhiều chứng cớ về tiềm năng của cắt đốt thần kinh giao cảm thận bằng năng lượng tần số radio để làm giảm huyết áp một cách an toàn ở các bệnh nhân THA kéo dài không đáp ứng với điều trị bằng thuốc tích cực. Các kết quả dài hạn đã được báo cáo đối với các bệnh nhân THA kháng trị điều trị bằng hủy thần kinh giao cảm động mạch thận trong nghiên cứu nhãn mở Symplicity HTN-1 [19]. Các kết quả đó chứng minh không mất tác dụng điều trị đến 3 năm với giảm huyết áp đáng kể (tâm thu -33 mmHg; tâm trương -19 mmHg; p<0,01 thay đổi so với ban đầu). Symplicity HTN-2 là thử nghiệm ngẫu nhiên, có đối chứng đầu tiên ở các bệnh nhân THA nguyên phát kháng trị [16].
Theo dõi nhóm bệnh nhân đoàn hệ hủy thần kinh giao cảm động mạch thận ngay từ đầu cho thấy sự giảm đáng kể huyết áp trung bình tại thời điểm 6 tháng sau hủy thần kinh giao cảm (-32 mmHg) được duy trì tại thời điểm 12 tháng (-28 mmHg), không có sự khác biệt đáng kể giữa giảm huyết áp tại thời điểm 6 và 12 tháng (p=0,16). Các kết quả này phù hợp với các phản ứng dài hạn quan sát được trong thử nghiệm Symplicity HTN-1 và nghiên cứu sổ bộ hủy thần kinh giao cảm động mạch thận báo cáo sự giảm đáng kể HATT tại thời điểm 12 tháng (-23 mmHg) và 24 tháng (-32 mmHg) đối với 153 bệnh nhân THA kháng trị.
Tại thời điểm 6 tháng sau phân nhóm, 35 trong 51 bệnh nhân chứng trải qua hủy thần kinh giao cảm động mạch thận theo đề cương (HATT >160 mmHg). Trước khi điều trị hủy thần kinh giao cảm (6 tháng sau phân nhóm), HATT trung bình của nhóm đối chéo tăng từ 182,8±16,3 mmHg đến 190,0±19,6 mmHg. Tình trạng THA trong khi bệnh nhân đang dùng chế độ hạ áp ổn định có thể phản ánh khuynh hướng gia tăng huyết áp tự nhiên ở các bệnh nhân THA kháng trị và gợi ý chi phí tiềm năng khi trì hoãn điều trị hủy thần kinh giao cảm động mạch thận. Tuy nhiên, các bệnh nhân này đại diện cho nhóm bệnh nhân chứng ban đầu; loại bỏ các đối tượng không chọn hủy thần kinh giao cảm động mạch thận hoặc HATT không còn >160 mmHg dẫn đến sai lệch chọn lựa có thể gây ra sự khác biệt về huyết áp trước thủ thuật và chức năng thận. Tuy nhiên, nhóm đổi chéo có sự giảm đáng kể huyết áp tại thời điểm 6 tháng sau điều trị (-24 mmHg; p<0,001) tương tự như nhóm hủy thần kinh giao cảm ngay từ đầu, chứng tỏ tính lặp lại của các kết quả kết cục chính. Nên chú ý rằng các bệnh nhân đổi chéo không lặp lại thời gian tuân thủ 2 tuần trước lần khám 6 tháng sau thủ thuật, điều này được yêu cầu đối với các bệnh nhân nhóm hủy thần kinh giao cảm ngay từ đầu trước lần khám theo dõi 6 tháng. Có thể sự giảm HATT lớn hơn, không ý nghĩa ở nhóm hủy thần kinh giao cảm ngay từ đầu so với nhóm đổi chéo tại thời điểm 6 tháng liên quan với sự khác biệt về quản lý bệnh nhân trước lần khám 6 tháng sau thủ thuật. Các kết quả nhóm đổi chéo sau hủy thần kinh giao cảm phù hợp với các kết qủa trong thử nghiệm Symplicity HTN-1 (-25 mmHg tại thời điểm 6 tháng) [16].
Các dữ liệu này chứng minh tính an toàn của hủy thần kinh giao cảm động mạch thận bằng năng lượng tần số radio. Chức năng thận không thay đổi vào 6 và 12 tháng sau hủy thần kinh giao cảm (Bảng 6) cho thấy không có biến cố nặng của hủy thần kinh giao cảm đối với chức năng thận. Các dữ liệu sơ bộ từ một số lượng nhỏ bệnh nhân THA kháng trị và bệnh thận giai đoạn 3 đến 4 cho thấy đặc điểm an toàn tương tự thậm chí ở nhóm bệnh nhân suy thận trung bình đến nặng [20].
Trong nhóm đổi chéo, thủ thuật hủy thần kinh giao cảm động mạch thận gây ra 1 trường hợp bóc tách động mạch thận xảy ra trước khi đưa catheter Symplicity và 1 trường hợp tụt huyết áp cần nhập viện và điều chỉnh các thuốc hạ áp. Trong khoảng thời gian 6 đến 12 tháng sau phân nhóm ban đầu, 2 bệnh nhân đổi chéo trải qua các đợt THA cần nhập viện (1 bệnh nhân trải qua 2 lần).
Sự giảm đáng kể huyết áp tại phòng khám được duy trì ở các bệnh nhân tiếp tục điều trị nhiều thuốc sau hủy thần kinh giao cảm động mạch thận, và quan trọng là đến nay không có tình trạng tụt huyết áp có triệu chứng kéo dài. Một đợt tụt huyết áp tại thời điểm hủy thần kinh được điều trị bằng truyền dịch và thay đổi chế độ thuốc hạ áp. Tác dụng hạ áp duy trì của hủy thần kinh giao cảm động mạch thận trong nghiên cứu này và các nghiên cứu khác với catheter Symplicity gợi ý rằng có thể không có các thay đổi quá mức trong cơ chế điều hòa ngược hoặc chứng cớ tái phân bố thần kinh giao cảm động mạch thận xảy ra đến 3 năm sau thủ thuật [21],[22]. Có thể rằng điểm trung tâm của phản xạ thụ thể áp lực thích nghi để duy trì huyết áp mới sau thủ thuật hủy thần kinh giao cảm [23]. Sự cải thiện tính nhạy cảm phản xạ áp lực tim sau điều trị hủy thần kinh giao cảm được báo cáo ở một bệnh nhân THA kháng trị [24].
Nghiên cứu tiền lâm sàng ở mô hình động vật heo khẳng định rằng hủy thần kinh năng lượng thấp bằng cách sử dụng hệ thống catheter Symplicity có thể hủy bỏ các dây thần kinh giao cảm nằm bên trong động mạch thận với ít tổn thương hơn hủy thần kinh bằng phẫu thuật và lành hoàn toàn bất kỳ tổn thương thành động mạch trong vòng 6 tháng [25]. Không có bất kỳ thành phần viêm ở các động mạch được điều trị cũng như không có bất kỳ hẹp hoặc huyết khối ở các động mạch heo phù hợp với đặc điểm an toàn của hủy thần kinh giao cảm động mạch thận ở các thử nghiệm Symplicity HTN-1 và HTN-2 trên người [25]. Ngoài ra, hệ thống hủy thần kinh giao cảm động mạch thận Symplicity cung cấp mức độ an toàn bằng cách thành lập lưu đồ được thiết kế đặc hiệu trong máy phát đo và kiểm soát nhiệt độ, kháng trở, và thời gian ứng dụng năng lượng để tối ưu hóa tính an toàn và hiệu quả.
Các thay đổi thuốc hạ áp được cho phép khi có chỉ định sau khi kết cục chính tại thời điểm 6 tháng được đáp ứng. Mặc dù cả việc tăng và giảm số lượng thuốc và liều kê đơn được quan sát, có khuynh hướng giảm thuốc hạ áp sau hủy thần kinh giao cảm động mạch thận. Nên lưu ý rằng mục đích của thử nghiệm là làm giảm huyết áp và do đó giảm nguy cơ tim mạch đối với các bệnh nhân THA kéo dài; không có dự định giảm sử dụng thuốc hoặc chữa trị hoàn toàn THA, sẽ là một mục tiêu không tưởng trong THA với mức độ này.
2.5. HẠN CHẾ CỦA NGHIÊN CỨU
Nghiên cứu này thiếu theo dõi huyết áp lưu động. Các nghiên cứu viên cố gắng thu thập dữ liệu huyết áp lưu động trong 6 tháng đầu của thử nghiệm nhưng bởi vì sự không tuân thủ của bệnh nhân và các hồ sơ không đầy đủ, các dữ liệu này không được sử dụng. Sau kết cục 6 tháng, các hồ sơ huyết áp 24 giờ không được thu thập. Mặc dù không được xác định hoàn toàn nhưng có thể với phương pháp hủy thần kinh giao cảm động mạch thận, các yếu tố phản ứng của huyết áp có thể xuất hiện với huyết áp tại phòng khám, trong khi các yếu tố này thấp hơn các yếu tố kém phản ứng hơn biểu hiện trong huyết áp lưu động [26]. Ngoài ra, nghiên cứu này không làm mù bệnh nhân và nhân viên đo đáp ứng huyết áp với can thiệp hủy thần kinh giao cảm động mạch thận [17]. Các thiếu sót này sẽ được đề cập trong thử nghiệm hủy thần kinh giao cảm Symplicity HTN-3 sắp tới trong tăng huyết áp kháng trị, trong đó sự thay đổi huyết áp 24 giờ là một kết cục thứ phát quan trọng, nghiên cứu được làm mù, và một thủ thuật giả hủy thần kinh giao cảm động mạch thận được kết hợp vào thiết kế nghiên cứu [27].
3. KẾT LUẬN
Hủy thần kinh giao cảm động mạch thận bằng cách sử dụng hệ thống catheter Symplicity dẫn đến duy trì giảm huyết áp trong 12 tháng ở các bệnh nhân THA nặng không đáp ứng đối với ≥3 thuốc hạ áp. Các bệnh nhân đổi chéo sang hủy thần kinh giao cảm động mạch thận từ nhóm chứng sau 6 tháng giảm huyết áp tương đương. Các biến chứng liên quan thủ thuật ít gặp và dễ dàng điều trị. Tại thời điểm 12 tháng, thử nghiệm Symplicity HTN-2 chứng minh tính an toàn và lợi ích của phương pháp hủy thần kinh giao cảm động mạch thận đối với các bệnh nhân THA kháng trị, không kiểm soát.
BS. TRẦN CÔNG DUY
Đại học Y Dược TP. Hồ Chí Minh
TÀI LIỆU THAM KHẢO
1. Kearney PM, et al. Global burden of hypertension: analysis of worldwide data. Lancet. 2005;365:217-223.
2. Mahfoud F, et al. Treatment strategies for resistant arterial hypertension. Deutsches Arzteblatt Internation. 2011;108:725-731.
3. Persell SD. Prevalence of resistant hypertension in the United States, 2003-2008. Hypertension. 2011;57:1076-1080.
4. Schlaich MP, Krum H, Sobotka PA, Esler MD. Renal denervation and hypertension. Am J Hypertens. 2011;24:635-642.
5. Chobanian AV, Bakris GL, et al. Seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure. Hypertension. 2003;42:1206-1252.
6. Grassi G. Assessment of sympathetic cardiovascular drive in human hypertension: achievements and perspectives. Hypertension. 2009;54:690-697.
7. Esler M, et al. Assessment of human sympathetic nervous system activity from measurements of norepiniephrine turnover. Hypertension.1988;11:3-20
8. Rumantir MS, et al. Neural mechanisms in human obesity-related hypertension. J Hypertens. 1999;17:1125-1133.
9. Bell-Reuss E, et al. Effect of renal sympathetic nerve stimulation on proximal water and sodium reabsorption. J Clin Invest. 1976;57:1104-1107.
10. Kirchheim H, et al. Sympathetic modulation of renal hemodynamics, renin release and sodium excretion. Klin Wochenschr. 1989;67:858-864.
11. Stella A, Zanchetti A. Functional role of renal afferents. Physiol Rev. 1991;71:659-682.
12. DiBona GF, Kopp UC. Neural control of renal function. Physiol Rev. 1997;77:75-197.
13. Schlaich MP, et al. Sympathetic activation in chronic renal failure. J Am Soc Nephrol. 2009;20:933-939.
14. Smith RH, Thompson JE. Splanchnicectomy for essential hypertension: results in 1,266 cases. JAMA. 1953;152:1501-1504.
15. Krum H, et al. Catheter-based renal sympathetic denervation for resistant hypertension: a multicentre safety and proof-of principle cohort study. Lancet. 2009;373:1275-1281.
16. Investigators Symplicity HTN-1. Catheter-based renal sympathetic denervation for resistant hypertension: durability of blood pressure reduction out to 24 months. Hypertension. 2011;57:911-917.
17. Esler MD, et al. Renal sympathetic denervation in patients with treatment-resistant hypertension (the Symplicity HTN-2 trial): a randomized controlled trial. Lancet. 2010;376:1903-1909.
18. Levey AS, et al. Modification of Diet in Renal Disease Study Group. A more accurate method to estimate glomerular filtration rate from serum creatinine: a new prediction equation. Ann Intern Med. 1999;130:461-470.
19. Krum HBN, Schlaid M. Long-term follow-up of catheter-based renal sympathetic denervation for resistant hypertension confirms durable blood pressure reduction. J Am Coll Cardiol. 2012; 59:E1704.
20. Hering D, et al. Renal denervation in moderate to severe CKD. J Am Soc Nephrol. 2012;23:1250-1257.
21. Schlaich MP, et al. Renal denervation as a therapeutic approach for hypertension: novel implications for an old concept. Hypertension. 2009;54:1195-1201.
22. Krum H, et al. Device-based antihypertensive therapy: therapeutic modulation of the autonomic nervous system. Circulation. 2011;123:209-215.
23. Grassi G, et al. Baroreflex control of sympathetic nerve activity in essential and secondary hypertension. Hypertension. 1998;31:68-72.
24. Schlaid MP, et al. Renal sympathetic-nerve ablation for uncontrolled hypertension. N Eng J Med. 2009;361:932-934.
25. Rippy MK, et al. Catheter-based renal sympathetic denervation: chronic preclinical evidence for renal artery safety. Clin Res Cardiol. 2011;100:1095-1101.
26. Mancia G, Parati G. Office compared with ambulatory blood pressure in assessing response to antihypertensive treatment: a meta-analysis. J Hypertens. 2004;22:435-445.
27. Kandazri DE, et al. Catheter-based renal denervation for resistant hypertension: rationale and design of the SYMPLICITY HTN-3 trial. Clin Cardiol. 2012;35:528-535.







