Đây là thông tin tổng hợp từ một Thử nghiệm ngẫu nhiên, mù đôi, đối chứng với giả dược, theo dõi 1 năm.
Mục tiêu:Nghiên cứu đối chứng giả dược này đánh giá hiệu quả và tính an toàn dài hạn của các chất ức chế men dipeptidyl peptidase-4, linagliptin ở bệnh nhân đái tháo đường type 2 kèm suy thận nặng.
Biên dịch và tổng hợp: TS.BS.Đỗ Thị Nam Phương
Thiết kế nghiên cứu:Trong 1 năm, 133 bệnh nhân đái tháo đường type 2 (HbA1c 7,0-10,0%) kèm suy thận nặng (ước tính độ lọc cầu thận [eGFR] < 30 mL / phút / 1,73 m2) được chọn ngẫu nhiên và phân mù đôi vào nhóm dùng linagliptin 5 mg (n = 68) hoặc giả dược (n = 65) một lần mỗi ngày, thêm vào điều trị nền hiện tại. Các tiêu chí hiệu quả chính là sự thay đổi HbA1c từ lúc đầu đến tuần 12. Tiêu chí hiệu quả và an toàn được đánh giá sau 1 năm.
Kết quả:Ở tuần thứ 12, HbA1c trung bình giảm 0,76% với linagliptin và 0.15% với giả dược (sự khác biệt -0.60%; 95% CI (-0,89)-(-0,31); P< 0.0001). Sự cải thiện HbA1c được duy trì với linagliptin (-0,71%) so với giả dược (0.01%) sau 1 năm (sự khác biệt -0,72%, (-1,03)-(-0,41); P< 0.0001). Nghĩa là liều insulin giảm 6,2 đơn vị với linagliptin và 0,3 đơn vị với giả dược. Tỷ lệ các tác dụng phụ tương tự trong 2 nhóm sau 1 năm (94,1 so với 92,3%). Tỷ lệ hạ đường huyết nặng với linagliptin và giả dược là tương đối thấp (ba bệnh nhân mỗi nhóm). Linagliptin và giả dược có ít ảnh hưởng đến chức năng thận (thay đổi trung bình trong eGFR, -0,8 so với -2,2 mL / phút / 1,73 m2), và không có suy thận liên quan đến thuốc xảy ra.
Kết luận:Ở bệnh nhân bị bệnh đái tháo đường type 2 kèm suy thận nặng, linagliptin đem lại những cải thiện có ý nghĩa lâm sàng trong việc kiểm soát đường huyết với nguy cơ hạ đường huyết nặng rất thấp, sự ổn định trọng lượng cơ thể, và không có trường hợp suy thận liên quan đến thuốc. Tiềm năng tiết kiệm insulin và đảm bảo tính an toàn dài hạn trên thận của linagliptin cần được nghiên cứu thêm.
Tổng quan
Tỷ lệ bệnh đái tháo đường, chủ yếu là type 2, trên toàn cầu ước tính sẽ tăng từ 8,3% (366 triệu người trưởng thành) năm 2011, lên 9,9% (552 triệu người trưởng thành) năm 2030 (1). Song song với sự gia tăng này, sự phổ biến của bệnh thận mãn tính (BTM) đang gia tăng trên toàn thế giới (2,3). Bệnh tiểu đường đã được xác định là nguyên nhân hàng đầu của BTM, có thể tiến triển đến bệnh thận giai đoạn cuối hoặc tăng nguy cơ tử vong (3,4). Các bệnh lý này gây nên một gánh nặng cho bệnh nhân và hệ thống y tế, đặc biệt là ở các nước đang phát triển (5,6).
Mục tiêu điều trị bệnh tiểu đường là giảm nguy cơ, hoặc làm chậm sự tiến triển của bệnh thận mạn thông qua việc kiểm soát tối ưu đường huyết (7). Tuy nhiên, hầu hết các loại thuốc để hạđường huyết đều bị ảnh hưởng bởi chức năng thận và do đó cần tránh hoặc giảm liều ở bệnh nhân suy thận(8,9). Như vậy, một nhu cầu rất lớn là việc điều trị tối ưu bệnh tiểu đường ở những bệnh nhân bị bệnh tiểu đường type 2 kèm bệnh thận mạn.
Các chất ức chế men Dipeptidyl peptidase-4 (DPP-4) là một trong những nhóm thuốchạ đường huyết mới. Trong nhóm thuốc này, linagliptin là thuốc duy nhất gần như không thải qua đường thận, chỉ có 5% liều dùng được bài tiết qua thận (10,11). Điều này trái ngược với các chất ức chế DPP-4 khác, chẳng hạn như sitagliptin, vildagliptin, saxagliptin, và alogliptin được chủ yếu là bài tiết qua thận (12). Như vậy, linagliptin không cần chỉnh liều ở bệnh nhân suy giảmchức năng thận (13,14). Sitagliptin, saxagliptin và vildagliptin cần được điều chỉnh liều ở những bệnh nhân có độ thanh thải creatinin <50 ml / phút, bao gồm cả những người có bệnh thận giai đoạn cuối cần được lọc máu (12).
Những nghiên cứu lâm sàng trước đây đã chứng minh linagliptin cải thiện việc kiểm soát đường huyết ở bệnh nhân đái tháo đường týp 2 với đơn trị liệu (15-17) hoặc kết hợp với metformin (18), metformin / sulfonylurea (19), hoặc với một thiazolidinedione (20). Những nghiên cứu này đã chứng minh sự an toàn tổng thể và khả năng dung nạp của linagliptin (21). Mục tiêu của nghiên cứu này là chứng minh hiệu quả lâu dài, tính an toàn và dung nạp của linagliptin so với giả dược khi dùng kết hợp với điều trịhạ đường huyết nền ở những bệnh nhân bị bệnh tiểu đường type 2 và suy thận nặng trong 52 tuần.
THIẾT KẾ NGHIÊN CỨU VÀ PHƯƠNG PHÁP
Dân số nghiên cứu
Những người tham gia nghiên cứu là phụ nữ (không sinh nở hoặc đang dùng phương pháp ngừa thai) và đàn ông từ 18-80 tuổi, được chẩn đoán ĐTĐ type 2 trước đó và đang được điều trị với thuốc hạ đường huyết, gồm: insulin, sulfonylurea, glinides, pioglitazone và ức chế α-glucosidase. Những thuốc điều trị này được duy trì không thay đổi ít nhất 8 tuần trước khi vào nghiên cứu. Tiêu chuẩn thu nhận khi sàng lọc: suy thận nặng (bệnh thận mạn độ 4/5), độ lọc cầu thận (eGFR) tính theo phương trình MDRD (Modification of Diet in Renal Disease)< 30ml/p/1.73m2 (không lọc thận); HbA1c > 7 và ≤ 10% (> 53 và ≤ 86 mmol/mol) và chỉ số khối cơ thể ≤ 45 kg/m2. Tiêu chuẩn loại trừ gồm: nhồi máu cơ tim (NMCT), đột quỵ, hoặc cơn thiếu máu não thoáng quatrong vòng 6 tháng trước đó; bất kỳ yêu cầu lọc thận cấp trong vòng 3 tháng trước đó; ghép thận; suy giảm chức năng gan; vàsử dụng bất kỳ chất ức chế DPP-4 kháchoặc thuốc giảm béo trong vòng 3 tháng trước.
Nghiên cứu này được thực hiện theo quy định của Tuyên bố Helsinki và Hội nghị quốc tế về các nguyên tắc thực hành lâm sàng tốt. Quy trình nghiên cứu được chấp thuận bởi ủy ban y đức độc lập hoặc hội đồng xét duyệt tại mỗi địa điểm tham gia. Tất cả những người tham gia nghiên cứu đều ký giấy đồng ý.
Thiết kế nghiên cứu
Nghiên cứu ngẫu nhiên, mù đôi, có đối chứng giả dược, nhóm nghiên cứu song song này đã được thực hiện tại 53 điểm nghiên cứu tại sáu quốc gia (Úc, Hồng Kông, Israel, New Zealand, Ukraine, và Hoa Kỳ). Nghiên cứu gồm: giai đoạn 2 tuần đầu làchạy thử với giả dược, sau đó là điều trị mù đôi trong 52 tuần, và cuối cùng là giai đoạn theo dõi 1 tuần.
Những người tham gia nghiên cứu thỏa tiêu chuẩn sàng lọc và theo đủ 2 tuần khởi động với giả được sẽ được phân ngẫu nhiên (1:1) để nhận điều trị mù đôi với một trong hai: linagliptin (5 mg/ngày) hoặc giả dược trên nền điều trị chuẩn của họ trong vòng 52 tuần. Sự phân bổ này được phân tầng theo HbA1c (≤8 hay>8% [≤ 64 hay >64 mmol/mol]) và điều trị hạ đường huyết nền. Nghiên cứu viên và người tham gia đều mù về thời gian nghiên cứu và kết quả phân tích tạm thời.
Để đánh giá hiệu quả hạ đường huyết của việc thêm linagliptin, liều điều trị nền hiện tại được duy trìtrong 12 tuần đầu (trừ khi việc điều chỉnh liều được yêu cầu vì lý do an toàn). Trong suốt thời gian điều trị 40 tuần, điều trị nền có thể được điều chỉnh theo các thông số đường máu.
Liệu pháp cứu hộ (bất kỳ thay đổi trong điều trị hoặc liều điều trị hạ đường huyết nền trong tuần 1-12 và/hoặc bổ sung insulin trong tuần 1-52) có thể được khởi động khi đáp ứng hạ đường huyết kém: đường huyết đói >240 mg/ml (>13.3 mmol / L) trong tuần 1-12, đường huyết đói > 200 mg/dL (> 11.1 mmol / L) trong tuần 12-52, hoặc đường huyết đo ngẫu nhiên bất kỳ >400 mg/dL (>22.2 mmol/L). Những bệnh nhân có đường huyết không đáp ứng vớiliệu pháp cứu hộ sẽ được ngừng nghiên cứu.
Những xét nghiệm thường quy và định lượng HbA1c và đường huyết được thực hiện tại phòng thí nghiệm trung tâm (thiết bị Clearstone; Canada, Hoa Kỳ, Singapore, và/hoặc Pháp).
Tiêu chí nghiên cứu
Tiêu chí chính về tính hiệu quả là sự thay đổi HbA1c ở tuần 12 so với ban đầu, từ đó xác định tính ưu việt của linagliptin so với giả dược. Tiêu chí phụ về hiệu quả bao gồm những thay đổi HbA1c, đường huyết đói, điều trị hạ đường huyết nền, và trọng lượng cơ thể trong vòng 52 tuần so với ban đầu.
Tiêu chí an toàn và khả năng dung nạp bao gồm tần suất và cường độ các biến cố bất lợi, rút lui khỏi nghiên cứu do biến cố bất lợi, khám lâm sàng, điện tâm đồ 12 chuyển đạo, dấu hiệu sống còn, và các xét nghiệm trong suốt 52 tuần. Biến cố hạ đường huyết và cơn hạ đường huyết nghiêm trọng cũng được ghi lại (22). Ngoài ra, một ủy ban biến cố lâm sàng độc lập (Clinical Event Committee) sẽxem xét hồi cứu, trong điều kiện mù, tất cả các báo cáo vềđiều trị cấp cứu các biến cố tử vong và nghi ngờ về biến cố tim mạch và đánh giá liệu các biến cố ghi nhận được có nằm trongtiêu chí nghiên cứu (tử vong do tim mạch, đột quỵ, nhồi máu cơ tim và nhập viện vì đau thắt ngực không ổn định) đã được định nghĩa trước đó.
Phân tích thống kê
Giả sử rằng độ lệch chuẩn của sự thay đổi HbA1c so với ban đầu là 1,0% trong cả hai nhóm điều trị, tổng cộng cần có 50 bệnh nhân trong mỗi nhóm để đạt độ mạnh 93% giúp phát hiện sự khác biệt 0.7% của HbA1c thay đổi từ lúc đầu đến tuần 12. Thêm 15 bệnh nhân vào mỗi nhóm đối với những bệnh nhân có khả năng bị thiếu giá trị HbA1c ban đầu hoặc không có bất kỳ giá trị HbA1c trong lúc điều trị, kết quả sẽ có 65 bệnh nhân trong mỗi nhóm điều trị (tỷ lệ bỏ cuộc 25%).
Tiêu chí chính về tính hiệu quả, thay đổi HbA1c từ lúc đầu đến tuần 12, đã được tính thử khi dùnggiả thuyết tính ưu việt của linagliptin so với giả dược với mức có ý nghĩa 5% ở cả hai bên. Một phân tích để xác định quy trình được thực hiện sau khi tất cả những người tham gia nghiên cứu hoàn thành 12 tuần đầu tiên. Lỗi loại I được kiểm soát đối với các tiêu chí đánh giá chính ở 12 tuần.
Sự thay đổi HbA1c từ lúc đầu đến tuần 12 và 52 được đánh giá khi sử dụng ANCOVA với điều trị và thuốc hạ đường huyết nền như tác dụng phân loại cố định và HbA1c liên tục, và chức năng thận ở mức ban đầu như biến số tuyến tính. Phân tích này được thực hiện trên các nhóm Bệnh nhân được phân tích đầy đủ (Full Analysis Set- FAT) sử dụng quan sát cuối cùng tính về trước (Last Observation Carried Forward- LOCF) để quy dữ liệu bị mất. Các FAS bao gồm người được phân ngẫu nhiên nhận được ≥ 1 liều điều trị và những người có kết quả đo HbA1c ban đầu và ≥ 1 lần đo lúc đang điều trị. ANCOVAs cũng được sử dụng để đánh giá những thay đổi đường huyết đói vào tuần 12 và 52 trong FAS (LOCF) và sự thay đổi trọng lượng cơ thể ở tuần 52 trong FAS những trường hợp quan sát được.
Hồi quy logistic với HbA1c ban đầu, điều trị (linagliptin hoặc giả dược), liệu pháp hạ đường huyết nền, chức năng thận ban đầu, và tương tác chức năng thận– điều trị ban đầu là đồng biến số được sử dụng để đánh giá tỷ lệ bệnh nhân đạt được HbA1c mục tiêu (< 7,0% [ < 53 mmol / mol]) trong FAS. Hồi quy logistic với điều trị, liệu pháp hạ đường huyết nền, chức năng thận ban đầu như đồng biến số cũng được sử dụng để phân tích tỷ lệ bệnh nhân sử dụng liệu pháp cứu hộ trên FAS (quan sát các trường hợp). Tất cả các giá trị đo sau khi uống thuốc cứu hộđược xem là mất dấu.
Những thay đổi trong liệu pháphạ đường huyết nền và tính an toàn được phân tích trong nhóm bệnh nhân được điều trị (Treated Set) sử dụng thống kê mô tả. Nhóm được điều trị bao gồm những người được phân ngẫu nhiên nhận được ≥ 1 liều điều trị.
KẾT QUẢ
Phân bố bệnh nhân
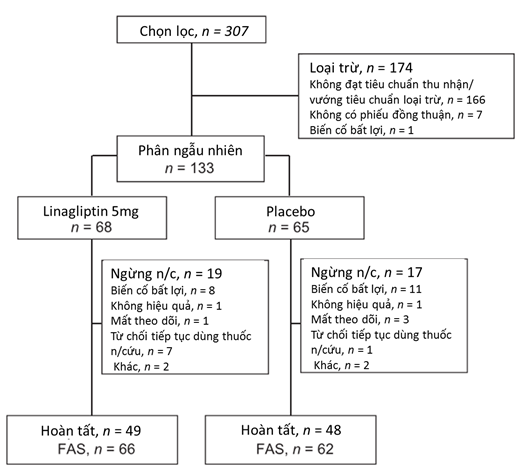
Tổng cộng có 133 bệnh nhân được phân ngẫu nhiên để nhận linagliptin hoặc giả dược trên nền liệu pháp hạ đường huyết của họ (68 so với 65 bệnh nhân, tương ứng với mỗi nhóm). Phân tích tính hiệu quả chính được thực hiện trên 128 bệnh nhân (FAS). Trong số đó, 106 bệnh nhân (linagliptin, 56; placebo, 50) có đủ dữ liệu ban đầu đến tuần 12, và dữ liệu cho các bệnh nhân còn lại được sử dụng LOCF do họ bị mất dấu hoặc dữ liệu của họ được ghi nhận sau khi dùng liệu pháp cứu hộ. Số bệnh nhân hoàn thành nghiên cứu sau 1 năm là 97 bệnh nhân (72,9%) (linagliptin, 72,1%; placebo, 73,8%) (Hình 1). Những lý do chính ngừng nghiên cứu là biến cố bất lợi (linagliptin, 11,8%; placebo, 16,9%) và từ chối để tiếp tục dùng thuốc nghiên cứu (linagliptin, 10,3%;.. placebo,1,5%). Một bệnh nhân ở nhóm linagliptin từ chối tiếp tục nghiên cứu do không nhận thấy hiệu quả. Những người khác từ chối việc tiếp tục mà không có lý do. Nguyên nhân ngừng nghiên cứu khác là do thiếu hiệu quả điều trị (linagliptin, 1.5%; placebo, 1,5%) và mất theo dõi (linagliptin, 1.5%; placebo, 4,6%). Thời gian dùng thuốc điều trị trung bình là 313 ngày trong nhóm linagliptin và 299 ngày trong nhóm giả dược. Thời gian dùng thuốc trung bình là 364 ngày trong cả hai nhóm.
Đặc điểm dân số nghiên cứu
Đặc điểm nhân trắc học và đặc điểm lâm sàng khá tương đồng giữa hai nhóm (Bảng 1). Tuổi trung bình 64,4 ± 10,3; chỉ số khối cơ thể trung bình 32,0 ± 5,8 kg/m2 và HbA1c trung bình 8,2 ± 1,0% (66 ± 11 mmol/mol). Nhìn chung, hầu hết bệnh nhân là người da trắng (73,7%). Tỷ lệ nam (60,2%) nhiều hơn nữ (39,8%), tỷ lệ nam trong nhóm linagliptin cao hơn so với nhóm dùng giả dược (66,2% so với 53,8%). Hơn một nửa số bệnh nhân ≥ 65 tuổi (55,6%), béo phì (BMI ≥ 30 kg/m2, 66,2%), và có HbA1c ≥ 8% (≥ 64 mmol/mol; 54,7%). Hầu hết bệnh nhân (96,1%) có bệnh đái tháo đường type 2 > 5 năm và được điều trị hạ đường huyết với đơn trị liệu (76,7%), 63,9% được điều trị với insulin đơn trị và 18,0% với liệu pháp phối hợp insulin. Các loại thuốc dùng đồng thời phổ biến nhất (linagliptin so với giả dược) là thuốc hạ áp (94,1 so với 100,0%), thuốc hạ lipid máu (77,9 so với 80,0%), và acid acetylsalicylic (67,6 so với 69,2%). Các chẩn đoán đồng thời thường gặp nhất là bệnh tăng huyết áp (94,1 so với 100,0%), bệnh thận do đái tháo đường (88,2 so với 95,4%), bệnh võng mạc đái tháo đường (63,2 so với 53,8%), và hội chứng chuyển hóa (54,4 so với 61,5%). Tất cả các bệnh nhân đều được xác định có suy thận nặng ở thời điểm sàng lọc. Tuy nhiên, do biến động thông thường của chức năng thận ở giai đoạn tiến triển của bệnh thận, 14,3% bệnh nhân có eGFR trong khoảng 30-60 ml/phút/1,73m2 ở xét nghiệm ban đầu (đánh giá ≥ 2 tuần sau khi sàng lọc). Có 92,7% bệnh nhân trong nhóm linagliptin vẫn có suy thận nặng tại xét nghiệm ban đầu(Bảng 1). Ngoài ra, công thức sử dụng để tính eGFR hơi khác nhau tại thời điểm sàng lọc giữa các phòng thí nghiệm trung tâm và đánh giá ban đầu của chương trình nghiên cứu linagliptin. Bệnh nhân được phân ngẫu nhiên dựa trên tính toán eGFR ở phòng thí nghiệm trung tâm, không bao gồm chủng tộc, trong khi giá trị eGFR trong số liệu ban đầu được phân loại dựa trên công thức tínhtừ chương trình nghiên cứu linagliptin, trong đó có yếu tố chủng tộc.
Tính hiệu quả
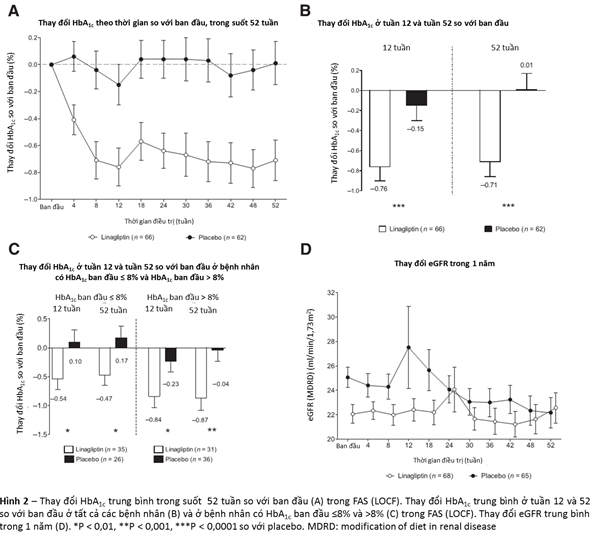
Thay đổi HbA1c trung bình trong thời gian nghiên cứu so với ban đầu được hiển thị trong hình 2A. Ở tuần 12 (tiêu chíđánh giá chính) và 52 (tiêu chí phụ), linagliptin trội hơn giả dược trong việc làm giảm HbA1c (Hình 2B). Khác biệt về điều trị giữa linagliptin so với giả dược là -0.60% (95% CI -0,89 đến-0,31; P < 0.0001) ở tuần 12 và -0.72% (95% CI -1,03 đến -0,41; P < 0.0001) ở tuần 52. Kết quả tương tự cũng được thấy trong các phân nhóm với HbA1c cơ bản ≤ 8 và >8% (≤64 và >64 mmol/mol) (Hình 2C). Tỷ lệ bệnh nhân có HbA1c ban đầu ≥ 7% và đạt được mục tiêu của HbA1c < 7% (53 mmol/mol) ở tuần 52 trong nhóm linagliptin có xu hướng cao hơn so với giả dược (18,0 so với 9,8%; tỷ số chênh 2,886, 95% CI 0,769-10,836; P = 0,2225).
Đường huyết đói ở cả hai nhóm linagliptin và giả dược đều giảm tương tự nhau ở tuần 12 so với ban đầu (thay đổi trị số trung bình, -0,49 so với -0,39 mmol/L; khác biệt điều trị, -0,10; 95% CI -1,35-1,16; P = 0,8802). Một kết quả tương tự cũng được thấy ở tuần 52 (thay đổi trị số trung bình, -0,30 so với -0,38 mmol/L; khác biệt điều trị, 0,07; 95% CI, -0,82-0,97; P = 0,8698).
Tỷ lệ bệnh nhân có ≥ 1 thay đổi trong điều trị nền hạ đường huyết hàng ngày từ lúc đầu đến tuần 52 là tương tự giữa các nhóm (47,1 vs.50.8%). Trong nhóm linagliptin, 81,3% bệnh nhân với≥ 1 lần giảm liều trong điều trị nền và 34,4% có ≥ 1 tăng liều. Trong nhóm giả dược, 42,4% bệnh nhân có ≥ 1 lần giảm liều và 60,6% có ≥ 1 tăng liều. Liệu pháp insulin nền đã được điều chỉnh ở 28 bệnh nhân trong nhóm linagliptin và giả dược (51,9 so với 50,9% số bệnh nhân được điều trị insulin). Sự thay đổi tỷ lệ trung bình của liều insulin hàng ngày là -9,4% ở nhóm linagliptin và -0,5% ở nhóm dùng giả dược. Kết quả này cho thấy sự thay đổi liều insulin trung bình là -6.2 (±4.7) đơn vị trong nhóm linagliptin và -0.3 (±2.1) đơn vị trong nhóm giả dược. Chi tiết về các thay đổi trung bình điều trị bằng insulin nền theo thời gian được cung cấp trong hình bổ sung 1. Ngoài ra, những thay đổi trong điều trị sulfonylurea nền xảy ra trong 5 bệnh nhân trong mỗi nhóm điều trị (38,5 so với 55,5% số bệnh nhân được điều trị bằng sulfonylurea). Kết thúc nghiên cứu, không có bệnh nhân nào dùng thuốc sulfonylurea trong nhóm linagliptin, nhưng liều trung bình hằng ngày lại tăng 5,0% trong nhóm placebo.
Tỷ lệ bệnh nhân dùng liệu pháp cứu hộ thấp hơn trong nhóm linagiptin so với nhóm giả dược (24,2 so với 48,4%). Tỷ số chênh (odd ratio) của việc dùng liệu pháp cứu hộ thấp hơn trong nhóm linagiptin so với nhóm giả dược (odd ratio, 0,345; 95% CI 0,160-0,747; P=0,0069).
Sau thời gian điều trị 1 năm, cân nặng đều giảm trong cả hai nhóm. Ở tuần 52, cân nặng thay đổi so với ban đầu là -1,83 kg trong nhóm linagliptin so với -0,29 kg trong nhóm giả dược (khác biệt điều trị, -1,53 kg; 95% CI -4,11-1,04; P=0,2370)
Tính an toàn và dung nạp
Trong thời gian điều trị 1 năm, tỷ lệ tổng thể các biến cố bất lợi tương tự giữa các nhóm linagliptin và giả dược (94,1 so với 92,3%; Bảng 2).Tỷ lệ bệnh nhân có biến cố bất lợi liên quan đến thuốc cũng tương tự nhau giữanhóm linagliptin và giả dược (45,6 so với 44,6%). Hạ đường huyết (42,6 so với 40,0%) và tăng đường huyết (4,4 so với 3,1%) là biến cố bất lợi liên quan đến thuốc phổ biến nhất trong nhóm linagliptin và giả dược. Những biến cố thường gặp nhất (>5% trong bất kỳ nhóm nào) được tóm tắt trong Bảng 2. Đa số biến cố bất lợi có cường độ nhẹ hoặc trung bình ở cả hai nhóm.
Trong thời gian điều trị 1 năm, số lượng nhỏ bệnh nhân có hạ đường huyết nặng ở cả hai nhóm (linagliptin, 3 [4.4%]; giả dược, 3 [4.6%]) (Bảng 2). Hạ đường huyết có triệu chứng được ghi nhận với một tỷ lệ tương tự ở cả hai nhóm (linagliptin, 24 [33,5%]; placebo, 22 [33,8%]). Hạ đường huyết không triệu chứng xảy ra nhiều hơn ở nhóm linagliptin (38 [55,9%] so với 23 [35,4%]). Điều này dẫn đến tỷ lệ hạ đường huyết tổng thể cao hơn ở bệnh nhân điều trị với linagliptin so với giả dược (43 [63,2%] so với 32 [49,2%]). Nhìn chung, phần lớn các bệnh nhân bị hạ đường huyết được sử dụng insulin đơn trị liệu hoặc kết hợp với một/nhiều thuốc hạ đường huyết khác (linagliptin, 36 [83,7%]; placebo, 27 [84.4%]). Sự khác biệt về tần suấthạ đường huyết tổng thể giữa các bệnh nhân được điều trị bằng linagliptin và những người được điều trị bằng giả dược đáng chú ý là chỉ khác nhau trong vòng 12 tuần đầu điều trị khi điều trị nền đã được cố định (12 tuần đầu tiên, 33 [48,5%] so với 17 [26,2%] ; 40 tuần sau, 34 [50.0%] so với 29 [44,6%]).
Chức năng thận theo thời gian được đánh giá như một chỉ số về tính an toàn. Giá trị trung bình eGFR không giảm một cách có ý nghĩa lâm sàng trong cả hai nhóm linagliptin và giả dược (khác biệt trung bình từ lúc đầu đến giá trị cuối cùng trong lúc điều trị là -0,8 so với -2,2 mL/phút/1,73 m2). Thay đổi eGFR trung bình theo thời gian trong vòng 1 năm được biểu hiện trong hình 2D. Tần suất biến cố bất lợi liên quan đến bệnh thận và tiết niệu tương tự giữa hai nhóm linagliptin và giả dược (25,0 so với 21,5%). Không ghi nhận trường hợp suy thận nào liên quan đến linagliptin. Nồng độ đáy linagliptin tương tự nhau ở các lần thăm khám (từ ̴7-10 nmol/L). Tỷ lệbiến cố tim mạch do ủy ban biến cố lâm sàng độc lập (Clinical Event Committee) xem xét đánh giá tương tự nhau ở cả hai nhóm (Bảng 2). Ba trường hợp tử vong trong mỗi nhóm được ghi nhận trong thời gian nghiên cứu. Không trường hợp nào nghi ngờ có liên quan đến thuốc điều trị.
KẾT LUẬN
Thử nghiệmngẫu nhiên, mù đôi, đối chứng giả dược theo dõi trong vòng 1 năm này đã được thiết kế và được hỗ trợ để đánh giá sự an toàn lâu dài, khả năng dung nạp và hiệu quả của một thuốc hạ đường huyết uống sử dụng trên những bệnh nhân với đái tháo đường type 2 và suy thận nặng. Kết quả cho thấy việc bổ sung thuốcức chế men DPP-4 đường uống, linagliptin (5 mg mỗi ngày một lần) vào điều trị hạ đường huyết nền giúp giảm HbA1c có ý nghĩa lâm sàng sau 12 tuần đã được duy trì trong 52 tuần. Trong suốt nghiên cứu,linagliptin được dung nạp tốt, với độ an toàn và khả năng dung nạp tương tự với giả dược trong dân số những bệnh nhân dễ bị tổn thương này. Đặc biệt, ghi nhận trong nhóm linagliptin: nguy cơ hạ đường huyết nặng rất thấp, trọng lượng cơ thể ổn định, và không có trường hợp suy thậnliên quan đến thuốc.
Kiểm soát đường huyết là nền tảng trong điều trị bệnh đái tháo đường (7). Một vài thử nghiệm lâm sàng lớn đã chứng minh mối liên hệ giữa tăng đường huyết và sự tiến triển các biến chứng mạch máu nhỏ, chẳng hạn như bệnh thận mạn, ở bệnh nhân đái tháo đường type 2 (23-25). Tuy nhiên, việc lựa chọn thuốc điều trị hạ đường huyết bị giới hạn ở những bệnh nhân có bệnh đái tháo đường type 2 kèm bệnh thận mạn, vì nhiều thuốc hạ đường huyết đường uống được thải bởi thận. Do đó, ở những bệnh nhân với suy thận nặng, hầu hết các phương pháp điều trị hoặc không được khuyến khích hoặc chống chỉ định (ví dụ, thuốc ức chế men glucosidase, metformin, glucagon-like peptide-1 receptor agonists, và một số các sulfonylurea thế hệ đầu tiên) hoặc phải giảm liều đáng kể (ví dụ, sulfonylurea thế hệ thứ hai, repaglinide, và thuốc ức chế men DPP-4) (8,9). Mặc dù bệnh thận mạn tiến triển không ảnh hưởng đến chuyển hóa thiazolidinediones, các thuốc nhóm này cũng phải được sử dụng một cách thận trọng vì làm tăng nguy cơ giữ nước và suy tim (26).
Trong nghiên cứu này, việc thêm linagliptin vào điều trị hạ đường huyết nền cho thấy giảm HbA1c đáng kể về mặt lâm sàng, 0,7% sau 52 tuần ở bệnh nhân đái tháo đường type 2 kèm suy thận nặng. Kết quả này cũng giống với những nghiên cứu 24 tuần trước đó, ghi nhận rằng linagliptin (5 mg mỗi ngày một lần) được sử dụng một mình hoặc kết hợp với các thuốc điều trị đái tháo đường giúp giảm HbA1c từ 0,5-0,9% so với giả dược, ở những bệnh nhân đái tháo đường type 2 không kiểm soát được và chức năng thận bình thường hoặc suy thận nhẹ đến trung bình (15,17,18,20). Những nghiên cứu này đã cho thấy linagliptin cải thiện chỉ số HbA1c ở bệnh nhân có chức năng thận khác nhau, từ bình thường đến suy thận nặng.
So sánh về hiệu quả của các thuốc ức chế DPP-4 khác còn hạn chế do sự khác biệt trong thiết kế nghiên cứu và quần thể bệnh nhân; tuy nhiên, những cải thiện HbA1c ở bệnh nhân đái tháo đường type 2 và suy thận vừa hoặc nặng với linagliptin là tương tự, hoặc cao hơn, so với những người được điều trị với thuốc ức chế DPP-4 khác. Giảm HbA1c so với giả dược là -0,4 đến -0,7% đối với vildagliptin sau 52 tuần (27) và 0,4 và 0,7% đối với saxagliptin sau 12 và 52 tuần (28,29). Nghĩa là sự thay đổi chỉ số HbA1c so với ban đầu với sitagliptin là 0,7% sau 54 tuần trong một nghiên cứu so sánh chủ động kéo dài (30). Điều đáng chú ý là linagliptin, trái ngược với các thuốc ức chế DPP-4 khác, không cần điều chỉnh liều ở bệnh nhân suy thậnnặng, trong khi đó một nghiên cứu gần đây ghi nhận rằng sitagliptin thường được sử dụng ở liều không thích hợp trên những bệnh nhân bị bệnh tiểu đường type 2 kèm suy thận, và chỉ có 15% bệnh nhân có suy thận vừa đến giai đoạn cuối nhận được liều như khuyến cáo (31).
HbA1c là một chức năng của cả hai mức độ đường máu lúc đói và sau ăn (32). Việc giảm đường huyết lúc đói quan sát thấy với linagliptin so với giả dược có vẻ không đủ giải thích cho sự thay đổi chỉ số HbA1c, như vậy việc giảm đường huyết sau ăn, có thể xảy ra dựa trên liệu pháp incretin, có thể có những đóng góp đáng kể hơn việc giảm đường huyết đói. Điều này được thấy trong những quan sát trước đó về tác động tích cực của linagliptin trênđường huyết sau ăn (15,18).
Cải thiện việc kiểm soát đường huyết dài hạn với linagliptin có liên quan với xu hướng giảm điều trị insulin nền trong nghiên cứu này. Điều này có thể giúp tối ưu hóa điều trị bệnh đái tháo đường nhưng cần những nghiên cứu sâu hơnđể đảm bảo việc xác định mức độ của tác dụng này. Sử dụng linagliptin cũng liên quan với sự suy giảm số lượng nhỏ eGFR hơn giả dược mặc dù chức năng thận kém hơn một chút lúc ban đầu. Tuy nhiên, nhiều yếu tố có thể ảnh hưởng đến sựtiến triển của bệnh thận trong dân số này, và nghiên cứu lâm sàng dài hạn hơn là cần thiết để tìm hiểu tác động tiềm năng của linagliptin trên chức năng thận. Cùng với một phát hiện trước đó cho thấy việc dùng linagliptin không làm thay đổi ở bệnh nhân chức năng thận bình thường, suy thận nhẹ hoặc vừa (33), các dữ liệu dược động học từ nghiên cứu này xác nhận linagliptin không làm tăng ở bất kỳ mức độ suy thận nào.
Kiểm soát đường huyết trở thành một vấn đề trong bệnh thận mạn tiến triển vì nguy cơ hạ đường huyết thứ phát do giảm tạo đường ở thận và giải phóng insulin giống như của một số thuốc hạ đường huyết và/hoặc các chất chuyển hóa của chúng (34). Nghiên cứu này cho thấy các biến cố hạ đường huyết có triệu chứng và cơn hạ đường huyết nghiêm trọng xảy ra với tần suất tương tự trong các nhóm linagliptin và giả dược. Tỷ lệ cao hơn của biến cố hạ đường huyết không triệu chứng rất có thể giải thích bởi các protocol định sẵntrong điều trị nền ở 12 tuần đầu tiên của nghiên cứu này.
Bệnh nhân tiểu đường loại 2 và bệnh thận mạn có nguy cơ cao mắc bệnh tim mạch. Cục quản lý Thực phẩm và Dược Hoa Kỳ đòi hỏi bằng chứng cho thấy liệu pháp điều trị bệnh đái tháo đường không làm tăng một cách không thể chấp nhận được nguy cơ tim mạch (35). Phân tích hồi cứu dữ liệu từ thuốcức chế DPP- 4 không ghi nhận bất kỳ việc tăng nguy cơ tim mạch (36). Trong một phân tích gộp tiến cứu và định trước, linagliptin giúp giảm tỉ lệ biến cố tim mạch (37). Trong nghiên cứu hiện tại, tỷ lệ tử vong và nguy cơ biến cố tim mạch là tương tự giữa các nhóm linagliptin và giả dược, nhưng mẫu nghiên cứu nhỏ. Một thử nghiệm tiến cứu lớn đang được tiến hành(CAROLINA; clinicaltrials.gov: NCT01243424) sẽ đánh giá hiệu quả của linagliptin trên kết cục tim mạch.
Nghiên cứu nàybị giới hạn bởi việc loại trừ những bệnh nhân bệnh thận giai đoạn cuối cần lọc máu mãn tính, mà có thể ảnh hưởng đến ngoại suy dữ liệu dân số này. Tuy nhiên, linagliptin được biết có ái lực cao với DPP-4, việc chạy thận nhân tạo được dự đoán là không có tác dụng trên việc dùng thuốc. Ngoài ra, nồng độ linagliptin đã được chứng minh không tăng có ý nghĩa ở bệnh nhân bệnh thận giai đoạn cuối so với mức độ suy thận khác (14). Vì vậy, không có sự khác biệt trong việc sử dụng linagliptin ở bệnh nhân cóbệnh thận mạn giai đoạn 1-4 và bệnh nhân bệnh thận giai đoạn cuối (bệnh thận mạn giai đoạn 5) có thể ảnh hưởng đến tính hiệu quả hay tính an toàn của linagliptin.
Để kết luận, thử nghiệm mù đôi đối chứng với giả dược này giúp đánh giá tính an toàn vàhiệu quả của một thuốc ức chế DPP-4 độc quyền trên những bệnh nhân có bệnh đái tháo đường type 2 và suy thận nặng. Những kết quả này khẳng định linagliptin giúpcải thiện việc kiểm soát đường huyết một cách có ý nghĩa lâm sàng mà không có tác dụng phụ không thể chấp nhận trong dân số bệnh nhân dễ bị tổn thương này. Điều này hỗ trợ việc sử dụng linagliptin như một lựa chọn điều trị mỗi ngày một lần ở bệnh nhân đái tháo đường type 2 và suy thận nặng, không có sự bất tiện trong việc điều chỉnh liều lượng hoặc đánh giá chức năng thận thường xuyên hơn để chỉnh liều. Ngoài ra, chức năng thận với linagliptin vẫn ổn định theo thời gian, và tổng liều Insulin được giảm thiểu. Những nghiên cứu để đánh giá những quan sát này hiện đang tiếp tục được tiến hành.
Tài liệu tham khảo:
References
1. Whiting DR, Guariguata L, Weil C, Shaw J.IDF diabetes atlas: global estimates of theprevalence of diabetes for 2011 and 2030.Diabetes Res Clin Pract 2011;94:311–321
2. Grassmann A, Gioberge S, Moeller S,Brown G. ESRD patients in 2004: globaloverview of patient numbers, treatmentmodalities and associated trends. NephrolDial Transplant 2005;20:2587–2593
3. Atkins RC. The epidemiology of chronickidney disease. Kidney Int Suppl 2005;94:S14–S18
4. Molitch ME, DeFronzo RA, Franz MJ,et al.; American Diabetes Association.Nephropathy in diabetes. Diabetes Care
2004;27(Suppl. 1):S79–S83
5. American Diabetes Association. Economiccosts of diabetes in the U.S. In 2007.Diabetes Care 2008;31:596–615
6. Khuwaja AK, Khowaja LA, Cosgrove P.The economic costs of diabetes in developingcountries: some concerns and
recommendations. Diabetologia 2010;53:389–390; author reply 391–392
7. American Diabetes Association. Standardsofmedical care in diabetesd2011.DiabetesCare 2011;34(Suppl. 1):S11–S61
8. Bakris GL. Recognition, pathogenesis, andtreatment of different stages of nephropathyin patients with type 2 diabetes mellitus.Mayo Clin Proc 2011;86:444–456
9. Shrishrimal K, Hart P, Michota F. Managingdiabetes in hemodialysis patients:observations and recommendations. Cleve
Clin J Med 2009;76:649–655
10. Blech S, Ludwig-Schwellinger E, Gräfe-Mody EU, Withopf B, Wagner K. Themetabolism and disposition of the oral
dipeptidyl peptidase-4 inhibitor, linagliptin,in humans. Drug Metab Dispos2010;38:667–678
11. Heise T, Graefe-Mody EU, H€uttner S, RingA, Trommeshauser D, Dugi KA. Pharmacokinetics,pharmacodynamics and tolerabilityof multiple oral doses of linagliptin, adipeptidyl peptidase-4 inhibitor in maletype 2 diabetes patients. Diabetes Obes
Metab 2009;11:786–794
12. Deacon CF. Dipeptidyl peptidase-4 inhibitorsin the treatment of type 2 diabetes:a comparative review. Diabetes ObesMetab
2011;13:7–18
13. DeaconCF,Holst JJ. Linagliptin, a xanthinebaseddipeptidyl peptidase-4 inhibitor withan unusual profile for the treatment of type2 diabetes. Expert Opin Investig Drugs2010;19:133–140
14. Graefe-Mody U, Friedrich C, Port A, et al.Effect of renal impairment on the pharmacokineticsof the dipeptidyl peptidase-
4 inhibitor linagliptin(*). Diabetes ObesMetab 2011;13:939–946
15. Del Prato S, Barnett AH, Huisman H,Neubacher D,WoerleH-J, Dugi KA. Effectof linagliptin monotherapy on glycaemic
control and markers of b-cell function inpatientswith inadequately controlled type2 diabetes: a randomized controlled trial.
Diabetes Obes Metab 2011;13:258–267
16. Forst T, Uhlig-Laske B, Ring A, RitzhauptA, Graefe-Mody U, Dugi KA. The oralDPP-4 inhibitor linagliptin significantly
lowers HbA1c after 4 weeks of treatmentin patients with type 2 diabetes mellitus.Diabetes Obes Metab 2011;13:542–550
17. Kawamori R, Inagaki N, Araki E, et al.Linagliptin monotherapy provides superiorcare.diabetesjournals.org DIABETES CARE 7McGill and Associatesglycaemic control versus placebo or voglibosewith comparable safety in Japanesepatients with type 2 diabetes: a randomized,placebo and active comparator-controlled,double-blind study. Diabetes Obes Metab2012;14:348–357
18. Taskinen MR, Rosenstock J, Tamminen I,et al. Safety and efficacy of linagliptin asadd-on therapy to metformin in patients
with type 2 diabetes: a randomized, doubleblind,placebo-controlled study. DiabetesObes Metab 2011;13:65–74
19. Owens DR, Swallow R, Dugi KA, WoerleHJ. Efficacy and safety of linagliptin inpersons with type 2 diabetes inadequately
controlled by a combination of metforminand sulphonylurea: a 24-week randomizedstudy. Diabet Med 2011;28:1352–1361
20. Gomis R, Espadero RM, Jones R, WoerleHJ, Dugi KA. Efficacy and safety of initialcombination therapy with linagliptin and
pioglitazone in patients with inadequatelycontrolled type 2 diabetes: a randomized,double-blind, placebo-controlled study.Diabetes Obes Metab 2011;13:653–661
21. Schernthaner G, Barnett AH, Emser A,et al. Safety and tolerability of linagliptin:a pooled analysis of data fromrandomized
controlled trials in 3572 patients withtype 2 diabetes mellitus. Diabetes ObesMetab 2012;14:470–478
22. Workgroup on Hypoglycemia, AmericanDiabetes Association. Defining and reportinghypoglycemia in diabetes: a report
from the American Diabetes AssociationWorkgroup on Hypoglycemia. DiabetesCare 2005;28:1245–1249
23. UK Prospective Diabetes Study (UKPDS)Group. Effect of intensive blood-glucosecontrol with metformin on complications
in overweight patients with type 2diabetes (UKPDS 34). Lancet 1998;352:854–865
24. UK Prospective Diabetes Study (UKPDS)Group. Intensive blood-glucose controlwith sulphonylureas or insulin compared
with conventional treatment and risk ofcomplications in patients with type 2 diabetes(UKPDS 33). Lancet 1998;352:837–853
25. Ohkubo Y, Kishikawa H, Araki E, et al.Intensive insulin therapy prevents theprogression of diabetic microvascularcomplications in Japanese patients withnon-insulin-dependent diabetes mellitus:a randomized prospective 6-year study.Diabetes Res Clin Pract 1995;28:103–117
26. Chapelsky MC, Thompson-Culkin K,Miller AK, Sack M, Blum R, Freed MI.Pharmacokinetics of rosiglitazone in patients
with varying degrees of renal insufficiency.J Clin Pharmacol 2003;43:252–259
27. Kothny W, Shao Q, Groop PH,Lukashevich V. One-year safety, tolerabilityand efficacy of vildagliptin in patientswith type 2 diabetes and moderate or severerenal insufficiency. Diabetes Obes Metab.12 Jun 2012. [Epub ahead of print]28. Nowicki M, Rychlik I, Haller H, WarrenML, Suchower L, Gause-Nilsson I;D1680C00007 Investigators. Saxagliptinimproves glycaemic control and is welltolerated in patients with type 2 diabetesmellitus and renal impairment. DiabetesObes Metab 2011;13:523–532
29. Nowicki M, Rychlik I, Haller H, et al.Long-term treatment with the dipeptidylpeptidase-4 inhibitor saxagliptin in patientswith type 2 diabetes mellitus andrenal impairment: a randomised controlled52-week efficacy and safety study.Int J Clin Pract 2011;65:1230–1239
30. Chan JCN, Scott R, Arjona Ferreira JC,et al. Safety and efficacy of sitagliptin inpatients with type 2 diabetes and chronic
renal insufficiency. Diabetes Obes Metab2008;10:545–555
31. Meyers JL, Candrilli SD, Kovacs B.Type 2 diabetes mellitus and renal impairmentin a large outpatient electronicmedical records database: rates of diagnosisand antihyperglycemic medicationdose adjustment. Postgrad Med2011;123:133–143
32. Monnier L, Lapinski H, Colette C. Contributionsof fasting and postprandialplasma glucose increments to the overall
diurnal hyperglycemia of type 2 diabeticpatients: variations with increasinglevels of HbA(1c). Diabetes Care 2003;26:881–885
33. Friedrich C, Emser A,Woerle H-J, Graefe-Mody U. Renal impairment has no clinicallyrelevant effect on the long-termexposure of linagliptin in patients withtype 2 diabetes. Am J Ther. In press
34. Ritz E. Limitations and future treatmentoptions in type 2 diabetes with renal impairment.Diabetes Care 2011;34(Suppl.2):S330–S334
35. Drucker DJ, Goldfine AB. Cardiovascularsafety and diabetes drug development.Lancet 2011;377:977–979
36. Verge D, López X. Impact of GLP-1 andGLP-1 receptor agonists on cardiovascularrisk factors in type 2 diabetes. Curr
Diabetes Rev 2010;6:191–200
37. Johansen OE, Neubacher D, von EynattenM, Patel S, Woerle H-J. Cardiovascularsafety with linagliptin in patients with type2 diabetes mellitus: a pre-specified, prospective,and adjudicatedmeta-analysis of aphase 3 programme. Cardiovasc diabetol2012;11:38







