Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction
The NEW ENGLAND JOURNAL of MEDICINE
Lược dịch và hiệu đính: ThS.BS TRẦN CÔNG DUY
Khoa Nội Tim Mạch, Bệnh viện Chợ Rẫy
Bộ môn Nội Tổng Quát, Đại học Y Dược TP. Hồ Chí Minh
TÓM TẮT
BỐI CẢNH
Ở các bệnh nhân đái tháo đường (ĐTĐ) típ 2, thuốc ức chế kênh đồng vận chuyển natri-glucose 2 (SGLT2) làm giảm nguy cơ nhập viện do suy tim có thể thông qua các cơ chế không phụ thuộc insulin. Y văn cần nhiều dữ liệu hơn về các tác dụng của thuốc ức chế SGLT2 ở bệnh nhân suy tim với phân suất tống máu thất trái giảm bất kể có hoặc không có ĐTĐ típ 2.
PHƯƠNG PHÁP
Thử nghiệm pha 3 có đối chứng với giả dược này phân nhóm ngẫu nhiên 4744 bệnh nhân suy tim với phân độ NYHA II, III hoặc IV và phân suất tống máu thất trái ≤40% được điều trị dapagliflozin (liều 10 mg một lần mỗi ngày) hoặc giả dược trên nền điều trị theo khuyến cáo. Kết cục chính là tổ hợp của suy tim nặng hơn (nhập viện hoặc khám khẩn cấp cần điều trị thuốc suy tim đường tĩnh mạch) hoặc tử vong do tim mạch.
KẾT QUẢ
Trong thời gian trung vị 18,2 tháng, kết cục chính xảy ra ở 386 trường hợp trong 2373 bệnh nhân (16,3%) ở nhóm dapagliflozin và 502 trường hợp trong 2371 bệnh nhân (21,2%) ở nhóm giả dược (tỉ số nguy cơ HR=0,74; khoảng tin cậy (KTC) 95%: 0,65-0,85; P<0,001). Biến cố suy tim nặng hơn đầu tiên xảy ra ở 237 bệnh nhân (10,0%) trong nhóm dapagliflozin và 326 bệnh nhân (13,7%) trong nhóm giả dược (HR=0,70; KTC 95%: 0,59-0,83). Tử vong do nguyên nhân tim mạch xảy ra ở 227 bệnh nhân (9,6%) trong nhóm dapagliflozin và 273 bệnh nhân (11,5%) trong nhóm giả dược (HR=0,82; KTC 95%: 0,69-0,98); tử vong do mọi nguyên nhân xảy ra lần lượt ở 276 bệnh nhân (11,6%) và 329 bệnh nhân (13,9%) (HR=0,83; KTC 95%: 0,71-0,97). Những phát hiện ở các bệnh nhân ĐTĐ tương tự ở bệnh nhân không có ĐTĐ. Tần số biến cố bất lợi liên quan thiếu dịch, rối loạn chức năng thận và hạ đường huyết không khác nhau giữa hai nhóm điều trị.
KẾT LUẬN
Ở những bệnh nhân suy tim với phân suất tống máu giảm, nguy cơ suy tim nặng hơn hoặc tử vong do nguyên nhân tim mạch thấp hơn ở những bệnh nhân được điều trị dapagliflozin so với giả dược bất kể có hay không có ĐTĐ. (DAPA-HF ClinicalTrials.gov, NCT03036124).
NỘI DUNG
Các thử nghiệm lâm sàng lớn ở bệnh nhân ĐTĐ típ 2 cho thấy thuốc ức chế kênh SGLT2 giảm nguy cơ nhập viện do suy tim. Hầu hết bệnh nhân trong các thử nghiệm này không có suy tim tại thời điểm ban đầu, do đó lợi ích của điều trị ức chế SGLT2 chủ yếu phản ánh phòng ngừa suy tim mới mắc. Giảm nguy cơ nhập viện do suy tim được ghi nhận sớm sau khi phân nhóm ngẫu nhiên, đặt ra khả năng thuốc này có các cơ chế tác dụng khác với các cơ chế đã được đưa ra để giải thích các lợi ích tim mạch của điều trị giảm đường huyết. Ngoài tác dụng lợi tiểu và ảnh hưởng huyết động của ức chế SGLT2, các ảnh hưởng trên chuyển hóa cơ tim, các kênh vận chuyển ion, xơ hóa, adipokines và chức năng mạch máu cũng được đề ra. Các tác động này cùng với sự bảo vệ chức năng thận sẽ cũng có lợi cho bệnh nhân suy tim không có ĐTĐ, trong đó ức chế SGLT2 chưa được kiểm định. Thử nghiệm DAPA-HF (Dapagliflozin and Prevention of Adverse Outcomes in Heart Failure) được thiết kế để đánh giá hiệu quả và tính an toàn của thuốc ức chế SGLT2 dapagliflozin ở bệnh nhân suy tim với phân suất tống máu giảm bất kể có hay không có ĐTĐ.
PHƯƠNG PHÁP NGHIÊN CỨU
Thiết kế và giám sát thử nghiệm
Ủy ban quản trị thiết kế và giám sát việc thực hiện và phân tích thử nghiệm qua hợp tác với nhà tài trợ AstraZeneca. Thử nghiệm được thực hiện và báo cáo theo đề cương và kế hoạch phân tích thống kê đã được đăng trên NEJM.org. Thử nghiệm được chấp thuận bởi ủy ban đạo đức tại mỗi trung tâm. Tính an toàn của bệnh nhân trong thử nghiệm được giám sát bởi ủy ban theo dõi dữ liệu và tính an toàn độc lập. Các phân tích của nhà tài trợ được thực hiện lại bởi một nhóm độc lập tại Đại học Glasgow. Bản nháp đầu tiên của bản thảo được chuẩn bị bởi tác giả chính, người không bị giới hạn khi truy cập vào dữ liệu, và được đánh giá và biên tập bởi tất cả các tác giả. Tất cả tác giả quyết định đăng ký bản thảo để xuất bản và xác nhận sự chính xác và tính đầy đủ của dữ liệu và sự tuân thủ của thử nghiệm theo đề cương.
Đối tượng nghiên cứu
Tiêu chuẩn nhận vào bao gồm những bệnh nhân ít nhất 18 tuổi, phân suất tống máu ≤40%, phân độ NYHA (New York Heart Association) II, III hoặc IV. Các bệnh nhân cần có nồng độ NT-proBNP (N-terminal pro–B-type natriuretic peptide) huyết tương ít nhất 600 pg/mL (hoặc ≥400 pg/mL nếu bệnh nhân đã nhập viện vì suy tim trong vòng 12 tháng trước). Bệnh nhân rung nhĩ hoặc cuồng nhĩ trên điện tâm đồ ban đầu cần có nồng độ NT-proBNP ít nhất 900 pg/mL bất kể có tiền sử nhập viện do suy tim hay không.
Bệnh nhân cần được điều trị chuẩn suy tim bằng dụng cụ (máy chuyển nhịp khử rung cấy được, điều trị tái đồng bộ tim, hoặc cả hai) và thuốc điều trị chuẩn, bao gồm ức chế men chuyển, ức chế thụ thể angiotensin hoặc sacubitril–valsartan với chẹn beta trừ khi điều trị đó bị chống chỉ định hoặc gây ra tác dụng phụ không chấp nhận được. Ngoài ra, thuốc kháng thụ thể mineralocorticoid được khuyến khích sử dụng. Các liều thuốc được điều chỉnh ở từng cá nhân theo khuyến cáo của các hướng dẫn. Các bệnh nhân ĐTĐ típ 2 tiếp tục sử dụng thuốc giảm đường huyết nhưng liều có thể được điều chỉnh khi cần. Liều insulin và sulfonylurea có thể được giảm để giảm thiểu nguy cơ hạ đường huyết (như ở các bệnh nhân với nồng độ HbA1C <7%).
Tiêu chuẩn loại trừ gồm điều trị ức chế SGLT2 gần đây hoặc tác dụng phụ không chấp nhận được liên quan với ức chế SGLT2, ĐTĐ típ 1, triệu chứng tụt huyết áp hoặc huyết áp tâm thu dưới 95 mmHg, và độ lọc cầu thận ước tính (eGFR) dưới 30 ml/phút/1,73 m2 da (hoặc chức năng thận giảm nhanh).
Phương pháp tiến hành
Tất cả bệnh nhân đồng thuận bằng văn bản viết và đi vào thời gian sàng lọc 14 ngày, trong lúc đó tiêu chuẩn nhận vào và loại trừ được kiểm tra và thông tin ban đầu được thu thập. Sau khi tầm soát, các bệnh nhân được phân ngẫu nhiên vào nhóm dapagliflozin (liều 10mg/lần/ngày) hoặc giả dược theo kế hoạch ngẫu nhiên cố định, ẩn và sử dụng các phương pháp cân bằng để đảm bảo tỉ số 1:1 của hai chế độ điều trị. Các nghiên cứu viên sử dụng hệ thống tương tác giọng nói hoặc Webresponse để xác định nhóm điều trị. Sự phân bố ngẫu nhiên được phân tầng dựa vào chẩn đoán ĐTĐ típ 2 (như đã được chẩn đoán xác định hoặc HbA1C ≥6,5% [≥48 mmol/mol]) tại thời điểm sàng lọc.
Các bệnh nhân được đánh giá 14 ngày và 60 ngày sau phân nhóm ngẫu nhiên, tập trung đánh giá suy tim và tình trạng dịch thể, các biến cố bất lợi, đánh giá chức năng thận và nồng độ kali. Các lần khám tiếp theo vào thời điểm 4 tháng và mỗi 4 tháng sau đó (thông tin bổ sung có thể xem thêm trên tạp chí New England Journal of Medicine-NEJM.org). Toàn bộ kế hoạch đánh giá được quy định trong đề cương thử nghiệm. Ngưng dapagliflozin hoặc giả dược nếu mang thai hoặc nhiễm toàn ceton do ĐTĐ xảy ra. Giảm liều (5 mg dapagliflozin hoặc giả dược) hoặc tạm ngưng trong trường hợp giảm eGFR cấp tính, thiếu dịch hoặc tụt huyết áp (hoặc để tránh những trường hợp này), sau đó tăng liều hoặc khởi trị lại nếu có thể.
Kết cục
Kết cục chính là tổ hợp của suy tim nặng hơn hoặc tử vong do nguyên nhân tim mạch. Một đợt suy tim nặng hơn là nhập viện ngoài kế hoạch hoặc khám khẩn cấp cần điều trị thuốc suy tim đường tĩnh mạch.
Kết cục phụ chính là tổ hợp của nhập viện do suy tim hoặc tử vong do tim mạch. Kết cục phụ khác là tổng số lần nhập viện do suy tim (bao gồm tái nhập viện) và tử vong do tim mạch; sự thay đổi tổng điểm số triệu chứng của bộ câu hỏi Kansas City Cardiomyopathy từ thời điểm ban đầu đến 8 tháng, được đánh giá theo thang điểm từ 0 đến 100, với điểm số cao hơn cho thấy ít triệu chứng hơn và thay đổi ≥5 điểm được xem có ý nghĩa lâm sàng; tổ hợp của chức năng thận xấu hơn, được định nghĩa suy giảm kéo dài eGFR ≥50%, bệnh thận giai đoạn cuối (được định nghĩa eGFR <15 ml/phút/1,73 m2 da kéo dài [ ≥28 ngày ], lọc máu kéo dài hoặc ghép thận), hoặc tử vong do thận; và tử vong do bất kỳ nguyên nhân. Tất cả kết cục được xem xét bởi các thành viên của ủy ban biến cố lâm sàng, những người không biết được phân nhóm thử nghiệm, theo tiêu chí được định trước.
Các phân tích tính an toàn được xác định trước bao gồm các biến cố bất lợi nghiêm trọng, các biến cố bất lợi liên quan với ngưng điều trị thử nghiệm, các biến cố bất lợi quan tâm (như thiếu dịch, các biến cố thận, các biến cố hạ đường huyết nặng, gãy xương, nhiễm toan ceton do ĐTĐ và đoạn chi), hoại tử Fournier và các xét nghiệm lưu ý. Dữ liệu về các biến cố bất lợi khác không được thu thập thường quy theo dữ liệu an toàn của dapagliflozin.
Phân tích thống kê
844 biến cố kết cục chính sẽ cung cấp độ mạnh của thử nghiệm 90% để phát hiện tỉ số nguy cơ 0,80 so sánh giữa dapagliflozin và giả dược, sử dụng mức apha hai đuôi 0,05. Với tỉ suất mới mắc hàng năm được ước tính là 11% trong nhóm giả dược, nhóm tác giả ước tính thu nhận khoảng 4500 bệnh nhân sẽ cung cấp đủ số biến cố chính dựa vào khoảng thời gian thu nhận 18 tháng và thời gian theo dõi trung bình khoảng 24 tháng. Nghiên cứu sử dụng thủ thuật kiểm định đóng với kiểm định kết cục chính và phụ theo phân tầng dược định trước. Sai lầm loại I được kiểm soát ở mức alpha hai đuôi 0,0499 với so sánh nhiều biến số trong kết cục chính, phụ và một phân tích thử nghiệm giữa kỳ.
Nghiên cứu bao gồm dữ liệu từ tất cả bệnh nhân trải qua phân nhóm ngẫu nhiên trong phân tích các kết cục chính và phụ theo phân bố ngẫu nhiên ban đầu. Đặc điểm ban đầu được trình bày ở dạng trung bình và độ lệch chuẩn, trung vị và khoảng tứ phân vị hoặc phần trăm. Nghiên cứu sử dụng mô hình đo lặp lại để phân tích các chỉ số dọc (như HbA1C và cân nặng) và ước tính sự khác biệt trung bình giữa các nhóm điều trị với khoảng tin cậy 95%. Dữ liệu thời gian đến biến cố được đánh giá bằng ước tính Kaplan-Meier và mô hình tỉ lệ nguy cơ Cox phân tầng theo tình trạng ĐTĐ, tiền sử nhập viện do suy tim và nhóm điều trị; đối với kết cục thận, độ lọc cầu thận ước tính ban đầu được sử dụng thay vì tiền sử nhập viện do suy tim. Mô hình Cox được sử dụng để tính tỉ số nguy cơ, khoảng tin cậy 95% và trị số P hai đuôi và mô hình tỉ lệ bán tham số để tính tổng biến cố (bao gồm tái phát).
Tổng điểm triệu chứng của bộ câu hỏi Kansas City Cardiomyopathy được phân tích như kết cục gộp bao gồm tình trạng sống còn của bệnh nhân tại thời điểm 8 tháng với sự thay đổi điểm số từ ban đầu đến 8 tháng ở những bệnh nhân còn sống. Sự thống nhất của hiệu quả điều trị được đánh giá ở 14 phân nhóm được định trước. Phân tích tính an toàn được thực hiện với những bệnh nhân được phân nhóm ngẫu nhiên và nhận ít nhất một liều dapagliflozin hoặc giả dược. Phép kiểm Fisher chính xác được dùng để so sánh tỉ lệ các biến cố bất lợi. Tất cả phân tích được thực hiện bằng phần mềm Stata, phiên bản 15 (StataCorp) và R, phiên bản 3.5.1 (R Foundation for Statistical Computing).
KẾT QUẢ
Đặc điểm dân số nghiên cứu
Từ 15/2/2017 đến 17/8/2018, tổng cộng 4744 bệnh nhân được phân nhóm ngẫu nhiên sử dụng dapagliflozin hoặc giả dược tại 410 trung tâm ở 20 quốc gia (Hình 1).
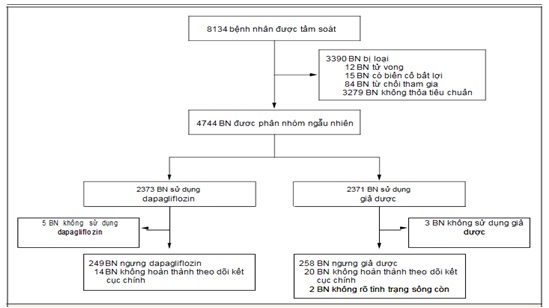
Hình 1. Quy trình nhận bệnh và theo dõi
Đặc điểm của bệnh nhân và điều trị suy tim được cân bằng tốt giữa các nhóm tại thời điểm ban đầu (Bảng 1). Tại thời điểm tầm soát, 42% bệnh nhân ở mỗi nhóm thử nghiệm có tiền sử ĐTĐ típ 2 và có thêm khoảng 3% bệnh nhân trong mỗi nhóm mới được chẩn đoán ĐTĐ.
Bảng 1. Đặc điểm ban đầu của dân số nghiên cứu
| Đặc điểm | Dapagliflozin (N=2373) |
Giả dược (N=2371) |
| Tuổi-năm | 66,2 ± 11,0 | 66,5 ± 10,8 |
| Giới nữ – tần số (%) | 564 (23,8) | 545 (23,0) |
| Chỉ số khối cơ thể | 28,2 ± 6,0 | 28,1 ± 5,9 |
| Chủng tộc-tần số (%) | ||
| Da Trắng | 1662 (70,0) | 1671 (70,5) |
| Da Đen | 122 (5,1) | 104 (4,4) |
| Châu Á | 552 (23,3) | 564 (23,8) |
| Khác | 37 (1,6) | 32 (1,3) |
| Vùng-tần số (%) | ||
| Bắc Mỹ | 335 (14,1) | 342 (14,4) |
| Nam Mỹ | 401 (16,9) | 416 (17,5) |
| Châu Âu | 1094 (46,1) | 1060 (44,7) |
| Châu Á-Thái Bình Dương | 543 (22,9) | 553 (23,3) |
| Phân độ chức năng NYHA-tần số (%) | ||
| II | 1606 (67,7) | 1597 (67,4) |
| III | 747 (31,5) | 751 (31,7) |
| IV | 20 (0,8) | 23 (1,0) |
| Tần số tim-lần/phút | 71,5 ± 11,6 | 71,5 ± 11,8 |
| Huyết áp tâm thu-mmHg | 122,0 ± 16,3 | 121,6 ± 16,3 |
| Phân suất tống máu thất trái – % | 31,2 ± 6,7 | 30,9 ± 6,9 |
| NT-proBNP trung vị (tứ phân vị)-pg/ml | 1428 (857-2655) | 1446 (857-2641) |
| Nguyên nhân chính của suy tim-tần số (%) | ||
| Thiếu máu cục bộ cơ tim | 1316 (55,5) | 1358 (57,3) |
| Không do thiếu máu cục bộ cơ tim | 857 (36,1) | 830 (35,0) |
| Không rõ | 200 (8,4) | 183 (7,7) |
| Tiền sử nội khoa-tần số (%) | ||
| Nhập viện do suy tim | 1124 (47,4) | 1127 (47,5) |
| Rung nhĩ | 916 (38,6) | 902 (38,0) |
| ĐTĐ | 993 (41,8) | 990 (41,8) |
| Độ lọc cầu thận ước đoán | ||
| Trung bình-ml/ph/1,73 m2 | 66,0 ± 19,6 | 65,5 ± 19,3 |
| Tỉ lệ <60 ml/ph/1,73 m2-tần số/tổng số (%) | 962/2372 (40,6) | 964/2371 (40,7) |
| Điều trị dụng cụ – tần số (%) | ||
| Máy khử rung-chuyển nhịp cấy được | 622 (26,2) | 620 (26,1) |
| Điều trị tái đồng bộ tim | 190 (8,0) | 164 (6,9) |
| Thuốc suy tim-tần số (%) | ||
| Lợi tiểu | 2216 (93,4) | 2217 (93,5) |
| Ức chế men chuyển | 1332 (56,1) | 1329 (56,1) |
| Ức chế thụ thể angiotensin II | 675 (28,4) | 632 (26,7) |
| Sacubitril-valsartan | 250 (10,5) | 258 (10,9) |
| Ức chế beta | 2278 (96,0) | 2280 (96,2) |
| Kháng thụ thể mineralocorticoid | 1696 (71,5) | 1674 (70,6) |
| Digitalis | 445 (18,8) | 442 (18,6) |
| Thuốc giảm đường huyết-tần số/tổng số (%) | ||
| Biguanide | 504/993 (50,8) | 512/990 (51,7) |
| Sulfonylurea | 228/993 (23,0) | 210/990 (21,2) |
| Ức chế DDP-IV | 161/993 (16,2) | 149/990 (15,1) |
| Đồng vận thụ thể GLP-1 | 11/993 (1,1) | 10/990 (1,0) |
| Insulin | 274/993 (27,6) | 266/990 (26,9) |
Kết cục
Kết cục gộp chính gồm suy tim nặng hơn (nhập viện hoặc khám khẩn cấp cần điều trị thuốc suy tim đường tĩnh mạch) hoặc tử vong do nguyên nhân tim mạch xảy ra ở 386 bệnh nhân (16,3%) ở nhóm dapagliflozin và 502 bệnh nhân (21,2%) ở nhóm giả dược (HR=0,74; KTC 95%: 0,65-0,85; P <0,001) (Bảng 2 và Hình 2A).
Tỉ lệ biến cố của tất cả ba thành phần của kết cục chính thiên về dapagliflozin; số biến cố lớn nhất của suy tim nặng hơn là nhập viện. Trong các bệnh nhân điều trị dapagliflozin, 231 (9,7%) trường hợp nhập viện do suy tim so với 318 bệnh nhân (13,4%) sử dụng giả dược (HR=0,70; KTC 95%: 0,59-0,83) (Hình 2B). Tử vong do nguyên nhân tim mạch xảy ra ở 227 bệnh nhân (9,6%) điều trị dapagliflozin và ở 273 (11,5%) sử dụng giả dược (HR=0,82; KTC 95%: 0,69-0,98) (Hình 2C). Trong thời gian thử nghiệm, số bệnh nhân cần điều trị dapagliflozin để phòng ngừa một biến cố chính là 21 (KTC 95%: 15-38).
Tỉ lệ kết cục gộp phụ gồm nhập viện do suy tim hoặc tử vong do nguyên nhân tim mạch ở nhóm dapagliflozin thấp hơn nhóm giả dược (HR=0,75; KTC 95%: 0,65-0,85; P <0,001) (Bảng 2). Có tổng cộng 567 biến cố lần đầu và tái phát (340 lần nhập viện do suy tim và 227 trường hợp tử vong do nguyên nhân tim mạch ở 382 bệnh nhân) ở nhóm dapagliflozin và 742 biến cố (469 lần nhập viện do suy tim và 273 trường hợp tử vong do nguyên nhân tim mạch ở 495 bệnh nhân) ở nhóm giả dược, tỉ số tỉ lệ 0,75 (KTC 95%: 0,65-0,88; P <0,001).
Sự tăng tổng điểm triệu chứng trong bộ câu hỏi Kansas City Cardiomyopathy (cho thấy ít triệu chứng hơn) ở nhóm dapagliflozin lớn hơn nhóm giả dược tại tháng thứ 8 so với thời điểm ban đầu (Bảng 2). Nhiều bệnh nhân ở nhóm dapagliflozin hơn nhóm giả dược tăng ít nhất 5 điểm trong tổng điểm (sự khác biệt tối thiểu có ý nghĩa) (58,3% so với 50,9%; tỉ số số chênh OR=1,15; KTC 95%: 1,08-1,23) và ít bệnh nhân hơn giảm đáng kể điểm số (25,3% so với 32,9%; OR=0,84; KTC 95%: 0,78-0,90; P <0,001). Tỉ lệ kết cục gộp về thận không khác biệt giữa hai nhóm điều trị (Bảng 2).
Bảng 2. Các kết cục tim mạch và biến cố bất lợi quan tâm
| Biến số | Dapagliflozin (N=2373) | Biến cố/100 BN-năm | Giả dược (N=2371) |
Biến cố/100 BN-năm | Tỉ số nguy hại hoặc sự khác biệt (KTC 95%) |
Trị số P |
| Kết cục hiệu quả | ||||||
| Kết cục gộp chính-tần số (%) | 383 (16,3) | 11,6 | 502 (21,2) | 15,6 | 0,74 (0,65 – 0,85) | <0,001 |
| Nhập viện hoặc khám khẩn cấp do suy tim | 237 (10,0) | 7,1 | 326 (13,7) | 10,1 | 0,70 (0,59 – 0,83) | NA |
| Nhập viện do suy tim | 231 (9,7) | 6,9 | 318 (13,4) | 9,8 | 0,70 (0,59 – 0,83) | NA |
| Khám suy tim khẩn cấp | 10 (0,4) | 0,3 | 23 (1,0) | 0,7 | 0,43 (0,20 – 0,90) | NA |
| Tử vong do tim mạch | 227 (9,6) | 6,5 | 273 (11,5) | 7,9 | 0,82 (0,69 – 0,98) | NA |
| Kết cục phụ | ||||||
| Tử vong do tim mạch hoặc nhập viện do suy tim – tần số/tổng số (%) | 382 (16,1) | 11,4 | 495 (20,9) | 15,3 | 0,75 (0,65 – 0,85) | <0,001 |
| Tổng số lần nhập viện do suy tim và tử vong do tim mạch | 567 | – | 742 | – | 0,75 (0,65 – 0,88) | <0,001 |
| Thay đổi tổng điểm triệu chứng KCCQ tại thời điểm 8 tháng | 6,1 ± 18,6 | – | 3,3 ± 19,2 | – | 1,18 (1,11 – 1,26) | <0,001 |
| Chức năng thận xấu hơn | 28 (1,2) | 0,8 | 39 (1,6) | 0,71 (0,44 – 1,16) | NA | |
| Tử vong do bất kỳ nguyên nhân | 276 (11,6) | 7,9 | 329 (13,9) | 0,83 (0,71 – 0,97) | NA | |
| Kết cục an toàn | ||||||
| Ngưng thuốc do biến cố bất lợi | 111/2368 (7,5) | – | 116/2368 (4,9) | – | – | 0,79 |
| Biến cố bất lợi quan tâm | – | – | ||||
| Thiếu dịch | 178/2368 (7,5) | – | 162/2368 (6,8) | – | – | 0,40 |
| Biến cố thận bất lợi | 153/2368 (6,5) | – | 170/2368 (7,2) | – | – | 0,36 |
| Gãy xương | 49/2368 (2,1) | – | 50/2368 (2,1) | – | – | 1,00 |
| Đoạn chi | 13/2368 (0,5) | – | 12/2368 (0,5) | – | – | 1,00 |
| Hạ đường huyết nặng | 4/2368 (0,2) | – | 4/2368 (0,2) | – | – | NA |
| Nhiễm toan ceton do ĐTĐ | 3/2368 (0,1) | – | 0 | – | – | NA |
| Hoại tử Fournier | 0 | – | 1/2368 (<0,1) | – | – | NA |
| Chỉ số xét nghiệm và chỉ số khác | ||||||
| Thay đổi từ ban đầu đến 8 tháng | ||||||
| HbA1C – % | -0,21 ± 1,14 | – | 0,04 ±1,29 | – | -0,24 (-0,34; -0,13) | <0,001 |
| Creatinine – mg/dL | 0,07 ± 0,24 | – | 0,04 ± 0,25 | – | 0,02 (0,01; 0,03) | <0,007 |
| Hematocrit – % | 2,31 ± 3,90 | – | -,019 ± 3,81 | – | 2,41 (2,21; 2,62) | <0,001 |
| NT-proBNP – pg/ml | -1,96 ± 2387 | – | 101 ± 2944 | – | -303 (-457; -150) | <0,001 |
| Cân nặng | -0,88 ± 3,86 | – | 0,10 ± 4,09 | – | -0,87 (-1,11; -0,62) | <0,001 |
| Huyết áp tâm thu – mmHg | -1,92 ± 14,92 | – | -0,38 ± 15,27 | – | -1,27 (-2,09; -0,45) | 0,002 |
BN: bệnh nhân; NA: không có (vì trị số P đối với các kết cục hiệu quả chỉ được báo cáo đối với các kết cục trong chiến lược kiểm định thống kê).
Tổng 276 bệnh nhân (11,6%) ở nhóm dapagliflozin và 329 bệnh nhân (13,9 %) ở nhóm giả dược tử vong do bất kỳ nguyên nhân (HR=0,83; KTC 95%: 0,71-0,97) (Hình 2D).
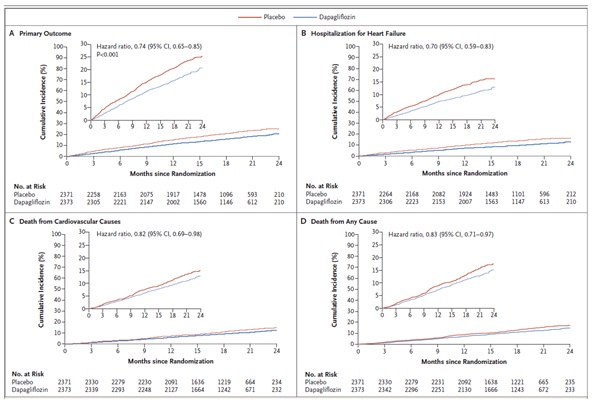
Hình 2. Các kết cục tim mạch. A. Primary outcome: Kết cục chính; B. Hospitalization for heart failure: Nhập viện do suy tim; C. Death from cardiovascular causes: Tử vong do nguyên nhân tim mạch; D. Death from any cause: Tử vong do bất kỳ nguyên nhân. (Chụp từ tài liệu gốc)
Ảnh hưởng của dapagliflozin trên kết cục chính nhìn chung đồng nhất ở các phân nhóm bất kể bệnh nhân có hay không có ĐTĐ tại thời điểm ban đầu, mặc dù các bệnh nhân có phân độ chức năng NYHA III hoặc IV dường như có lợi ít hơn các bệnh nhân có NYHA độ II (Hình 3). Trong một phân tích dưới nhóm hậu kiểm gồm các bệnh nhân sử dụng sacubitril-valsartan ban đầu, tỉ số nguy cơ so sánh kết cục chính ở nhóm dapagliflozin và giả dược là 0,75 (KTC 95%: 0,50-1,13) so với 0,74 (KTC 95%: 0,65-0,86) ở những bệnh nhân không sử dụng sacubitril–valsartan.
Những thay đổi từ ban đầu đến 8 tháng về các trị số HbA1C, hematocrit, creatinine, NT-proBNP, huyết áp tâm thu và cân nặng được trình bày ở Bảng 2.
Tính an toàn
Tổng 8 bệnh nhân (5 ở nhóm dapagliflozin và 3 ở nhóm giả dược) được loại trừ khỏi phân tích tính an toàn vì không sử dụng dapagliflozin hoặc giả dược (Bảng 2). Các biến cố bất lợi nghiêm trọng liên quan thiếu dịch xảy ra ở 29 bệnh nhân (1,2%) của nhóm dapagliflozin và 40 bệnh nhân (1,7%) ở nhóm giả dược (P=0,23). Các biến cố bất lợi nghiêm trọng về thận xảy ra ở 38 (1,6%) bệnh nhân của nhóm dapagliflozin và 65 bệnh nhân (2,7%) của nhóm giả dược (P=0,009). Các biến cố bất lợi hiếm khi dẫn đến ngưng điều trị. Nhóm dapagliflozin không tăng quá mức biến cố bất lợi nào.
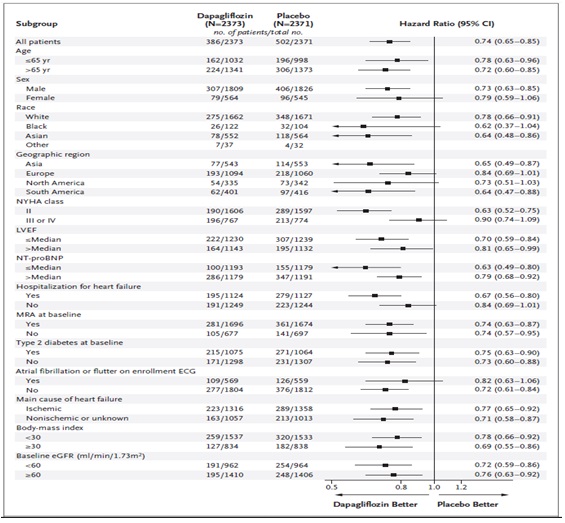
Hình 3. Kết cục gộp chính theo các phân nhóm.
Age: tuổi; Sex: giới tính; Race: chủng tộc; Geographic region: vùng địa lý; NYHA class: phân độ NYHA; LVEF: phân số tống máu thất trái; Hospitalization for heart failure: nhập viện do suy tim; MRA at baseline: kháng thụ thể mineralocorticoid tại thời điểm ban đầu; Type 2 diabetes at baseline: ĐTĐ típ 2 tại thời điểm ban đầu; Atrial fibrillation or flutter on enrollment ECG: rung nhĩ hoặc cuồng nhĩ trên ECG lúc chọn vào; Main cause of heart failure: nguyên nhân chính của suy tim; Body-mass index: chỉ số khối cơ thể; Baseline eGFR (ml/phút/1,73 m2). (Chụp từ tài liệu gốc)
BÀN LUẬN
Trong thử nghiệm ngẫu nhiên, có đối chứng với giả dược này gồm các bệnh nhân suy tim với phân suất tống máu thất trái giảm, nguy cơ kết cục gộp chính gồm suy tim nặng hơn (nhập viện hoặc khám khẩn cấp cần điều trị thuốc suy tim đường tĩnh mạch) hoặc tử vong do nguyên nhân tim mạch ở nhóm dapagliflozin thấp hơn giả dược. Mỗi thành phần trong ba thành phần của kết cục gộp ít gặp hơn ở nhóm dapagliflozin, tương tự như tổng số lần nhập viện do suy tim và tử vong do nguyên nhân tim mạch. Sử dụng dapagliflozin cũng dẫn đến ít triệu chứng suy tim hơn khi đánh giá bằng bộ câu hỏi Kansas City Cardiomyopathy. Những lợi ích có ý nghĩa lâm sàng xảy ra sớm sau khi phân nhóm ngẫu nhiên và được quan sát thấy ở các bệnh nhân đang dùng các liệu pháp điều trị suy tim khác theo khuyến cáo.
Dapagliflozin có hiệu quả ở 55% bệnh nhân không có ĐTĐ típ 2 tương tự như ở bệnh nhân có ĐTĐ. Sự chứng minh các lợi ích tim mạch của thuốc ức chế SGLT2 ở các bệnh nhân không có ĐTĐ ủng hộ các giả thuyết trước đây rằng thuốc này có các tác dụng có lợi khác ngoài giảm đường huyết. Do đó, các phát hiện của nghiên cứu này có tiềm năng mở rộng vai trò điều trị của dapagliflozin vượt ra khỏi các bệnh nhân ĐTĐ.
Giảm nguy cơ kết cục chính nhìn chung đồng nhất ở các phân nhóm khác nhau được định trước, mặc dù một phân nhóm cho thấy có thể khác biệt về lợi ích điều trị ở các bệnh nhân có phân độ NYHA III hoặc IV ít hơn độ II. Tuy nhiên, những phát hiện ở các phân nhóm khác với tình trạng bệnh nặng hơn (như phân suất tống máu thất trái giảm nhiều hơn, chức năng thận xấu hơn, và nồng độ NT-proBNP tăng) lại không đồng nhất với ghi nhận từ phân nhóm theo phân độ NYHA.
Dân số nghiên cứu này khác với các bệnh nhân trong các thử nghiệm trước đây của thuốc ức chế SGLT2 bởi vì dân số nghiên cứu này có nguy cơ nhập viện do suy tim hoặc tử vong do nguyên nhân tim mạch cao hơn các thử nghiệm trước đây. Hầu hết bệnh nhân trong thử nghiệm DAPA-HF đã được điều trị bằng lợi tiểu quai và kháng thụ thể mineralocorticoid, chúng ta chưa biết được liệu dapagliflozin sẽ gây lợi tiểu ở nhóm bệnh nhân khác hay không. Tác động đó có thể dẫn đến thiếu dịch và chức năng thận xấu hơn hay không chưa được biết rõ vì nhiều bệnh nhân có bệnh thận mạn. Không có biến cố bất lợi nào thường gặp (xảy ra ở <8% bệnh nhân, không có sự khác biệt giữa các nhóm) và các biến cố bất lợi nghiêm trọng trên thận nhìn chung không phổ biến và ít gặp ở nhóm dapagliflozin. Nhìn chung, ít bệnh nhân ngưng dapagliflozin hoặc giả dược do bất kỳ biến cố bất lợi (<5% bệnh nhân ở mỗi nhóm điều trị). Hạ đường huyết nặng và nhiễm toan ceton do đái tháo đường hiếm gặp và cả hai biến cố bất lợi chỉ xảy ra ở các bệnh nhân ĐTĐ.
Thử nghiệm này có một số hạn chế. Nghiên cứu đã sử dụng các tiêu chuẩn nhận bệnh và loại trừ, có thể giới hạn tính khái quát của các kết quả. Ít hơn 5% bệnh nhân là người Da Đen và tương đối ít bệnh nhân rất cao tuổi với nhiều bệnh đồng mắc. Ít bệnh nhân sử dụng sacubitril-valsartan, thuốc này hiệu quả hơn so với chỉ sử dụng thuốc ức chế hệ renin-angiotensin trong việc giảm tỉ lệ nhập viện do suy tim và tử vong do nguyên nhân tim mạch. Tuy nhiên, các cơ chế hoạt động giả định của ức chế SGLT2 và ức chế neprilysin khác nhau, và trong phân tích dưới nhóm hậu kiểm, lợi ích của dapagliflozin tương tự ở các bệnh nhân có và không có điều trị sacubitril-valsartan.
KẾT LUẬN
Ở các bệnh nhân suy tim với phân suất tống máu thất trái giảm, những bệnh nhân sử dụng thuốc ức chế SGLT2 dapagliflozin có nguy cơ thấp hơn các biến cố suy tim nặng hơn hoặc tử vong do nguyên nhân tim mạch và điểm số triệu chứng tốt hơn những bệnh nhân sử dụng giả dược bất kể có hoặc không có ĐTĐ.
TÀI LIỆU THAM KHẢO
McMurray J.J.V, Solomon S.D., Inzucchi S.E., et al (2019), “Dapagliflozin in Patients with Heart Failure and Reduced Ejection Fraction”, the New England Journal of Medicine, 381:1995-2008.
Cảm ơn AstraZeneca đã hỗ trợ nhằm mục đích cập nhật và giáo dục y khoa.







