TS. PHẠM HỮU VĂN
(…)
3.2. Tiêu chuẩn chẩn đoán rung nhĩ
Ở nhiều bệnh nhân, chẩn đoán AF rất đơn giản, ví dụ: các triệu chứng điển hình liên quan đến các đặc điểm đặc trưng trên ECG 12 chuyển đạo tiêu chuẩn cho thấy cần phải quản lý AF. Chẩn đoán trở nên khó khăn hơn trong bối cảnh các đợt AF không có triệu chứng hoặc AF được phát hiện trên các thiết bị theo dõi dài hạn, đặc biệt là các thiết bị không cung cấp ECG (xem Mục 10). Để phòng ngừa chẩn đoán AF không phù hợp, lực lượng đặc nhiệm này tiếp tục khuyến nghị cần phải có tài liệu ECG để bắt đầu phân tầng nguy cơ và quản lý AF. Trong thực hành hiện tại, xác nhận ECG có thể gồm nhiều lựa chọn: không chỉ khi AF vẫn tồn tại trên ECG 12 chuyển đạo tiêu chuẩn mà còn cả các thiết bị một và nhiều chuyển đạo cung cấp ECG (xem Dữ liệu bổ sung trực tuyến, Bảng bằng chứng bổ sung S1). Điều này không bao gồm các thiết bị đeo không phải ECG và các thiết bị khác thường sử dụng quang điện di (photoplethysmography). Người ta lưu ý nhiều thử nghiệm AF quan trọng yêu cầu hai hoặc nhiều ECG ghi lại AF hoặc chẩn đoán AF đã được thiết lập trước khi phân nhóm ngẫu nhiên. [25–29] Khoảng thời gian AF cần thiết để chẩn đoán trên các thiết bị theo dõi không rõ ràng. Điện tâm đồ 12 đạo trình tiêu chuẩn đo được 10 giây, trong khi 30 giây trở lên trên các thiết bị điện tâm đồ một đạo trình hoặc nhiều đạo trình thường là ý kiến chung, mặc dù bằng chứng còn hạn chế.
Bảng khuyến cáo 1 — Khuyến cáo để chẩn đoán AF (xem thêm Bảng bằng chứng 1)
| Khuyến cáo | Classa | Levelb |
| Xác nhận bằng điện tâm đồ (12 chuyển đạo, nhiều chuyển đạo hoặc một chuyển đạo) được khuyến cáo để thiết lập chẩn đoán AF lâm sàng và bắt đầu phân tầng nguy cơ và điều trị.[25–29] |
I |
A |
AF: rung nhĩ
a Class khuyến cáo
b Mức độ bằng chứng
3.3. Các triệu chứng liên quan đến AF
Các triệu chứng liên quan đến các đợt AF rất đa dạng và phổ biến, không chỉ là hồi hộp thông thường (Hình 1). Các đợt AF không triệu chứng có thể xảy ra, [30] mặc dù 90% bệnh nhân AF mô tả các triệu chứng với mức độ nghiêm trọng khác nhau. [31] Ngay cả ở những bệnh nhân có triệu chứng, một số đợt AF có thể vẫn không có triệu chứng.[32,33] Sự có mặt hoặc không có triệu chứng không liên quan đến đột quỵ, thuyên tắc hệ thống hoặc tử vong.[34] Tuy nhiên, các triệu chứng ảnh hưởng đến chất lượng cuộc sống của bệnh nhân. [35,36] Các triệu chứng AF đặc hiệu ở tim như hồi hộp ít phổ biến hơn các triệu chứng không đặc hiệu như mệt mỏi, nhưng chúng làm giảm đáng kể chất lượng cuộc sống.[36,37] Mặc dù phụ nữ thường không được đại diện đầy đủ trong các thử nghiệm lâm sàng về AF, [38–40] các tài liệu hiện có cho thấy phụ nữ AF có vẻ có nhiều triệu chứng hơn và có chất lượng cuộc sống kém hơn. [41,42] Bệnh nhân AF báo cáo gánh nặng lo âu và mức độ trầm cảm cao hơn (tỷ lệ chênh lệch [OR], 1,08; khoảng tin cậy 95% [CI], 1,02–1,15; P = .009) so với dân số nói chung, [43,44] với tỷ lệ mắc các triệu chứng này cao hơn ở phụ nữ AF. [45]
Đánh giá các triệu chứng liên quan đến AF nên được ghi lại ban đầu, sau khi thay đổi phương pháp điều trị hoặc trước và sau khi can thiệp. Phân loại triệu chứng theo thang điểm mEHRA (Bảng 7) đã sửa đổi của Hội nhịp tim châu Âu (mEHRA) tương tự như phân loại chức năng của Hội tim mạch New York (NYHA) đối với suy tim. Nó tương quan với điểm số chất lượng cuộc sống trong các thử nghiệm lâm sàng, liên quan đến tiến triển và các sự kiện lâm sàng và có thể là điểm khởi đầu có giá trị trong thực hành thường quy để đánh giá gánh nặng và tác động của các triệu chứng cùng với bệnh nhân. [46–48] Lưu ý các triệu chứng cũng có thể liên quan đến các bệnh đi kèm chứ không chỉ thành phần AF. Các tác động liên quan đến bệnh nhân của các triệu chứng từ AF theo thời gian cũng có thể được đánh giá bằng cách sử dụng các biện pháp kết quả do bệnh nhân báo cáo (xem Mục 8.4).
Bảng khuyến cáo 2 Khuyến cáo để đánh giá triệu chứng ở bệnh nhân AF (xem thêm Bảng bằng chứng 2)
| Khuyến cáo | Classa | Levelb |
| Đánh giá tác động của các triệu chứng liên quan đến AF được khuyến cáo trước và sau những thay đổi lớn trong điều trị để thông báo cho việc ra quyết định chung và hướng dẫn các lựa chọn điều trị.[17,36,46–55] |
I |
B |
AF: rung nhĩ
a Class khuyến cáo
b Mức độ bằng chứng
3.4. Đánh giá chẩn đoán AF mới
Tất cả bệnh nhân AF nên được đánh giá chẩn đoán toàn diện và xem xét lại tiền sử bệnh để xác định các yếu tố nguy cơ và/hoặc bệnh đi kèm cần điều trị tích cực. Bảng 8 hiển thị các xét nghiệm chẩn đoán cần thiết cho bệnh nhân AF.
Cần thực hiện điện tâm đồ 12 chuyển đạo ở tất cả bệnh nhân AF để xác nhận nhịp, xác định tần số thất và tìm kiếm các dấu hiệu của bệnh tim cấu trúc, khiếm khuyết dẫn truyền hoặc thiếu máu cục bộ. [56] Cần thực hiện xét nghiệm máu (chức năng thận, điện giải huyết thanh, chức năng gan, công thức máu, glucose/hemoglobin glycat hóa [HbA1c] và xét nghiệm tuyến giáp) để phát hiện bất kỳ tình trạng đi kèm nào có thể làm trầm trọng thêm AF hoặc làm tăng nguy cơ chảy máu và/hoặc huyết khối thuyên tắc. [57, 58]
Các cuộc điều tra khác sẽ phụ thuộc vào đánh giá cá nhân và chiến lược điều trị đã lên kế hoạch.[59–65] Siêu âm tim qua thành ngực (TTE) nên được thực hiện trong quá trình đánh giá ban đầu, trong đó điều này sẽ hướng dẫn các quyết định quản lý hoặc ở những bệnh nhân có thay đổi về các dấu hiệu hoặc triệu chứng tim mạch. Lực lượng đặc nhiệm thừa nhận khả năng tiếp cận TTE có thể bị hạn chế hoặc chậm trễ trong bối cảnh chăm sóc chính, nhưng điều này không nên làm chậm trễ việc bắt đầu dùng thuốc chống đông đường uống (OAC) hoặc các thành phần khác của AF-CARE khi được chỉ định. [66] Các chi tiết khác về TTE và đánh giá lại (ví dụ: nếu nhịp tim tăng cao hạn chế chẩn đoán hình ảnh hoặc khi có thay đổi về tình trạng lâm sàng) được trình bày trong Phần 8.3. Có thể cần chụp ảnh bổ sung bằng các phương thức khác nhau để hỗ trợ quản lý bệnh đi kèm và liên quan đến AF (xem Dữ liệu bổ sung trực tuyến, Hình S1)
Bảng khuyến cáo 3 — Khuyến cáo về đánh giá chẩn đoán ở những bệnh nhân mắc AF mới (xem thêm Bảng bằng chứng 3)
| Khuyến cáo | Classa | Levelb |
| Siêu âm tim qua thành ngực được khuyến cáo ở những bệnh nhân được chẩn đoán AF, điều này sẽ hướng dẫn các quyết định điều trị.[59,65,67] |
I |
C |
AF: rung nhĩ
a Class khuyến cáo
b Mức độ bằng chứng
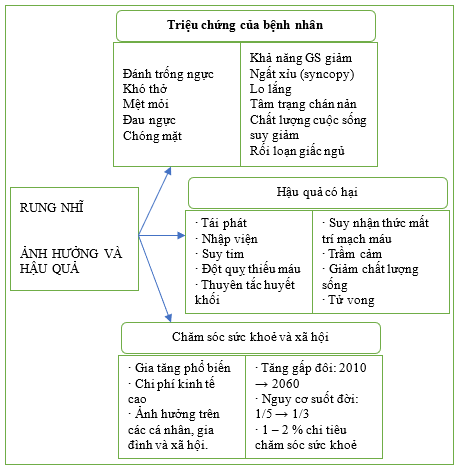
Hình 1. Tác động và kết quả liên quan đến AF lâm sàng. AF: rung nhĩ
Bảng 7 Phân loại triệu chứng của Hội nhịp tim châu Âu (mEHRA) đã sửa đổi
| Điểm số | Triệu chứng | Mô tả |
| 1 | Không AF | Không gây ra bất kỳ triệu chứng nào |
| 2a | Nhẹ | Hoạt động hàng ngày bình thường không bị ảnh hưởng do các triệu chứng liên quan đến AF |
| 2b | Trung bình | Hoạt động hàng ngày bình thường không bị ảnh hưởng do các triệu chứng liên quan đến AF, nhưng bệnh nhân gặp khó khăn triệu chứng |
| 3 | Nặng | Hoạt động hàng ngày bình thường bị ảnh hưởng do các triệu chứng liên quan đến AF |
| 4 | Kiệt sức | Hoạt động hàng ngày bình thường không còn được tiếp diễn |
AF: rung nhĩ
3.5. Các biến cố bất lợi liên quan đến AF
Rung nhĩ liên quan đến một loạt các biến cố bất lợi nghiêm trọng (Hình 1) (xem Dữ liệu bổ sung trực tuyến, Bảng bằng chứng bổ sung S2). Bệnh nhân AF cũng có tỷ lệ nhập viện và biến chứng cao do các tình trạng bệnh lý đi kèm. Hậu quả không tử vong phổ biến nhất ở những người bị AF là suy tim, xảy ra ở khoảng một nửa số bệnh nhân theo thời gian. Bệnh nhân bị AF có nguy cơ tương đối (RR) suy tim tăng gấp bốn đến năm lần so với những bệnh nhân không bị AF, như đã chứng minh trong hai phân tích tổng hợp (RR, 4,62; 95% CI, 3,13–6,83 và RR, 4,99; 95% CI, 3,0–8,22).[68,69] Các tác động bất lợi phổ biến tiếp theo từ AF là đột quỵ do thiếu máu cục bộ (RR, 2,3; 95% CI, 1,84–2,94), bệnh tim do thiếu máu cục bộ (RR, 1,61; 95% CI, 1,38–1,87) và các biến cố huyết khối thuyên tắc khác. [69–71] Các biến cố sau thường gồm các biến cố huyết khối tắc động mạch (được ưa chuộng hơn thuật ngữ toàn thân), mặc dù huyết khối tắc tĩnh mạch cũng liên quan đến AF.[72,73] Bệnh nhân AF cũng có nguy cơ suy giảm nhận thức cao hơn (tỷ lệ nguy cơ đã điều chỉnh [HR], 1,39; 95% CI, 1,25–1,53)74 và chứng mất trí (OR, 1,6; 95% CI, 1,3–2,0).[75–77] Cần lưu ý rằng hầu hết các nghiên cứu quan sát về các biến cố bất lợi đều có sự kết hợp giữa những bệnh nhân dùng và không dùng OAC. Khi kiểm soát cẩn thận các tác động gây nhiễu của đột quỵ, bệnh đi kèm và OAC, phơi nhiễm AF vẫn có liên quan đáng kể với chứng mất trí do mạch máu (HR, 1,68; 95% CI, 1,33–2,12; P < .001), nhưng không phải bệnh Alzheimer (HR, 0,85; 95% CI, 0,70–1,03; P = .09).[78]Adverse events associated with AF
Tỷ lệ nhập viện do AF thay đổi rất nhiều tùy thuộc vào nhóm dân số được nghiên cứu và có thể bị sai lệch do sai lệch lựa chọn. Trong một RCT của Hà Lan bao gồm những bệnh nhân AF được chẩn đoán lần đầu (trung bình 64 tuổi), tỷ lệ nhập viện do tim mạch là 7,0% đến 9,4% mỗi năm.79 Một nghiên cứu của Úc đã xác định được 473.501 ca nhập viện do AF trong 15 năm theo dõi (300 triệu người-năm), với mức tăng tương đối về số ca nhập viện do AF là 203% trong suốt thời gian nghiên cứu, trái ngược với mức tăng của tất cả các ca nhập viện là 71%. Tỷ lệ nhập viện theo độ tuổi đặc trưng tăng đặc biệt ở các nhóm tuổi lớn hơn.[80]
Rung nhĩ cũng liên quan đến việc tăng tỷ lệ tử vong. Năm 2017, AF góp phần gây ra hơn 250.000 ca tử vong trên toàn cầu, với tỷ lệ tử vong chuẩn hóa theo độ tuổi là 4,0 trên 100.000 người (khoảng không chắc chắn 95% là 3,9–4,2).[81] Nguyên nhân tử vong thường gặp nhất ở những bệnh nhân AF liên quan đến suy tim,[70] với mối quan hệ phức tạp với bệnh tim mạch và không phải tim mạch. [82] Nguy cơ tử vong do mọi nguyên nhân tăng gấp đôi (RR, 1,95; 95% CI, 1,50–2,54),[68] và tử vong do tim mạch (RR, 2,03; 95% CI, 1,79–2,30) [69] ở AF so với nhịp xoang. Ngay cả khi không có các yếu tố nguy cơ huyết khối thuyên tắc chính, tỷ lệ tử vong là 15,5 trên 1000 người-năm ở những người biểu hiện AF, so với 9,4 trên 1000 người-năm không có biểu hiện AF (HR điều chỉnh, 1,44; 95% CI, 1,38–1,50; P < .001).[78] Bệnh nhân bị chảy máu liên quan đến OAC có tỷ lệ tử vong cao hơn, gồm cả chảy máu nhẹ và chảy máu nặng (theo định nghĩa của thang điểm Huyết khối và Cầm máu Quốc tế).[83] Mặc dù dùng OAC, bệnh nhân bị AF vẫn có nguy cơ tử vong cao, điều này làm nổi bật tầm quan trọng của việc chú ý đến bệnh đi kèm.[84]
3.6. Cuồng nhĩ
Cuồng nhĩ (AFL) là một trong những chứng loạn nhịp nhĩ nhanh phổ biến nhất, với tỷ lệ mắc chung là 88 trên 100.000 người-năm, tăng lên 317 trên 100.000 người-năm ở những người trên 50 tuổi.[85] Các yếu tố nguy cơ đối với AFL và AF là tương tự nhau, và hơn một nửa số bệnh nhân mắc AFL sẽ phát triển AF. [85] Các nghiên cứu quan sát cho thấy nguy cơ huyết khối thuyên tắc tăng cao ở AFL.[86] Khi so sánh trực tiếp AFL với AF, một số nghiên cứu cho thấy nguy cơ đột quỵ tương tự và một số nghiên cứu khác cho thấy nguy cơ thấp hơn ở AFL,[87–90] có thể là do gánh nặng bệnh đi kèm khác nhau và tác động của các yếu tố gây nhiễu như triệt phá AFL/AF và chống đông máu (thường dừng lại ở AFL).[91]
4. Lộ trình của bệnh nhân và quản lý AF
4.1. Bệnh nhân làm trung tâm, quản lý AF đa ngành
4.1.1. Bệnh nhân là trung tâm của việc chăm sóc
Một phương pháp tiếp cận lấy bệnh nhân làm trung tâm và tích hợp để quản lý AF có nghĩa là làm việc với một mô hình chăm sóc tôn trọng kinh nghiệm, giá trị, nhu cầu và sở thích của bệnh nhân đối với việc lập kế hoạch, phối hợp và cung cấp dịch vụ chăm sóc. Một thành phần cốt lõi của mô hình này là mối quan hệ điều trị giữa bệnh nhân và nhóm chuyên gia chăm sóc sức khỏe đa ngành (Hình 2). Trong quản lý AF lấy bệnh nhân làm trung tâm, bệnh nhân không được coi là người thụ động tiếp nhận các dịch vụ chăm sóc sức khỏe mà là những người tham gia tích cực làm việc như những đối tác cùng với các chuyên gia chăm sóc sức khỏe. Quản lý AF lấy bệnh nhân làm trung tâm đòi hỏi phải tích hợp tất cả các khía cạnh của quản lý AF. Điều này bao gồm kiểm soát triệu chứng, khuyến nghị về lối sống, hỗ trợ tâm lý xã hội và quản lý các bệnh đi kèm, cùng với phương pháp điều trị y tế tối ưu gồm liệu pháp dược lý, chuyển nhịp tim và can thiệp triệt phá hoặc phẫu thuật (Bảng 9). Các dịch vụ nên được thiết kế để đảm bảo tất cả bệnh nhân đều có thể tiếp cận với một mô hình quản lý AF có tổ chức, gồm các dịch vụ chuyên khoa chăm sóc sức khỏe bậc ba khi được chỉ định (xem Dữ liệu bổ sung trực tuyến, Bảng S1, Bảng bằng chứng 4 và Bảng bằng chứng bổ sung S3). Điều quan trọng không kém là duy trì các lộ trình để bệnh nhân có thể nhanh chóng tái khám với các dịch vụ chuyên khoa khi tình trạng của họ thay đổi.
Bảng 9 Đạt được quản lý AF lấy bệnh nhân làm trung tâm
| • Điều trị tối ưu theo lộ trình AF-CARE, gồm: |
| ∘ [C] Quản lý bệnh đi kèm và yếu tố nguy cơ |
| ∘ [A] Tránh đột quỵ và huyết khối thuyên tắc |
| ∘ [R] Giảm các triệu chứng bằng cách kiểm soát nhịp và tần số |
| ∘ [E] Đánh giá và đánh giá lại động học |
| • Khuyến cáo về sinh hoạt |
| • Hỗ trợ tâm lý xã hội |
| • Giáo dục và nâng cao nhận thức cho bệnh nhân, thành viên gia đình và người chăm sóc |
| • Phối hợp liền mạch giữa chăm sóc ban đầu và chăm sóc AF chuyên khoa |
| Cách triển khai quản lý AF lấy bệnh nhân làm trung tâm: |
| • Quyết định chung |
| • Phương pháp tiếp cận nhóm đa ngành |
| • Giáo dục và trao quyền cho bệnh nhân, nhấn mạnh vào việc tự chăm sóc |
| • Chương trình giáo dục có cấu trúc cho các chuyên gia chăm sóc sức khỏe |
| • Hỗ trợ công nghệ (e-Health, m-Health, y học từ xa)* |
AF: rung nhĩ; AF-CARE: rung nhĩ—[C] Quản lý bệnh đi kèm và yếu tố nguy cơ, [A] Tránh đột quỵ và huyết khối thuyên tắc, [R] Giảm các triệu chứng bằng cách kiểm soát nhịp tim và tốc độ, [E] Đánh giá và đánh giá lại động học.
* e-Health đề cập đến các dịch vụ chăm sóc sức khỏe được cung cấp bằng các phương pháp điện tử; m-Health, đề cập đến các dịch vụ chăm sóc sức khỏe được hỗ trợ bởi các thiết bị di động; và y học từ xa đề cập đến chẩn đoán hoặc điều trị từ xa được hỗ trợ bằng công nghệ viễn thông
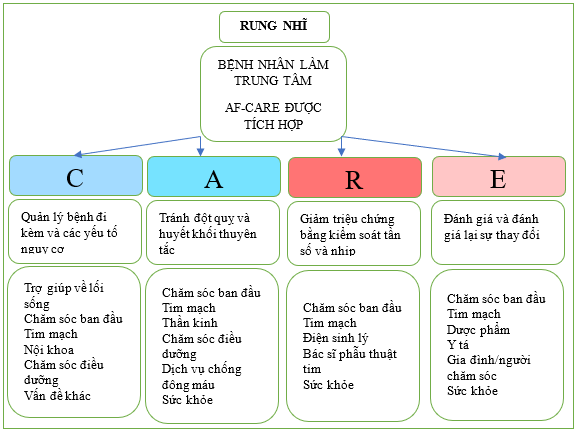
Hình 2. Phương pháp tiếp cận đa ngành đối với việc quản lý AF. Những người chăm sóc chính tham gia vào cộng đồng và các cơ sở bệnh viện để cung cấp dịch vụ chăm sóc tối ưu, lấy bệnh nhân làm trung tâm cho những bệnh nhân sống chung với AF.
AF-CARE, rung nhĩ—[C] Quản lý bệnh đi kèm và yếu tố nguy cơ (Comorbidity and risk factor management), [A] Tránh đột quỵ và huyết khối thuyên tắc (Avoid stroke and thromboembolism), [R] Giảm các triệu chứng bằng cách kiểm soát nhịp và tần số (Reduce symptoms by rate and rhythm control), [E] Đánh giá và đánh giá lại động học (Evaluation and dynamic reassessment)
4.1.2. Giáo dục và quyết định chung
Lời khuyên rõ ràng về cơ sở lý luận cho các phương pháp điều trị, khả năng điều chỉnh phương pháp điều trị và việc ra quyết định chung có thể giúp bệnh nhân sống chung với AF (xem Dữ liệu bổ sung trực tuyến, Bảng S2). [92] Mối quan hệ cởi mở và hiệu quả giữa bệnh nhân và các nhà chuyên môn chăm sóc sức khỏe là rất quan trọng, với việc ra quyết định chung được phát hiện là cải thiện kết quả cho việc quản lý OAC và loạn nhịp. [93,94] Khi sử dụng phương pháp tiếp cận chung, cả bác sĩ lâm sàng và bệnh nhân đều tham gia vào quá trình ra quyết định (ở mức độ mà bệnh nhân ưa chuộng). Thông tin được chia sẻ theo cả hai hướng. Hơn nữa, cả bác sĩ lâm sàng và bệnh nhân đều bày tỏ sở thích của mình và thảo luận về các lựa chọn. Trong số các quyết định điều trị tiềm năng, không có phương pháp điều trị nào cũng là một khả năng. [95] Có một số bộ công cụ có sẵn để tạo điều kiện thuận lợi cho việc này, mặc dù hầu hết đều tập trung vào các quyết định kháng đông. Ví dụ, Bộ công cụ ra quyết định chung (http // afibguide.com, http: // afibguide. com/ clinician) và điểm số Chuyển nhịp tim đường tĩnh mạch thành công cho rung nhĩ (SIC-AF) đã được chứng minh là làm giảm xung đột quyết định so với cách chăm sóc thông thường ở những bệnh nhân bị AF. [93,94] Các tổ chức hỗ trợ bệnh nhân cũng có thể đóng góp quan trọng vào việc cung cấp kiến thức dễ hiểu và có thể hành động được về AF và các phương pháp điều trị (ví dụ: các nhóm hỗ trợ địa phương và các tổ chức từ thiện quốc tế, chẳng hạn như http://afa-international.org). Vì AF là một căn bệnh mãn tính hoặc tái phát ở hầu hết bệnh nhân, nên giáo dục đóng vai trò trung tâm để trao quyền cho bệnh nhân, gia đình và người chăm sóc của họ.
4.1.3. Giáo dục các nhà chuyên môn chăm sóc sức khỏe
Khoảng trống về kiến thức và kỹ năng trên tất cả các lĩnh vực chăm sóc AF luôn được mô tả giữa các bác sĩ tim mạch, bác sĩ thần kinh, bác sĩ chuyên khoa nội khoa, bác sĩ cấp cứu, bác sĩ đa khoa, điều dưỡng và các bác sĩ hành nghề y tế liên quan. [96–98] Các nhà chuyên môn chăm sóc sức khỏe tham gia vào việc quản lý AF đa ngành phải có kiến thức về tất cả các lựa chọn có sẵn để chẩn đoán và điều trị. [99–101] Trong thử nghiệm STEEER-AF, [99] việc tuân thủ thực tế các hướng dẫn thực hành lâm sàng đối với AF trên sáu quốc gia ESC là kém. Những phát hiện này làm nổi bật nhu cầu quan trọng về đào tạo và giáo dục phù hợp cho các chuyên gia chăm sóc sức khỏe.[102]
Giáo dục có mục tiêu cụ thể cho các chuyên gia chăm sóc sức khỏe có thể nâng cao kiến thức và dẫn đến việc sử dụng OAC phù hợp hơn để phòng ngừa huyết khối thuyên tắc. [103] Tuy nhiên, các can thiệp giáo dục cho các nhà cung cấp dịch vụ chăm sóc sức khỏe thường không đủ để tác động bền vững đến hành vi. [104] Có thể cần các công cụ khác, chẳng hạn như phản hồi tích cực, [103] các công cụ hỗ trợ quyết định lâm sàng, [105] tư vấn chuyên gia, [106] hoặc học tập sức khoẻ điện tử.[107]
4.1.4. Quản lý AF toàn diện
Bằng chứng ngày càng tăng về sự khác biệt trong tỷ lệ mắc AF, tỷ lệ lưu hành, các yếu tố nguy cơ, bệnh đi kèm và kết quả theo giới tính. [108] Phụ nữ được chẩn đoán mắc AF thường lớn tuổi hơn, bị tăng huyết áp và suy tim với phân suất tống máu bảo tồn (HFpEF) nhiều hơn và ít được chẩn đoán mắc bệnh động mạch vành (CAD). [109] Các nghiên cứu đăng ký đã báo cáo sự khác biệt về kết quả, với tỷ lệ mắc bệnh và tử vong cao hơn ở phụ nữ, mặc dù những điều này có thể bị ảnh hưởng do tuổi và gánh nặng bệnh đi kèm. [110–112] Phụ nữ mắc AF có thể có nhiều triệu chứng hơn và báo cáo chất lượng cuộc sống thấp hơn. [41,113] Không rõ liệu điều này có liên quan đến việc đánh giá y tế chậm trễ ở phụ nữ hay có sự khác biệt thực sự giữa các giới tính hay không. Mặc dù có nhiều triệu chứng hơn, nhưng phụ nữ ít có khả năng trải qua quá trình triệt phá AF hơn nam giới, mặc dù liệu pháp thuốc chống loạn nhịp dường như có liên quan đến nhiều biến cố loạn nhịp hơn ở phụ nữ.[109] Những quan sát này đòi hỏi phải nghiên cứu thêm về sự khác biệt về giới tính để ngăn ngừa sự chênh lệch và bất bình đẳng trong việc chăm sóc. Các khía cạnh đa dạng khác như tuổi, chủng tộc, dân tộc và các vấn đề chuyển giới, cũng như các yếu tố quyết định xã hội (gồm tình trạng kinh tế xã hội, khuyết tật, trình độ học vấn, hiểu biết về sức khỏe và khu vực nông thôn/thành thị) là những yếu tố quan trọng góp phần gây ra bất bình đẳng cần được xem xét tích cực để cải thiện kết quả cho bệnh nhân.[114]
4.2. Các nguyên tắc của AF-CARE
Hướng dẫn ESC năm 2024 về quản lý AF đã biên soạn và phát triển các phương pháp tiếp cận trước đây để tạo ra các nguyên tắc quản lý nhằm hỗ trợ việc triển khai các hướng dẫn này và do đó cải thiện việc chăm sóc và kết quả của bệnh nhân. Ngày càng có nhiều bằng chứng cho thấy các công cụ hỗ trợ lâm sàng [115–118] có thể hỗ trợ quản lý theo phương pháp tốt nhất, với lưu ý bất kỳ công cụ nào cũng chỉ là hướng dẫn và tất cả bệnh nhân đều cần được quan tâm cá thể hóa. Phương pháp AF-CARE bao gồm nhiều nguyên tắc đã được thiết lập trong việc quản lý AF, nhưng thực hiện theo định dạng có hệ thống, định hướng thời gian với bốn trụ cột điều trị thiết yếu (Hình 3; hình minh họa trung tâm). Quản lý chung với từng bệnh nhân là điểm khởi đầu của phương pháp AF-CARE. Đáng chú ý là phương pháp này tính đến cơ sở bằng chứng ngày càng tăng cho thấy các liệu pháp điều trị AF hiệu quả nhất khi giải quyết được các tình trạng sức khỏe liên quan. Việc tìm kiếm cẩn thận các bệnh đi kèm và các yếu tố nguy cơ [C] này là rất quan trọng và nên được áp dụng cho tất cả các bệnh nhân được chẩn đoán mắc AF. Tiếp theo, cần xem xét việc tránh đột quỵ và huyết khối thuyên tắc [A] ở những bệnh nhân có các yếu tố nguy cơ, tập trung vào việc sử dụng liệu pháp kháng đông máu phù hợp. Sau đó, áp dụng phương pháp giảm các triệu chứng và bệnh tật liên quan đến AF bằng cách sử dụng hiệu quả kiểm soát nhịp tim và nhịp điệu [R], phương pháp này cũng có thể làm giảm thời gian nằm viện hoặc cải thiện tiên lượng ở một số bệnh nhân được chọn. Cần cân nhắc lợi ích tiềm tàng của việc kiểm soát nhịp, cùng với việc xem xét tất cả các nguy cơ liên quan, ở tất cả bệnh nhân tại mỗi điểm tiếp xúc với các chuyên gia chăm sóc sức khỏe. Vì AF và các bệnh đi kèm liên quan thay đổi theo thời gian, nên cần có các mức đánh giá [E] và đánh giá lại khác nhau ở mỗi bệnh nhân và các phương pháp tiếp cận này phải mang tính động. Do sự thay đổi lớn trong đáp ứng với liệu pháp và bệnh sinh lý thay đổi của AF theo tuổi tác và bệnh đi kèm tiến triển, nên việc đánh giá lại cần được đưa vào lộ trình chăm sóc tiêu chuẩn để ngăn ngừa các kết cục bất lợi cho bệnh nhân và cải thiện sức khỏe cộng đồng.
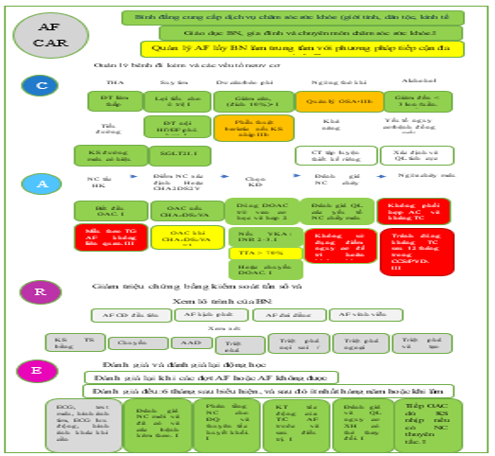
Hình 3. Minh họa trung tâm. Lộ trình bệnh nhân cho AF-CARE (xem Hình 4, 5, 6 và 7 để biết lộ trình [R] cho AF được chẩn đoán lần đầu, kịch phát, dai dẳng và vĩnh viễn).
AF, rung nhĩ; AF-CARE, rung nhĩ—[C] Quản lý bệnh đi kèm và yếu tố nguy cơ, [A] Tránh đột quỵ và huyết khối thuyên tắc, [R] Giảm các triệu chứng bằng cách kiểm soát nhịp tim và tần số, [E] Đánh giá và đánh giá lại động học; CCS: hội chứng vành mạn tính; CHA2DS2-VA: suy tim sung huyết, tăng huyết áp, tuổi ≥75 (2 điểm), đái tháo đường, đột quỵ/thiếu máu cục bộ thoáng qua/huyết khối thuyên tắc động mạch trước đó (2 điểm), bệnh mạch máu, tuổi 65–74; DOAC: thuốc chống đông đường uống trực tiếp; ECG: điện tâm đồ; HFrEF: suy tim có phân suất tống máu giảm; INR: tỷ lệ chuẩn hóa quốc tế của thời gian prothrombin; OAC: thuốc chống đông đường uống; OSA: ngưng thở khi ngủ do tắc nghẽn; PVD: bệnh mạch máu ngoại biên; SGLT2: đồng vận chuyển natri-glucose-2; VKA: chất đối kháng vitamin K. AAD: thuốc chống loạn nhịp.
a Là một phần của quá trình quản lý toàn diện các yếu tố nguy cơ tim mạch chuyển hóa.
AF-CARE dựa trên các Hướng dẫn ESC trước đây, ví dụ như phương pháp tiếp cận tích hợp tập trung vào kết quả năm bước trong Hướng dẫn ESC năm 2016 về quản lý AF, [119] và lộ trình Chăm sóc AF tốt hơn (ABC) trong Hướng dẫn ESC năm 2020 về chẩn đoán và quản lý AF. [120] Việc tổ chức lại thành AF-CARE dựa trên sự phát triển song song của các phương pháp tiếp cận và công nghệ mới (đặc biệt là kiểm soát nhịp), với bằng chứng mới liên tục cho thấy mọi khía cạnh của việc quản lý AF đều hiệu quả hơn khi các bệnh đi kèm và các yếu tố nguy cơ đã được xem xét. Điều này gồm việc quản lý liên quan đến lợi ích của triệu chứng, cải thiện tiên lượng, phòng ngừa huyết khối thuyên tắc và phản ứng với các chiến lược kiểm soát nhịp và tần số. AF-CARE nêu rõ nhu cầu đánh giá và theo dõi cá thể hóa ở mọi bệnh nhân, với phương pháp tiếp cận chủ động tính đến cách bệnh nhân, AF của họ và các bệnh đi kèm liên quan thay đổi theo thời gian. Các nguyên tắc AF-CARE đã được áp dụng cho các lộ trình bệnh nhân khác nhau để dễ dàng triển khai vào chăm sóc lâm sàng thường quy. Điều này gồm việc quản lý AF được chẩn đoán lần đầu (Hình 4), AF kịch phát (Hình 5), AF dai dẳng (Hình 6) và AF vĩnh viễn (Hình 7)
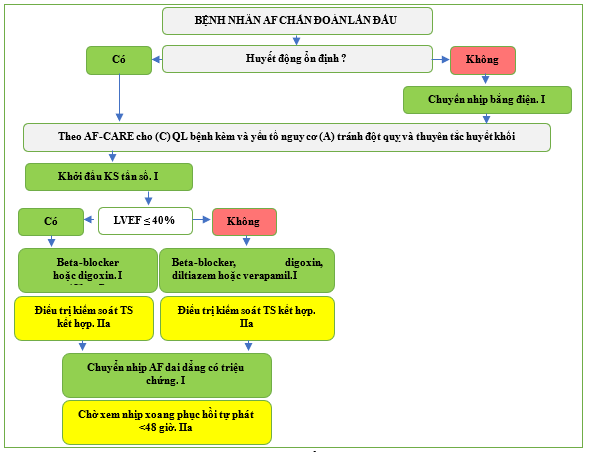
Hình 4. [R] Lộ trình cho bệnh nhân AF được chẩn đoán lần đầu.
AF, rung nhĩ; AF-CARE, Rung nhĩ—[C] Quản lý bệnh đi kèm và yếu tố nguy cơ, [A] Tránh đột quỵ và huyết khối thuyên tắc, [R] Giảm triệu chứng bằng cách kiểm soát tần số và nhịp tim, [E] Đánh giá và đánh giá lại động lực; LVEF: phân suất tống máu thất trái. Sau khi đi theo lộ trình cho AF được chẩn đoán lần đầu, bệnh nhân AF tái phát nên tham gia lộ trình AF-CARE [R] cho AF kịch phát, dai dẳng hoặc vĩnh viễn, tùy thuộc vào loại AF của chúng. TS: tần số. KS: kiểm soát.
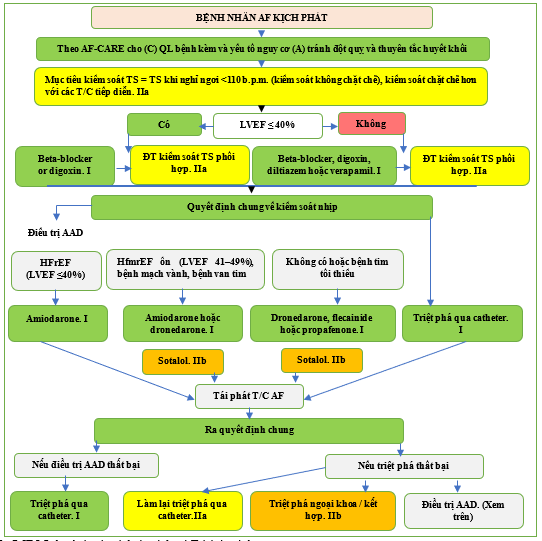
Hình 5 [R] Lộ trình cho bệnh nhân AF kịch phát.
AF: rung nhĩ; AF-CARE: rung nhĩ—[C] Quản lý bệnh đi kèm và yếu tố nguy cơ, [A] Tránh đột quỵ và huyết khối thuyên tắc, [R] Giảm triệu chứng bằng cách kiểm soát tần số và nhịp tim, [E] Đánh giá và đánh giá lại động lực; b.p.m: nhịp mỗi phút; HFmrEF: suy tim có phân suất tống máu giảm nhẹ; HFrEF: suy tim có phân suất tống máu giảm; LVEF: phân suất tống máu thất trái. ĐT: điều trị. T/C: triệu chứng. AAD: thuốc chống loạn nhịp. TS: tần số. a Ở những bệnh nhân HFrEF: Class I nếu có khả năng cao mắc bệnh cơ tim do nhịp tim nhanh; và Class IIa ở những bệnh nhân được chọn để cải thiện tiên lượng.
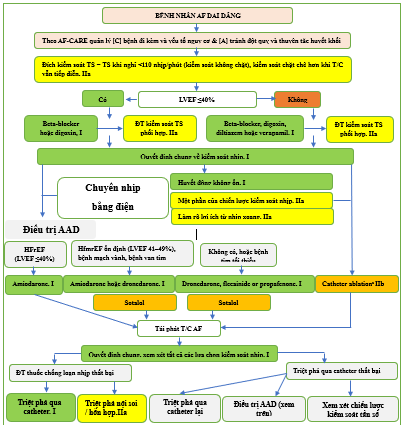
Hình 6 [R] Lộ trình cho bệnh nhân AF dai dẳng.
AF: rung nhĩ; AF-CARE, Rung nhĩ—[C] Quản lý bệnh đi kèm và yếu tố nguy cơ, [A] Tránh đột quỵ và huyết khối thuyên tắc, [R] Giảm triệu chứng bằng cách kiểm soát tần số và nhịp tim, [E] Đánh giá và đánh giá lại động lực; b.p.m: nhịp mỗi phút; HFmrEF: suy tim có phân suất tống máu giảm nhẹ; HFrEF: suy tim có phân suất tống máu giảm; LVEF: phân suất tống máu thất trái. ĐT: điều trị. TS: tần số. T/C: triệu chứng. AAD: thuốc chống loạn nhịp. a Ở những bệnh nhân HFrEF: Class I nếu có khả năng cao mắc bệnh cơ tim do nhịp tim nhanh; và Class IIa ở những bệnh nhân được chọn để cải thiện tiên lượng.
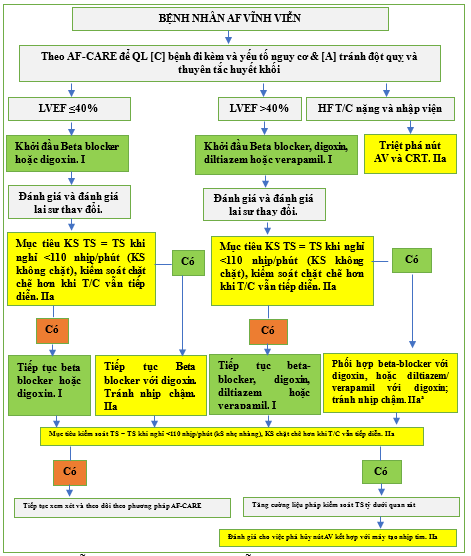
Hình 7. [R] Đường dẫn cho bệnh nhân AF vĩnh viễn.
AF: rung nhĩ; AF-CARE, Rung nhĩ—[C] Quản lý bệnh đi kèm và yếu tố nguy cơ, [A] Tránh đột quỵ và thuyên tắc huyết khối tắc, [R] Giảm triệu chứng bằng cách kiểm soát nhịp tim và tần số, [E] Đánh giá và đánh giá lại động lực; b.p.m: nhịp mỗi phút; CRT: liệu pháp tái đồng bộ tim; HF: suy tim; LVEF: phân suất tống máu thất trái. KS: kiểm soát. TS: tần số. T/C: triệu chứng. AF vĩnh viễn là quyết định chung được đưa ra giữa bệnh nhân và bác sĩ không có kế hoạch thực hiện thêm bất kỳ nỗ lực nào để phục hồi nhịp xoang. a Lưu ý chỉ nên sử dụng kết hợp thuốc chẹn beta với diltiazem hoặc verapamil theo tư vấn của chuyên gia và theo dõi bằng ECG lưu động để kiểm tra.
(Vui lòng xem tiếp trong kỳ sau)
TÀI LIỆU THAM KHẢO
- Giugliano RP, Ruff CT, Braunwald E, Murphy SA, Wiviott SD, Halperin JL, et al. Edoxaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2013;369: 2093–104. https://doi.org/10.1056/NEJMoa1310907
- Granger CB, Alexander JH, McMurray JJ, Lopes RD, Hylek EM, Hanna M, et al. Apixaban versus warfarin in patients with atrial fibrillation. N Engl J Med 2011;365: 981–92. https://doi.org/10.1056/NEJMoa1107039
- Patel MR, Mahaffey KW, Garg J, Pan G, Singer DE, Hacke W, et al. Rivaroxaban versus warfarin in nonvalvular atrial fibrillation. N Engl J Med 2011;365:883–91. https://doi. org/10.1056/NEJMoa1009638
- Stroke prevention in atrial fibrillation study. Final results. Circulation 1991;84:527–39. https://doi.org/10.1161/01.CIR.84.2.527
- Mannina C, Jin Z, Matsumoto K, Ito K, Biviano A, Elkind MSV, et al. Frequency of cardiac arrhythmias in older adults: findings from the subclinical atrial fibrillation and risk of ischemic stroke (SAFARIS) study. Int J Cardiol 2021;337:64–70. https://doi.org/10.1016/j. ijcard.2021.05.006
- Schnabel RB, Pecen L, Ojeda FM, Lucerna M, Rzayeva N, Blankenberg S, et al. Gender differences in clinical presentation and 1-year outcomes in atrial fibrillation. Heart 2017;103:1024–30. https://doi.org/10.1136/heartjnl-2016-310406
- Simantirakis EN, Papakonstantinou PE, Chlouverakis GI, Kanoupakis EM, Mavrakis HE, Kallergis EM, et al. Asymptomatic versus symptomatic episodes in patients with paroxysmal atrial fibrillation via long-term monitoring with implantable loop recorders. Int J Cardiol 2017;231:125–30. https://doi.org/10.1016/j.ijcard.2016.12.025
- Verma A, Champagne J, Sapp J, Essebag V, Novak P, Skanes A, et al. Discerning the incidence of symptomatic and asymptomatic episodes of atrial fibrillation before and after catheter ablation (DISCERN AF): a prospective, multicenter study. JAMA Intern Med 2013;173:149–56. https://doi.org/10.1001/jamainternmed.2013.1561
- Sgreccia D, Manicardi M, Malavasi VL, Vitolo M, Valenti AC, Proietti M, et al. Comparing outcomes in asymptomatic and symptomatic atrial fibrillation: a systematic review and meta-analysis of 81,462 patients. J Clin Med 2021;10:3979. https://doi.org/ 10.3390/jcm10173979
- Holmes DN, Piccini JP, Allen LA, Fonarow GC, Gersh BJ, Kowey PR, et al. Defining clinically important difference in the atrial fibrillation effect on quality-of-life score. Circ Cardiovasc Qual Outcomes 2019;12:e005358. https://doi.org/10.1161/ CIRCOUTCOMES.118.005358
- Jones J, Stanbury M, Haynes S, Bunting KV, Lobban T, Camm AJ, et al. Importance and assessment of quality of life in symptomatic permanent atrial fibrillation: patient focus groups from the RATE-AF trial. Cardiology 2020;145:666–75. https://doi.org/10.1159/ 000511048
- Abu HO, Wang W, Otabil EM, Saczynski JS, Mehawej J, Mishra A, et al. Perception of atrial fibrillation symptoms: impact on quality of life and treatment in older adults. J Am Geriatr Soc 2022;70:2805–17. https://doi.org/10.1111/jgs.17954
- Rienstra M, Vermond RA, Crijns HJ, Tijssen JG, Van Gelder IC; RACE Investigators. Asymptomatic persistent atrial fibrillation and outcome: results of the RACE study. Heart Rhythm 2014;11:939–45. https://doi.org/10.1016/j.hrthm.2014.03.016
- Rienstra M, Hobbelt AH, Alings M, Tijssen JGP, Smit MD, Brugemann J, et al. Targeted therapy of underlying conditions improves sinus rhythm maintenance in patients with persistent atrial fibrillation: results of the RACE 3 trial. Eur Heart J 2018;39:2987–96.
https://doi.org/10.1093/eurheartj/ehx739 - Mulder BA, Van Veldhuisen DJ, Crijns HJ, Tijssen JG, Hillege HL, Alings M, et al. Digoxin in patients with permanent atrial fibrillation: data from the RACE II study. Heart Rhythm 2014;11:1543–50. https://doi.org/10.1016/j.hrthm.2014.06.007
- Kloosterman M, Crijns H, Mulder BA, Groenveld HF, Van Veldhuisen DJ, Rienstra M, et al. Sex-related differences in risk factors, outcome, and quality of life in patients with permanent atrial fibrillation: results from the RACE II study. Europace 2020;22: 1619–27. https://doi.org/10.1093/europace/euz300
- Park YJ, Park JW, Yu HT, Kim TH, Uhm JS, Joung B, et al. Sex difference in atrial fibrillation recurrence after catheter ablation and antiarrhythmic drugs. Heart 2023;109: 519–26. https://doi.org/10.1136/heartjnl-2021-320601
- Kupper N, van den Broek KC, Widdershoven J, Denollet J. Subjectively reported symptoms in patients with persistent atrial fibrillation and emotional distress. Front Psychol 2013;4:192. https://doi.org/10.3389/fpsyg.2013.00192
- Schnabel RB, Michal M, Wilde S, Wiltink J, Wild PS, Sinning CR, et al. Depression in atrial fibrillation in the general population. PLoS One 2013;8:e79109. https://doi.org/ 10.1371/journal.pone.0079109
- Gleason KT, Dennison Himmelfarb CR, Ford DE, Lehmann H, Samuel L, Han HR, et al. Association of sex, age and education level with patient reported outcomes in atrial fibrillation. BMC Cardiovasc Disord 2019;19:85. https://doi.org/10.1186/s12872-019- 1059-6
- Schnabel RB, Pecen L, Rzayeva N, Lucerna M, Purmah Y, Ojeda FM, et al. Symptom burden of atrial fibrillation and its relation to interventions and outcome in Europe. J Am Heart Assoc 2018;7:e007559. https://doi.org/10.1161/JAHA.117.007559
- Wynn GJ, Todd DM, Webber M, Bonnett L, McShane J, Kirchhof P, et al. The European Heart Rhythm Association symptom classification for atrial fibrillation: validation and improvement through a simple modification. Europace 2014;16:965–72. https://doi. org/10.1093/europace/eut395
- Kotecha D, Bunting KV, Gill SK, Mehta S, Stanbury M, Jones JC, et al. Effect of digoxin vs bisoprolol for heart rate control in atrial fibrillation on patient-reported quality of life: the RATE-AF randomized clinical trial. JAMA 2020;324:2497–508. https://doi.org/10. 1001/jama.2020.23138
- Kotecha D, Ahmed A, Calvert M, Lencioni M, Terwee CB, Lane DA. Patient-reported outcomes for quality of life assessment in atrial fibrillation: a systematic review of measurement properties. PLoS One 2016;11:e0165790. https://doi.org/10.1371/ journal.pone.0165790
- Mantovan R, Macle L, De Martino G, Chen J, Morillo CA, Novak P, et al. Relationship of quality of life with procedural success of atrial fibrillation (AF) ablation and postablation AF burden: substudy of the STAR AF randomized trial. Can J Cardiol 2013;29:1211–7.
https://doi.org/10.1016/j.cjca.2013.06.006 - Samuel M, Khairy P, Champagne J, Deyell MW, Macle L, Leong-Sit P, et al. Association of atrial fibrillation burden with health-related quality of life after atrial fibrillation ablation: substudy of the cryoballoon vs contact-force atrial fibrillation ablation (CIRCA-DOSE) randomized clinical trial. JAMA Cardiol 2021;6:1324–8. https://doi. org/10.1001/jamacardio.2021.3063
- Sandhu RK, Smigorowsky M, Lockwood E, Savu A, Kaul P, McAlister FA. Impact of electrical cardioversion on quality of life for the treatment of atrial fibrillation. Can J Cardiol 2017;33:450–5. https://doi.org/10.1016/j.cjca.2016.11.013
- Terricabras M, Mantovan R, Jiang CY, Betts TR, Chen J, Deisenhofer I, et al. Association between quality of life and procedural outcome after catheter ablation for atrial fibrillation: a secondary analysis of a randomized clinical trial. JAMA Netw Open 2020;3:
e2025473. https://doi.org/10.1001/jamanetworkopen.2020.25473 - Zenger B, Zhang M, Lyons A, Bunch TJ, Fang JC, Freedman RA, et al. Patient-reported outcomes and subsequent management in atrial fibrillation clinical practice: results from the Utah mEVAL AF program. J Cardiovasc Electrophysiol 2020;31:3187–95.
https://doi.org/10.1111/jce.14795 - Arbelo E, Aktaa S, Bollmann A, D’Avila A, Drossart I, Dwight J, et al. Quality indicators for the care and outcomes of adults with atrial fibrillation. Europace 2021;23:494–5. https://doi.org/10.1093/europace/euaa253
- Kvist LM, Vinter N, Urbonaviciene G, Lindholt JS, Diederichsen ACP, Frost L. Diagnostic accuracies of screening for atrial fibrillation by cardiac nurses versus radiographers. Open Heart 2019;6:e000942. https://doi.org/10.1136/openhrt-2018-000942
- Hijazi Z, Oldgren J, Siegbahn A, Granger CB, Wallentin L. Biomarkers in atrial fibrillation: a clinical review. Eur Heart J 2013;34:1475 80. https://doi.org/10.1093/eurheartj/ eht024
- Berg DD, Ruff CT, Morrow DA. Biomarkers for risk assessment in atrial fibrillation. Clin Chem 2021;67:87–95. https://doi.org/10.1093/clinchem/hvaa298
- Tops LF, Schalij MJ, Bax JJ. Imaging and atrial fibrillation: the role of multimodality imaging in patient evaluation and management of atrial fibrillation. Eur Heart J 2010;31: 542–51. https://doi.org/10.1093/eurheartj/ehq005
- Obeng-Gyimah E, Nazarian S. Advancements in imaging for atrial fibrillation ablation: is there a potential to improve procedural outcomes? J Innov Card Rhythm Manag 2020; 11:4172–8. https://doi.org/10.19102/icrm.2020.110701
- Romero J, Husain SA, Kelesidis I, Sanz J, Medina HM, Garcia MJ. Detection of left atrial appendage thrombus by cardiac computed tomography in patients with atrial fibrillation: a meta-analysis. Circ Cardiovasc Imaging 2013;6:185–94. https://doi.org/10.1161/ CIRCIMAGING.112.000153
- Bisbal F, Benito E, Teis A, Alarcón F, Sarrias A, Caixal G, et al. Magnetic resonance imaging-guided fibrosis ablation for the treatment of atrial fibrillation: the ALICIA trial. Circ Arrhythm Electrophysiol 2020;13:e008707. https://doi.org/10.1161/CIRCEP.120. 008707
- Khurram IM, Habibi M, Gucuk Ipek E, Chrispin J, Yang E, Fukumoto K, et al. Left atrial LGE and arrhythmia recurrence following pulmonary vein isolation for paroxysmal and persistent AF. JACC Cardiovasc Imaging 2016;9:142–8. https://doi.org/10.1016/j.jcmg. 2015.10.015
- Marrouche NF, Wilber D, Hindricks G, Jais P, Akoum N, Marchlinski F, et al. Association of atrial tissue fibrosis identified by delayed enhancement MRI and atrial fibrillation catheter ablation: the DECAAF study. JAMA 2014;311:498–506. https:// doi.org/10.1001/jama.2014.3
- Roney CH, Sillett C, Whitaker J, Lemus JAS, Sim I, Kotadia I, et al. Applications of multimodality imaging for left atrial catheter ablation. Eur Heart J Cardiovasc Imaging 2021; 23:31–41. https://doi.org/10.1093/ehjci/jeab205
- Potter A, Augustine DX, Ingram TE. Referring for echocardiography: when not to test. Br J Gen Pract 2021;71:333–4. https://doi.org/10.3399/bjgp21X716441
- Troughton RW, Asher CR, Klein AL. The role of echocardiography in atrial fibrillation and cardioversion. Heart 2003;89:1447–54. https://doi.org/10.1136/heart.89.12.1447
- Odutayo A, Wong CX, Hsiao AJ, Hopewell S, Altman DG, Emdin CA. Atrial fibrillation and risks of cardiovascular disease, renal disease, and death: systematic review and meta-analysis. BMJ 2016;354:i4482. https://doi.org/10.1136/bmj.i4482
- Ruddox V, Sandven I, Munkhaugen J, Skattebu J, Edvardsen T, Otterstad JE. Atrial fibrillation and the risk for myocardial infarction, all cause mortality and heart failure: a systematic review and meta-analysis. Eur J Prev Cardiol 2017;24:1555–66. https://doi. org/10.1177/2047487317715769
- Bassand JP, Accetta G, Al Mahmeed W, Corbalan R, Eikelboom J, Fitzmaurice DA, et al. Risk factors for death, stroke, and bleeding in 28,628 patients from the GARFIELD-AF registry: rationale for comprehensive management of atrial fibrillation. PLoS One 2018; 13:e0191592. https://doi.org/10.1371/journal.pone.0191592
- Bassand JP, Accetta G, Camm AJ, Cools F, Fitzmaurice DA, Fox KA, et al. Two-year outcomes of patients with newly diagnosed atrial fibrillation: results from GARFIELD-AF. Eur Heart J 2016;37:2882–9. https://doi.org/10.1093/eurheartj/ ehw233
- Hornestam B, Adiels M, Wai Giang K, Hansson PO, Björck L, Rosengren A. Atrial fibrillation and risk of venous thromboembolism: a Swedish nationwide registry study. Europace 2021;23:1913–21. https://doi.org/10.1093/europace/euab180
- Lutsey PL, Norby FL, Alonso A, Cushman M, Chen LY, Michos ED, et al. Atrial fibrillation and venous thromboembolism: evidence of bidirectionality in the atherosclerosis risk in communities study. J Thromb Haemost 2018;16:670–9. https://doi.org/10.
1111/jth.13974 - Koh YH, Lew LZW, Franke KB, Elliott AD, Lau DH, Thiyagarajah A, et al. Predictive role of atrial fibrillation in cognitive decline: a systematic review and meta-analysis of 2.8 million individuals. Europace 2022;24:1229–39. https://doi.org/10.1093/europace/
euac003 - Papanastasiou CA, Theochari CA, Zareifopoulos N, Arfaras-Melainis A, Giannakoulas G, Karamitsos TD, et al. Atrial fibrillation is associated with cognitive impairment, allcause dementia, vascular dementia, and Alzheimer’s disease: a systematic review and meta-analysis. J Gen Intern Med 2021;36:3122–35. https://doi.org/10.1007/s11606- 021-06954-8
- Giannone ME, Filippini T, Whelton PK, Chiari A, Vitolo M, Boriani G, et al. Atrial fibrillation and the risk of early-onset dementia: a systematic review and meta-analysis. J Am Heart Assoc 2022;11:e025653. https://doi.org/10.1161/JAHA.122.025653
- Zuin M, Roncon L, Passaro A, Bosi C, Cervellati C, Zuliani G. Risk of dementia in patients with atrial fibrillation: short versus long follow-up. A systematic review and meta-analysis. Int J Geriatr Psychiatry 2021;36:1488–500. https://doi.org/10.1002/gps. 5582
- Mobley AR, Subramanian A, Champsi A, Wang X, Myles P, McGreavy P, et al. Thromboembolic events and vascular dementia in patients with atrial fibrillation and low apparent stroke risk. Nat Med 2024. https://doi.org/10.1038/s41591-024- 03049-9.
79. Wijtvliet E, Tieleman RG, van Gelder IC, Pluymaekers N, Rienstra M, Folkeringa RJ, et al. Nurse-led vs. usual-care for atrial fibrillation. Eur Heart J 2020;41:634–41. https://doi.org/10.1093/eurheartj/ehz666 - Wong CX, Brooks AG, Lau DH, Leong DP, Sun MT, Sullivan T, et al. Factors associated with the epidemic of hospitalizations due to atrial fibrillation. Am J Cardiol 2012;110: 1496–9. https://doi.org/10.1016/j.amjcard.2012.07.011
- Dai H, Zhang Q, Much AA, Maor E, Segev A, Beinart R, et al. Global, regional, and national prevalence, incidence, mortality, and risk factors for atrial fibrillation, 1990– 2017: results from the Global Burden of Disease Study 2017. Eur Heart J Qual Care Clin Outcomes 2021;7:574–82. https://doi.org/10.1093/ehjqcco/qcaa061
- Țica O, Țica O, Bunting KV, deBono J, Gkoutos GV, Popescu MI, et al. Post-mortem examination of high mortality in patients with heart failure and atrial fibrillation. BMC Med 2022;20:331. https://doi.org/10.1186/s12916-022-02533-8
- Bassand JP, Virdone S, Badoz M, Verheugt FWA, Camm AJ, Cools F, et al. Bleeding and related mortality with NOACs and VKAs in newly diagnosed atrial fibrillation: results from the GARFIELD-AF registry. Blood Adv 2021;5:1081–91. https://doi.org/10.1182/ bloodadvances.2020003560
84. Pokorney SD, Piccini JP, Stevens SR, Patel MR, Pieper KS, Halperin JL, et al. Cause of death and predictors of all-cause mortality in anticoagulated patients with nonvalvular atrial fibrillation: data from ROCKET AF. J Am Heart Assoc 2016;5:e002197. https://doi.
org/10.1161/JAHA.115.002197
85. Granada J, Uribe W, Chyou PH, Maassen K, Vierkant R, Smith PN, et al. Incidence and predictors of atrial flutter in the general population. J Am Coll Cardiol 2000;36:2242–6. https://doi.org/10.1016/S0735-1097(00)00982-7 - Vadmann H, Nielsen PB, Hjortshoj SP, Riahi S, Rasmussen LH, Lip GY, et al. Atrial flutter and thromboembolic risk: a systematic review. Heart 2015;101:1446–55. https:// doi.org/10.1136/heartjnl-2015-307550
- Lelorier P, Humphries KH, Krahn A, Connolly SJ, Talajic M, Green M, et al. Prognostic differences between atrial fibrillation and atrial flutter. Am J Cardiol 2004;93:647–9. https: // doi.org /10.1016 /j.amjcard. 2003.11.042
- Biblo LA, Yuan Z, Quan KJ, Mackall JA, Rimm AA. Risk of stroke in patients with atrial flutter. Am J Cardiol 2001;87:346–9, A9. https://doi.org/10.1016/S0002-9149(00)
01374-6
89. Corrado G, Sgalambro A, Mantero A, Gentile F, Gasparini M, Bufalino R, et al. Thromboembolic risk in atrial flutter. The FLASIEC (FLutter Atriale Società Italiana di Ecografia Cardiovascolare) multicentre study. Eur Heart J 2001;22:1042–51. https://doi.org/10.1053/euhj.2000.2427
90. Lin YS, Chen TH, Chi CC, Lin MS, Tung TH, Liu CH, et al. Different implications of heart failure, ischemic stroke, and mortality between nonvalvular atrial fibrillation and atrial flutter–a view from a national cohort study. J Am Heart Assoc 2017;6: e006406. https://doi.org/10.1161/JAHA.117.006406 - Giehm-Reese M, Johansen MN, Kronborg MB, Jensen HK, Gerdes C, Kristensen J, et al. Discontinuation of oral anticoagulation and risk of stroke and death after ablation for typical atrial flutter: a nation-wide Danish cohort study. Int J Cardiol 2021;333:110–6.
https://doi.org/10.1016/j.ijcard.2021.02.057 - Gallagher C, Rowett D, Nyfort-Hansen K, Simmons S, Brooks AG, Moss JR, et al. Patient-centered educational resources for atrial fibrillation. JACC Clin Electrophysiol 2019;5:1101–14. https://doi.org/10.1016/j.jacep.2019.08.007
- Chung MK, Fagerlin A, Wang PJ, Ajayi TB, Allen LA, Baykaner T, et al. Shared decision making in cardiac electrophysiology procedures and arrhythmia management. Circ Arrhythm Electrophysiol 2021;14:e007958. https :// doi.org /10.1161/CIRCEP. 121. 007958
- Wang PJ, Lu Y, Mahaffey KW, Lin A, Morin DP, Sears SF, et al. A randomized clinical trial to evaluate an atrial fibrillation stroke prevention shared decision-making pathway. J Am Heart Assoc 2022;12:e028562. https://doi.org/10.1161/JAHA.122.028562
- Seaburg L, Hess EP, Coylewright M, Ting HH, McLeod CJ, Montori VM. Shared decision making in atrial fibrillation: where we are and where we should be going. Circulation 2014;129:704–10. https:// doi.org / 10.1161 / CIRCULATIONAHA .113. 004498
- Zhang J, Lenarczyk R, Marin F, Malaczynska-Rajpold K, Kosiuk J, Doehner W, et al. The interpretation of CHA2DS2-VASc score components in clinical practice: a joint survey by the European Heart Rhythm Association (EHRA) scientific initiatives committee, the EHRA young electrophysiologists, the Association of Cardiovascular Nursing and Allied Professionals, and the European Society of Cardiology council on stroke.Europace 2021;23:314–22. https://doi.org/10.1093/europace/euaa358
- Omoush A, Aloush S, Albashtawy M, Rayan A, Alkhawaldeh A, Eshah N, et al. Nurses’ knowledge of anticoagulation therapy for atrial fibrillation patients: effectiveness of an educational course. Nurs Forum 2022;57:825–32. https://doi.org/10.1111/nuf.12770
- Heidbuchel H, Dagres N, Antz M, Kuck KH, Lazure P, Murray S, et al. Major knowledge gaps and system barriers to guideline implementation among European physicians treating patients with atrial fibrillation: a European Society of Cardiology international educational needs assessment. Europace 2018;20:1919–28. https://doi.org/10.1093/ europace/euy039
- Bunting KV, Van Gelder IC, Kotecha D. STEEER-AF: a cluster-randomized education trial from the ESC. Eur Heart J 2020;41:1952–4. https://doi.org/10.1093/eurheartj/ ehaa421
- Tanner FC, Brooks N, Fox KF, Gonçalves L, Kearney P, Michalis L, et al. ESC core curriculum for the cardiologist. Eur Heart J 2020;41:3605–92. https://doi.org/10.1093/ eurheartj/ehaa641
- Astin F, Carroll D, De Geest S, Fernandez-Oliver AL, Holt J, Hinterbuchner L, et al. A core curriculum for the continuing professional development of nurses working in cardiovascular settings: developed by the education committee of the Council on Cardiovascular Nursing and Allied Professions (CCNAP) on behalf of the European Society of Cardiology. Eur J Cardiovasc Nurs 2015;14:S1–17. https://doi.org/10.1177/ 1474515115580905
- Sterlinski M, Bunting KV, Boriani G, Boveda S, Guasch E, Mont L, et al. STEEER-AF Trial Team. Design and deployment of the STEEER-AF trial to evaluate and improve guideline adherence: a cluster-randomised trial by the European Society of Cardiology and European Heart Rhythm Association. Europace 2024:euae178. https://doi.org/ 10.1093/europace/euae178
- Vinereanu D, Lopes RD, Bahit MC, Xavier D, Jiang J, Al-Khalidi HR, et al. A multifaceted intervention to improve treatment with oral anticoagulants in atrial fibrillation (IMPACT-AF): an international, cluster-randomised trial. Lancet 2017;390:1737–46
https://doi.org/10.1016/S0140-6736(17)32165-7 - Franchi C, Antoniazzi S, Ardoino I, Proietti M, Marcucci M, Santalucia P, et al. Simulation-based education for physicians to increase oral anticoagulants in hospitalized elderly patients with atrial fibrillation. Am J Med 2019;132:e634–47. https://doi. org/10.1016/j.amjmed.2019.03.052
- Baicus C, Delcea C, Dima A, Oprisan E, Jurcut C, Dan GA. Influence of decision aids on oral anticoagulant prescribing among physicians: a randomised trial. Eur J Clin Invest 2017;47:649–58. https://doi.org/10.1111/eci.12786
- Ono F, Akiyama S, Suzuki A, Ikeda Y, Takahashi A, Matsuoka H, et al. Impact of care coordination on oral anticoagulant therapy among patients with atrial fibrillation in routine clinical practice in Japan: a prospective, observational study. BMC Cardiovasc Disord 2019;19:235. https://doi.org/10.1186/s12872-019-1216-y
- Ferguson C, Hickman LD, Phillips J, Newton PJ, Inglis SC, Lam L, et al. An mHealth intervention to improve nurses’ atrial fibrillation and anticoagulation knowledge and practice: the EVICOAG study. Eur J Cardiovasc Nurs 2019;18:7–15. https://doi.org/ 10.1177/1474515118793051
- Lip GY, Laroche C, Popescu MI, Rasmussen LH, Vitali-Serdoz L, Dan GA, et al. Improved outcomes with European Society of Cardiology guideline-adherent antithrombotic treatment in high-risk patients with atrial fibrillation: a report from the EORP-AF general pilot registry. Europace 2015;17:1777–86. https://doi.org/10.1093/ europace/euv269
- Linde C, Bongiorni MG, Birgersdotter-Green U, Curtis AB, Deisenhofer I, Furokawa T, et al. Sex differences in cardiac arrhythmia: a consensus document of the European Heart Rhythm Association, endorsed by the Heart Rhythm Society and Asia Pacific
Heart Rhythm Society. Europace 2018;20:1565–1565ao. https://doi.org/10.1093/ europace/euy067 - Camm AJ, Accetta G, Al Mahmeed W, Ambrosio G, Goldhaber SZ, Haas S, et al. Impact of gender on event rates at 1 year in patients with newly diagnosed non-valvular atrial fibrillation: contemporary perspective from the GARFIELD-AF registry. BMJ Open 2017;7:e014579. https://doi.org/10.1136/bmjopen-2016-014579
- Emdin CA, Wong CX, Hsiao AJ, Altman DG, Peters SA, Woodward M, et al. Atrial fibrillation as risk factor for cardiovascular disease and death in women compared with men: systematic review and meta-analysis of cohort studies. BMJ 2016;532: h7013. https://doi.org/10.1136/bmj.h7013
- Tomasdottir M, Friberg L, Hijazi Z, Lindback J, Oldgren J. Risk of ischemic stroke and utility of CHA2 DS2 -VASc score in women and men with atrial fibrillation. Clin Cardiol 2019;42:1003–9. https://doi.org/10.1002/clc.23257
- Kloosterman M, Chua W, Fabritz L, Al-Khalidi HR, Schotten U, Nielsen JC, et al. Sex differences in catheter ablation of atrial fibrillation: results from AXAFA-AFNET 5.Europace 2020;22:1026–35. https://doi.org/10.1093/europace/euaa015
- Benjamin EJ, Thomas KL, Go AS, Desvigne-Nickens P, Albert CM, Alonso A, et al. Transforming atrial fibrillation research to integrate social determinants of health: a national heart, lung, and blood institute workshop report. JAMA Cardiol 2023;8:182–91. https://doi.org/10.1001/jamacardio.2022.4091
- Karlsson LO, Nilsson S, Bang M, Nilsson L, Charitakis E, Janzon M. A clinical decision support tool for improving adherence to guidelines on anticoagulant therapy in patients with atrial fibrillation at risk of stroke: a cluster-randomized trial in a Swedish primary care setting (the CDS-AF study). PLoS Med 2018;15:e1002528. https://doi. org/10.1371/journal.pmed.1002528
- Biersteker TE, Schalij MJ, Treskes RW. Impact of mobile health devices for the detection of atrial fibrillation: systematic review. JMIR Mhealth Uhealth 2021;9:e26161. https: // doi.org/ 10.2196 /26161
- Romiti GF, Pastori D, Rivera-Caravaca JM, Ding WY, Gue YX, Menichelli D, et al. Adherence to the ‘atrial fibrillation better care’ pathway in patients with atrial fibrillation: impact on clinical outcomes—a systematic review and meta-analysis of 285,000 patients. Thromb Haemost 2022;122:406–14. https://doi.org/10.1055/a-1515-9630
- Gallagher C, Elliott AD, Wong CX, Rangnekar G, Middeldorp ME, Mahajan R, et al. Integrated care in atrial fibrillation: a systematic review and meta-analysis. Heart 2017;103:1947–53. https://doi.org/10.1136/heartjnl-2016-310952
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J 2016;37:2893–962. https://doi.org/10.1093/eurheartj/ehw210
- Hindricks G, Potpara T, Dagres N, Arbelo E, Bax JJ, Blomström-Lundqvist C, et al. 2020 ESC Guidelines for the diagnosis and management of atrial fibrillation developed in collaboration with the European Association for Cardio-Thoracic Surgery (EACTS): the task force for the diagnosis and management of atrial fibrillation of the European Society of Cardiology (ESC) developed with the special contribution of the European Heart Rhythm Association (EHRA) of the ESC. Eur Heart J 2021; 42:373–498. https://doi.org/10.1093/eurheartj/ehaa 612







