BS. TRẦN MINH ĐỨC
BS. NGUYỄN THANH HIỀN
| Những từ viết tắt
ACEi (Angiotesin-Converting Enzyme inbihitor): Ức chế men chuyển Angiotensin. AHA/ACC/HFSA (American Heart Association/American College of Cardiology/Heart Failure of America): Hội Tim Hoa Kỳ/Trường môn Tim Hoa Kỳ/Hội Suy Tim Hoa Kỳ. ARB (Angiotensin-Receptor Blocker): Chẹn thụ thể Angiotensin. ARNI (Angiotensin receptor nephrilysin inbihitor): Ức chế nephrilysin thụ thể Angiotensin. BN: Bệnh nhân. CO (Cardiac Output): Cung lượng tim. ESC (European Society Cardiology): Hội Tim học Châu Âu. HFmrEF (Heart Failure with mild reduced Ejection Fraction): Suy tim với phân suất tống máu giảm nhẹ. HFpEF (Heart Failure with preserved Ejection Fraction): Suy tim với phân suất tống máu bảo tồn. HFrEF (Heart Failure with reduced Ejection Fraction): Suy tim với phân suất tống máu giảm. ICD (Implantable Cardioverter Defibrillator): Máy phá rung trong tim. LVEF (Left Ventricular Ejection Fraction): Phân suất tống máu thất trái. IABP (Intra Aortic Balloon Pump) Bóng đối xung động mạch chủ.
|
CABG (Coronary artery bypass graft): Phẫu thuật bắc cầu chủ vành.
MRA (Mineralcorticoid Receptor Antagonist): Đối kháng thụ thể mineralcorticoid. NMCT: Nhồi máu cơ tim. PCI (percutaneous coronary intervention): Can thiệp mạch vành qua da. RAAS (Renin angiotensin aldosterone system): Hệ Renin angiotensin aldosterone. SGLT2i (Sodium GLucose Transporter 2 inbihitor): Ức chế đồng vận chuyển natri- glucose 2. ST: Suy tim. STEMI (ST Elevation Myocardial Infraction): NMCT cấp có ST chênh lên. NSTEMI (Non-ST Elevation Myocardial Infraction): NMCT cấp không có ST chênh lên. LVEDV (Left Ventricular End Diastolic Volume): Thể tích thất trái cuối kỳ tâm trương. MRI (Magnetic Resonance Imaging): Hình ảnh cộng hưởng từ. CRP (C reactive Protein): Protein hoạt hóa C. MACE (Major Adverse Cardiac Event): Biến cốtim mạch chính. SPECT (Single Photon Emission Computed Tomography): Chụp vi tính cắt lớp phóng xạ đơn photon. CMR (Cardiac Magnetic Resonance): Cộng hưởng từ tim.
|
- Dịch tễ học và sinh lý bệnh của ST sau NMCT
Trong hơn 2 thập kỷ qua, mặc dù có những tiến bộ rõ rệt trong điều trị, tuy nhiên bệnh mạch vành và NMCTvẫn là nguyên nhân thường gặp nhất đưa đến tình trạng ST. Trong thực hành lâm sàng, để đơn giản hóa trong việc quản lý, điều trị và tiên lượng, dựa vào những tiến trình theo thời gian của NMCT và sự phát triển ST sau đó, các nhà lâm sàng chia thành 3 thể khác biệt dựa trên sinh lý bệnh, đặc điểm lâm sàng và kết cục: (1) ST khởi phát ngay tại thời điểm NMCT, (2) ST phát triển trong tiến trình nằm viện vì NMCT, (3) ST khởi phát sau xuất viện từ lần nhập viện trước đó (hình 1)[2], [6,7]. Bên cạnh đó, còn có một thể khác là BN có ST mạn trước đó, nay nhập viện vì đợt cấp mất bù của ST với yếu tố thúc đẩy là NMCT. Thể này có tiên lượng kém hơn do có nhiều bệnh đồng mắc, lớn tuổi, đa số là nữ giới, đưa đến tình trạng tái nhập viện và tử vong nhiều hơn so với các thể được nhắc trước đó[5]. Tuy nhiên, trong khuôn khổ của bài viết, chúng tôi chỉ xin phép đề cập đến các thể ST phát triển sau NMCT.
Hình 1. Tiến trình sinh lý bệnh của ST sau NMCT[7
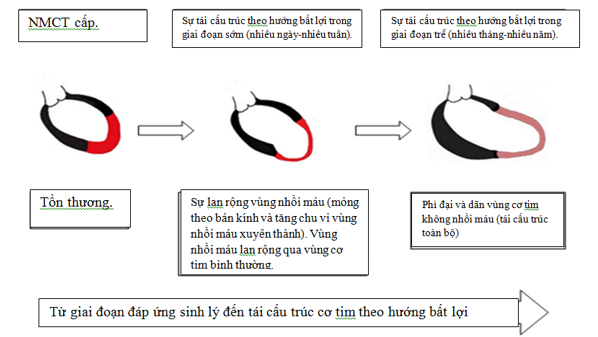
1.1 ST phát triển từ thời điểm nhập viện vì NMCT:
Có 2 cơ chế chính trong giai đoạn cấp tính này: cơ chế Frank-Starling và tăng hoạt động hệ thống thần kinh thể dịch (hình 2). NMCT được đặc trưng là sự hoại tử tế bào cơ tim, đưa đến tình trạng suy bơm cấp tính, giảm CO. Chính vì thế, ở kỳ tâm thu tiếp theo, LVEDV tăng để bù trừ cho sự giảm CO. Tuy nhiên, về lâu dài, chỉ mình cơ chế Frank-Starling là không đủ, và hệ thống thần kinh giao cảm và renin-angiotensin-aldosterone cũng đóng góp vào quá trình này[4].
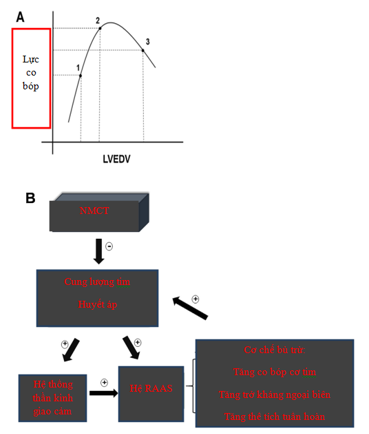
Hình 2. Đáp ứng pha cấp trong NMCT. Đặc trưng của NMCT là sự hoại tử tế bào cơ tim do việc cung cấp oxy bị giảm bởi sự tắc nghẽn mạch vành. Việc giảm CO và huyết áp đã thúc đẩy nhiều cơ chế bù trừ để ngăn chặn sự trụy tuần hoàn. (A) Mô tả cơ chế của hiện tượng Frank-Starling, cho thấy đường cong mối quan hệ giữa thể tích-áp lực. Chức năng co bóp của cơ tim thay đổi theo LVEDV, (điểm 1-2), thất trái căng lên khi LVEDV tăng, điều đó đồng nghĩa lực co bóp cơ tim tăng lên. Tuy nhiên khi thất trái căng quá mức (điểm 2-3), lực co bóp lại giảm xuống. Trong quá trình suy bơm xảy ra đột ngột sau NMCT, LVEF giảm, đưa đếm giảm CO và LVEDV. Để tái lập CO trong chu chuyển tim tiếp theo, LVEDV tăng để bù trừ CO. (B) Cơ chế bù trừ của hệ thống thần kinh giao cảm và hệ renin-angiotensin-aldosterone khi giảm CO và huyết áp, từ đó làm tăng co bóp cơ tim, tăng trở kháng mạch máu ngoại biên, tăng thể tích tuần hoàn[4].
Bên cạnh đó, còn có các yếu tố như tổn thương cơ tim do hoại tử, hiện tượng choáng váng cơ tim, biến chứng cơ học như đứt cơ trụ, thủng vách liên thất, vỡ thành tự do (hình 3). Trong vòng 30 phút từ khi xuất hiện thiếu máu, cấu trúc cơ tim có sự thay đổi và phù, đưa đến sự tiến triển là chết tế bào cơ tim sau 3 giờ thiếu máu. Tái tưới máu bản thân như là con sóng thứ 2 đưa đến tổn thương thông qua giải phóng các gốc oxy hóa tự do. Mặc dù đạt được tái tưới máu thượng tâm mạc thành công, thuyên tắc do những mảnh vỡ huyết khối có thể đưa đến rối loạn chức năng vi mạch tiến triển và thiếu máu cơ tim. Hiện tượng đáp ứng viêm, tình trạng ST có trước đó, bệnh đồng mắc như thiếu máu, bệnh thận mạn, bệnh phổi tắc nghẽn mạn tính, là những yếu tố khởi kích, cũng đóng vai trò sự chết tế bào, đưa đến sự phát triển ST[4].
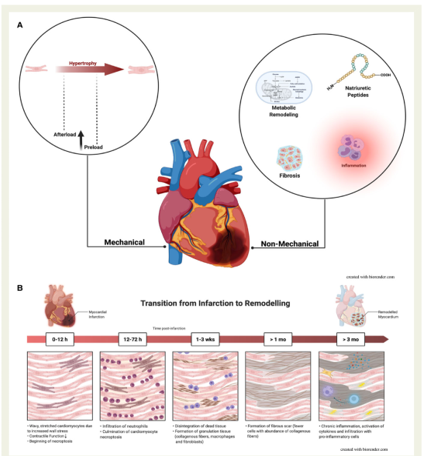
Hình 3. (A) Sinh lý bệnh của tái cấu trúc thất trái sau NMCT. Bên trái là tăng hậu tải kéo dài, đưa đến tăng tiền tải, thúc đẩy lực tăng cơ học của mô, hoạt hóa tiến trình phì đại đưa đến tăng trưởng tế bào cơ và tái cấu trúc. Bên phải là rối loạn chuyển hóa, đưa đến việc sản xuất năng lượng không tối ưu (tái cấu trúc chuyển hóa), hoạt hóa hệ thần kinh giao cảm và renin-angiotensin-aldosterone thông qua peptide bài niệu natri, hoạt hóa tiền viêm, thay đổi chất nền ngoại bào đưa đến xơ hóa cơ tim, thúc đẩy tiến trình mở rộng tái cấu trúc thất trái sau NMCT. (B) Thay đổi mô học của tim theo quá trình NMCT. Quá tải áp lực và thể tích đưa đến căng thành cơ tim và giảm chức năng thất, thâm nhiễm các tế bào miễn dịch đưa đến tạo xơ và chết tế bào cơ tim. Quá trình viêm mạn và các yếu tố kích hoạt khác là môi trường cho sự phát triển chất nền ngoại bào và thúc đẩy tái cấu trúc mạn tính[3].
Trong khi tần suất ST ngay tại thời điểm NMCT tăng lên (từ 4% trong giai đoạn 1992-1996 lên 12-13% trong gia đoạn 2001-2011), tỷ lệ ST trong thời gian nằm viện giảm (từ 39% đến 4-28%). Tỷ lệ ST ngay tại thời điểm NMCT tăng lên có thể giải thích bằng cải thiện sự chăm sóc trước khi nhập viện, đưa đến giảm tỷ lệ tử vong ngoại viện. Trên phương diện khác, với kỷ nguyên của can thiệp mạch vành qua da, so với tiêu sợi huyết, đã cứu nguy nhiều vùng cơ tim hơn, giúp làm giảm tần suất ST trong bệnh viện. Trong sổ bộ quốc gia SWEDEHEART, tần suất ST sau NMCT giảm từ 46% trong kỷ nguyên tiêu sợi huyết (năm 1996) xuống còn 28% trong thời kỳ PCI (năm 2008) (hình 4).
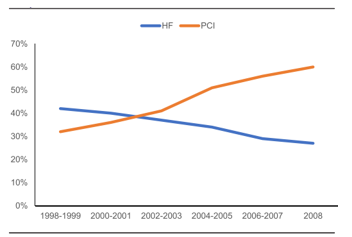
Hình 4. Tỷ lệ phần trăm BN bị NMCT được can thiệp mạch vành qua da (PCI) và xuất hiện suy tim (HF) trong thời gian nằm viện – nghiên cứu SWEDEHEART[6]
1.2. ST phát triển sau nhập viện vì NMCT (Heart failure developing after myocardial infarction hospitalization):
ST phát triển trong thời gian nằm viện sau NMCT là hậu quả của chết tế bào cơ tim và tạo xơ, là yếu tố khởi kích hoạt hóa hệ thần kinh thể dịch mạn tính (điều hòa hướng lên hệ renin-angiotensin-aldosterone và hệ thần kinh giao cảm) và tái cấu trúc thất trái. Tái cấu trúc thất trái thường gặp ở nam, BN có nhồi máu diện rộng, tái tưới máu trễ vùng thượng tâm mạc và giường vi mạch hoặc không thành công. Tái cấu trúc thất trái đưa đến thay đổi hình dạng thất trái, đưa đến mỏng cơ tim, hở 2 lá cơ năng, thúc đẩy sự mất tế bào cơ tim. Đây là một quá trình thích nghi kém, lâu dài đưa đến thay đổi hệ thống tim mạch và thúc đẩy tiến triển ST sau NMCT (hình 5):
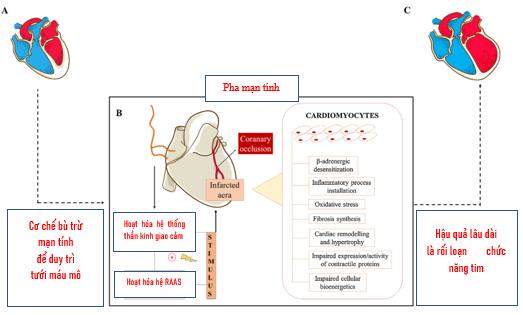
Hình 5. Những biến cố mạn tính xuất hiện sau NMCT và thúc đẩy ST. (A) Tim của người khỏe mạnh bơm máu để duy trì oxy cho cơ thể. (B) quá trình thích nghi lâu dài sau NMCT để bù trừ cho tưới máu mô cơ quan, đó là kích hoạt hệ thống thần kinh giao cảm và renin-angiotensin-aldosterone, chính vì điều này đưa vào vòng xoắn bệnh lý, làm cho tế bào cơ tim giảm nhạy cảm với kích hoạt adrenergic, đưa đến hiện tượng viêm, các gốc oxy hóa tự do, các yếu tố tăng trưởng thúc đẩy tái cấu trúc, phì đại cơ tim, suy giảm biểu lộ/hoạt hóa các protein có chức năng co bóp, mất ổn định năng lượng màng tế bào. (C) Tim trở nên yếu ớt, không đủ khả năng tái tưới máu mô cơ quan, gọi là ST sau NMCT[4].
ST phát triển sau xuất viện rất thường gặp: chiếm khoảng 13% tại thời điểm 30 ngày và 20-30% sau xuất viện 1 năm vì NMCT. Tần suất cao nhất trong những tháng đầu tiên, sau đó giảm dần và ổn định với tần suất 1.3-2.2% vào những năm sau đó[6].
- Ảnh hưởng lâm sàng của ST sau NMCT
Sự phát triển của ST sau NMCT có ảnh hưởng ý nghĩa lên kết cục, bất kể thể ST. Ở những BN có tiền căn NMCT trước đó, ST làm tăng tỷ lệ tử vong toàn bộ lên 3 lần và tử vong do tim mạch lên 4 lần. Thời điểm phát hiện ST cũng ảnh hưởng lên biến cố bất lợi.BN phát triển ST sau 3 ngày NMCT có tỷ lệ tử vong cao hơn 43% so với những BNkhông ST trong 3 ngày đầu tiên. Điều này có thể do những yếu tố nguy cơ và cơ chế khác nhau. Trong nghiên cứu French Brittany Regional Infract Observatory cho thấy ST cấp là yếu tố dự đoán mạnh mẽ nhất tử vong nội viện(tỷ số nguy cơ [HR]: 3.85;95% khoảng tin cậy [CI]: 2.30 to 6.44) ở BN STEMI được PCI. BN nhập viện với ST cấp trong sổ bộ GRACE (Global Registry of Acute Coronary Events) có tỷ lệ tử vong nội viện (8.9% so với 0.9%) và 6 tháng (9.6% so với 2.9%) so với BN không có ST cấp (P<0.001). ST cấp và rối loạn chức năng tâm thu thất trái có tỷ lệ rối loạn nhịp tim cao hơn (bao gồm đột tử do tim, rối loạn nhịp thất, rung nhĩ mới khởi phát), biến chứng cơ học, biến cố xuất huyết lớn theo Bleeding Academic Research Consortium (BARC), bệnh thận do thuốc cản quang[6].
- Sự cần thiết cho việc tầm soát và phòng ngừa ST
Theo Hội Tim Châu Âu và Hội Tim Hoa Kỳ, việc tầm soát và phòng ngừa STsau NMCT là vấn đề cấp thiết mang tính chất toàn cầu và rất quan trong. Chẩn đoán sai và chậm trễ trong điều trị, đặc biệt là tái tưới máu sớm ở BN NMCT với ST chênh lên, làm ảnh hưởng đến tiên lượng và tăng chi phí điều trị. Đồng thời nhấn mạnh rằng việc theo dõi sau xuất viện nhóm BN này một cách kỹ lưỡng giúp cải thiện việc tuân trị, giảm nhập viện do nguyên nhân tim mạch. Chính vì thế, việc nhận ra các yếu tố nguy cơ và kết hợp các chỉ dấu sinh học giúp phát hiện ST sau NMCT, từ đó đề ra cách tiếp cận đa phương thức giúp hỗ trợ các nhà lâm sàng trong việc xác định sớm những BN có yếu tố nguy cơ (hình 6), bắt đầu khởi trị sớm ST theo hướng dẫn[6]. Các yếu tố nguy cơ lâm sàng khác nhau lên ST sau NMCT được trình bày ở bảng 1
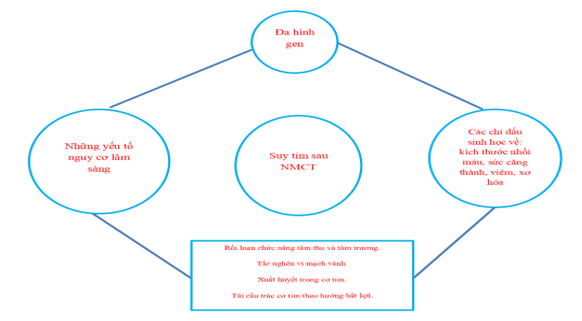
Hình 6: Tiếp cận đa phượng diện những yếu tố dự đoán ST sau NMCT[6].
Bảng 1. Những yếu tố nguy cơ lâm sàng cho ST.[6]
| Những yếu tố nguy cơ lâm sàng | Tăng yếu tố nguy cơ ST sau NMCT |
| Tuổi, theo 10 năm tăng dần | 20-50% |
| Giới tính nữ | 15-34% |
| Tiền căn NMCT trước đó | 21-89% |
| Tăng huyết áp | 7-70% |
| Đái tháo đường | 30-42% |
| Độ lọc cầu thận, cho mỗi mức giảm 10mL/phút/1.73m2 | 10% |
| Nhịp tim, tăng cho mỗi 10 nhịp/phút | 7-23% |
| Rung nhĩ | 20-51% |
Tuổi:
Tần suất ST nội viện ở nhóm 75-85 tuổi cao gấp 3 lần so với 25-54 tuổi. Sau xuất viện, tần suất ST cao gấp 6 lần ở nhóm lớn tuổi.[6].
Giới tính:
Trong một số nghiên cứu, giới tính nữ là yếu tố nguy cơ độc lập của ST sau NMCT, chiếm từ 15% đến 34%. Có nhiều lý do cho việc này, thứ nhất là BN nữ nhập viện vì NMCT thường lớn tuổi hơn, tình trạng chức năng kém, nhiều bệnh đồng mắc hơn so với nam giới. Thứ nhì là do ít được tiếp cận hệ thống chăm sóc y tế, chưa chỉ định đúng tái tưới máu, điều này có thể giải thích nguy cơ ST cao hơn ở nữ giới[6].
Số lượng và định khu vùng động mạch liên quan đến nhồi máu:
Bệnh nhiều nhánh mạch vành thường có gánh nặng xơ vữa cao, rối loạn nội mạc và đáp ứng viêm hệ thống ưu thế hơn, thường gặp ở những BN lớn tuổi, có bệnh đồng mắc đi kèm là đái tháo đường và suy thận. Bệnh nhiều nhánh mạch vành thường đi kèm với HFrEF, tăng biến cố tim mạch chính, bao gồm ST, lên tới 80%. [6].
Tiền căn NMCT trước đó:
Tiền căn NMCT làm tăng nguy cơ ST lên 21-89%, điều này có thể giải thích vì tình trạng rối loạn chức năng tâm thu/tâm trương trước đó[6].
Tăng huyết áp:
Nhiều nghiên cứu chỉ ra rằng tăng huyết áp làm tăng yếu tố nguy cơ của ST từ 7% đến 70%. BNST có tăng huyết áp thường gặp tình trạng tổn thương vi mạch và xuất huyết trong cơ tim, bên cạnh đó đi kèm là tình trạng hoạt hóa hệ thống thần kinh thể dịch và tái cấu trúc thất trái[6].
Nhip tim nhanh:
Nhịp tim nhanh là yếu tố nguy cơ của ST sau NMCT, cứ tăng mỗi 10 nhịp, tần suất tăng 7-23%. Nhịp tim nhanh phản ánh mức độ nghiêm trọng của NMCT[6].
Rung nhĩ:
BN NMCT có biến chứng rung nhĩ mới khởi phát khoảng 2-21% và làm tăng nguy cơ ST sau NMCT khoảng 20-51%[6].
Đái tháo đường:
Sau NMCT, tần suất ST ở BN đái tháo đường là 60-70% cao hơn so với BN không có. Sau khi hiệu chỉnh những bệnh đồng mắc khác đi kèm với đái tháo đường, tần suất ST sau NMCT vẫn còn cao, từ 30-42%.BN đái tháo đường thường có tái cấu trúc thất trái và ST nhiều hơn, điều này có thể do rối loạn chức năng vi mạch và tâm trương. Những yếu tố này cũng tương đồng ở BN đái tháo đường trước đó hoặc được chẩn đoán cùng thời điểm NMCT[6].
Bệnh thận mạn:
Bệnh thận mạn làm tăng yếu tố nguy cơ của ST sau NMCT lên 2 lần, đó là do sự thúc đẩy có xơ vữa mạch máu, bệnh nhiều nhánh mạch vành, cơ hội được tái tưới máu ít hơn, đưa đến làm tăng kích thước vùng nhồi máu và rối loạn chức năng thất trái nặng hơn. Bệnh cạnh đó, bệnh thận mạn đưa đến tình trạng quá tải dịch, tăng huyết áp thứ phát, thiếu máu, tình trạng viêm mạn tính, thay đổi hệ renin-angiotensin-aldosterone, là một trong những rào cản trong việc kê các thuốc tứ trụ điều trị ST[6].
Các chỉ dấu sinh học:
Các chỉ dấu đánh giá kích thước nhồi máu
Troponin của tim, là một chỉ dấu sinh học được chọn để chẩn đoán NMCT, được đo ở pha bình nguyên (48-72 giờ sau khởi phát triệu chứng NMCT) kết hợp với MRI tim để xác định kích thước vùng nhồi máu. Nhiều nghiên cứu cho thấy có mối tương quan giữa troponin, CK-MB và biến cố tim mạch lớn, bao gồm ST[3], [6].
Peptide bài niệu natri
Bên cạnh troponin, peptide bài niệu natri tương quan với kích thước nhồi máu và rối loạn chức năng tim. Sự thay đổi nồng độ BNP sau NMCT theo kiểu đơn pha, đạt đỉnh sau 16 giờ nhập viện, tuy nhiên, một số trường hợp lại diễn tiến 2 pha, với pha 2 sau 5 ngày, và điều đó làm tăng nguy cơ tái cấu trúc cơ tim và ST[3], [6].
Các chỉ dấu sinh học của hiện tượng viêm
Có nhiều bằng chứng cho thấy đáp ứng viêm kéo dài và lan rộng làm tăng nguy cơ tái cấu trúc thất trái và ST. Nhiều nghiên cứu đánh giá hiện tượng viêm thông qua các chỉ dấu như CRP, tỷ lệ neutrophil/lympho dự đoán MACE, ST. Cytokine là tác nhân điều hòa phản ứng viêm. Trong một nghiên cứu với 4939 BN NMCT, IL-6 là yếu tố độc lập dự đoán MACE và ST. IL-32 là một cytokine tiền viêm mới phát hiện thúc đẩy sự phóng tích các cytokine viêm khác như yếu tố hoại tử u α, IL-1β, IL-6, IL-8, IL-18. Xuan và cộng sự cho thấy IL-32 là yếu tố dự đoán tử vong tim mạch và ST sau NMCT[3], [6].
Các chỉ dấu sinh học của thận
Tỷ lệ phân suất lọc cầu thận (estimated glomerular filtration-eGFR) là một yếu tố dự đoán ST sau NMCT. Nghiên cứu VALIANT cho thấy yếu tố nguy cơ của ST tăng lên 10% cho tương ứng với giảm mức lọc cầu thận 10mL/phút/1.73m2. Cystatin C là một chỉ dấu của suy giảm chức năng thận, không giống với creatinine, nó không ảnh hưởng bởi tuổi, giới, khối cơ. Trong nghiên cứu SOLID-TIMI 52 trên BN NMCT, cystatin C cung cấp thêm yếu tố phân tầng nguy cơ, bao gồm cả nhập viện vì ST[3], [6].
Các chỉ dấu sinh học về xơ hóa
Chất ức chế tạo u (Suppressor of tumourgenesis-ST2), thuộc họ gia đình IL-1, liên quan đến quá trình tái cấu trúc và xơ hóa cơ tim. Có 2 đồng phân là phối tử xuyên màng và dạng hòa tan. sST2 là dạng hòa tan gắn kết với IL-33, thúc đẩy chết tế bào và xơ hóa. Nhiều nghiên cứu cho thấy vai trò của sST2 trong tiên lượng ST, tuy nhiên vai trò trong NMCT còn hạn chế.
Galectin-3, một lectin gắn kết với β-galactoside, được bài tiết chủ yếu bởi các đại thực bào được hoạt hóa, phản ánh mức độ xơ hóa và tái cấu trúc trong tổn thương cơ tim. Trường môn Tim Hoa Kỳ/Hội Tim Hoa Kỳ (American College of Cardiology/American Heart Association) khuyến cáo sử dụng sST2 và galectin-3 trong tiên lượng ST. Một nghiên cứu tiến cứu bao gồm các BN bị NMCT, galectin-3 làm tăng yếu tố nguy cơ tử vong và ST sau khi hiệu chỉnh mức độ nghiêm trọng của NMCT, bệnh đồng mắc và sST2[3], [6].
Hình ảnh học:
Siêu âm tim
Siêu âm tim là hình ảnh học thường được dùng để đánh giá cấu trúc cơ tim sau NCMT. Siêu âm tim trong những ngày đầu sau NMCT thường không chính xác, đó là do hiện tượng choáng váng cơ tim, do đó cần phải lặp lại siêu âm tim sau đó.
Chức năng tâm thu
Giảm LVEF là yếu tố nguy cơ phát triển ST. LVEF giảm 5% bằng chụp thất đồ làm tăng 12-18% nguy cơ phát triển ST ra viện vì NMCT. Tương tự như vậy, LVEF giảm 5% được đánh giá bằng siêu âm tim sau 5-20 tháng vì NMCT làm tăng nguy cơ ST lên đến 20%.
Do hiện tượng bù trừ của những vùng tăng động hoặc vùng không ảnh hưởng cho những vùng nhồi máu, chỉ số thang điểm vận động vùng (wall motion score index-WMSI) phản ánh bất thường vận động vùng tốt hơn so với LVEF. Trong một nghiên cứu 144 BN bị NMCT, WMSI>1.5 làm tăng nguy cơ tử vong tim mạch, đau thắt ngực không ổn định, ST, độc lập với LVEF. Trong nghiên cứu của Moller và cộng sự, cứ tăng WMSI lên 0.2, nguy cơ ST tăng lên 1.21 lần (95% khoảng tin cậy 1.07-1.37, P=0.002) và tử vong lên 1.5 lần (95% khoảng tin cậy 1.1-1.21, P<0.0001). Nghiên cứu của Jurado-roman và cộng sự cho thấy WMS dự đoán mạnh mẽ tử vong và ST hơn LVEF.
Rối loạn chức năng thất phải cũng đóng góp ý nghĩa sự phát triển ST sau NMCT. Sự di chuyển vòng van 3 lá thì tâm thu (The tricuspid annular plane systolic excursion-TAPSE) thường dùng để đánh giá chức năng thất phải. ỞBN NMCT, TAPSE ≤14 mm dự đoán biến cô tim mạch sớm, bao gồm choáng tim. Tuy nhiên, TAPSE chỉ đánh giá được chức năng theo trục dài của thất phải, nó không tốt bằng phân suất thay đổi diện tích.
Chức năng tâm trương
Đánh giá Doppler chuẩn bằng lưu lượng qua van 2 lá cung cấp thêm những thông tin ở BN sau NMCT. Moller và cộng sự thực hiện một phân tích tổng hợp của 12 nghiên cứu cho thấy kiểu hình hạn chế đổ đầy làm tăng tỷ lệ tử vong do mọi nguyên nhân và ST. Hình ảnh học Doppler mô với E/e’>15 dự đoán mạnh mẽ tử vong và sự phát triển ST sau NMCT.
Tái cấu trúc thất trái
Tái cấu trúc thất trái được định nghĩa là tăng thể tích cuối kỳ tâm trương thất trái lên 20%. Tiến trình này được thúc đẩy bởi kích thước vùng nhồi máu lớn, NMCT xuyên thành, tắc nghẽn vi mạch, xuất huyết cơ tim, tuổi cao. Trong thời đại này, có hơn một nửa trường hợp có hiện tượng tái cấu trúc sau 1 năm NMCT được đánh giá bằng siêu âm tim, và tăng 2.7 lần nguy cơ nhập viện vì ST so với những BN không có hiện tượng này[3], [6].
Siêu âm tim đánh dấu mô
Siêu âm tim đánh dấu mô đánh giá sự biến dạng cơ tim theo vùng và toàn bộ. Sức căng trục dài toàn bộ (đáy-đỉnh) thường được sử dụng nhất và tối ưu hơn so với LVEF, đặc biệt trong những ngày đầu sau NCMT. Nghiên cứu của Ersboll và cộng sự trên BN NMCT với LVEF>40%, sức căng trục dài toàn bộ (đáy-đỉnh)>-14 làm tăng 5 lần nguy cơ ST và 12 lần tử vong tim mạch. Sức căng diện tích toàn bộ, một thông số trên siêu âm tim 3D, đánh giá sức căng dọc và chu vi, dự đoán độc lập MACE và nhập viện vì ST. [3], [6]
Siêu âm tim có chất cản quang
Siêu âm tim có cản quang sử dụng những bong bóng nhỏ tiêm vào tĩnh mạch hoặc mạch vành, giúp phân biệt thiếu máu cơ tim đảo ngược và không đảo ngược, giúp đánh giá sống còn cơ tim. Tín hiệu giảm tưới máu là do hiện tượng tắc nghẽn vi mạch, nó tương đồng với MRI. Để phát hiện hiện tượng no-reflow, siêu âm tim có chất cản quang nên được đánh giá sau 24-48 giờ can thiệp mạch vành. Hiện tượng no-reflow sau NMCT là một yếu tố tiên lượng độc lập sự hồi phục thất trái và kết cục bất lợi bao gồm ST[3], [6].
Siêu âm tim gắng sức
Siêu âm tim gắng sức sử dụng dobutamine đánh giá vùng sống còn cơ tim, là một yếu tố dự đoán độc lập kết cục bất lợi, bao gồm ST, sau 2-7 ngày NMCT[3], [6].
Cộng hưởng từ tim (Cardiac Magnetic Resonance – CMR)
Kích thước nhồi máu
Hình ảnh học cộng hưởng từ thường được dùng là tiêu chuẩn vàng trong đánh giá kích thước vùng nhồi máu bằng hình ảnh tăng tín hiệu muộn. Một phân tích tổng hợp sử dụng MRI tim và SPECT cho thấy cứ tăng 5% kích thước vùng nhồi máu, nguy cơ nhập viện vì ST tăng 20%. Bên cạnh đó, MRI lại không đóng góp thêm giá trị tiên lượng so với LVEF trong Non-STEMI, có thể là do sự khác biệt mức độ tổn thương cơ tim so với STEMI[3], [6].
Tắc nghẽn vi mạch
Tắc nghẽn vi mạch được đánh giá bằng hiện tượng thiếu tái tưới máu vi tuần hoàn, mặc dù đạt được tái tưới máu hệ mạch vành thượng tâm mạc. Tắc nghẽn vi mạch có thể xác định bằng lõi giảm đậm độ bên cạnh vùng tăng tín hiệu trong cả giai đoạn sớm (sự tắc nghẽn vi mạch sớm) và tăng tín hiệu muộn (tắc nghẽn vi mạch trễ). Tắc nghẽn vi mạch làm tăng nguy cơ tái cấu trúc, kích thước nhồi máu, cứ mỗi tăng 10% vùng tắc nghẽn vi mạch làm tăng 80% nhập viện vì ST, 114% tử vong do mọi nguyên nhân[3], [6].
Xuất huyết trong cơ tim
Nếu tổn thương cơ tim sau NMCT nặng và toàn bộ hệ vi mạch vành bị tổn thương, hồng cầu sẽ thoát mạch và gây xuất huyết cơ tim, có thể phát hiện bằng vùng giảm đậm độ trong lõi NMCT trên tín hiệu T2. Nhiều nghiên cứu cho thấy sắt tích tụ trong cơ tim thúc đẩy đáp ứng tiền viêm và tái cấu trúc thất trái theo hướng bất lợi. Nhiều nghiên cứu nhỏ cho thấy xuất huyết cơ tim có liên quan đến kết cục bất lợi, bao gồm ST so với hiện tượng tắc nghẽn vi mạch[3], [6].
Xơ hóa nhiều lớp
Trong nghiên cứu DANAMI 3 ( Danish Study of Optimal Acute Treatment of Patients with ST-segment Elevation Myocardial Infraction) sử dụng MRI cho thấy xơ hóa nhiều lớp cơ tim (được đặc trưng bởi tăng tín hiệu muộn nhiều diện tích cơ tim) làm tăng 3 lần tử vong do mọi nguyên nhân và nhập viện vì ST sau khi hiệu chỉnh các yếu tố lâm sàng và kích thước NMCT[3], [6].
Theo dõi từ xa
Ở những BN được chẩn đoán ST, hệ thống theo dõi từ xa bao gồm các thiết bị được cấy ghép như máy khử rung tim, liệu pháp điều trị tái đồng bộ tim giúp phát hiện ST mất bù cấp, từ đó giảm nguy cơ nhập viện vì ST. Tuy nhiên, hầu hết các nghiên cứu cho thấy những dụng cụ này không có lợi ích đến tỷ lệ tử vong, ngoại trừ trong thử nghiệm IN-TIME (Biotronik Home Monitoring technology), theo dõi từ xa làm giảm thang điểm lâm sàng cộng gộp và tử vong do mọi nguyên nhân. Phân tích của 3 thử nghiệm TRUST, ECOST, IN-TIME cho thấy giảm 36-38% tử vong do mọi nguyên nhân và nhập viện vì ST mất bù cấp, đó có thể do phát hiện sớm hơn các trường hợp rối loạn nhịp tim và mất đồng bộ 2 thất[6].
- Ngăn ngừa và điều trị suy tim sau nhồi máu
Điều trị trong giai đoạn cấp tính
Lợi ích của việc điều trị tái tưới máu giúp làm giảm kích thước vùng nhồi máu, cải thiện chức năng tâm thu thất trái đã được chứng minh. Vì vậy, trong giai đoạn cấp tính luôn luôn phải đặt vấn đề tái tưới máu cho mọi BN. Lựa chọn thời gian và phương thức tái tưới máu phù hợp với từng BN.
Ở BNST sau NMCT mức độ nhẹ (Killip 2) có thể gặp tình trạng giảm oxy mô. Trong trường hợp này, việc cung cấp oxy qua cannula mũi hoặc mặt nạ có túi dự trữ giúp cải thiện giảm oxy mô. Nếu tình trạng giảm oxy mô không cải thiện, cần xem xét các phương pháp thông khí cơ học không xâm lấn. Chiến lược điều trị lợi tiểu được sử dụng khi có tình trạng khó thở hoặc quá tải thể tích tuần hoàn. Sử dụng lợi tiểu quai đường tĩnh mạch vừa giúp bài tiết muối nước và đem lại hiệu ứng dãn mạch. Nếu tình trạng khó thở không cải thiện, cần xem xét đến nitroglycerin, làm giảm tiền tải và cải thiện triệu chứng. Việc thêm ACEi có thể xem xét trong giai đoạn này, lưu ý cần theo dõi nồng độ Kali máu, chức năng thận.
Trong trường hợp giảm tưới máu mô xảy ra mà chưa có dấu hiệu choáng tim, xem xét sử dụng thuốc tăng co bóp cơ tim như dobutamine, levosemidan.
Tiên lượng ở BN choáng tim sau NMCT cực kỳ tồi tệ, với tần suất là 7%, và tỷ lệ tử vong lên đến >50%. Thử nghiệm SHOCK (Should We Emergently Revascularize Occluded Coronaries for Cardiogenic Shock) đánh giá vai trò của tái tưới máu sớm trong BN choáng tim so với điều trị nội khoa. Kết quả của nghiên cứu là giảm không ý nghĩa tử vong 30 ngày, tuy nhiên tỷ lệ tử vong 6 tháng và sống còn 6 năm lại cải thiện ở nhóm tái tưới máu sớm. Do vậy ACC/AHA khuyến cáo tái tưới máu cấp cứu bằng PCI hoặc CABG được khuyến cáo ở BN choáng tim do suy bơm sau STEMI bất kể thời điểm khởi phát. Khi các liệu pháp điều trị nội khoa không hiệu quả, bên cạnh việc tái tưới máu sớm, bất chấp thời gian khởi phát triệu chứng, việc sử dụng các thiết bị hỗ trợ cơ học như IABP làm giảm quá tải áp lực tâm thu, tăng áp lực tâm trương, tăng tưới máu mạch vành, qua đó cải thiện chức năng tim. Sử dụng các thiết bị hỗ trợ cơ học thất trái (Left ventricular assist devices – LVAD) như một phương tiện bắc cầu để chờ tim hồi phục, có hiệu quả tốt hơn rất nhiều so với IABP[8].
Điều trị nội khoa
Chẹn beta giao cảm
Chẹn beta giao cảm ngăn chặn tác động có hại của hệ thống thần kinh giao cảm thông qua việc ức chế thụ thể β1-adrenergic, qua đó làm giảm tiêu thụ oxy cơ tim thông qua giảm nhịp tim, hậu tải, co bóp cơ tim, ngăn chặn rối loạn nhịp thất và giảm kích thước vùng nhồi máu. Cùng với ACEi, ARB, statin, chẹn beta giao cảm ức chế gián tiếp MMPs. Những bằng chứng có lợi của chẹn beta giao cảm lên kết cục sau NMCT đến từ trước kỷ nguyên tiêu sợi huyết.Trong một phân tích tổng hợp của 31 nghiên cứu ngẫu nhiên, sử dụng chẹn beta giao cảm làm giảm tử vong do mọi nguyên nhân sau NMCT 23%, tuy nhiên vẫn chưa có nhiều nghiên cứu trên nhóm BN có rối loạn chức năng thất trái và ST trong thời gian nằm viện vì NMCT.
Trong nghiên cứu SAVE và AIRE, là những nghiên cứu đánh giá vai trò của ACEi trên BN NMCT có rối loạn chức năng thất trái đi kèm, chẹn beta giao cảm làm giảm tiến triển đến ST nặng lần lượt là 21% và 42%. Trong nghiên cứu CARPICORN, carvedilol chỉ định ở BN NMCT có rối loạn chức năng tâm thu (LVEF<40%) giảm tử vong do mọi nguyên nhân 23% và nhập viện vì ST là 14% so với giả dược.
Mặc dù việc sử dụng lâu dài chẹn beta giao cảm làm giảm 40% nguy cơ tái nhập viện vì ST, tuy nhiên việc bắt đầu sớm trong 24 giờ đầu sau NMCT có nguy cơ cao đưa đến choáng tim và tử vong ở BNST so với giả dược. Vì vậy, ở những BN có chống chỉ định chẹn beta giao cảm trong những ngày đầu tiên sau NMCT, cần thiết phải đánh giá sau đó lại chỉ định dùng sớm, bắt đầu với các thuốc tác dụng ngắn, sau đó chuyển sang các thuốc có tác dụng kéo dài như carvediol, metoprolol ở BNST sau NMCT[1], [3], [6,7,8,9,10].
Ức chế men chuyển angiotensin và chẹn thụ thể angiotensin
Sự kích hoạt hệ thống renin-angiotenin-aldosterone đóng vai trò cực kỳ quan trọng trong tiến trình tái cấu trúc, xơ hóa và phát triển ST sau NMCT. ACEi ức chế angiotensin I thành angiotensin II, qua đó ngăn chặn quá trình co mạch và bài tiết aldosterone thông qua angiotensin II.ARB ức chế angiotensin II thông qua gắn kết thụ thể angiotensin II.
Việc bắt đầu sớm ACEi trong khoảng 0-36 giờ sau khởi phát triệu chứng của NMCT làm giảm tỷ lệ tử vong30 ngày 7% và ST 4%. Lợi ích tuyệt đối đạt được ở nhóm nguy cơ cao (Killip II, III, nhịp tim>100 lần/phút lúc nhập viện), NMCT thành trước. Điều quan trọng là, lợi ích sống còn đạt được 40% trong ngày đầu tiên điều trị, nhấn mạnh việc bắt đầu sớm ACEi, trừ khi tụt huyết áp. Những lợi ích tích cực của ACEi còn đạt được trong những nghiên cứu dài hạn. ACEi bắt đầu trong 3-16 ngày sau NMCT làm giảm yếu tố nguy cơ tử vong tương đối 26% và tái nhập viện vì ST 27%.
ARB được dùng ở những BN không dung nạp với ACEi vì tác dụng phụ. Nhiều nghiên cứu cho thấy valsartan và lorsartan có ảnh hưởng tích cực lên tử vong và nhập viện vì ST[1], [3], [6-10].
Đối kháng thụ thể aldosterone
Aldosterone hoạt động ở ống lượn xa bằng cách tăng tái hấp thu natri và nước, qua đó làm tăng thể tích dịch ngoại bào. Ở tim, thụ thể mineralcorticoid thúc đẩy quá trình viêm, phì đại, xơ hóa. Trong nghiên cứu EPHESUS, tuyển những BN sau NMCT với LVEF<40% và có triệu chứng ST hoặc đái tháo đường. Kết quả của nghiên cứu là đối kháng thụ thể aldosterone là eplerenone giảm tử vong do mọi nguyên nhân và nhập viện vì ST là 15%, tử vong do nguyên nhân tim mạch 17%. Tác động này đạt được nếu bắt đầu sớm eplerenone trong 7 ngày đầu sau NMCT[1], [3], [6-10].
Ức chế neprilysin thụ thể angiotensin (Angiotensin receptor-neprilysin inbihitor – ARNI)
ARNI bao gồm 2 thành phần: sacubitril ức chế thoái giáng các peptide chống bài niệu, valsartan ức chế con đường thụ thể angiotensin. Thử nghiệm PARADIGM HF cho thấy lợi ích của ARNI so với enalapril ở BN HFrEF. Phân tích dưới nhóm cũng không có sự khác biệt kết cục giữa 2 nhóm thiếu máu và không thiếu máu cơ tim. Tuy nhiên trong thử nghiệm PARADISE-MI cho thấy sacubitril/valsartan không có lợi ích khác biệt so với ramipril ở BN sau NMCT có rối loạn chức năng tâm thu thất trái. Gần đây, Zheng và cộng sự ARNI giúp ngăn ngừa tái cấu trúc thất trái, cải thiện chức năng tim mạch, giảm biến cố tim mạch lớn. [1], [3], [6-10]
Chất kích hoạt soluble guanylate cyclase
Ở bệnh nhân HFrEF có sự giảm chuyển hóa NO, đưa đến giảm chuyển hóa cyclic guanosine monophosphate (cGMP), sự giảm này có tương quan với rối loạn nội mạch, bệnh lý vi mạch, rối loạn cơ tim. Vericiguat, một chất kích hoạt soluble guanylate cyclase, có hiệu quả làm giảm NTproBNP, được thử nghiệm trong pha 3 của nghiên cứu VICTORIA (Vericiguat Global Study in Subjects with HFrEF), cho thấy giảm 10% kết cục tiên phát so với placebo, tuy nhiên phân tích dưới nhóm giữa thiếu máu cơ tim và không thiếu máu cơ tim thì đang chờ kết quả[1], [3], [6], [7], [8].
Ức chế đồng vận chuyển natri-glucose 2 (SGLT2i)
Thuốc ức chế đồng vận chuyển natri-glucose 2 empagliflozin làm giảm nguy cơ tử vong do tim mạch hoặc nhập viện do ST ở BNST mạn tính, nhưng liệu empagliflozin có cải thiện kết quả lâm sàng khi bắt đầu dùng trong BN nhập viện vì ST cấp thì chưa rõ. Trong thử nghiệm mù đôi EMPULSE (EMPagliflozin in patients hospitalized with acUte heart faiLure who have been StabilizEd), 530 BN được chẩn đoán ban đầu là ST cấp tính mới hoặc ST mạn tính mất bù bất kể khả năng tống máu thất trái. BN được phân làm 2 nhóm: một nhóm được điều trị empaglipozin 10 mg so với giả dược, bắt đầu khi lâm sàng ổn định (thời gian trung bình từ khi nhập viện đến khi phân nhóm ngẫu nhiên, 3 ngày) và được điều trị trong tối đa 90 ngày[1], [3], [6-10].
Kết quả của nghiên cứu cho thấy empagliflozin cải thiện 36% lợi ích lâm sàng bao gồm tử vong do mọi nguyên nhân, giảm tỷ lệ tái nhập viện hay khám đột xuất vì ST, cải thiện triệu chứng ST so với giả dược (tỷ số thắng:1.35 95% CI: 1.09-1.68, p = 0.054). Empagliflozin cải thiện chất lượng cuộc sống thông qua thang điểm KCCQ-TSS đáng kể tại thời điểm 90 ngày so với giả dược (HR 4.45 95% CI: 0.32-0.86, p = 0.0347). Lợi ích này độc lập với EF, bất kể tình trạng đái tháo đường type 2. Tuy nhiên, điều đáng tiếc là thử nghiệm loại trừ BN NMCT, trong tương lai, 3 thử nghiệm: EMMY (Impact of EMpagliflozin on Cardiac Function and Biomarkers of Heart Failure in Patients With Acute MYocardial Infarction), EMPACT-MI (Trial to Evaluate the Effect of EMPAgliflozin on Hospitalisation for Heart Failure and Mortality in Patients With aCuTe Myocardial Infarction), DAPA-MI (Trial to Evaluate the Effect of Dapagliflozin on the Incidence of Heart Failure or Cardiovascular Death in Patients Without Diabetes With Acute Myocardial Infarction) sẽ trả lời câu hỏi còn bỏ ngỏ này[1], [3], [6-10].
Statin
Statin là nhóm thuốc giảm lipid máu thông qua ức chế men 3-hydroxy-3-methylglutarylcoenzyme A reductase, ổn định nội mô, kháng viêm, chống tăng sinh liên quan đến tiến trình xơ vữa. Trong nghiên cứu IDEAL và PROVE IT-TIME, statin liều cao (atorvastatin 80 mg) giảm yếu tố nguy cơ ST lần lượt là 26% và 45% so với liều thấp và trung bình. Việc bắt đầu sớm statin (thường trong 24 giờ đầu nhập viện) làm giảm nhập viện vi ST 2.5 lần và tử vong nội viện 3 lần[1], [3], [6-10].
Điều trị khác
Máy khử rung tim cấy ghép (implatable cardioverter defibrillator- ICD)
BN có rối loạn chức năng thất trái sau NMCT tăng yếu tố nguy cơ đột tử do rối loạn nhịp nguy hiểm. ICD được khuyến cáo cho phòng chống tiên phát đột tử do tim ở BN có bệnh tim thiếu máu cục bộ sau 40 ngày NMCT, với LVEF ≤35%, NYHA II-III đã điều trị nội khoa, kỳ vọng sống tốt >1 năm[1], [3], [6], [7], [8].
Điều trị tế bào gốc
Tế bào gốc tủy xương bao gồm các tế bào từ trung mô, nội mạc, và tạo máu. Tế bào gốc nội mạc có thể lấy từ máu ngoại biên hoặc mô thai nhi. Nhiều thử nghiệm lâm sàng cho thấy ảnh hưởng tich cực của tế bào gốc lên chức năng thất trái sau NMCT, tuy nhiên cơ chế chính xác còn chưa biết. Hiện tượng tân sinh mạch máu, hiệu ứng cận tiết từ mô xung quanh, tại tế bào cơ tim còn sống là những cơ chế có thể nghĩ đến, trong thử nghiệm REPAIR-AMI (Re-infusion of Enriched Progenitor Cells and Infarct Remodeling in Acute Myocardial Infarction), bao gồm 204 BN được nhận tế bào gốc tủy xương tiêm vào mạch vành trong 3 đến 7 ngày sau NMCT. Sau 12 tháng, BN được nhận có cải thiện tái tưới máu, NMCT tái phát và tử vong do mọi nguyên nhân. Trong thử nghiệm BALANCE (Clinical Benefit and Long-Term Outcome After Intracoronary Autologous Bone Marrow Cell Transplantation in Patients With Acute Myocardial Infarction), có 62 BN được tiêm tế bào gốc vào lòng mạch vành, sau 5 năm có cải thiện thể tích cuối kỳ tâm thu và tâm trương cũng như phân suất tống máu[1], [3], [6], [7],[8].
- Kết luận
Sự phát triển của ST sau NMCT kết hợp với nhiều biến cố bất lợi, làm giảm chất lượng cuộc sống và tỷ lệ sống còn lâu dài. Hiện tại, hệ thống đánh giá giúp phân tầng nguy cơ chính xác bao gồm lâm sàng, gene, chỉ dấu sinh học, hình ảnh học giúp xác định và tiên lượng ST sau NMCT còn thiếu. Việc xác định đúng và chính xác thời điểm là cơ hội cho BN bắt đầu sớm các thuốc điều trị theo hướng dẫn, từ đó giảm tái cấu trúc thất trái, tử vong và tái nhập viện vì ST.
Tóm tắt các biện pháp điều trị NMCT trong và sau xuất viện nêu ở bảng 2 và hình 7
Bảng 2. Những điều trị chính ở BNST sau NMCT
| Điều trị | Điểm chính cần lưu ý | Thừ nghiệm quan trọng |
| Chẹn beta giao cảm | Việc sử dụng sớm (trong 24 giờ) liều cao chẹn beta giao cảm thì không có lợi, nên tránh ở bệnh nhân ST sau NMCT hoặc có nguy cơ cao và choáng tim: tuổi >70 tuổi, HA<120mmHg, nhịp nhanh xoang >110 lần/phút, nhịp chậm <60 lần/phút.
BN có chống chỉ định trong vòng 24 giờ đầu tiên cần phải đánh giá việc dùng sớm sau đó. |
CAPRICORN, COMMIT-CCS 2 |
| ACEi | ACEi nên được bắt đầu sớm trong 24 giờ đầu ở BNST có EF ≤40%. Lợi ích sống còn có ý nghĩa đạt được trong những ngày đầu tiên (40%), do đó việc bắt đầu sớm là quan trọng. Chống chỉ định bao gồm: huyết áp tâm thu <90-100mmHg, choáng, tổn thương thận cấp, suy thận, dị ứng thuốc. | SAVE, AIRE, TRACE |
| ARB | ARB được chỉ định ở BN không dung nạp ACEi. Đặc biệt, valsartan không thua gì so với captopril trong nghiên cứu VALIANT. | OPTIMAAL, VALIANT |
| Đối vận aldosterone | Việc bắt đầu sớm eplerenone (<7 ngày) ở BN có EF ≤40% và có triệu chứng ST (hoặc đái tháo đường) giảm tử vong và đột tử do tim. Ảnh hưởng của eplerenone phụ thuộc vào thời gian và nên dùng trong 7 ngảy đầu sau NMCT. Chống chỉ định: creatinine ≥2.5mg/dL ở nam, 2mg/dL ở nữ, Kali máu ≥5mEq/L. | EPHESUS, ALBATROSS |
| Tái tưới máu sớm | Tái tưới máu sớm (càng sớm càng tốt) là điều trị duy nhất làm giảm tử vong ở BN NMCT có choáng tim. | SHOCK |
| Hỗ trợ tuần hoàn cơ học | Trong NMCT, việc sử dụng thường quy IABP không có chỉ định để làm giảm kích thước vùng nhồi máu và quản lý choáng tim. | IABP SHOCK II, IMPRESS |
AIRE: Acute Infarction Ramipril Efficacy;
ALBATROS: Aldosterone Lethal effects Blocked in Acute MI Treated with or without Reperfusion to improve Outcome and Survival at Six months follow-up;
CAPRICORN: Carvedilol Post-Infarct Survival Control in Left Ventricular Dysfunction Study;
COMMIT-CCS2: Clopidogrel and Metoprolol in Myocardial Infarction Trial/Second Chinese Cardiac Study;
EPHESUS: Eplerenone Post-Acute Myocardial Infarction Heart Failure Efficacy and Survival;
IABP SHOCK II: Intra-aortic Balloon Pump Should We Emergently Revascularize Occluded Coronaries for Cardiogenic Shock II;
IMPRESS: Impella versusIABP reduces mortality in STEMI patients treated with primary PCI in severe cardiogenic shock;
OPTIMAAL: Optimal Trial in Myocardial Infarction with Angiotensin II Antagonist Losartan;
SAVE: Survival and Ventricular Enlargement;
SHOCK: Should We Emergently Revascularize Occluded Coronaries for Cardiogenic Shock;
TRACE: TRAndolapril Cardiac Evaluation; VALIANT: VALsartan In Acute myocardial iNfarction Trial.
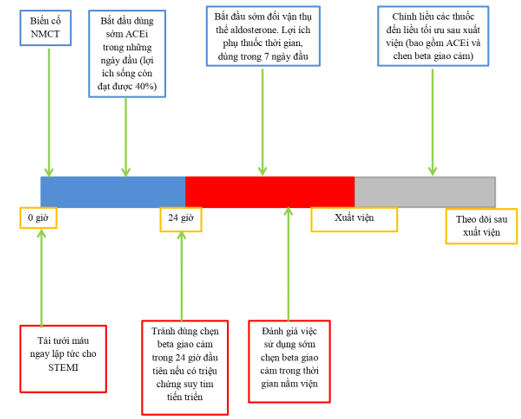
Hình 7. Các giai đoạn và biệp pháp điều trị và dự phòng suy tim sau NMCT[1]
Tài liệu tham khảo
- Bahit MC et al, Post-Myocardial Infarction Heart Failure. J Am Coll Cardiol HF 2018;6:179–86
- Eapen ZR et al, Defining Heart Failure End Points in ST Segment Elevation Myocardial Infarction Trials Integrating Past Experiences to Chart a Path Forward. Circ Cardiovasc Imaging. 2012;5:594-600.
- Frantz S et al, Left ventricular remodelling post-myocardial infarction: pathophysiology, imaging, and novel therapies. European Heart Journal (2022) 43, 2549–2561.
- Grabiel-Costa D et al, The pathophysiology of myocardial infarction-induced heart failure. Pathophysiology 2018 Dec;25(4):277-284. doi: 10.1016/j.pathophys.2018.04.003.
- Harrington J et al, Acute Decompensated Heart Failure in the Setting of Acute Coronary Syndrome. JACC: Heart Failure. Volume 10, Issue 6, June 2022, Pages 404-414.
- Jenca D et al, Heart failure after myocardial infarction: incidence and predictors. ESC Heart Failure 2021; 8: 222–237.
- Leanca SA et al, Left Ventricular Remodeling after Myocardial Infarction: From Physiopathology to Treatment. Life 2022, 12, 1111
- Minicucci MF et al, Heart Failure After Myocardial Infarction:Clinical Implications and Treatment. Clinical Cardiology · July 2011.
- G: Post-myocardial Infarction Heart Failure: A Review on Management of Drug Therapies. Cureus 2022; 14(6): e25745. DOI 10.7759/cureus.25745.
- AA and Clark: Long-Term Pharmacological Management of Reduced Ejection Fraction Following Acute Myocardial Infarction: Current Status and Future Prospects. International Journal of General Medicine 2021;14: 7797–7805







