BS. NGUYỄN THANH HIỀN
BS. TRẦN DUY BÁCH *
* Khoa Tim mạch tổng quát, BV Nhân dân 115
I. MỞ ĐẦU
Suy tim cấp (STC) là một tình trạng lâm sàng nghiêm trọng, đòi hỏi phải nhập viện khẩn cấp và thường đi kèm với tỷ lệ tử vong cao cũng như nguy cơ tái nhập viện đáng kể. Trong bối cảnh đó, việc tìm kiếm các phương pháp điều trị (ĐT) mới nhằm cải thiện tiên lượng cho người bệnh luôn là ưu tiên hàng đầu.
Nhóm thuốc ức chế SGLT2 (SGLT2i) ban đầu được dự định là một phương pháp ĐT hỗ trợ cho bệnh đái tháo đường type2 (ĐTĐ2), nhưng đến thời điểm hiện tại nhóm thuốc này đã trở thành một trụ cột không ngờ của phác đồ ĐT suy tim (ST). Trong vài năm gần đây, giới y học đã chứng kiến sự gia tăng chóng mặt của nhóm thuốc này, bắt đầu với kết quả tình cờ của các thử nghiệm (TN) đánh giá mức độ an toàn của liệu pháp ĐT tăng cường đường huyết ở những bệnh nhân (BN) tim mạch (TM) và đỉnh điểm là việc chứng minh giảm tỷ lệ nhập viện vì ST và TM, và giảm tỷ lệ tử vong (TV) trong quần thể ST chuyên biệt. Lợi ích trên ĐT ST tim của SGLT2i không phụ thuộc vào tình trạng đường huyết của BN, nhưng các cơ chế bảo vệ TM nổi bật vẫn là một chủ đề của các cuộc tranh luận và nghiên cứu khoa học đang diễn ra. Gần đây, các bằng chứng mới đã cho thấy SGLT2i cũng có vai trò quan trọng trong điều trị STC. Việc khởi trị các thuốc ức chế SGLT2i trong thời gian BN nhập viện vì STC đã được chứng minh là an toàn và hiệu quả trong các TN lâm sàng ngẫu nhiên có đối chứng, và hiện có một số TN tiến cứu khác đang được tiến hành.
Tuy nhiên, bổ sung bằng chứng từ thực hành lâm sàng thực tế – vốn thường đi kèm với mức độ theo dõi bệnh nhân ít chặt chẽ hơn so với trong các thử nghiệm lâm sàng – vẫn là điều quan trọng. Điều này càng trở nên đáng lưu ý khi thực tế cho thấy dưới 1% số bệnh nhân suy tim phân suất tống máu giảm (HFrEF) đủ điều kiện đang được điều trị theo đúng liều đích của các liệu pháp theo hướng dẫn điều trị (GDMT). Điều này nhấn mạnh sự cần thiết phải tận dụng mọi cơ hội để khởi trị các thuốc này. Điều này đặc biệt quan trọng đối với SGLT2i, vì việc kê đơn sớm trong bối cảnh STC mang lại lợi ích lâm sàng đáng kể trong vòng 30 đến 90 ngày sau khi bắt đầu ĐT, và chỉ sau 15 ngày đã có cải thiện rõ rệt về chất lượng cuộc sống và mở ra một hướng tiếp cận ĐT đầy tiềm năng (1,2,3). Bai viết này sẽ trình bày những hướng dẫn hiện nay trong sử dụng SGLT2i ở BN nhập viện vì STC dựa trên các bằng chứng gần đây.
II. CƠ CHẾ TÁC DỤNG CỦA SGLT2i TRONG SUY TIM VÀ SUY TIM CẤP
Các kết quả không được dự đoán trước chứng minh lợi ích TM của SGLT2i trong các TN lâm sàng đầu tiên của nhóm thuốc này cũng như trong các nghiên cứu (NC) tiếp theo đó đã xác nhận kết quả khả quan trên quần thể BN ST, điều này thúc đẩy một loạt các NC về cơ chế tác động của các thuốc này. Nhóm SGLT2i dường như có tác động toàn thân trên nhiều phân tử và hệ thống sinh lý qua trung gian độc lập với hoạt động chống tăng đường huyết. Cơ chế tác động của thuốc, được phân chia dựa trên có lợi ích trực tiếp hay gián tiếp lên cơ tim (4,5) (tham khảo thêm chi tiết cơ chế tác dụng của thuốc trong bài “Thuốc ức chế SGLT2: trụ cột mới trong phác đồ điều trị suy tim. Chuyên đề tim mạch học tp Hồ Chí Minh 2022” (5))
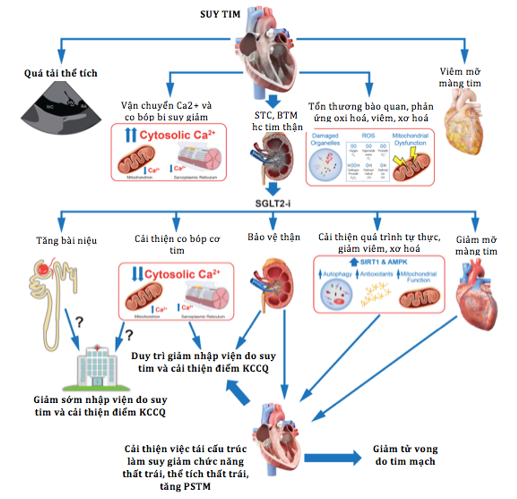
Hình 1. Các cơ chế đề xuất trên tác dụng lợi ích của SGLT2 đối với ST. Rất nhiều cơ chế có lợi của SGLT2i trong ST đã được công nhận, bao gồm tăng bài niệu, cải thiện khả năng vận chuyển Ca2+, bảo vệ trục tim thận, và giảm viêm trong nhiều con đường, bao gồm cả những cơ chế phát sinh từ mỡ màng tim. Các cơ chế giảm sớm nhập viện do ST, và cải thiện điểm số bệnh cơ tim của thành phố Kansas (KCCQ) vẫn còn chưa được biết rõ, nhưng có thể có liên quan đến việc tăng cường bài niệu và cải thiện sự co bóp cơ tim. Các dữ liệu về hình ảnh học đã chứng minh khả năng tu sửa tích cực trong tái cấu trúc dài hạn, điều này có thể được giải thích bằng sự suy giảm của các con đường gây viêm và xơ hoá.Các chữ viết: STC – suy thận cấp, BTM – bệnh thận mạn, hc – hội chứng, PSTM – phân suất tống máu (4)
Dưới đây là tóm tắt từng cơ chế giúp giải thích tác dụng bảo vệ tim (cardioprotective effects) của SGLT2i trong STC:
(1). Lợi tiểu thẩm thấu và thải natri (Osmotic diuresis & Natriuresis): SGLT2i ức chế tái hấp thu glucose ở ống lượn gần → tăng glucose niệu kéo theo nước ra khỏi cơ thể (lợi tiểu thẩm thấu), đồng thời, do giảm tái hấp thu natri → tăng thải natri qua nước tiểu (natriuresis), hệ quả dẫn tới giảm thể tích huyết tương và sung huyết phổi nhanh chóng mà không gây mất điện giải quá mức như lợi tiểu quai và giảm tiền tải (preload) cho tim → giảm áp lực trong buồng tim và giảm khó thở.
(2). Giảm áp lực đổ đầy thất trái và cải thiện chức năng tâm trương. Trong STC, thất trái giãn và áp lực cuối tâm trương tăng cao, SGLT2i giúp giảm thể tích dịch tuần hoàn → giảm áp lực trong thất trái, giảm áp lực tĩnh mạch phổi → cải thiện triệu chứng khó thở, tăng độ đàn hồi (compliance) thất trái, qua đó giúp tối ưu hóa huyết động mà không làm giảm cung lượng tim.
(3). Cải thiện chuyển hóa cơ tim. Trong suy tim, tim sử dụng glucose kém hiệu quả. SGLT2i làm tăng nồng độ ketone trong máu → tim sử dụng ketone bodies như một nguồn năng lượng hiệu quả hơn, giúp cơ tim hoạt động hiệu quả hơn trong điều kiện thiếu năng lượng, giảm tiêu hao oxy
(4). Bảo vệ thận – hiệu ứng tim thận. SGLT2i làm giảm tái hấp thu Na+ ở ống gần → nhiều Na+ đến macula densa → co tiểu động mạch đến cầu thận → giảm tăng lọc cầu thận (glomerular hyperfiltration), điều này giúp bảo vệ thận trong điều kiện huyết động không ổn định (như suy tim cấp), Bảo tồn chức năng thận góp phần ổn định nội môi và duy trì đáp ứng với lợi tiểu.
(5). Giảm viêm và stress oxy hóa. SGLT2i ức chế các yếu tố viêm như IL-6, TNF-α, giảm stress oxy hóa và quá trình xơ hóa cơ tim, ngăn chặn tiến triển tái cấu trúc tim (remodeling) hậu STC.
(6). Điều hòa hệ thần kinh thể dịch (neurohormonal modulation). SGLT2i có khả năng gián tiếp ức chế hệ RAAS (renin-angiotensin-aldosterone system), hệ thần kinh giao cảm, giúp làm giảm hậu tải, hạ huyết áp nhẹ, ngăn cản tiến triển suy tim mạn.
(7). Tăng tạo hồng cầu và cải thiện cung cấp oxy. SGLT2i kích thích nhẹ sản xuất erythropoietin tại thận → tăng hematocrit, qua đó giúp cải thiện khả năng vận chuyển oxy đến mô, giúp cơ tim hoạt động hiệu quả hơn, đặc biệt trong giai đoạn cấp thiếu oxy tương đối.
Các tác dụng trên diễn ra đồng thời, tạo nên hiệu ứng phối hợp giúp cải thiện triệu chứng, huyết động, chức năng tim và tiên lượng ngắn hạn sau 15–90 ngày kể từ khi khởi trị. Đây là lý do SGLT2i được khuyến nghị khởi trị sớm ngay khi bệnh nhân đã ổn định trong đợt nhập viện vì suy tim cấp (6-12).
III. BẰNG CHỨNG LÂM SÀNG
Sự phân tách nhanh chóng của các đường cong sống còn khi sử dụng thuốc SGLT2i trong các TN lâm sàng tiêu biểu về suy tim sung huyết (CHF), như DAPA-HF (Dapagliflozin ở bệnh nhân suy tim với phân suất tống máu giảm) và EMPEROR-Reduced (Kết cục tim mạch và thận với Empagliflozin trong suy tim), đã làm nổi bật lợi ích lâm sàng sớm của các thuốc này.
Trong NC DAPA-HF, sự phân tách đáng kể của các đường cong Kaplan-Meier xuất hiện sau 28 ngày kể từ khi ngẫu nhiên hóa (HR: 0,51; KTC 95%: 0,28 đến 0,94; P = 0,03), trong khi ở nghiên cứu EMPEROR-Reduced, các đường cong tách biệt sau 12 ngày (HR: 0,76; KTC 95%: 0,67 đến 0,87; P < 0,0001). Các nghiên cứu gần đây về thời gian mang lại lợi ích của thuốc SGLT2i cho thấy sự giảm nhanh chóng và có ý nghĩa lâm sàng nguy cơ TV do TM hoặc suy tim tiến triển (WHF). Những phát hiện này nhấn mạnh lợi ích toàn diện của thuốc SGLT2i, càng củng cố thêm vai trò của chúng trong ĐT STC (10, 13,14).
Thử nghiệm SOLOIST-WHF (Tác động của Sotagliflozin lên các biến cố tim mạch ở bệnh nhân đái tháo đường type 2 sau khi suy tim tiến triển) đã đánh giá vai trò của nhóm thuốc gliflozin ở bệnh nhân nhập viện do STC hoặc mới xuất viện (trong vòng 3 ngày sau xuất viện). Đây là một thử nghiệm đa trung tâm, mù đôi, ngẫu nhiên, với 1222 BN ĐTĐ2 mới nhập viện do suy tim xấu dần, theo dõi trung vị là 9 tháng. Sotagliflozin (một thuốc ức chế đồng vận chuyển natri-glucose type 1 và 2 – SGLT1/SGLT2) hoặc giả dược được sử dụng ở 48,8% BN trước khi xuất viện và ở 51,2% BN ngay sau khi xuất viện, với thời điểm bắt đầu trung vị là 2 ngày. Tỷ lệ biến cố (tính theo 100 BN-năm) thấp hơn ở nhóm sotagliflozin so với nhóm giả dược (51,0 so với 76,3; HR: 0,67; KTC 95%: 0,52–0,85; P < 0,001). Cũng ghi nhận một xu hướng (không có ý nghĩa thống kê) giảm tỷ lệ TV do mọi nguyên nhân (10,6% so với 12,5%; HR: 0,84; KTC 95%: 0,58–1,22) và TV do TM (13,5% so với 16,3%; HR: 0,82; KTC 95%: 0,59–1,14). Trong phân tích hậu kiểm của NC SOLOIST-WHF, khởi trị sotagliflozin trước khi xuất viện làm giảm đáng kể tiêu chí gộp tại 90 ngày (HR: 0,54; KTC 95%: 0,35–0,82; P = 0,004) và tại 30 ngày (HR: 0,49; KTC 95%: 0,27–0,91; P = 0,023), cũng như giảm TV do mọi nguyên nhân tại 90 ngày (HR: 0,39; KTC 95%: 0,17–0,88; P = 0,024). Kết quả này vẫn còn ý nghĩa sau khi hiệu chỉnh theo giới tính, tuổi, mức lọc cầu thận ước tính (eGFR), nồng độ NT-proBNP, LVEF, và việc sử dụng thuốc đối kháng thụ thể mineralocorticoid (MRAs) (15,16).
Trong NC EMPULSE (Empagliflozin ở BN nhập viện vì STC đã được ổn định), 530 BN bị STC khởi phát mới hoặc ST mạn mất bù cấp (không phân biệt LVEF) được ngẫu nhiên hóa ngay sau khi ổn định lâm sàng (thời gian trung vị từ lúc nhập viện đến ngẫu nhiên: 3 ngày). Việc dùng empagliflozin sớm trong thời gian nằm viện giúp giảm đáng kể tiêu chí chính gộp tại 90 ngày (bao gồm TV do mọi nguyên nhân, số lần biến cố ST, thời gian đến biến cố ST đầu tiên, và cải thiện ≥5 điểm trong thang điểm triệu chứng tổng thể của bảng câu hỏi Kansas City Cardiomyopathy). Tỷ lệ thắng (win ratio) phân tầng là 1,36 (P = 0,005). Hiệu quả này ổn định trên nhiều nhóm BN, bao gồm cả STC khởi phát mới, ST mạn mất bù, có hay không có ĐTĐ, và LVEF. Vì ứ dịch tồn lưu là yếu tố dự báo kết cục xấu, việc nhận biết và kiểm soát nó là mục tiêu ĐT quan trọng trong giai đoạn nhập viện. Phân tích hậu kiểm của NC EMPULSE cũng đánh giá các tiêu chí liên quan đến giảm ứ dịch — bao gồm giảm cân (weight loss – WL), giảm cân sau điều chỉnh liều lợi tiểu quai trung bình (WL-adjusted) và điểm số lâm sàng của tình trạng ứ dịch, tại các thời điểm 15, 30 và 90 ngày — nhằm đánh giá mối liên quan với tiên lượng ngắn hạn. BN ĐT với empagliflozin giảm đáng kể ở tất cả các chỉ số này, trong đó giảm cân rõ rệt vào ngày 15 liên quan đến khả năng cải thiện lâm sàng cao hơn tại ngày 90. Ferreira và cộng sự đã đánh giá sự thay đổi kết cục lâm sàng và hiệu quả ĐT tùy theo thời điểm ngẫu nhiên hóa kể từ khi nhập viện. Những BN được ngẫu nhiên muộn hơn (3–5 ngày) có nguy cơ biến cố cao hơn so với nhóm được ngẫu nhiên sớm hơn (1–2 ngày). Ngoài ra, hiệu quả ĐT với empagliflozin rõ rệt hơn ở nhóm ngẫu nhiên muộn (WR: 1,69; KTC 95%: 1,26–2,25) nhưng ít hơn ở nhóm ngẫu nhiên sớm (WR: 1,04; KTC 95%: 0,74–1,44), với p cho tương tác = 0,029. Phát hiện này có thể được giải thích bởi thực tế rằng BN được ngẫu nhiên sớm hơn có tình trạng ổn định lâm sàng sớm hơn, cần liều lợi tiểu thấp hơn, và là nhóm nguy cơ thấp hơn. Ngoài ra, trong phân tích tiếp theo của NC EMPULSE, kết cục chính không bị ảnh hưởng bởi việc sử dụng MRAs nền (17,18).
NC EMPA-RESPONSE-AHF (Tác động của Empagliflozin lên các kết cục lâm sàng ở BN ST mất bù cấp) đã tuyển chọn 80 BN ST mất bù cấp, trong đó 47% là ST khởi phát mới (de novo HF), được ngẫu nhiên dùng empagliflozin 10 mg/ngày hoặc giả dược trong vòng 24 giờ kể từ khi nhập viện. Empagliflozin làm giảm tiêu chí gộp gồm: ST xấu đi trong thời gian nằm viện, tái nhập viện vì ST hoặc TV trong vòng 60 ngày, so với giả dược [4 ca (10%) so với 13 ca (33%); P = 0,014] (7).
Trong một phân tích phụ của NC DELIVER (Dapagliflozin trong ST với phân suất tống máu bảo tồn hoặc hơi giảm), bao gồm BN mới nhập viện do ST có phân suất tống máu giảm nhẹ (HFmrEF) hoặc bảo tồn (HFpEF), khi đã ổn định và không còn dùng thuốc tĩnh mạch, dapagliflozin làm giảm tiêu chí chính gồm st xấu đi hoặc TV do TM lần lượt là 22% ở nhóm BN mới nhập viện và 18% ở nhóm không nhập viện gần đây, trong khi tỷ lệ tác dụng phụ tương đương ở cả hai nhóm. Mức độ giảm nguy cơ tương đối ở tiêu chí chính là tương tự giữa các BN có và không có tiền sử nhập viện vì suy tim gần đây (19).
NC DAPA-RESPONSE-AHF (Kết cục lâm sàng của Dapagliflozin ở BN STC) tuyển chọn 87 BN STC trong vòng 24 giờ sau khi nhập viện. Dapagliflozin cải thiện đáng kể thang điểm khó thở (dyspnoea) bằng thang đo hình ảnh thị giác (VAS) so với giả dược và giảm tỷ lệ tái nhập viện trong vòng 30 ngày. Tuy nhiên, thuốc không ảnh hưởng đến tỷ lệ suy tim xấu đi (WHF) hoặc tỷ lệ tử vong (20).
Một phân tích gộp gần đây xác nhận rằng việc sử dụng sớm thuốc ức chế SGLT2 trong bối cảnh STC giúp giảm 62% nguy cơ biến cố ST, bao gồm: tái nhập viện vì ST, nhập viện khoa cấp cứu, thăm khám cấp cứu, hoặc cần tăng cường điều trị trong các lần tái khám ngoại trú (21). Các kết quả chính từ các thử nghiệm đối chứng ngẫu nhiên (RCTs) NC thuốc ức chế SGLT2 trong giai đoạn cấp tính được tóm tắt trong Bảng 1 (3).
| RCT (năm) | Bệnh nhân | Thời điểm bắt đầu SGLT2i | Loại và liều thuốc SGLT2 | Tiêu chí chính | Kết quả chính |
| EMPA-RESPONSE-AHF (2020) | Bệnh nhân suy tim cấp (AHF) | Trong vòng 24 giờ nhập viện. | Empagliflozin 10 mg 1 lần/ngày | Thay đổi điểm khó thở trong thang điểm VAS, đáp ứng lợi tiểu, thay đổi nồng độ NT-proBNP và thời gian nằm viện. | • Không có sự khác biệt về kết cục chính giữa nhóm empagliflozin và giả dược.
• Empagliflozin làm giảm kết cục suy tim dần trong viện, tái nhập viện hoặc tử vong tại ngày thứ 60 so với giả dược (4(10%) so với 13(33%); p = 0.014). |
| SOLOIST-WHF (2020) | BN ĐTĐ 2 nhập viện vì ST xấu dần và được điều trị với lợi tiểu chích. | 48,8% BN trước xuất viện và trong vòng 2 ngày sau xuất viện ở 51,2% | Sotagliflozin 200 mg một ngày (có thể tăng đến 400 mg tùy tác dụng phụ). | Tổng tử vong do tim mạch và nhập viện và tái khám khẩn do suy tim (biến cố lần đầu và các lần sau). | • Tồng số biến cố mỗi 100 người-năm theo kết cục chính thấp hơn ở nhóm sotagliflozin so với giả dược (51 so với 76.3, HR=0.67, KTC 95%, 0.52-0.85; P<0.001)
• Tỷ lệ tử vong do tim mạch ở nhóm sotagliflozin là 10.6 so với 12.5 ở nhóm giả dược (HR 0.82; KTC 95%, 0.59-1.14). |
| EMPULSE (2022) | Bệnh nhân suy tim cấp mới phát hiện hoặc suy tim mạn mất bù. | Thời gian trung vị từ lúc nhập viện đến lúc phân ngẫu nhiên: 3 ngày. | Empagliflozin 10 mg 1 lần/ ngày | Tiêu chí gộp phân cấp của TV do mọi nguyên nhân, số biến cố ST và thời gian đến khi xảy ra biến cố ST lần đầu hoặc sự cải thiện >5 điểm trong thang điểm KCCQ tại ngày 90 so với ban đầu. | • Bệnh nhân ở nhóm empagliflozin đạt lợi ích lâm sàng tốt hơn nhóm giả dược ( tỉ lệ thắng là 1.36; KTC 95%, 1.09-1.68; P=0.0054) |
| EMPAG-HF (2022) | Bệnh nhân suy tim mất bù cấp | Trong vòng 12h sau nhập viện | Empagliflozin 25 mg 1 lần/ ngày | Tổng lượng nước tiểu trong 5 ngày | • Empagliflozin giúp tăng 25% lượng nước tiểu qua 5 ngày (trung bình 10.8 L so với 8.7 L ở giả dược, khác biệt nhóm ước tính là 2.2 L; KTC 95%, 8.4- 3.6; P=0.003) |
| DAPA-RESPONSE- AHF (2023) | Bệnh nhân suy tim cấp | Trong vòng 24h sau nhập viện | Dapagliflozin 10 mg 1 lần/ ngày | Khác biệt về diện tích dưới đường cong của thang điểm khó thở VAS trong 4 ngày đầu | • Dapagliflozin giúp giảm rõ rệt diện tích dưới đường cong của thang điểm khó thở VAS khi so với giả dược (3192.2+/- 1631.9 mm x h so với 4713.1+/- 1714.9 mm x h; P< 0.001).
• Mức giảm tương đối của NT-proBNP so với mức nền của nhóm dapagliflozin lớn hơn so với giả dược (-34.89% so với -10.085%; P=0.001). |
| DICTATE-AHF (2024) | Bệnh nhân suy tim cấp và đang hoặc sắp có kế hoạch điều trị với lợi tiểu chích | Trong vòng 24h sau nhập viện | Dapagliflozin 10 mg 1 lần/ ngày | Hiệu quả lợi tiểu thông qua tổng trọng lượng thay đổi trên mỗi liều lợi tiểu quai | • Tổng lượng nước tiểu trong 4 ngày nhiều hơn ở nhóm dapagliflozin so với giả dược (18600 mL so với 13700 mL; P= 0.031).
• Dapagliflozin giúp giảm tái nhập viện trong 30 ngày sau xuất viện. Về tác dụng lợi tiểu không khác biệt giữa dapagliflozin với chăm sóc thông thường (tỷ lệ chênh là 0.65; KTC 95% 0.41-1.02; P=0.06) |
Bảng 1. Thiết kế và kết quả chính của các thử nghiệm lâm sàng trong suy tim cấp.
III. HIỆU QUẢ LỢI ÍCH LÊN CHỨC NĂNG THẬN VÀ KALI MÁU
1. Khám phá chi tiết về bảo vệ chức năng thận
Các thuốc ức chế hệ renin-angiotensin (RAAS), ARNI và SGLT2i có ảnh hưởng đáng kể đến chức năng thận do gây ra các thay đổi trong sinh lý thận. Thuốc SGLT2i điều hòa lại chức năng thận bằng cách thiết lập lại đường cong chức năng thận và tác động đến mối quan hệ giữa áp lực thủy tĩnh trong cầu thận và quá trình thải natri (natri niệu). Tác động này được trung gian thông qua cơ chế phản hồi ống-cầu thận (tubuloglomerular feedback) và chống lại sự thay đổi ở tiểu động mạch đến và đi của cầu thận gây ra bởi hoạt động quá mức của hệ thần kinh giao cảm. Những thay đổi này làm thay đổi phân suất lọc sinh lý, gây ra ảnh hưởng baroreceptor và hóa học tại macula densa, và có thể ảnh hưởng đến chức năng ống thận (22). Sự giảm cấp tính áp lực trong cầu thận có thể giúp giảm hậu tải và tiền tải thất trái, đồng thời giảm huyết áp và độ cứng động mạch. Các cơ chế này có thể giải thích cho hiện tượng giảm eGFR ban đầu (early dip) – đây là một hiệu ứng dược lý học, không liên quan đến sự suy giảm chức năng thận lâu dài hay tác dụng phụ trên thận (23). Ở BN ĐTĐ, mức giảm eGFR cấp tính có xu hướng rõ rệt hơn, có thể phản ánh tình trạng áp lực cầu thận ban đầu cao hơn. Việc giảm nhẹ và thoáng qua eGFR sau khi khởi trị thuốc ức chế SGLT2 không nên được hiểu là sự suy giảm chức năng thận, mà nên được xem là phản ứng bảo vệ cầu thận đối với sự ức chế đồng vận chuyển natri-glucose. Vì vậy, hiện tượng này không nên là lý do để ngưng điều trị. Thông qua việc tăng bài niệu và lượng nước tiểu, các thuốc này có thể hỗ trợ điều trị nhằm đạt mức giảm dịch ròng tốt hơn trước khi xuất viện, mà không gây tổn thương chức năng thận (24,25).
Trong NC EMPAG-HF (Tác động của việc khởi trị sớm empagliflozin lên bài niệu và chức năng thận ở BN ST mất bù cấp), BN ST mất bù cấp được ngẫu nhiên dùng empagliflozin hoặc giả dược trong vòng 12 giờ kể từ khi nhập viện. Việc bổ sung sớm empagliflozin vào phác đồ lợi tiểu tiêu chuẩn mang lại lợi ích điều trị mà không gây lo ngại về an toàn thận. Cụ thể, tổng lượng nước tiểu tích lũy trong 5 ngày tăng 25% ở nhóm empagliflozin (trung vị 10,8 L so với 8,7 L ở nhóm giả dược; chênh lệch ước tính: 2,2 L; P = 0,003), mà không ảnh hưởng đến chức năng thận (eGFR: 51 ± 19 so với 54 ± 17 mL/phút/1,73 m²), lượng protein niệu tổng (492 ± 845 vs. 503 ± 847 mg/g creatinin; P = 0,975) và α1-microglobulin niệu (55,4 ± 38,6 so với 31,3 ± 33,6 mg/g creatinin; P = 0,066). Không có sự khác biệt có ý nghĩa thống kê về biến đổi eGFR giữa hai nhóm tại các thời điểm sau ngẫu nhiên hóa (26).
2. Thuộc tính giảm sung huyết
Việc bổ sung thuốc SGLT2i vào liệu pháp lợi tiểu thông thường giúp tăng lượng nước tiểu bài xuất và giảm liều trung bình hàng ngày của thuốc lợi tiểu quai, mà không ảnh hưởng đến chức năng thận. Trong NC EMPA-RESPONSE-AHF, lượng nước tiểu tích lũy đến ngày thứ 4 cao hơn rõ rệt ở nhóm dùng empagliflozin so với giả dược, mà không làm tăng tỷ lệ các biến cố bất lợi trên thận (7).
NC DICTATE-AHF (Hiệu quả và độ an toàn của dapagliflozin trong STC) cho thấy ở BN STC tải dịch, dapagliflozin có liên quan đến việc giảm liều thuốc lợi tiểu quai (và ít cần tăng liều lợi tiểu tĩnh mạch hơn để đạt được mức giảm cân tương đương với ĐT tiêu chuẩn), mặc dù không có sự giảm có ý nghĩa thống kê về hiệu quả lợi tiểu theo cân nặng (27).
NC DAPA-RESPONSE-AHF cho thấy nhóm dapagliflozin có lượng nước tiểu tích lũy và hiệu quả lợi tiểu cao hơn so với nhóm giả dược vào ngày thứ 4, với tỷ lệ suy giảm chức năng thận tương đương nhau (20).
Trong NC EMPULSE, tổn thương thận cấp xảy ra ở 7,7% BN dùng empagliflozin so với 12,1% ở nhóm giả dược. Sự thay đổi nồng độ creatinine từ ban đầu đến giá trị cuối cùng trong quá trình điều trị là tương tự nhau ở cả hai nhóm. Các tác giả cũng ghi nhận rằng hiện tượng giảm nhẹ eGFR quan sát thấy ở thời điểm bắt đầu ĐT không còn xuất hiện sau 90 ngày theo dõi (17). Không ghi nhận lo ngại nào về an toàn trong NC SOLOIST-WHF, khi tỷ lệ tổn thương thận cấp (AKI) ở nhóm dùng sotagliflozin tương đương với nhóm giả dược (15).
NC DAPA-RESIST (So sánh dapagliflozin với metolazone trong ST kháng lợi tiểu quai) đã ngẫu nhiên hóa 61 BN STC kháng lợi tiểu để dùng dapagliflozin 10 mg/ngày hoặc metolazone 5–10 mg/ngày trong tối đa 3 ngày liên tiếp, với thời gian theo dõi trung vị 90 ngày. Mặc dù dapagliflozin không hiệu quả hơn metolazone trong việc giảm mức độ ứ dịch, nhưng nó gây ít giảm nồng độ natri và kali máu hơn, đồng thời làm tăng chỉ số ure máu (BUN) và creatinine huyết thanh ít hơn. Việc sử dụng sớm thuốc ức chế SGLT2 có liên quan đến mức giảm ứ dịch tốt hơn và hồ sơ an toàn rất khả quan khi phối hợp với lợi tiểu quai hoặc lợi tiểu nhóm thiazide-like (28).
Trong thực hành lâm sàng, việc theo dõi sát chức năng thận là rất quan trọng. Không khuyến cáo khởi trị dapagliflozin ở BN có eGFR < 25 mL/phút/1,73 m², và không nên khởi trị empagliflozin nếu eGFR < 20 mL/phút/1,73 m².
3. Hiệu quả lên nồng độ kali
Tăng kali máu (hyperkalaemia) là một thách thức thường gặp ở BN ST, chịu ảnh hưởng bởi hoạt hóa thần kinh-hormone liên quan đến suy tim, các bệnh lý kèm theo như bệnh thận mạn (CKD) và ĐTĐ, cũng như việc sử dụng đồng thời các thuốc ĐT nền của ST như ARNI và thuốc đối kháng thụ thể mineralocorticoid (MRAs). Sự hiện diện của tăng kali máu có thể hạn chế nghiêm trọng việc khởi trị hoặc tăng liều nhanh các thuốc ĐT ST.
Một phân tích gộp từ các nghiên cứu EMPEROR-Reduced và EMPEROR-Preserved (nghiên cứu empagliflozin ở BN HFpEF) chủ yếu ở bối cảnh BN ngoại trú mạn tính cho thấy rằng empagliflozin giúp giảm tiêu chí gộp gồm tăng kali máu do bác sĩ báo cáo hoặc nhu cầu sử dụng thuốc gắn kali, so với giả dược (6,5% so với 7,7%; HR: 0,82; KTC 95%: 0,71–0,95; P = 0,01). Empagliflozin cũng giảm tỷ lệ chung của tăng kali máu (6,1% so với 7,2%; HR: 0,83; KTC 95%: 0,71–0,97; P = 0,018) mà không làm tăng đáng kể nguy cơ hạ kali máu. Lợi ích này được ghi nhận ở nhiều phân nhóm khác nhau, bao gồm các mức phân suất tống máu (LVEF), tình trạng đái tháo đường, và việc sử dụng MRAs, đặc biệt rõ rệt ở bệnh nhân có eGFR thấp (29).
Một phân tích gộp khác gồm 5 thử nghiệm lâm sàng (11.123 bệnh nhân đã dùng MRAs) cho thấy rằng: Phối hợp thuốc SGLT2i với MRAs làm giảm đáng kể nguy cơ tăng kali máu so với việc dùng MRAs đơn thuần (HR: 0,61; KTC 95%: 0,50–0,75; P < 0,00001) (30).
Những kết quả này làm nổi bật vai trò tiềm năng của SGLT2i trong việc phòng ngừa tăng kali máu, đặc biệt là sau khi khởi trị hoặc tăng liều các thuốc ĐT ST khác, từ đó tăng khả năng dung nạp với ARNI và MRAs.
IV. CHIẾN LƯỢC SỬ DỤNG THUỐC ỨC CHẾ SGLT2 TRONG SUY TIM CẤP
1. Thời điểm khởi trị sớm thuốc ức chế SGLT2
Bản cập nhật trọng tâm năm 2023 của Hướng dẫn ESC về ST đưa ra khuyến cáo mức I cho chiến lược khởi trị nhanh chóng và tăng liều sớm các thuốc ĐT ST ngay trước khi xuất viện và trong các lần tái khám sớm sau nhập viện. Hiện tại, cách tiếp cận được khuyến nghị là khởi đầu với liều thấp của cả bốn nhóm thuốc chính nếu tình trạng BN cho phép, ưu tiên khởi trị tất cả nhóm thuốc hơn là tối ưu liều từng nhóm riêng lẻ. Việc phối hợp các thuốc cứu sống trong ST đã được chứng minh là cải thiện đáng kể các tiêu chí lâm sàng cứng (hard endpoints) ở quần thể BN SR (31,32). Trong trường hợp không thể bắt đầu được đồng thời cả 4 thuốc tứ trụ, chúng ta sẽ bắt đầu từ 2-3 thuốc hay từng thuốc tùy theo tình trạng của BN và đánh giá sát để có kế hoạch phối hợp sớm các thuốc còn lại nếu được.
NC STRONG-HF chứng minh rằng việc khởi trị và/hoặc tăng liều các thuốc uống ĐT ST (gồm ức chế men chuyển ACE, ARBs hoặc ARNI, chẹn beta, và MRAs) trong vòng 2 ngày trước xuất viện hoặc ngay sau xuất viện là an toàn và hiệu quả, giúp cải thiện tiên lượng rõ rệt mà không gây lo ngại về độ an toàn (33). Dù thuốc SGLT2i không được đánh giá trực tiếp trong NC này, khuyến cáo hiện tại cũng bao gồm empagliflozin và dapagliflozin, dựa trên bằng chứng gần đây. Việc khởi trị sớm trong giai đoạn nằm viện và duy trì sau xuất viện mang lại lợi ích lâm sàng trong vòng chưa đến 2 tuần. Tuy nhiên, dữ liệu về hiệu quả dài hạn của nhóm thuốc này vẫn còn hạn chế. Mặc dù hiện tại ít bằng chứng so sánh trình tự khởi trị các thuốc, đặc biệt ở BN HFrEF mới khởi phát (de novo HF), ngày càng có xu hướng đưa vào đồng thời cả bốn nhóm thuốc nền sau khi BN được ổn định, kết hợp với thuốc lợi tiểu theo nhu cầu để giảm và phòng ứ dịch. Nhờ tác dụng bảo vệ mạch máu và hormone, SGLT2i có thể dùng an toàn ở BN rối loạn chức năng thận và/hoặc tăng kali máu ở mức cho phép, giúp tạo điều kiện khởi trị các thuốc ĐT ST khác. SGLT2i còn giúp tăng khả năng dung nạp với các thuốc nền khác, vì vậy trình tự khởi trị hợp lý rất quan trọng để đảm bảo an toàn khi bổ sung các thuốc khác về sau. Tuy nhiên, việc sử dụng phối hợp nhiều thuốc ĐT ST đòi hỏi thận trọng, cần theo dõi xét nghiệm thường xuyên, đặc biệt là trong giai đoạn tăng liều và khi BN có tái phát STC (3,34).
Trong thực hành lâm sàng, nên khởi trị thuốc SGLT2i sớm trong thời gian nằm viện, tốt nhất là trước khi xuất viện, đối với BN nhập viện vì STC. Điều này chỉ áp dụng cho BN không có: tụt huyết áp có triệu chứng, cần tăng liều lợi tiểu, nhiễm trùng tiểu hoặc tiền sử bệnh tiết niệu, sử dụng thuốc tăng co bóp tim hoặc thuốc giãn mạch tĩnh mạch trong vòng 6 giờ qua, hoặc có chống chỉ định rõ ràng. Kết hợp ARNIs và thuốc SGLT2i là an toàn, với các bằng chứng cho thấy liệu pháp ĐT toàn diện ST giúp kéo dài thời gian sống không biến cố thêm 8 năm ở người lớn 50 tuổi. Theo khuyến cáo ESC 2019 về đái tháo đường, thuốc SGLT-2i là lựa chọn ĐT đầu tay ưu tiên cho BN HFrEF mới được chẩn đoán ĐTĐ típ 2, ngay cả khi chưa từng dùng metformin trước đó. Hiệu quả ĐT ST của nhóm thuốc SGLT2i là tương đồng trong toàn nhóm, bất kể sự khác biệt về ái lực với thụ thể. Gần đây, cập nhật trọng tâm năm 2024 của Hiệp hội Tim mạch Hoa Kỳ (ACC) về lộ trình quyết định đồng thuận của chuyên gia trong đánh giá lâm sàng, quản lý và tiên lượng ở bệnh nhân nhập viện vì suy tim trong đồng thuận 2024 cũng chỉ rõ các bằng chứng hiện nay ủng hộ việc sử dụng thuốc SGLT2i trong lúc nằm viện nhằm giảm thêm tỷ lệ mắc bệnh và TV ở BN ST, trên nhiều mức phân suất tống máu thất trái khác nhau, dù có hay không mắc ĐTĐ2. Hiện đã có đủ bằng chứng để khuyến cáo khởi trị hoặc tiếp tục sử dụng nhóm thuốc này trong bệnh viện, đối với BN nhập viện vì ST mất bù cấp (hình 2). Nếu không thể khởi trị trước khi xuất viện, nên bắt đầu trong vòng 3 ngày sau đó (xem hình 3). Tuy nhiên, chiến lược ĐT có thể khác nhau giữa ST mới khởi phát và STC tái phát: (1) Ở BN ST mới khởi phát, SGLT2i nên được khởi trị để tác động vào quá trình bệnh lý nền và khôi phục huyết động cơ bản. (2) Ở BN STC tái phát (ST mất bù cấp), quyết định ĐT nên dựa trên mức độ dung nạp thuốc, ĐT ST trước đó, nguyên nhân nhập viện, tiền sử BN và chức năng thận nền (12, 34, 35, 36,37).
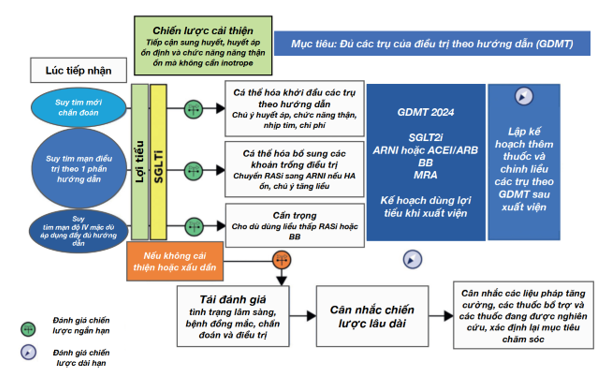
Hình 2. Tăng liều điều trị theo hướng dẫn (GDMT) ở BN HFrEF theo biểu hiện ban đầu và tiến triển lâm sàng. BN HFrEF mất bù cần đượcdùng lợi tiểu và khởi trị thuốc SGLT2i, trừ khi có chống chỉ định hoặc hạn chế về chi phí. Với những BN có tiến triển cải thiện (biểu tượng hướng gió màu xanh lá), nên tối ưu hóa ĐT GDMT (Nếu là chẩn đoán suy tim mới, nên cố gắng khởi trị cả 4 trụ cột GDMT. Nếu bn đã bị suy tim mạn và đang dùng một phần các thuốc GDMT, cần cá nhân hóa ĐT để bổ sung những thành phần còn thiếu, bao gồm xem xét chuyển từ ACEi/ARB sang ARNI nếu phù hợp. Thận trọng với bn st mạn giai đoạn IV (NYHA Class IV) có tình trạng mất bù, vì những bn này có thể không dung nạp được ngay cả liều thấp của chẹn beta và thuốc ức chế RAS. Tuy nhiên, vẫn nên cố gắng điều chỉnh liều nếu có thể. Đối với BN có diễn tiến lâm sàng ngắn hạn không cải thiện hoặc xấu đi (biểu tượng hướng gió màu cam), cần đánh giá lại các bệnh đồng mắc và xem xét các chẩn đoán khác. Với BN diễn tiến xấu dần kéo dài (biểu tượng la bàn) cũng nên được đánh giá lại, cân nhắc về mục tiêu ĐT, khả năng tiếp cận các phương pháp ĐT chuyên sâu hơn, và các phương pháp ĐT thử nghiệm. Mục tiêu lý tưởng là: Khởi trị đầy đủ cả 4 trụ cột ĐT GDMT cho HFrEF ngay trong thời gian nằm viện, trên nền liệu pháp lợi tiểu thích hợp, đồng thời, cần có kế hoạch tiếp tục bổ sung và tăng liều GDMT sau khi xuất viện (34).
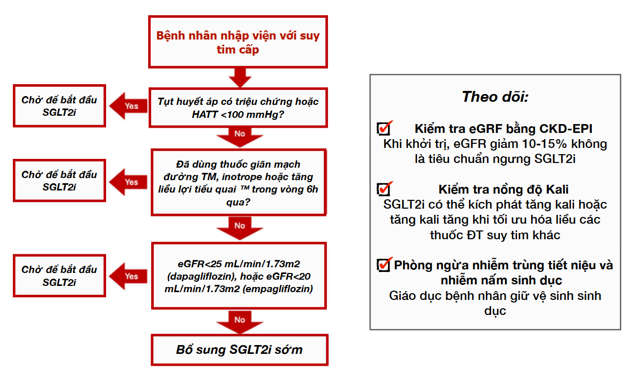
Hình 3. Lưu đồ thực tiễn để khởi trị nhanh thuốc ức chế SGLT2 trong bệnh viện (3)
Yếu tố xã hội, trí tuệ và trình độ giáo dục của BN cũng có thể ảnh hưởng đến khả năng dùng thuốc đúng cách, tăng nguy cơ bỏ thuốc hoặc ngừng thuốc trước và sau xuất viện, điều này liên quan đến tăng nguy cơ biến cố bất lợi. Trong thực tế, nhiều yếu tố khiến việc sử dụng hoặc tăng liều các thuốc này bị hạn chế, bao gồm: tuổi cao, tụt huyết áp, suy thận, tăng kali máu, chi phí điều trị, khó tiếp cận dịch vụ y tế, và sự trì hoãn từ phía nhân viên y tế (3, 38). Nhập viện là cơ hội vàng để tối ưu hóa ĐT ST trong một môi trường được theo dõi chặt chẽ. Khởi trị thuốc SGLT2i trong giai đoạn này (trong thời gian nằm viện và trước khi xuất viện) giúp đánh giá tốt hơn khả năng dung nạp và các tác dụng phụ, tăng tiềm năng lợi ích của việc khởi trị sớm, tạo ra một cơ hội bổ sung để tối ưu hóa việc ĐT bằng thuốc cũng như theo dõi các tác dụng bất lợi có thể xảy ra, từ đó tăng khả năng đạt được liều mục tiêu trong cả giai đoạn theo dõi ngắn hạn và dài hạn. Tuy nhiên còn nhiều rào cản để kê đơn thuốc này (lựa chọn của BN, giá, giảm thể tích tuần hoàn và tổn thương thận cấp (AKI) liên quan, hạ đường huyết, toan ceton do đái tháo đường (DKA), và nhiễm trùng đường tiết niệu – sinh dục) và chúng ta cần có chiến lược để tăng sử dụng thuốc (hình 4) (36, 39). Dù các tác dụng phụ của thuốc SGLT2i nhìn chung có thể kiểm soát được và các biến cố nghiêm trọng là hiếm gặp, các chiến lược ĐT nên bao gồm việc thành lập nhóm đa chuyên khoa thực hiện điều trị theo hướng dẫn (GDMT – guideline-directed medical therapy), phối hợp giữa dược sĩ và bác sĩ, điều chỉnh nhẹ phù hợp với từng BN và xử lý kịp thời trong các trường hợp bệnh cấp tính hoặc phẫu thuật lớn có thể cải thiện việc tối ưu hóa ĐT ST trong thời gian nằm viện và sau khi xuất viện (36, 40).
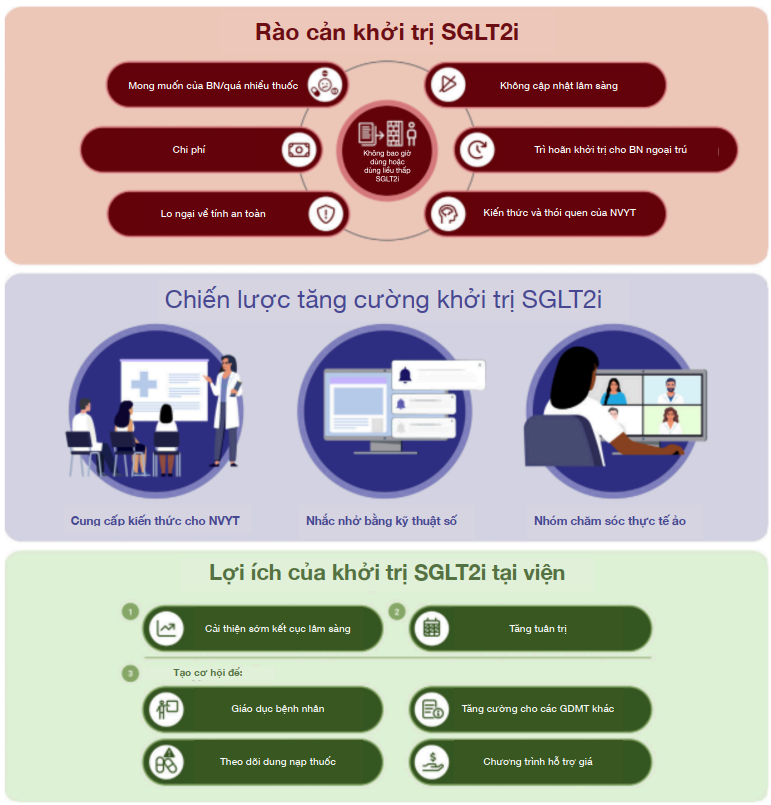
Hình 4. Thách thức và cơ hội trong việc khởi trị thuốc ức chế SGLT2 cho bệnh nhân nội trú (39)
2. Liều dùng
Liều dùng: Dapagliflozin và empagliflozin thường được sử dụng với liều 10 mg mỗi ngày, uống vào bất kỳ thời điểm nào trong ngày, không phụ thuộc vào bữa ăn.
Lưu ý: Dapagliflozin chống chỉ định ở bệnh nhân có eGFR < 25 mL/phút/1,73m², còn empagliflozin chống chỉ định bệnh nhân có eGFR < 20 mL/phút/1,73m²
3. Một số tình huống đặc biệt
3.1. Huyết áp thấp ở bệnh nhân suy tim cấp
Trong bối cảnh STC, các giá trị huyết áp cần được diễn giải dựa trên tình trạng lâm sàng và tiến triển của BN. Trong một NC gần đây về STC, những BN có huyết áp tâm thu thấp nhưng không có dấu hiệu giảm tưới máu cơ quan có tiên lượng tương tự như những BN có huyết áp bình thường. Thật vậy, phân nhóm lâm sàng dựa trên tình trạng sung huyết và tưới máu là yếu tố then chốt, vì chỉ số huyết áp đơn lẻ không đủ để định hướng ĐT hay dự báo tiên lượng. Phần lớn BN trong giai đoạn cấp đều có tình trạng sung huyết nhưng tưới máu tốt (kiểu hình “ướt và ấm” theo phân loại Forrester), do đó không có chống chỉ định trong việc tiếp tục hoặc khởi trị các liệu pháp ĐT ST theo hướng dẫn (GDMT) sau khi đã đạt được sự ổn định lâm sàng.
Trong các trường hợp STC có huyết áp thấp, cần loại trừ tình trạng sốc tim (được định nghĩa là huyết áp tâm thu <90 mmHg kèm theo dấu hiệu giảm tưới máu cơ quan), vì hướng xử trí điều trị sẽ tuân theo các khuyến cáo riêng cho sốc tim. Đáng chú ý, cần lưu ý rằng trong giai đoạn đầu của sốc tim, giảm tưới máu có thể xảy ra mà không có hạ huyết áp rõ rệt, vì huyết áp có thể vẫn được duy trì nhờ cơ chế co mạch bù trừ, nhưng phải đánh đổi bằng giảm oxy hóa và tưới máu mô. Trong 48 giờ đầu sau nhập viện, mục tiêu điều trị chính là: ổn định huyết động, giải quyết tình trạng quá tải thể tích và sung huyết, đảm bảo tưới máu và oxy mô đầy đủ. Ở giai đoạn này, việc tiếp tục hoặc khởi trị liệu pháp ĐT ST nên được cân nhắc dựa trên kiểu hình lâm sàng cụ thể. Thông thường, ở các kiểu hình STC như “khô và lạnh” hoặc “ướt và lạnh”, có thể cần giảm liều hoặc ngừng tạm thời một số thuốc ĐT ST – đặc biệt là thuốc chẹn beta và/hoặc ức chế hệ renin–angiotensin.
Sau 48 giờ đầu, liệu pháp ĐT ST có thể được khởi trị, khởi trị lại hoặc điều chỉnh liều tăng dần, tùy theo diễn biến lâm sàng và đặc điểm cá nhân của BN (ví dụ: đã có GDMT tối ưu hay chưa, STC mới khởi phát, v.v.). Thông thường, nên khởi đầu hoặc tái khởi đầu bằng các thuốc ít ảnh hưởng đến huyết áp, chẳng hạn như SGLT2i hoặc khởi đầu liều thấp của thuốc đối kháng thụ thể mineralocorticoid (MRA), sau đó thêm dần các thuốc khác và tăng dần liều một cách thận trọng. Quá trình tăng liều này có thể kéo dài 4–6 tuần, cần theo dõi chặt chẽ và điều chỉnh liều từng bước nhỏ, mỗi loại thuốc được thêm vào một cách tuần tự. Mọi nỗ lực nên được thực hiện để khởi trị đầy đủ các liệu pháp nền tảng, trừ khi có chống chỉ định rõ ràng. Khuyến nghị lâm sàng sư dụng SGLT2i nêu trong box và hình 5. Cần nhớ, theo dõi sát HA, cân bằng dịch và chức năng thận, đặc biệt trong 24-48h đầu (41)
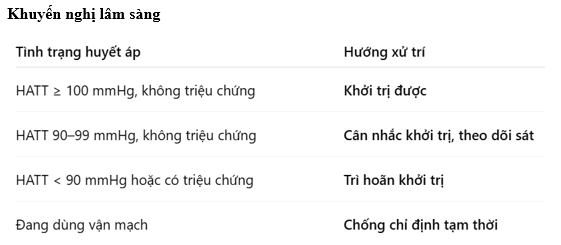
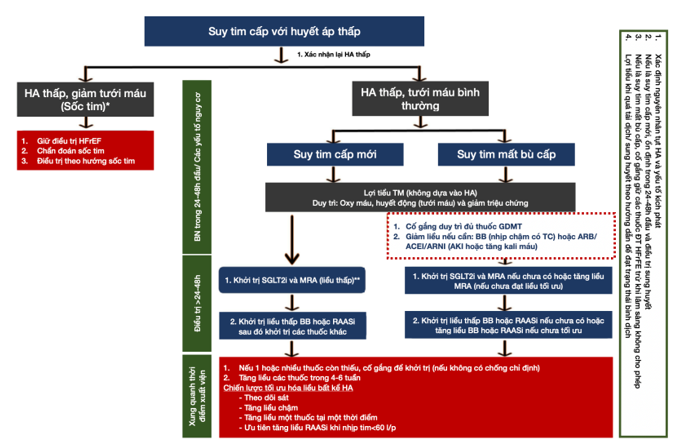
Hình 4. Thuật toán đề xuất (proposed algorithm) để tối ưu hóa điều trị ở bệnh nhân suy tim phân suất tống máu giảm (HFrEF) có huyết áp thấp trong bối cảnh suy tim cấp (AHF).
Phần này tổng hợp từ các hướng dẫn và nghiên cứu mới nhất (ESC 2023, AHA/ACC/HFSA 2022, EMPULSE, DAPA-HF (41).
3.2. Người cao tuổi
Người cao tuổi hay có đa bệnh lý và nhạy cảm với mất nước, rối loạn huyết động, đồng thời nguy cơ nguy cơ hạ huyết áp tư thế, té ngã cao hơn, nên phả thận trọng khi sử dụng. Nhìn chung, người ≥ 75 tuổi, ổn định có thể khởi trị được liều chuẩn. Người có hạ áp tư thế hoặc mất nước theo dõi sát, bù dich nếu cần. người trên 85 tuổi, yếu. dễ ngã cần cân nhắc lợi ích và nguy cơ. Cần chú ý uống đủ nước, theo dõi hạ HA tư thế và không cần chỉnh liều theo tuổi (12,42,43).
V. KẾT LUẬN VÀ KHUYẾN CÁO
Việc sử dụng sớm thuốc SGLT2i trong thời gian nằm viện hoặc ngay sau khi xuất viện ở BN STC là an toàn và đã cho thấy lợi ích tiên lượng rõ ràng, mặc dù vẫn còn thiếu dữ liệu dài hạn. Việc khởi trị sớm trong STC, ngay trong quá trình nhập viện, mang lại lợi ích lâm sàng sớm (15–90 ngày) và giảm tái nhập viện, đồng thời điều này giúp vượt qua sự trì hoãn trong điều trị – thường xảy ra ngoài môi trường bệnh viện, đặc biệt khi việc ĐT do các bác sĩ không chuyên về tim mạch đảm trách. Nên khuyến khích việc khởi trị đồng thời liệu pháp y học tứ trụ liều thấp ở những BN nhập viện vì ST. Tuy nhiên, việc sử dụng đồng thời các liệu pháp ĐT ST có thể làm giảm tạm thời eGFR sau khi khởi trị sớm, điều này có thể góp phần làm trì hoãn việc bắt đầu và điều chỉnh liều các phương pháp điều trị cứu sống này. Trong phần lớn các trường hợp, suy giảm chức năng thận chỉ là tạm thời, với chức năng thận trở lại mức ban đầu hoặc duy trì ổn định về lâu dài. Vì vậy, trong giai đoạn cấp, việc sử dụng sớm cần được cá nhân hóa dựa trên tình trạng huyết động, mức độ ứ trệ và chức năng thận.
Các thuốc SGLT2i không cho thấy có tương tác đáng kể với các liệu pháp ĐT ST khác và được xem là lựa chọn ĐT hàng đầu trong hầu hết các trường hợp nhờ hồ sơ an toàn và khả năng dung nạp thuận lợi. Cần đẩy mạnh ứng dụng rộng rãi trong thực hành, đi kèm cập nhật kiến thức và thay đổi thói quen kê đơn.
TÀI LIỆU THAM KHẢO
- WG et al: Cardiac, renal, and metabolic effects of sodium–glucose co-transporter 2 inhibitors: a position paper from the European Society of Cardiology ad-hoc task force on sodium–glucose co-transporter 2 inhibitors. European Journal of Heart Failure (2021). doi:10.1002/ejhf.2286
- S. SGLT2 inhibitors in Patients Admitted for Acute Heart Failure: The Earlier the Better. THE AMERICAN JOURNAL OF CARDIOLOGY. 2024. Volume 214; p:177-179
- R et al. Early administration of SGLT2 inhibitors in hospitalized patients: A practical guidance from the current evidence. ESC Heart Failure (2025) DOI: 10.1002/ehf2.15293.
- T, Gong. T: SGLT2 inhibitors: a new pillar of the heart failure regimen. Rev. Cardiovasc. Med. 2021 vol. 22(4), 1253-1269.
- Nguyễn Thanh Hiền, Trần Nguyễn Thu Thủy. Thuốc ức chế SGLT2: trụ cột mới trong phác đồ điều trị suy tim. Chuyên đề tim mạch học tp Hồ Chí Minh 2022
- Heerspink HJLet al. SGLT2 inhibitors in the treatment of diabetes and cardiovascular disease: A review of the evidence. Circulation. 2016;134(10):752–772.
- Butler J, et al. Empagliflozin Initiated in Patients Hospitalized for Acute Heart Failure: A Multinational Randomized Trial (EMPA-RESPONSE-AHF). JACC Heart Fail. 2020;8(9):798–807.
- Voors AA, et al. The SGLT2 inhibitor empagliflozin in patients hospitalized for acute heart failure: A randomized, double-blind, placebo-controlled trial. Lancet. 2022;400(10358):731–739. (EMPULSE trial)
- Ferrannini E, Mark M, Mayoux E. CV protection in the EMPA-REG OUTCOME trial: A “thrifty substrate” hypothesis. Diabetes Care. 2016; 39(7): 1108–1114.
- McMurray JJV, et al. DAPA-HF Trial Investigators. Dapagliflozin in patients with heart failure and reduced ejection fraction. N Engl J Med. 2019;381(21):1995–2008.
- Packer M. Sodium–glucose cotransporter 2 inhibitors: Role in the treatment of heart failure with reduced ejection fraction. Trends Cardiovasc Med. 2020; 30(8) :404–412.
- 2022 AHA/ACC/HFSA Guidelines for the Management of Heart Failure Journal of the American College of Cardiology.
- Packer M et al. Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med 2020; 383:1413-1424. doi:10.1056/NEJMoa2022190
- Chen K et al. Time to benefit of sodium-glucose cotransporter-2 inhibitors among patients with heart failure. JAMA Netw Open 2023;6: e2330754. doi:10.1001/ jamanetworkopen.2023.30754
- Bhatt DL et al. Sotagliflozin in patients with diabetes and recent worsening heart failure. N Engl J Med 2021; 384:117-128. doi:10.1056/NEJMoa2030183
- Pitt B et al. Effect of sotagliflozin on early mortality and heart failure-related events. JACC Heart Fail 2023; 11:879-889. doi:10.1016/j. jchf.2023.05.026
- Voors AA, et al. The SGLT2 inhibitor empagliflozin in patients hospitalized for acute heart failure: a multinational randomized trial. Nat Med 2022; 28: 568-574.
doi:10.1038/s41591-021-01659-1 - Biegus J, et al. Impact of empagliflozin on decongestion in acute heart failure: the EMPULSE trial. Eur Heart J 2023;44: 41-50. doi:10.1093/eurheartj/ehac530
- Solomon SD et al. Dapagliflozin in heart failure with mildly reduced or preserved ejection fraction. N Engl J Med 2022;387: 1089-1098. doi:10.1056/NEJMoa2206286
- Emara AN ET AL. The clinical outcomes of dapagliflozin in patients with acute heart failure: a randomized controlled trial (DAPA-RESPONSE-AHF). Eur J Pharmacol 2023;15:176179. doi:10. 1016/j.ejphar.2023.176179
- Ul Amin N et al. SGLT2 inhibitors in acute heart failure: a meta-analysis of randomized controlled trials. Dent Health 2022; 10:2356. doi:10.3390/healthcare10122356
- Beltrami M et al. The treatment of heart failure in patients with chronic kidney disease: doubts and new developments from the last ESC guidelines. J Clin Med 2022; 11:2243. doi:10.3390/jcm11082243
- The EMPA-KIDNEY Collaborative Group. Empagliflozin in patients with chronic kidney disease. N Engl J Med 2023; 388:117-127. doi:10.1056/NEJMoa2204233
- Petrie MC et al. Effect of Dapagliflozin on worsening heart failure and cardiovascular death in patients with heart failure with and without diabetes. JAMA 2020;323: 1353-1368. doi:10.1001/jama.2020.1906
- Mullens W et al. Renal effects of guideline-directed medical therapies in heart failure: a consensus document from the heart failure Association of the European Society of Cardiology. Eur J Heart Fail 2022; 24:603-619. doi:10.1002/ejhf.2471
- Schulze PC et al. Effects of early empagliflozin initiation on diuresis and kidney function in patients with acute decompensated heart failure (EMPAG-HF). Circulation 2022;146: 289-298. doi:10.1161/CIRCULATIONAHA.122.059038
- Cox ZL et al. Efficacy and safety of dapagliflozin in patients with acute heart failure. J Am Coll Cardiol 2024; 83:1295-1306. doi: 10.1016/j.jacc.2024.02.009
- Yeoh SE et al. Dapagliflozin vs. metolazone in heart failure resistant to loop diuretics. Eur Heart J 2023;44: 2966-2977. doi:10.1093/eurheartj/ehad341
- Ferreira JP et al. Empagliflozin and serum potassium in heart failure: an analysis from EMPEROR-pooled. Eur Heart J 2022; 43:2984-2993. doi:10.1093/eurheartj/ehac306
- Neuen BL et al. Sodium-glucose cotransporter 2 inhibitors and risk of hyperkalemia in people with type 2 diabetes: a meta-analysis of individual participant data from randomized. Controlled Trials Circ 2022;145: 1460-1470. doi:10.1161/CIRCULATIONAHA.121.057736
- McDonagh TA et al. 2023 focused update of the 2021 ESC guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2023;44: 3627-3639. doi:10.1093/eurheartj/ehad195
- Packer M, McMurray JJV. Rapid evidence-based sequencing of foundational drugs for heart failure and a reduced ejection fraction. Eur J Heart Fail 2021; 23:882-894. doi:10.1002/
2149 - Mebazaa A et al. Safety, tolerability and efficacy of up-titration of guideline-directed medical therapies for acute heart failure (STRONG-HF): a multinational, openlabel, randomised, trial. Lancet Lond Engl 2022; 400:1938-1952. doi:10.1016/S0140-6736(22)02076-1
- Hollenberg SM et al. 2024 ACC expert consensus decision pathway on clinical assessment, management, and trajectory of patients hospitalized with heart failure focused update. J Am Coll Cardiol 2024; 84: doi: 10.1016/j.jacc.2024.06.002
- Ferreira JP. Use of sodium glucose co-transporter 2 inhibitors in acute heart failure: a practical guidance. ESC Heart Fail 2022; 9:4344-4347.
- K et al. Glucose Cotransporter-2 Inhibitors: Who, When & How? Guidance for Use from a Multidisciplinary Practical Approach. Inter J of clin med. 2024, 15:415-425.
- MH et al. In‑hospital initiation of sodium‑glucose co‑transporter‑2 inhibitors in patients with acute heart failure. Heart Failure Reviews (2025) 30:89–101.
- Reach G. Patient non-adherence and healthcare-provider inertia are clinical myopia. Diabetes Metab 2008;34: 382-385
- Unlu O, Bhatt AS, Blood AJ. Use of sodium–glucose cotransporter 2 inhibitors
in hospitalized patients. JACC Adv 2024; 3:101024 - Bhatt AS et al. Virtual optimization of guideline-directed medical therapy in hospitalized patients with heart failure with reduced ejection fraction: the IMPLEMENT-HF pilot study. Eur J Heart Fail 2021; 23:1191-1201. doi:10.1002/ejhf.2163
- H et al. Clinical management and therapeutic optimization of patients with heart failure with reduced ejection fraction and low blood pressure. A clinical consensus statement of the Heart Failure Association (HFA) of the ESC. European Journal of Heart Failure (2025). doi:10.1002/ejhf.3618
- Butler J, et al. Efficacy and Safety of SGLT2 Inhibitors in Older Patients with Heart Failure.J Am Geriatr Soc. 2022;70(4):1043–1053.
- N et al. The efficacy and safety of sodium-glucose cotransporter 2 inhibitors in patients aged over 80 years with heart failure. ESC Heart Failure 2025; 12: 2087–2097







