Yamashita Y, Morimoto T, Muraoka N, và cộng sự
Lược dịch: BS.CKII NGUYỄN TRẦN TUYẾT TRINH
Giảng viên bộ môn Nội Tổng quát, Đại học Y Dược TP.HCM
ĐẶT VẤN ĐỀ
Thời gian điều trị kháng đông tối ưu trên bệnh nhân ung thư có thuyên tắc phổi (PE) cấp nguy cơ thấp là vấn đề quan trọng trên lâm sàng. Tuy nhiên cho đến hiện tại dữ liệu liên quan đến vấn đề này vẫn còn hạn chế. Việc kéo dài thời gian sử dụng kháng đông có thể mang lại lợi ích trong việc dự phòng các biến cố huyết khối; tuy nhiên, việc điều trị này cũng có thể làm tăng nguy cơ xuất huyết.
PHƯƠNG PHÁP
Đây là thử nghiệm lâm sàng ngẫu nhiên, đa trung tâm, nhãn mở, đánh giá kết cục mù được tiến hành tại 32 trung tâm nghiên cứu tại Nhật Bản. Bệnh nhân ung thư có PE nguy cơ thấp được định nghĩa là có điểm PESI giản lược bằng 1, được phân nhóm ngẫu nhiên sử dụng rivaroxaban 6 hoặc 12 tháng theo tỷ lệ 1:1. Kết cục chính là tỷ lệ tái phát thuyên tắc huyết khối tĩnh mạch (VTE) sau 18 tháng. Kết cục phụ quan trọng là tỷ lệ xuất huyết nặng sau 18 tháng theo tiêu chí ISTH. Giả thuyết chính được kiểm định là điều trị 18 tháng vượt trội điều trị 6 tháng theo kết cục chính.
KẾT QUẢ
Từ tháng 2 năm 2021 đến tháng 3 năm 2023, 179 bệnh nhân đã được phân nhóm ngẫu nhiên, và sau khi loại trừ một bệnh nhân không đồng ý tham gia, 178 bệnh nhân đã được đưa vào phân tích theo dự kiến điều trị (ITT): 89 bệnh nhân trong nhóm điều trị rivaroxaban 18 tháng và 89 bệnh nhân trong nhóm điều trị rivaroxaban 6 tháng. Độ tuổi trung bình là 65.7 tuổi; 47% bệnh nhân là nam giới, và 12% có triệu chứng PE tại thời điểm bắt đầu. Kết cục chính về tái phát VTE xảy ra ở 5 trong số 89 bệnh nhân (5.6%) trong nhóm rivaroxaban 18 tháng và 17 trong số 89 bệnh nhân (19.1%) trong nhóm rivaroxaban 6 tháng (OR = 0.25; [95% CI, 0.09–0.72]; P=0.01). Trong số 22 trường hợp tái phát VTE, 5 bệnh nhân có triệu chứng; 11 bệnh nhân tái phát PE, trong đó có 2 bệnh nhân tắc động mạch chính và 4 bệnh nhân tắc động mạch thùy; và tái phát huyết khối tĩnh mạch sâu được ghi nhận ở 11 bệnh nhân, trong đó có 3 bệnh nhân với huyết khối tĩnh mạch sâu đoạn gần. Kết cục phụ quan trọng về xuất huyết nặng xảy ra ở 7 trong số 89 bệnh nhân (7.8%) trong nhóm rivaroxaban 18 tháng và 5 trong số 89 bệnh nhân (5.6%) trong nhóm rivaroxaban 6 tháng (OR = 1,43; [95% CI, 0.44–4.70]; P=0.55).
KẾT LUẬN
Ở bệnh nhân ung thư có PE nguy cơ thấp (sPESI =1), sử dụng rivaroxaban trong 18 tháng vượt trội so với 6 tháng trong dự phòng tái phát VTE.
ĐĂNG KÝ: URL: https://www.clinicaltrials.gov; Số đăng ký: NCT04724460

Bệnh nhân ung thư có thể kéo dài tuổi thọ nhờ những tiến bộ trong chẩn đoán và điều trị ung thư sớm, cũng như kiểm soát các biến chứng trong quá trình điều trị ngày càng trở nên quan trọng về mặt lâm sàng từ góc độ tim mạch – ung thư.1 Thuyên tắc phổi (PE) là một trong những biến chứng nghiêm trọng ở bệnh nhân ung thư.2 PE đã được báo cáo phát hiện trong 3.6% trường hợp chụp cắt lớp vi tính (CT) ngực thường quy để đánh giá ung thư.3 Bệnh nhân ung thư có PE nguy cơ thấp, bao gồm PE phát hiện tình cờ và các trường hợp nhẹ đã trở nên khá phổ biến trong thực hành lâm sàng hàng hiện nay. Bệnh nhân PE có nguy cơ tái phát VTE trong dài hạn, và nguy cơ này có thể được dự phòng bằng kháng đông.4 Tuy nhiên, dữ liệu trên bệnh nhân ung thư có PE nguy cơ thấp vẫn còn hạn chế và các chiến lược kháng đông tối ưu cho nhóm bệnh nhân này vẫn là vấn đề đang được tranh luận.
Hiện nay, các hướng dẫn trên thế giới khuyến cáo sử dụng kháng đông kéo dài hơn 6 tháng cho bệnh nhân PE có ung thư đang hoạt động.5-7 Tuy nhiên, một số hướng dẫn khuyến cáo các chiến lược quản lý tương tự cho bệnh nhân PE được phát hiện tình cờ5,6 và PE nhẹ8 với mức độ bằng chứng không chắc chắn. Một nghiên cứu quan sát trước đây cho thấy rằng bệnh nhân ung thư có PE nguy cơ thấp, chẳng hạn như PE được phát hiện tình cờ, có nguy cơ tái phát VTE tương đối cao,9 điều này gợi ý rằng những bệnh nhân này có thể được hưởng lợi từ điều trị kháng đông kéo dài. Vì chưa có thử nghiệm lâm sàng ngẫu nhiên nào về vấn đề này, chúng tôi đã tiến hành thử nghiệm ONCO PE để đánh giá hiệu quả và độ an toàn của các chiến lược dự phòng tái phát VTE bằng rivaroxaban với thời gian dự phòng khác nhau trên bệnh nhân ung thư có PE nguy cơ thấp.
PHƯƠNG PHÁP
Thiết kế nghiên cứu
Thử nghiệm ONCO PE (NCT04724460) là thử nghiệm lâm sàng ngẫu nhiên, đa trung tâm, nhãn mở và đánh giá kết cục mù, do nhà nghiên cứu khởi xướng, tiến hành tại 32 trung tâm ở Nhật Bản. Nghiên cứu được tiến hành để so sánh chiến lược kháng đông với rivaroxaban trong 18 tháng và 6 tháng ở bệnh nhân ung thư có PE nguy cơ thấp. Các kết cục lâm sàng được đánh giá sau 18 tháng ở giai đoạn mở rộng của một nghiên cứu được tiến hành trước đó. Trong nghiên cứu đã được tiến hành trước đó như đề cập, các kết cục được đánh giá sau 12 tháng kể từ khi thực hiện các chiến lược điều trị khác nhau.10 Nghiên cứu được tài trợ bởi Bayer Yakuhin Co, Ltd, công ty này không tham gia vào thiết kế nghiên cứu; thu thập, phân tích, diễn giải dữ liệu; hoặc việc viết báo cáo. Thiết kế nghiên cứu đã được báo cáo chi tiết trước đó.11 Dữ liệu đã được xem xét bởi một ủy ban giám sát dữ liệu và an toàn độc lập. Thử nghiệm được tiến hành theo các nguyên tắc Helsinki và được hội đồng đạo đức của Đại học Kyoto và các trung tâm tham gia nghiên cứu phê duyệt. Dữ liệu liên quan đến nghiên cứu này sẽ được tác giả liên lạc cung cấp khi có các yêu cầu hợp lý.
Dân số nghiên cứu
Vì chưa có định nghĩa rõ ràng về PE nguy cơ thấp, trong thử nghiệm này chúng tôi sử dụng thang điểm PESI giản lược (sPESI) để phân tầng nguy cơ PE,12 và PE với sPESI là 1 (không có thành phần điểm số sPESI nào khác ngoài ung thư) được định nghĩa là PE nguy cơ thấp. Các bệnh nhân trưởng thành có ung thư đang hoạt động, được chẩn đoán xác định PE nguy cơ thấp, mới mắc bằng chụp CT, đủ điều kiện để tham gia nghiên cứu. Ung thư đang hoạt động được định nghĩa là ung thư thỏa mãn một trong các tiêu chí sau: ung thư được chẩn đoán mới trong vòng 6 tháng trước khi phân nhóm ngẫu nhiên; đang điều trị ung thư (phẫu thuật, hóa trị, xạ trị, v.v.) trong vòng 6 tháng trước khi phân nhóm ngẫu nhiên; hiện tại đang điều trị ung thư (phẫu thuật, hóa trị, xạ trị, v.v.); tái phát, xâm lấn tại chỗ hoặc di căn xa; hoặc ung thư huyết học chưa thoái triển hoàn toàn.13 Các tiêu chí loại trừ chính bao gồm bệnh nhân đang sử dụng kháng đông tại thời điểm chẩn đoán, bệnh nhân có chống chỉ định với rivaroxaban, và bệnh nhân có tiên lượng sống ≤6 tháng. Tất cả bệnh nhân phải đồng thuận bằng văn bản khi tham gia nghiên cứu.
Phân nhóm ngẫu nhiên và điều trị
Các bệnh nhân đủ điều kiện được phân nhóm ngẫu nhiên theo tỷ lệ 1:1 vào sử dụng rivaroxaban trong vòng 18 tháng hoặc trong vòng 6 tháng theo mô hình nhãn mở. Việc ngẫu nhiên hóa được thực hiện tập trung thông qua hệ thống thu thập dữ liệu điện tử sử dụng thuật toán tối thiểu ngẫu nhiên để cân bằng các phân bổ điều trị trong các trung tâm nghiên cứu.
Rivaroxaban được sử dụng theo các chính sách tại mỗi cơ sở, và không có hạn chế nào được đặt ra cho các chính sách, miễn là việc điều trị không vi phạm các tiêu chí loại trừ. Điều trị bằng thuốc kháng đông đường tiêm được chỉ định trước khi tham gia nghiên cứu, nhưng sau khi tham gia, bệnh nhân nhận liều rivaroxaban đầu tiên theo nhãn của sản phẩm đã được tiếp thị để điều trị PE tại Nhật Bản; liều này bao gồm 15 mg hai lần mỗi ngày trong 3 tuần đầu, sau đó là 15 mg một lần mỗi ngày. Việc quyết định không sử dụng tổng liều khởi đầu 30 mg/ngày được thực hiện theo quyết định của bác sĩ điều trị đối với những bệnh nhân được coi là có nguy cơ xuất huyết cao.
Định nghĩa về các đặc điểm dân số
Thang điểm sPESI có 6 biến số, bao gồm >80 tuổi, tiền sử ung thư, tiền sử bệnh tim phổi mạn tính, nhịp tim ≥110 nhịp/phút, huyết áp tâm thu <100 mmHg, và độ bão hòa oxy động mạch <90% tại thời điểm chẩn đoán, thang điểm dao động từ 0 đến 6 (0 là mức thấp nhất và 6 là mức nguy cơ tử vong cao nhất trong 30 ngày). Bệnh tim phổi mạn tính bao gồm suy tim và bệnh phổi mạn tính. Suy tim được chẩn đoán nếu bệnh nhân có tiền sử nhập viện do suy tim, nếu bệnh nhân có triệu chứng liên quan đến suy tim (điểm NYHA ≥2), hoặc nếu phân suất tống máu thất trái <40%. Bệnh phổi mạn tính được định nghĩa là dai dẳng nếu có một rối loạn trên phổi như hen suyễn, bệnh phổi tắc nghẽn mạn tính, hoặc bệnh phổi hạn chế.
Theo dõi
Các đợt thăm khám theo dõi bắt buộc được lên kế hoạch vào các thời điểm 3, 6 và 18 tháng, cùng với các đánh giá bổ sung cho việc chăm sóc lâm sàng thường quy nếu cần. Tại đợt thăm khám 6 tháng sau chẩn đoán (từ 151 đến 209 ngày), nhóm điều trị rivaroxaban 6 tháng ngừng điều trị, trong khi nhóm điều trị 18 tháng sẽ tiếp tục. Trong suốt thời gian theo dõi, việc sử dụng kháng đông được ghi nhận, bao gồm việc ngừng và khởi đầu các thuốc kháng đông, cùng với lý do và loại thuốc kháng đông. Việc ngừng sử dụng rivaroxaban kéo dài được định nghĩa là việc ngừng thuốc theo đề cương nghiên cứu hoặc kéo dài hơn 14 ngày vì bất kỳ lý do nào. Để đánh giá sự khác biệt tiềm ẩn về tần suất thực hiện chụp CT có tiêm thuốc cản quang giữa 2 nhóm, chúng tôi đã thu thập tất cả CT có tiêm thuốc cản quang trong suốt thời gian theo dõi. Để đảm bảo tuân thủ việc sử dụng rivaroxaban, đề cương nghiên cứu đã xác định trước phương pháp theo dõi chi tiết tại mỗi trung tâm.
Kết cục chính và kết cục phụ
Kết cục chính là VTE tái phát trong vòng 18 tháng. VTE tái phát bao gồm PE có hoặc không kèm theo DVT, được định nghĩa là sự xuất hiện của hình ảnh huyết khối mới hoặc xấu đi trong các động mạch phổi và tĩnh mạch sâu trên các xét nghiệm hình ảnh học (siêu âm hệ thống tĩnh mạch chi dưới, chụp CT, chụp đồng vị phóng xạ tưới máu phổi, chụp động mạch phổi và chụp tĩnh mạch) bất kể có triệu chứng.14 VTE tái phát bao gồm PE hoặc DVT được chẩn đoán tình cờ khi các xét nghiệm hình ảnh được thực hiện, thường là để theo dõi ung thư.15 Trong đề cương nghiên cứu, các xét nghiệm hình ảnh học theo dõi VTE không được khuyến nghị trừ khi nghi ngờ có VTE tái phát trên lâm sàng.
Kết cục phụ quan trọng là biến cố xuất huyết nặng trong vòng 18 tháng. Xuất huyết nặng được định nghĩa theo ISTH, bao gồm xuất huyết gây tử vong, xuất huyết có triệu chứng tại cơ quan quan trọng, và xuất huyết dẫn đến giảm nồng độ hemoglobin ≥2 g/dL hoặc cần truyền ≥2 đơn vị máu toàn phần hoặc hồng cầu.16 Các kết cục phụ khác bao gồm tử vong do mọi nguyên nhân, các biến cố tái phát VTE có triệu chứng, và tất cả các biến cố xuất huyết có ý nghĩa trên lâm sàng sau 18 tháng. Các biến cố cũng như mức độ trầm trọng được đánh giá bởi một ủy ban độc lập, các thành viên trong ủy ban không biết thông tin về các nhánh nghiên cứu.17
Phân tích thống kê
Giả thuyết chính là nhóm điều trị rivaroxaban 18 tháng vượt trội hơn 6 tháng về kết cục chính sau 18 tháng. Giả định tỷ lệ biến cố là 10% trong nhóm rivaroxaban 18 tháng và 22% trong nhóm 6 tháng được dựa trên các nghiên cứu trước đây.15,18 Để chứng minh sự vượt trội của điều trị rivaroxaban 18 tháng so với 6 tháng với độ đặc hiệu của nghiên cứu là 80% và α hai phía = 0.05, cần có 292 người tham gia, và chúng tôi dự định tuyển 330 người tham gia sau khi cân nhắc tỷ lệ bệnh nhân ngừng nghiên cứu sớm.
Kết cục chính được đánh giá trên nhóm dân số dự định điều trị, bao gồm tất cả các bệnh nhân đã được phân nhóm ngẫu nhiên sau khi loại trừ những bệnh nhân từ chối tham gia nghiên cứu. Đối với những bệnh nhân không gặp biến cố nào trong thời gian nghiên cứu, bệnh nhân sẽ được theo dõi cho đến ngày 545 hoặc ngày cuối cùng bệnh nhân có đánh giá hoàn chỉnh cho các kết quả nghiên cứu, tùy thuộc thời điểm nào đến trước. Các bệnh nhân mất liên lạc trước khi kết thúc thời gian nghiên cứu 18 tháng và những bệnh nhân không gặp các kết cục chính được ngưng theo dõi vào ngày cuối cùng khi bệnh nhân có đánh giá hoàn chỉnh cho các kết cục nghiên cứu. Những phân tích trên nhóm bệnh nhân tuân thủ đề cương và trên nhóm dân số có nhận thuốc điều trị cũng được thực hiện như là những phân tích độ nhạy. Các phân tích dưới nhóm định trước với các kiểm định xác định ảnh hưởng của các yếu tố lâm sàng trên các phân nhóm bệnh nhân này. Do một số kết cục nghiên cứu xuất hiện trong 6 tháng đầu chúng tôi đã thực hiện một phân tích tại thời điểm 180 ngày cho các kết cục chính và kết cục phụ quan trọng trong phân tích hậu nghiệm. Trong phân tích hậu nghiệm những bệnh nhân tử vong trong vòng 180 ngày và những người ghi nhận kết cục lâm sàng trong vòng 180 ngày sẽ bị loại trừ. Hơn nữa, để xác nhận độ tin cậy của nghiên cứu trên những bệnh nhân PE không triệu chứng hoặc rối loạn chức năng thất phải, chúng tôi đã thực hiện một phân tích hậu nghiệm khác sau khi loại trừ những bệnh nhân PE có triệu chứng hoặc rối loạn chức năng thất phải.
Chúng tôi so sánh tỷ lệ kết cục chính và kết cục phụ giữa 2 nhóm điều trị trong nhóm dân số dự định điều trị và tỷ lệ odds (ORs) cùng với khoảng tin cậy 95% tương ứng được tính bằng cách sử dụng các mô hình hồi quy logistic. Chúng tôi cũng ước lượng tỷ lệ ngừng điều trị rivaroxaban kéo dài ghi nhận lần đầu và tỷ lệ tích lũy kết cục chính và kết cục phụ quan trọng bằng phương pháp Kaplan-Meier, và sự khác biệt của các kết cục chính và kết cục phụ quan trọng được đánh giá bằng kiểm định log-rank. Mô hình tương tự hồi quy logistic được áp dụng để ước lượng giá trị P cho bất kỳ tương tác nào trong các phân tích dưới nhóm. Một bác sĩ (Y.Y.) và một nhà thống kê (T.M.) đã thực hiện tất cả các phân tích thống kê bằng phần mềm JMP phiên bản 14.0.0 (SAS Institute Inc, Cary, NC) và SAS phiên bản 9.4 (SAS Institute Inc). Các giá trị P được báo cáo là kiểm định hai phía, và giá trị P<0.05 được coi là có ý nghĩa thống kê. Vì không có kế hoạch điều chỉnh độ rộng của các khoảng tin cậy (CIs) và giá trị P tương tác của các phân tích dưới nhóm cho các so sánh nhiều lần, dữ liệu này nên được diễn giải như là kết quả tham khảo. Ngoài ra, vì sự thay đổi hiệu quả của các can thiệp và các biện pháp quản lý khác là ít khả năng xảy ra, nên không có kế hoạch hiệu chỉnh theo biến phân tầng.
KẾT QUẢ
Thu thập mẫu và đặc điểm dân số nghiên cứu
Từ tháng 2/2021 đến tháng 3/2023, tổng cộng 179 bệnh nhân đã được thu thập và phân nhóm ngẫu nhiên (Hình 1). Ủy ban điều hành đã kết thúc thử nghiệm sớm khi 54% kích thước mẫu ước tính đã thu thập được do việc tuyển dụng chậm trong đại dịch COVID-19. Sau khi loại trừ 1 bệnh nhân từ chối tham gia, 178 bệnh nhân đã được đưa vào nhóm dân số dự định điều trị: 89 bệnh nhân trong nhóm rivaroxaban 18 tháng và 89 bệnh nhân trong nhóm 6 tháng.
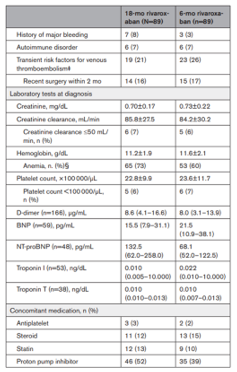
Đặc điểm lâm sàng của bệnh nhân tại thời điểm bắt đầu được cân bằng giữa 2 nhóm (Bảng 1). Độ tuổi trung bình là 65.7 tuổi; 47% bệnh nhân là nam giới; và 12% bệnh nhân có triệu chứng PE tại thời điểm bắt đầu. Về vị trí huyết khối, thuyên tắc động mạch trung tâm, chính, thùy, phân thùy và tiểu phân thùy lần lượt chiếm 13%, 12%, 30%, 30% và 20% của các bệnh nhân. Loại ung thư phổ biến nhất là ung thư đại tràng (12%), tiếp theo là ung thư tử cung (12%) và ung thư buồng trứng (11%; Bảng 1).
Điều trị rivaroxaban và kết quả chụp CT trong thời gian theo dõi
 Trung vị thời gian điều trị rivaroxaban (khoảng tứ phân) là 482 ngày (169–545 ngày) trong nhóm 18 tháng và 182 ngày (157–194 ngày) trong nhóm 6 tháng. Tỷ lệ ngừng thuốc nghiên cứu kéo dài lần đầu sau 210 ngày lần lượt là 23.6% trong nhóm 18 tháng và 87.9% trong nhóm 6 tháng (Hình 2). Trong số 89 bệnh nhân nhóm rivaroxaban 6 tháng, 12 bệnh nhân (13%) đã ngừng thuốc nghiên cứu sớm trong vòng 150 ngày, và 10 bệnh nhân (11%) tiếp tục sau 210 ngày. Các lý do phổ biến cho việc ngừng rivaroxaban trong nhóm rivaroxaban 18 tháng là các biến cố xuất huyết (29%) và ung thư tiến triển (26%), trong khi đó ở nhóm 6 tháng, lý do chủ yếu là do ngừng theo đề cương (79%; Bảng 2).
Trung vị thời gian điều trị rivaroxaban (khoảng tứ phân) là 482 ngày (169–545 ngày) trong nhóm 18 tháng và 182 ngày (157–194 ngày) trong nhóm 6 tháng. Tỷ lệ ngừng thuốc nghiên cứu kéo dài lần đầu sau 210 ngày lần lượt là 23.6% trong nhóm 18 tháng và 87.9% trong nhóm 6 tháng (Hình 2). Trong số 89 bệnh nhân nhóm rivaroxaban 6 tháng, 12 bệnh nhân (13%) đã ngừng thuốc nghiên cứu sớm trong vòng 150 ngày, và 10 bệnh nhân (11%) tiếp tục sau 210 ngày. Các lý do phổ biến cho việc ngừng rivaroxaban trong nhóm rivaroxaban 18 tháng là các biến cố xuất huyết (29%) và ung thư tiến triển (26%), trong khi đó ở nhóm 6 tháng, lý do chủ yếu là do ngừng theo đề cương (79%; Bảng 2).
Kết quả chụp CT ngực cản quang được thực hiện 309 lần trong nhóm 18 tháng và 305 lần trong nhóm 6 tháng trong vòng 18 tháng cho tất cả các mục đích (Bảng 3). Trung vị số lần chụp CT (khoảng tứ phân) là 3 (2–5) mỗi bệnh nhân trong nhóm rivaroxaban 18 tháng và 3 (1–5) mỗi bệnh nhân trong nhóm 6 tháng. Tỷ lệ chụp CT là 2.90 lần mỗi bệnh nhân-năm trong nhóm rivaroxaban 18 tháng và 2.70 lần mỗi bệnh nhân – năm trong nhóm 6 tháng.
Hình 1: Thu thập mẫu, phân nhóm ngẫu nhiên và theo dõi (Chụp từ tài liệu gốc)
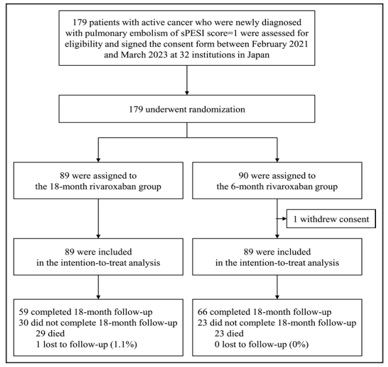 Bệnh nhân đã được phân nhóm ngẫu nhiên theo tỷ lệ 1:1 vào nhóm sử dụng rivaroxaban 18 tháng hoặc 6 tháng. Phân nhóm ngẫu nhiên được thực hiện tập trung thông qua hệ thống thu thập dữ liệu điện tử sử dụng thuật toán ngẫu nhiên tối thiểu để cân bằng việc phân bổ điều trị trong các trung tâm. sPESI là thang điểm PESI giản lược
Bệnh nhân đã được phân nhóm ngẫu nhiên theo tỷ lệ 1:1 vào nhóm sử dụng rivaroxaban 18 tháng hoặc 6 tháng. Phân nhóm ngẫu nhiên được thực hiện tập trung thông qua hệ thống thu thập dữ liệu điện tử sử dụng thuật toán ngẫu nhiên tối thiểu để cân bằng việc phân bổ điều trị trong các trung tâm. sPESI là thang điểm PESI giản lược
Bảng 1. Các đặc điểm lâm sàng của bệnh nhân tại thời điểm bắt đầu (Chụp từ tài liệu gốc)
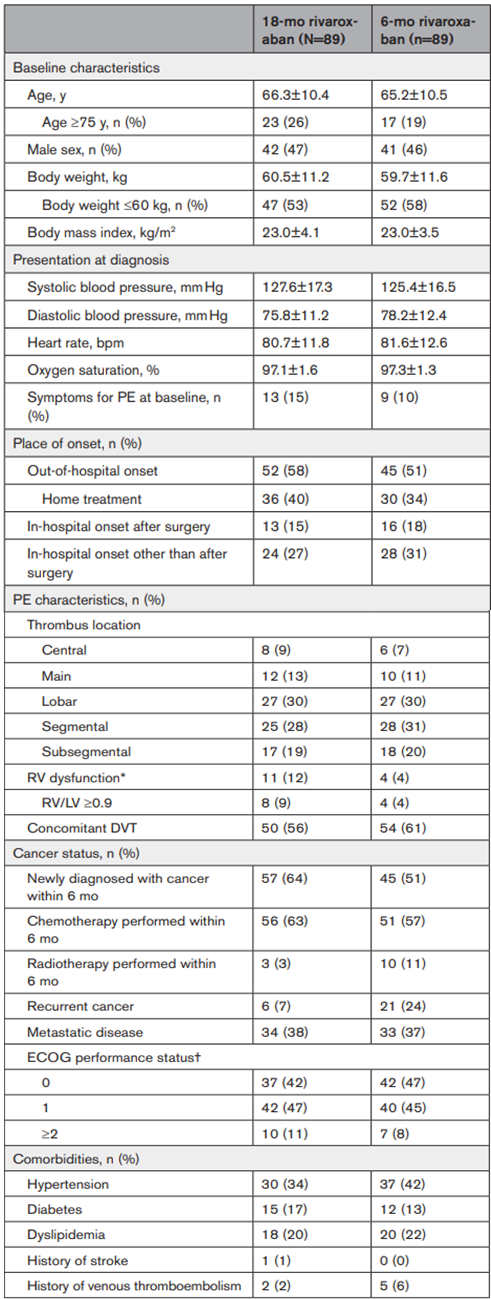 Các đặc điểm lâm sàng của bệnh nhân tại thời điểm bắt đầu nghiên cứu được trình bày trong dân số dự định điều trị. Các biến phân loại được trình bày dưới dạng số lượng và phần trăm, và các biến liên tục được trình bày dưới dạng trung bình±SD hoặc trung vị (khoảng tứ phân vị) dựa trên phân phối của chúng.
Các đặc điểm lâm sàng của bệnh nhân tại thời điểm bắt đầu nghiên cứu được trình bày trong dân số dự định điều trị. Các biến phân loại được trình bày dưới dạng số lượng và phần trăm, và các biến liên tục được trình bày dưới dạng trung bình±SD hoặc trung vị (khoảng tứ phân vị) dựa trên phân phối của chúng.
*Rối loạn chức năng RV được định nghĩa là có dấu hiệu giãn RV (RV/LV ≥0,9) trên chụp cắt lớp vi tính hoặc áp lực động mạch phổi tâm thu ước tính ≥40 mmHg qua siêu âm tim. Siêu âm tim được đánh giá ở 111 bệnh nhân.
†Giá trị trạng thái hoạt động ECOG dao động từ 0 đến 4, với các giá trị cao hơn cho thấy mức độ khuyết tật lớn hơn.
‡Các yếu tố nguy cơ tạm thời cho thuyên tắc huyết khối tĩnh mạch bao gồm phẫu thuật gần đây, bất động gần đây, du lịch đường dài, sử dụng catheter tĩnh mạch trung tâm, mang thai hoặc thời kỳ hậu sản, chấn thương chân gần đây, gãy xương hoặc bỏng, nhiễm trùng nặng, và sử dụng estrogen.
- Thiếu máu được chẩn đoán nếu giá trị hemoglobin <13 g/dL đối với nam và <12 g/dL đối với nữ.
Hình 2. Đường cong Kaplan-Meier cho việc ngừng rivaroxaban lần đầu kéo dài (Chụp từ tài liệu gốc)
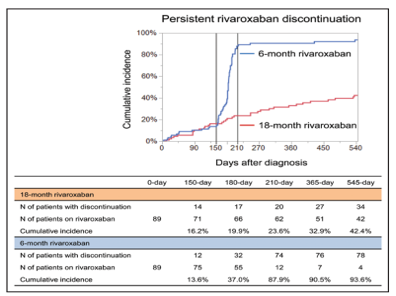 Các đường cong biến cố – thời gian của việc ngừng rivaroxaban lần đầu kéo dài trong vòng 18 tháng sau chẩn đoán. Ngừng rivaroxaban kéo dài được định nghĩa là việc ngừng sử dụng rivaroxaban theo đề cương nghiên cứu hoặc kéo dài hơn 14 ngày vì bất kỳ lý do nào. Các phân tích được thực hiện cho toàn bộ dân số có dự định điều trị
Các đường cong biến cố – thời gian của việc ngừng rivaroxaban lần đầu kéo dài trong vòng 18 tháng sau chẩn đoán. Ngừng rivaroxaban kéo dài được định nghĩa là việc ngừng sử dụng rivaroxaban theo đề cương nghiên cứu hoặc kéo dài hơn 14 ngày vì bất kỳ lý do nào. Các phân tích được thực hiện cho toàn bộ dân số có dự định điều trị
Kết cục chính
VTE tái phát ghi nhận ở 5 trong số 89 bệnh nhân (5.6%) trong nhóm rivaroxaban 18 tháng và 17 trong số 89 bệnh nhân (19.1%) trong nhóm 6 tháng (OR = 0.25 [95% CI, 0.09–0.72]; P=0.01; Bảng 2). Thời gian cho đến khi xảy ra kết cục chính được hiển thị trong Hình 3. VTE tái phát bao gồm 11 trường hợp PE, trong đó có 2 trường hợp tắc động mạch chính và 4 trường hợp tắc động mạch thùy, và 11 trường hợp DVT, bao gồm 3 trường hợp DVT đoạn gần. Trong số 22 biến cố VTE tái phát, 5 bệnh nhân có có triệu chứng, bao gồm 3 trường hợp PE và 2 trường hợp DVT. Trong số 17 biến cố VTE tái nhát nhưng không có triệu chứng, 13 biến cố (76%) bao gồm sự phát triển của huyết khối mới (Bảng 4). Kết quả của các phân tích theo đề cương và theo điều trị nhất quán với kết quả trong phân tích chính (Bảng 5 và 6; Hình 1 đến 4).
Kết cục phụ
Kết cục phụ quan trọng là xuất huyết nặng xảy ra ở 7 trong số 89 bệnh nhân (7.8%) nhóm rivaroxaban 18 tháng và 5 trong số 89 bệnh nhân (5.6%) nhóm rivaroxaban 6 tháng (OR = 1.43 [95% CI, 0.44–4.70]; P=0.55; Bảng 2). Thời gian đến khi xảy ra kết cục phụ quan trọng được hiển thị trong Hình 4. Vị trí phổ biến nhất của xuất huyết nặng là đường tiêu hóa dưới (33%), và mức độ nghiêm trọng của xuất huyết nặng chủ yếu thuộc loại 2 (92%;). Kết quả phân tích trên nhóm bệnh nhân tuân thủ đề cương và theo điều trị được trình bày trong Bảng 2..
Thông tin về các kết cục phụ khác trong 2 nhóm được cung cấp trong Bảng 2. Tử vong do mọi nguyên nhân xảy ra ở 29 trong số 89 bệnh nhân (32.6%) nhóm rivaroxaban 18 tháng và 23 trong số 89 bệnh nhân (25.8%) nhóm 6 tháng (OR = 1.39 [95% CI, 0.72–2.66]). VTE tái phát có triệu chứng xảy ra ở 1 trong số 89 bệnh nhân (1.1%) nhóm rivaroxaban 18 tháng và 4 trong số 89 bệnh nhân (4.5%) nhóm 6 tháng (OR = 0.24 [95% CI, 0.03–2.20]). Tất cả các biến cố xuất huyết có ý nghĩa trên lâm sàng xảy ra ở 20 trong số 89 bệnh nhân (22.5%) nhóm rivaroxaban 18 tháng và 18 trong số 89 bệnh nhân (20.2%) trong nhóm 6 tháng (OR = 1.14 [95% CI, 0.56–2.34]).
Phân tích dưới nhóm và phân tích độ nhạy
Các ước lượng điểm cho kết cục chính đều ủng hộ nhóm rivaroxaban 18 tháng trong toàn bộ phân tích dưới nhóm (Hình 5). Phân tích tại thời điểm 180 ngày cho các kết cục chính và kết cục phụ quan trọng cho thấy kết quả hoàn toàn nhất quán với kết quả chung (Hình 5). Phân tích độ nhạy trên kết cục chính và kết cục phụ quan trọng sau khi loại trừ những bệnh nhân PE có triệu chứng hoặc rối loạn chức năng tâm thất phải cho thấy kết quả nhất quán với các kết quả chung.
THẢO LUẬN
Thử nghiệm ONCO PE, trong đó tuyển chọn các bệnh nhân mắc ung thư đang hoạt động được chẩn đoán có PE nguy cơ thấp mới mắc trong đó không có các thành phần điểm số sPESI khác ngoài ung thư, đã cho thấy sử dụng rivaroxaban trong 18 tháng vượt trội hơn so với 6 tháng trong giảm tái phát VTE, đồng thời không làm tăng nguy cơ xuất huyết nặng.
Tỷ lệ mắc mới PE nguy cơ thấp, bao gồm PE được phát hiện tình cờ, ở bệnh nhân ung thư đã được báo cáo là gia tăng theo thời gian, một phần là do việc sử dụng thường xuyên CT để chẩn đoán và theo dõi ung thư cũng như những cải tiến trong công nghệ chụp CT.19-21 Một nghiên cứu gần đây đã báo cáo rằng khoảng một nửa số trường hợp PE ở bệnh nhân mắc ung thư được chẩn đoán tình cờ thông qua việc chụp CT thường quy để phân giai đoạn ung thư hoặc đánh giá phản ứng điều trị ung thư.21 Tầm quan trọng trên lâm sàng của PE nguy cơ thấp, bao gồm PE được phát hiện tình cờ và PE nhẹ, vẫn có thể còn gây tranh cãi. Lịch sử cho thấy, PE nguy cơ thấp được coi là một tình trạng ít nghiêm trọng hơn so với PE có triệu chứng hoặc PE vừa hoặc nặng. Tuy nhiên, một số nghiên cứu quan sát trước đây cho thấy nguy cơ tái phát VTE ở PE được phát hiện tình cờ tương tự như PE có triệu chứng.22,23 Điều này cho thấy nguy cơ gặp biến cố huyết khối có thể cao hơn ở những bệnh nhân có PE được phát hiện tình cờ so với những người không có. Dựa trên những phát hiện đó, các khuyến cáo trên thế giới hiện nay khuyến nghị áp dụng chiến lược kháng đông cho PE được phát tình cờ và PE nhẹ như cho tương tự PE có triệu chứng.5,6,8 Tuy nhiên, do thiếu bằng chứng vững chắc từ các thử nghiệm lâm sàng ngẫu nhiên, các chiến lược kháng đông tối ưu cho bệnh nhân ung thư có PE nguy cơ thấp vẫn còn gây tranh cãi, dẫn đến việc áp chiến lược kháng đông không nhất quán. Chưa có thử nghiệm lâm sàng ngẫu nhiên nào đánh giá thời gian tối ưu của kháng đông cho những bệnh nhân này, và vẫn chưa chắc chắn liệu kháng đông có nên được kéo dài hơn 6 tháng hay không.
Bảng 2. Các kết quả lâm sàng sau 18 tháng (Chụp từ tài liệu gốc)
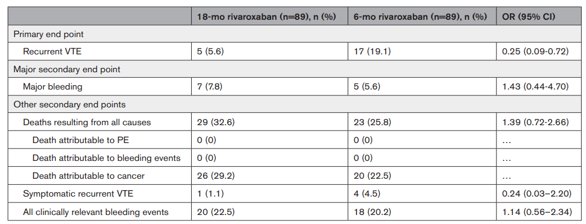
OR chỉ tỷ lệ odds; PE, thuyên tắc phổi; và VTE, thuyên tắc huyết khối tĩnh mạch.
Các phân tích được thực hiện cho toàn bộ dân số có dự định điều trị, bao gồm tất cả các bệnh nhân đã được phân nhóm ngẫu nhiên sau khi loại trừ những bệnh nhân từ chối tham gia. Đối với các bệnh nhân không gặp biến cố nào trong thời gian nghiên cứu, bệnh nhân sẽ được theo dõi cho đến ngày 545 hoặc ngày cuối cùng bệnh nhân có đánh giả hoàn chỉnh cho các kết quả nghiên cứu, tùy thuộc thời điểm nào đến trước.
Chúng tôi đã tính toán tỷ lệ odds, được tính toán bằng mô hình hồi quy logistic, cùng với khoảng tin cậy 95% tương ứng cho tất cả các kết cục lâm sàng, mà không được điều chỉnh cho các so sánh nhiều lần.
Thử nghiệm lâm sàng ngẫu nhiên này, những bệnh nhân PE với điểm sPESI là 1 được đưa vào nghiên cứu. Đây là nhóm bệnh nhân được coi là nguy cơ thấp và 88% trong nhóm này là PE không triệu chứng. Về mặt các biến cố huyết khối, điều trị kháng đông kéo dài với rivaroxaban đã cho thấy lợi ích trong việc dự phòng các biến cố huyết khối so với việc điều trị kháng đông giới hạn trong 6 tháng, điều này gợi ý cho những lợi ích tiềm tàng khi mở rộng thời gian điều trị kháng đông trên 6 tháng ở nhũng bệnh nhân này. Một phân tích gộp trước đây từ các nghiên cứu quan sát cho thấy tỷ lệ tái phát VTE sau 6 tháng là 5.8% ở bệnh nhân ung thư có PE được phát hiện tình cờ, và tỷ lệ này tăng lên 12% ở những bệnh nhân không được điều trị kháng đông.24 Nhất quán với báo cáo trước đó, thử nghiệm lâm sàng ngẫu nhiên hiện tại cho thấy tỷ lệ tái phát VTE sau 18 tháng là 19.1% ở những bệnh nhân có thời gian điều trị kháng đông trong 6 tháng, và tỷ lệ biến cố tăng lên sau 6 tháng, có thể là sau khi ngừng kháng đông. Điều đáng chú ý là trong nghiên cứu này cũng quan sát được một số trường hợp tái phát VTE là PE, bao gồm tắc động mạch chính và động mạch thùy cũng như DVT đoạn gần, những trường hợp này được coi là VTE có ý nghĩa lâm sàng. Mặt khác, chỉ một số ít các trường hợp tái phát VTE là có triệu chứng. Ngoài nguy cơ xảy ra các biến cố huyết khối, các bác sĩ lâm sàng cũng nên xem xét tầm quan trọng lâm sàng của các biến cố huyết khối.
Hình 3. Đường cong Kaplan-Meier cho kết cục chính (Chụp từ tài liệu gốc)
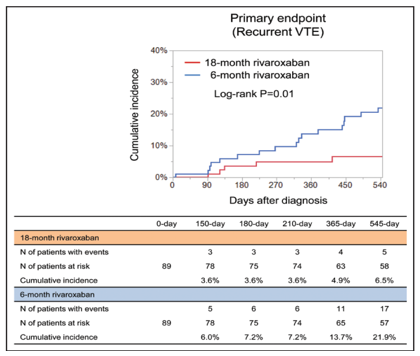 Các đường cong biến cố – thời gian của kết cục chính (tái phát VTE) trong vòng 18 tháng sau chẩn đoán. Số lượng bệnh nhân có biến cố cho thấy số lượng biến cố tích lũy.
Các đường cong biến cố – thời gian của kết cục chính (tái phát VTE) trong vòng 18 tháng sau chẩn đoán. Số lượng bệnh nhân có biến cố cho thấy số lượng biến cố tích lũy.
Đối với việc ra quyết định về các chiến lược kháng đông, nguy cơ xuất huyết liên quan đến kháng đông nên được xem xét.25 Đặc biệt, các bệnh nhân có thuyên tắc huyết khối tĩnh mạch liên quan đến ung thư có nguy cơ xuất huyết cao so với những người không mắc ung thư đang hoạt động ngay cả với các thuốc kháng đông đường uống trực tiệp, dẫn đến khó khăn trong việc đạt được sự cân bằng tốt lợi ích và nguy cơ trong điều trị kháng đông.26,27 Nghiên cứu SELECT-D cho thấy tỷ lệ tích lũy xuất huyết nặng sau 6 tháng là 6% ở nhóm bệnh nhân ung thư sử dụng rivaroxaban để điều trị VTE.15 Trong nghiên cứu này tỷ lệ tích lũy xuất huyết nặng sau 18 tháng là 7.8% trong nhóm sử dụng rivaroxaban 18 tháng, và không có sự khác biệt có ý nghĩa thống kê so với nhóm 6 tháng (5.6%). Các đường cong biến cố – thời gian cho xuất huyết nặng cho thấy biến cố có vẻ xuất hiện nhiều hơn trong 6 tháng đầu ở cả hai nhóm, và nguy cơ xuất huyết nặng không khác biệt đáng kể sau 6 tháng, điều này gợi ý rằng nguy cơ xuất huyết nặng liên quan đến rivaroxaban có thể nổi bật hơn trong giai đoạn đầu sau khi bắt đầu sử dụng thuốc, và việc tiếp tục sử dụng rivaroxaban sau giai đoạn đó có thể không làm tăng nguy cơ xuất huyết nặng. Tuy nhiên, nguy cơ xuất huyết có thể cao hơn khi điều trị kháng đông kéo dài, đặc biệt là ở những bệnh nhân có nguy cơ xuất huyết cao, các bác sĩ lâm sàng vẫn nên thận trọng về nguy cơ xuất huyết và dựa vào sự cân bằng giữa lợi ích – nguy cơ khi quyết định các chiến lược kháng đông cho những bệnh nhân này.
Một số hạn chế cần được lưu ý. Đầu tiên, thiết kế nhãn mở có thể tạo ra thiên lệch trong việc điều trị và đánh giá. Tất cả các kết cục lâm sàng đều được đánh giá bởi ủy ban độc lập, không biết về phân nhóm nghiên cứu; tuy nhiên, các chiến lược xét nghiệm chẩn đoán có thể đã bị ảnh hưởng bởi thiết kế nhãn mở, điều này có thể dẫn đến một số thiên lệch trong việc xác định kết cục chính. Tuy nhiên, đề cương nghiên cứu không khuyến nghị các xét nghiệm hình ảnh học theo dõi khác ngoài những xét nghiệm cho ung thư, và số lượng tuyệt đối cũng như tỷ lệ chụp CT cản quang tương đương giữa hai nhóm, cho thấy rằng không có ảnh hưởng rõ ràng nào của hai chiến lược kháng đông khác nhau đối với các chiến lược xét nghiệm chẩn đoán trong suốt thời gian theo dõi. Hơn nữa, để giảm thiểu ảnh hưởng của xét nghiệm chẩn đoán lên kết cục chính, chúng tôi cũng đã đánh giá VTE tái phát có triệu chứng và xác nhận xu hướng tương tự với kết cục chính. Thứ hai, thử nghiệm đã bị kết thúc sớm trước khi tuyển đủ cỡ mẫu ước tính. Ngoài ra, số lượng bệnh nhân đạt được kết cục chính thấp hơn mong đợi ở cả hai nhóm sử dụng rivaroxaban 18 tháng và 6 tháng. Mặc dù có hạn chế đó, sự vượt trội vẫn được thiết lập. Lý do có thể một phần là do các tỷ lệ biến cố ước tính được tính toán trong các dân số nghiên cứu khác nhau so với dân số nghiên cứu hiện tại15,18 và rằng tỷ lệ biến cố trong nhóm rivaroxaban 18 tháng thấp hơn nhiều so với dự kiến.
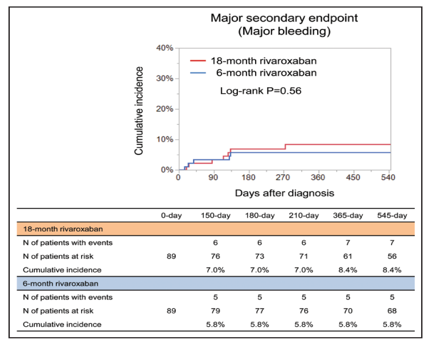
Hình 4. Đường cong Kaplan-Meier cho kết cục phụ quan trọng (Chụp từ tài liệu gốc)
Các đường cong biến cố – thời gian của kết cục phụ quan trọng (xuất huyết nặng) trong vòng 18 tháng sau chẩn đoán. Số lượng bệnh nhân có biến cố cho thấy số lượng biến cố tích lũy. Xuất huyết nặng được định nghĩa theo tiêu chí của ISTH, bao gồm xuất huyết gây tử vong, xuất huyết có triệu chứng tại cơ quan quan trọng, và xuất huyết dẫn đến giảm nồng độ hemoglobin ≥2 g/dL hoặc cần truyền ≥2 đơn vị máu toàn phần hoặc hồng cầu.
Do đó, khả năng ngẫu nhiên nên được xem xét. Thứ ba, sự tuân thủ điều trị rivaroxaban tương đối thấp so với cương nghiên cứu. Đặc biệt, một số bệnh nhân trong nhóm rivaroxaban 18 tháng đã ngừng sử dụng thuốc sớm do các biến cố xuất huyết hoặc tiến triển của ung thư. Vấn đề này có thể đã làm giảm thiểu nguy cơ xuất huyết nặng trong nhóm rivaroxaban 18 tháng trong phân tích dân số dự định điều trị. Mặc dù phân tích độ nhạy của dân số tuân thủ đề cương và dân số dự định điều trị đã xác nhận các kết quả của phân tích chính bao gồm xuất huyết nặng, các bác sĩ vẫn nên thận trọng về sự cân bằng giữa nguy cơ huyết khối và nguy cơ xuất huyết khi diễn giải kết quả nghiên cứu này. Thứ tư, chúng tôi đã đánh giá các tham số của các chẩn đoán hình ảnh tại mỗi cơ sở sử dụng các tiêu chí đã được xác định trước trong đề cương nghiên cứu, chứ không phải tại một phòng thí nghiệm trung tâm. Do đó, chúng tôi không thể đánh giá các tham số chi tiết như tỷ lệ thất phải/thất trái. Ngoài ra, chúng tôi cũng không đánh giá tất cả bệnh nhân bằng siêu âm tim. Cuối cùng, có thể có sự khác biệt về chủng tộc và sự khác biệt trong thực hành, tùy thuộc vào khu vực. Các kết quả hiện tại nên được ứng dụng một cách thận trọng.
KẾT LUẬN
Ở bệnh nhân mắc ung thư có PE nguy cơ thấp với điểm số sPESI = 1, sử dụng rivaroxaban 18 tháng vượt trội hơn so với 6 tháng về mặt các biến cố tái phát VTE.
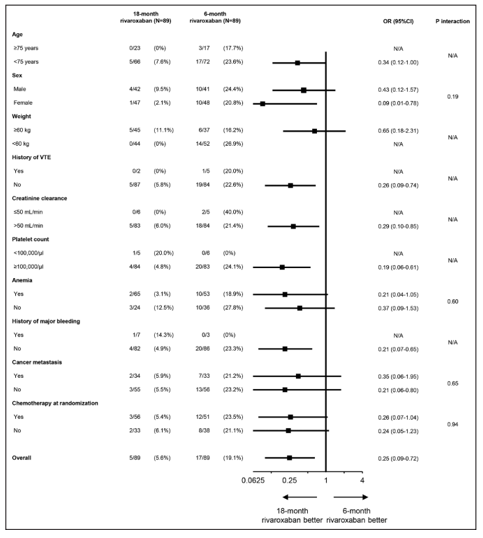
Hình 5. Các phân tích dưới nhóm cho kết cục chính
TÀI LIỆU THAM KHẢO
- Lyon AR, Lopez-Fernandez T, Couch LS, Asteggiano R, Aznar MC, Bergler-Klein J, Boriani G, Cardinale D, Cordoba R, Cosyns B, et al; ESC Scientific Document Group. 2022 ESC guidelines on cardio-oncology developed in collaboration with the European Hematology Association (EHA), the European Society for Therapeutic Radiology and Oncology (ES-TRO) and the International Cardio-Oncology Society (IC-OS). Eur Heart J. 2022;43:4229–4361. doi: 10.1093/eurheartj/ehac244
- Blom JW, Doggen CJ, Osanto S, Rosendaal FR. Malignancies, prothrombotic mutations, and the risk of venous thrombosis. JAMA. 2005;293:715–722. doi: 10.1001/jama.293.6.715
- Di Nisio M, Lee AY, Carrier M, Liebman HA, Khorana AA; Subcommittee on Haemostasis and Malignancy. Diagnosis and treatment of incidental venous thromboembolism in cancer patients: guidance from the SSC of the ISTH. J Thromb Haemost. 2015;13:880–883. doi: 10.1111/jth.12883
- Kyrle PA, Rosendaal FR, Eichinger S. Risk assessment for recurrent venous thrombosis. Lancet. 2010;376:2032–2039. doi: 10.1016/S0140-6736(10)60962-2
- Konstantinides SV, Meyer G, Becattini C, Bueno H, Geersing GJ, Harjola VP, Huisman MV, Humbert M, Jennings CS, Jiménez D, et al; ESC Scientific Document Group. 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Heart J. 2020;41:543–603. doi: 10.1093/eurheartj/ehz405
- Stevens SM, Woller SC, Kreuziger LB, Bounameaux H, Doerschug K, Geersing GJ, Huisman MV, Kearon C, King CS, Knighton AJ, et al. Antithrombotic therapy for VTE disease: second update of the CHEST Guideline and Expert Panel Report. Chest. 2021;160:e545–e608. doi: 10.1016/j.chest.2021.07.055
- Witt DM, Nieuwlaat R, Clark NP, Ansell J, Holbrook A, Skov J, Shehab N, Mock J, Myers T, Dentali F, et al. American Society of Hematology 2018 guidelines for management of venous thromboembolism: optimal management of anticoagulation therapy. Blood Adv. 2018;2:3257–3291. doi: 10.1182/bloodadvances.2018024893
- Key NS, Khorana AA, Kuderer NM, Bohlke K, Lee AYY, Arcelus JI, Wong SL, Balaban EP, Flowers CR, Gates LE, et al. Venous thromboembolism prophylaxis and treatment in patients with cancer: ASCO guideline update. J Clin Oncol. 2023;41:3063–3071. doi: 10.1200/JCO.23.00294
- den Exter PL, Hooijer J, Dekkers OM, Huisman MV. Risk of recurrent venous thromboembolism and mortality in patients with cancer incidentally diagnosed with pulmonary embolism: a comparison with symptomatic patients. J Clin Oncol. 2011;29:2405–2409. doi: 10.1200/JCO.2010.34.0984
- Weitz JI, Lensing AWA, Prins MH, Bauersachs R, Beyer-Westendorf J, Bounameaux H, Brighton TA, Cohen AT, Davidson BL, Decousus H, et al; EINSTEIN CHOICE Investigators. Rivaroxaban or aspirin for extended treatment of venous thromboembolism. N Engl J Med. 2017;376:1211–1222. doi: 10.1056/NEJMoa1700518
- Chatani R, Yamashita Y, Morimoto T, Muraoka N, Shioyama W, Shibata T, Nishimoto Y, Ogihara Y, Doi K, Oi M, et al; ONCO PE Trial Investigators. Home treatment for active cancer patients with low-risk pulmonary embolism: a predetermined companion report From the ONCO PE trial [published online March 8, 2024]. Circ J. doi: 10.1253/circj.CJ-24-0004. https://jstage.jst.go.jp/article/circj/advpub/0/advpub_CJ-24-0004/_article
- Jimenez D, Aujesky D, Moores L, Gomez V, Lobo JL, Uresandi F, Otero R, Monreal M, Muriel A, Yusen RD; RIETE Investigators. Simplification of the pulmonary embolism severity index for prognostication in patients with acute symptomatic pulmonary embolism. Arch Intern Med. 2010;170:1383–1389. doi: 10.1001/archinternmed.2010.199
- Raskob GE, van Es N, Verhamme P, Carrier M, Di Nisio M, Garcia D, Grosso MA, Kakkar AK, Kovacs MJ, Mercuri MF, et al. Edoxaban for the treatment of cancer-associated venous thromboembolism. N Engl J Med. 2018;378:615–624. doi: 10.1056/NEJMoa1711948
- Yamashita Y, Morimoto T, Muraoka N, Oyakawa T, Umetsu M, Akamatsu D, Nishimoto Y, Sato Y, Takada T, Jujo K, et al; ONCO DVT Study Investigators. Edoxaban for 12 months versus 3 months in patients with cancer with isolated distal deep vein thrombosis (ONCO DVT study): an open-label, multicenter, randomized clinical trial. Circulation. 2023;148:1665–1676. doi: 10.1161/CIRCULATIONAHA.123.066360
- Young AM, Marshall A, Thirlwall J, Chapman O, Lokare A, Hill C, Hale D, Dunn JA, Lyman GH, Hutchinson C, et al. Comparison of an oral factor Xa inhibitor with low molecular weight heparin in patients with cancer with venous thromboembolism: results of a randomized trial (SELECT-D). J Clin Oncol. 2018;36:2017–2023. Doi: 10.1200/JCO.2018.78.8034
- Schulman S, Kearon C; Subcommittee on Control of Anticoagulation of the Scientific and Standardization Committee of the International Society on Thrombosis and Haemostasis Standardization Committee of the International Society on Thrombosis and Haemostasis. Definition of major bleeding in clinical investigations of antihemostatic medicinal products in non-surgical patients. J Thromb Haemost. 2005;3:692–694. doi: 10.1111/j.1538-7836.2005.01204.x
- Bleker SM, Brekelmans MPA, Eerenberg ES, Cohen AT, Middeldorp S, Raskob G, Buller HR. Clinical impact of major bleeding in patients with venous thromboembolism treated with factor Xa inhibitors or vitamin K antagonists. an individual patient data meta-analysis. Thromb Haemost. 2017;117:1944–1951. doi: 10.1160/TH16-12-0946
- Yamashita Y, Morimoto T, Amano H, Takase T, Hiramori S, Kim K, Konishi T, Akao M, Kobayashi Y, Inoue T, et al; COMMAND VTE Registry Investigators. Anticoagulation therapy for venous thromboembolism in the real world: from the COMMAND VTE Registry. Circ J. 2018;82:1262–1270. doi: 10.1253/circj.CJ-17-1128
- Carrier M, Righini M, Wells PS, Perrier A, Anderson DR, Rodger MA, Pleasance S, Le Gal G. Subsegmental pulmonary embolism diagnosed by computed tomography: incidence and clinical implications: a systematic review and meta-analysis of the management outcome studies. J Thromb Haemost. 2010;8:1716–1722. doi: 10.1111/j.1538-7836.2010.03938.x
- Wiener RS, Schwartz LM, Woloshin S. Time trends in pulmonary embolism in the United States: evidence of overdiagnosis. Arch Intern Med. 2011;171:831–837. doi: 10.1001/archinternmed.2011.178
- Font C, Farrus B, Vidal L, Caralt TM, Visa L, Mellado B, Tassies D, Monteagudo J, Reverter JC, Gascon P. Incidental versus symptomatic venous thrombosis in cancer: a prospective observational study of 340 consecutive patients. Ann Oncol. 2011;22:2101–2106. doi: 10.1093/annonc/mdq720
- Kraaijpoel N, Bleker SM, Meyer G, Mahe I, Munoz A, Bertoletti L, Bartels-Rutten A, Beyer-Westendorf J, Porreca E, Boulon C, et al; UPE Investigators. Treatment and long-term clinical outcomes of incidental pulmonary embolism in patients with cancer: an international prospective cohort study. J Clin Oncol. 2019;37:1713–1720. doi: 10.1200/JCO.18.01977
- Farge D, Bounameaux H, Brenner B, Cajfinger F, Debourdeau P, Khorana AA, Pabinger I, Solymoss S, Douketis J, Kakkar A. International clinical practice guidelines including guidance for direct oral
anticoagulants in the treatment and prophylaxis of venous thromboembolism in patients with cancer. Lancet Oncol. 2016;17:e452–e466. doi: 10.1016/S1470-2045(16)30369-2
- van der Hulle T, den Exter PL, Planquette B, Meyer G, Soler S, Monreal M, Jimenez D, Portillo AK, O’Connell C, Liebman HA, et al. Risk of recurrent venous thromboembolism and major hemorrhage in cancer-associated incidental pulmonary embolism among treated and untreated patients: a pooled analysis of 926 patients. J Thromb Haemost. 2016;14:105–113. doi: 10.1111/jth.13172
- Klok FA, Huisman MV. How I assess and manage the risk of bleeding in patients treated for venous thromboembolism. Blood. 2020;135:724–734. doi: 10.1182/blood.2019001605
- Chatani R, Yamashita Y, Morimoto T, Mushiake K, Kadota K, Kaneda K, Nishimoto Y, Ikeda N, Kobayashi Y, Ikeda S, et al; COMMAND VTE Registry-2 Investigators. Cancer-associated venous thromboembolism in the direct oral anticoagulants era: insight from the COMMAND VTE Registry-2. Thromb Res. 2024;234:86–93. doi: 10.1016/j.thromres.2023.12.016
- Chatani R, Yamashita Y, Morimoto T, Kaneda K, Mushiake K, Kadota K, Nishimoto Y, Ikeda N, Kobayashi Y, Ikeda S, et al; COMMAND VTE Registry-2 Investigators. Transition of management strategies and long-term outcomes in cancer-associated venous thromboembolism from the warfarin era to the direct oral anticoagulant era. Eur J Intern Med. 2024;123:72–80. doi: 10.1016/j.ejim.2024.01.012







