ThS. BS. LÊ THỊ LAN HƯƠNG
BS.CK1. TRẦN CÔNG TRÌNH
PGS. TS. BS. PHẠM NGUYỄN VINH
(…)
1. Định nghĩa và mô bệnh học:
Theo phân loại Tổ chức Y tế Thế giới (WHO) về bệnh cơ tim năm 1995, viêm cơ tim được định nghĩa là “viêm các tế bào cơ tim dẫn đến rối loạn chức năng tim” và được liệt kê trong số “bệnh cơ tim chuyên biệt”. Viêm cơ tim được chẩn đoán trên sinh thiết mô cơ tim (EMB) theo các tiêu chí mô học, miễn dịch và hóa mô miễn dịch, và khuyến cáo sử dụng các kỹ thuật sinh học phân tử trên EMB để xác định các tác nhân vi-rút. Ngoài ra, viêm cơ tim do các tác nhân khác như nhiễm khuẩn, tự miễn và độc chất [8, 9].
Năm 1987, dựa vào tiêu chí mô học Dallas trong EMB [10], viêm cơ tim được định nghĩa là ‘thâm nhiễm viêm của cơ tim với hoại tử và/hoặc thoái hóa các tế bào cơ lân cận, không điển hình của tổn thương thiếu máu cục bộ do chi phối mạch vành. Phù mô kẽ thường xuất hiện trong các giai đoạn cấp tính của bệnh, cùng với viêm và hoại tử. Sự hiện diện và mức độ xơ hóa cũng là thông tin quan trọng. Mặc dù tiêu chuẩn mô học không phải là tiêu chuẩn vàng duy nhất để chẩn đoán viêm cơ tim, nhưng vẫn cần để phân loại các nguyên nhân khác nhau của viêm cơ tim dựa trên các tiêu chí mô học, tức là tế bào lympho, bạch cầu ái toan, tế bào đa hình (polymorphous), u hạt (granulomatous) và tế bào khổng lồ (Hình 3.1)
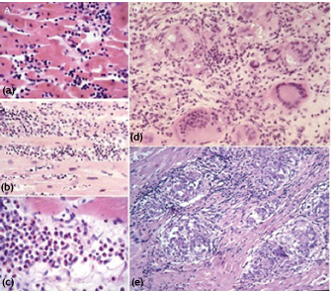
Hình 3.1 Phân nhóm mô học của bệnh cơ tim viêm (viêm cơ tim)[9]
(a) tế bào lympho
(b) tế bào đa hình
(c) bạch cầu ái toan
(d) tế bào khổng lồ
(e) bệnh sarcoidosis
Hơn nữa, ngày nay độ nhạy của EMB được gia tăng bằng cách sử dụng hóa mô miễn dịch với một bảng lớn các kháng thể đơn dòng và đa dòng [bao gồm kháng CD3, tế bào lympho T, chống CD68, đại thực bào và kháng nguyên bạch cầu chống người (HLA)-DR)]. Chẩn đoán viêm cơ tim với ngưỡng giá trị >14 bạch cầu/mm2, với sự hiện diện của tế bào lympho T > 7 tế bào/mm2 [11]. Đặc biệt, ở mức đại thể hay vi thể, tổn thương viêm cơ tim so với các tế bào cơ tim lân cận thường gặp đó là tổn thương dưới thượng mạc cơ tim thất trái và /hoặc phân bố từng mảng (patchy) ở nội mạc cơ tim [11](Hình 3.2).
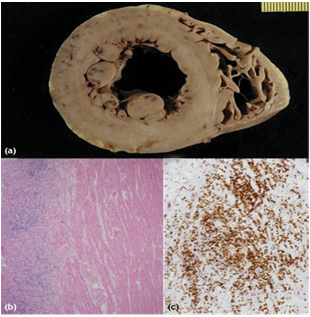
Hình 3.2 Trường hợp đột tử do tim do viêm cơ tim cấp [11].
- Hình cắt ngang của tim qua hai thất ghi nhận sự hiện diện của các vùng rối loạn sắc tố lan tỏa ( diffuse dyschromic) chủ yếu ở dưới thượng mạc và lớp giữa cơ tim, ngược lại thiếu máu cục bộ và tổn thương tái tưới máu thường ở lớp dưới nội mạc
- Mô học toàn thể thất trái với nhuộm HE (haematoxylin-eosin): tổn thương phù mô kẽ và thâm nhiễm viêm lan tỏa ở lớp ngoài thành thất trái
- Ở độ phóng đại cao hơn, tế bào lympho T dồi dào được nhìn thấy trên hóa mô miễn dịch (nhuộm miễn dịch CD3).
Ngày nay, EMB còn phát triển với tìm kiếm phân tử bộ gen vi-rút với axit deoxyribonucleic-axit ribonucleic (DNA-RNA) bằng kĩ thuật khuếch đại chuỗi polymerase phiên mã ngược (RT-PCR reverse transcription polymerase chain reaction) (Hình 3.3). Ngoài ra, để loại trừ nhiễm trùng toàn thân, xét nghiệm máu ngoại vi luôn được nghiên cứu song song với EMB; Định lượng tải lượng virus và xác định sự nhân lên của virus có thể bổ sung thêm giá trị chẩn đoán.
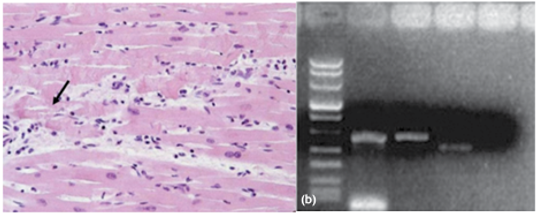
Hình 3.3 Chẩn đoán mô học và hình phân tử của viêm cơ tim do vi-rút lymphocytic trên EMB [9].
- Viêm cơ tim hoạt động với thâm nhiễm tế bào lympho và các ổ phân hủy tế bào cơ (mũi tên).
- Điện di gel (Gel electrophoresis): phản ứng chuỗi polymerase dương tính (PCR) đối với enterovirus. Lane 1: marker DNA (yếu tố VIII); lane 2: kiểm soát dương tính với enterovirus (180 pb); lane 3: EMB dương tính với enterovirus; và lane 4: giá trị âm tính (negative control)
Được kích hoạt bởi các yếu tố truyền nhiễm, nhưng cũng có các yếu tố độc hại, dị ứng hoặc các yếu tố khác, quá trình viêm cơ tim ở người biểu hiện với ba giai đoạn: (1) tổn thương cấp tính đối với tế bào cơ với hoại tử ban đầu và tiếp xúc với kháng nguyên nội bào, kéo dài vài ngày; (2) kích hoạt quá trình miễn dịch hoặc tự miễn dịch, hoạt hóa tế bào lympho T và giải phóng cytokine viêm (phù, thâm nhiễm tế bào lympho) và hoại tử tế bào cơ tiềm ẩn (giai đoạn bán cấp, vài tuần đến vài tháng), và nếu không được chữa lành sau giai đoạn 2 thì dẫn đến giai đoạn (3) tình trạng viêm đang diễn ra với tái cấu trúc thất trái và dẫn đến bệnh cơ tim giãn nỡ.
2. Tác nhân gây viêm cơ tim
Tác nhân gây viêm cơ tim được chia làm 4 nhóm chính: do vi rút, vi khuẩn, do thuốc và độc chất và do các bệnh lý viêm hệ thống. Trong đó, viêm cơ tim do vi rút là thường gặp nhất
Bảng 4.1 Tác nhân gây viêm cơ tim[8]
| Do nhiễm | |
| Vi rút | RNA virus: coxsackievirus và B, echovirus, poliovirus, cúm A và B, vi rút hợp bào hô hấp (respiratory syncytial virus), quai bị, sởi, rubella, viêm gan virus C, sốt xuất huyết, sốt vàng, chikungunya virus, Junin virus, Lassa fevervirus, dại, HIV-1
DNA virus: Adenoviruses, Parvovirus B19, Cytomegalovirus, Human Herpes virus-6, Epstein-Barr virus, Varicella-zoster virus, Herpes simplex virus, Variola virus, Vaccinia virus |
| Vi khuẩn | Staphylococcus, Streptococcus, Pneumococcus, Meningococcus, Gonococcus, Salmonella, Corynebacterium diphtheriae, Haemophilus influenzae, Mycobacterium tuberculosis, Mycoplasma pneumoniae, Brucella |
| Xoắn khuẩn | Borrelia (Lyme disease), Leptospira (Weil disease) |
| Nấm | Aspergillus, Actinomyces, Blastomyces, Candida, Coccidioides, Cryptococcus, Histoplasma, Mucormycoses, Nocardia, Sporothrix |
| Đơn bào | Trypanosoma cruzi, Toxoplasma gondii, Entamoeba, Leishmania |
| Rickettsial | Coxiella burnetii, R. rickettsii, R. tsutsugamuschi |
| Trung gian miễn dịch | |
| Dị ứng | Độc tố uốn ván, vaccine (như vaccine đậu mùa), bệnh huyết thanh
Thuốc: penicillin, cefaclor, colchicin, furosemid, isoniazid, lidocain, tatracyclin, sulfonamid, phenytoin, phenylbutazon, methyldopa, thiazid, diuretics, amitryptillin, immune-checkpoint inhibitors |
| Ghép | Thải ghép tim |
| Tự miễn | Viêm cơ tim tế bào lympho không nhiễm trùng, viêm cơ tim tế bào khổng lồ không nhiễm trùng
Liên quan đến bệnh tự miễn: lupus ban đỏ hệ thống, viêm khớp dạng thấp, hội chứng Churg-Strauss, Bệnh Kawasaki, viêm đại tràng, xơ cứng bì, viêm đa cơ, nhược cơ, đái tháo đường phụ thuộc insulin, nhiễm độc giáp, sarcoidosis, u hạt Wegener, thấp tim |
| Độc chất | |
| Thuốc | Amphetamines, anthracyclines, cocaine, cyclophosphamide, ethanol, fluorouracil, lithium, catecholamines, hemetine, interleukin-2, trastuzumab, clozapine |
| Kim loại nặng | Đồng, sắt, chì (tích lũy trong tế bào) |
| Động vật | Nọc bò cạp, rắn và nhện cắn, ong chích |
| Hóc-môn | U tủy thượng thận |
| Tác nhân vật lý | Tia xạ, điện giật |
3. Phân loại giai đoạn lâm sàng
Viêm cơ tim cấp chủ yếu là chẩn đoán lâm sàng, và theo các tiêu chuẩn gần đây Hội tim mạch Hoa Kỳ (AHA) và Hội tim mạch Châu Âu (ESC) chẩn đoán viêm cơ tim cấp khi các triệu chứng bắt đầu trong vòng một tháng [5, 8]. Viêm cơ tim cấp thường đi kèm với tăng Troponin I/T và hiện diện phù cơ tim trên cộng hưởng từ hoặc khi sinh thiết mô cơ tim ghi nhận hoại tử các tế bào cơ tim. Một số trường hợp có thể gặp viêm cơ tim thể tối cấp với tình trang suy sụp tuần hoàn nghiêm trọng cần dùng vận mạch hoặc hỗ trợ tuần hoàn cơ học [8].
Viêm cơ tim bán cấp là giai đoạn viêm cơ tim khi các triệu chứng từ một đến ba tháng, do yếu tố viêm còn khởi phát gây ra tình trạng viêm kéo dài [12]. Đôi khi theo đặc điểm lâm sàng và mô bệnh học, giai đoạn này cũng có thể là viêm cơ tim hồi phục hoặc giai đoạn thải virut.
Viêm cơ tim mãn tính là giai đoạn trung gian giữa viêm cơ tim cấp và bênh cơ tim do viêm mạn. Đây là một quá trình viêm đang diễn tiến đến xơ hóa, nhưng cũng có thể không có hoại tử hoặc bất thường trong tế bào cơ tim [5,13]. Theo hướng dẫn của ESC, viêm cơ tim mạn nếu triệu chứng kéo dài hơn ba tháng [8]. Và thuật ngữ này có thể chồng lấp với viêm cơ tim bán cấp.
Bệnh cơ tim do viêm mạn là tình trạng viêm mãn tính do sự xâm nhập liên tục các tế bào viêm của cơ tim nhưng không có dấu hiệu hoại tử cơ tim rõ ràng [13]. Bệnh tiến triển sẽ gây ra xơ hóa cục bộ hoặc lan tỏa các tế bào cơ tim. Tình trạng này xuất hiện sau 30 ngày từ khi xuất hiện các triệu chứng và đi kèm với tình trạng tái cấu trúc thất trái hoặc suy tim, với biểu hiện lâm sàng là bệnh cơ tim dãn do viêm hoặc bệnh cơ tim giảm động không dãn (hypokinetic non dilated cardiomyopathy)[8].
Bảng 5.1 Định nghĩa và phân loại các giai đoạn lâm sàng viêm cơ tim theo JCS 2023 [13]
| Giai đoạn | Định nghĩa | Thâm nhiễm tế bào viêm | Tổn thương viêm cơ tim |
| Viêm cơ tim cấp | Viêm cơ tim <30 ngày sau khi khởi phát , đặc trưng bởi thâm nhiễm tế bào viêm và tổn thương tế bào cơ tim (thoái hóa/hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim)
Khi không có EMB, diễn tiến lâm sàng và triệu chứng gợi ý viêm cơ tim, chẩn đoán lâm sàng viêm cơ tim cấp tính khi: 1) Tăng nồng độ Troponin hs 2) Phù cơ tim trên CMR |
+ | + |
| Viêm cơ tim mạn còn hoạt động | Viêm cơ tim ≥ 30 ngày sau khi khởi phát, đặc trưng là thâm nhiễm tế bào viêm và tổn thương tế bào cơ tim (thoái hóa/hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim)
Ngay cả khi tổn thương tế bào cơ tim không được quan sát thấy trên mô bệnh học, hiện diện của một trong các biểu hiện sau đây cho thấy khả năng viêm cơ tim mạn tính còn hoạt động: 1) Tăng liên tục nồng độ Troponin hs 2) Tế bào T dương tính với CD3 trong mô cơ tim ≥24/mm2 (5.8 tế bào/HPF) 3) Nhuộm Tenascin C (4C8) dương tính trong mô cơ tim |
+ | + |
| Viêm cơ tim mãn tính | Viêm cơ tim k≥30 ngày sau khi khởi phát, đặc trưng là thâm nhiễm tế bào viêm mà không bị tổn thương tế bào cơ tim. Đây là giai đoạn chuyển tiếp giữa viêm cơ tim cấp và bệnh cơ tim viêm mãn tính | + | – |
| Bệnh cơ tim do viêm mạn tính | Viêm cơ tim kéo dài ≥30 ngày sau khi khởi phát, kèm theo rối loạn vận động vùng. Về mặt mô học, có xơ hóa kèm theo bất thường tế bào cơ tim (thay đổi kích thước tế bào cơ tim) và thâm nhiễm tế bào viêm (thâm nhiễm bạch cầu ≥14 / mm2 trong mẫu mô với tế bào T dương tính CD3 ≥7 / mm2).
Không có bằng chứng tổn thương tế bào cơ tim (thoái hóa/hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim) |
+ | – |
| Bệnh cơ tim giãn do viêm | Đây là một phân nhóm của bệnh cơ tim giãn, đặc trưng về mặt mô học bởi thâm nhiễm tế bào viêm mà không có tổn thương tế bào cơ tim (thoái hóa / hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim). | + | – |
Hiện nay, vẫn còn sự khác biệt về định nghĩa và phân giai đoạn giữa các hiệp hội và đồng thuận chuyên gia (Bảng 5.2)
Bảng 5.2 Khác biệt trong các định nghĩa trong các hướng dẫn và đồng thuận chuyên gia hiện nay
| Giai đoạn | JCS 2009
[14] |
ESC 2013
[8] |
Đồng thuận chuyên gia 2020
[5] |
JCS 2023
[13] |
| Viêm cơ cấp | Viêm cơ tim <3 tháng(∼vài tháng) sau khi khởi phát | Viêm cơ tim <3 tháng(∼vài tháng) sau khi khởi phát | Viêm cơ tim <30 ngày sau khi khởi phát
|
|
| · Đặc trưng mô học bởi thâm nhiễm tế bào viêm
· Tổn thương tế bào cơ tim (thoái hóa/hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi của tế bào cơ tim) |
||||
| Viêm cơ tim mãn tính còn hoạt động | Không xác định | Không xác định | Không xác định | Viêm cơ tim >30 ngày sau khởi phát
Đặc trưng mô học bởi thâm nhiễm tế bào viêm. Tổn thương tế bào cơ tim (thoái hóa/ hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim) |
| Viêm cơ tim mãn tính | Viêm cơ tim >3 tháng (∼vài tháng) sau khi khởi phát | Viêm cơ tim >3 tháng sau khi khởi phát | Không mô tả | Viêm cơ tim >30 ngày sau khởi phát |
| Đặc trưng mô học bởi thâm nhiễm tế bào đơn nhân.
Tổn thương tế bào cơ tim (thoái hóa/hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim) |
Về mặt mô học, xơ hóa kèm theo bất thường tế bào cơ tim (thay đổi kích thước tế bào cơ tim…) và thâm nhiễm tế bào viêm (bạch cầu ≥ 14 / mm2 mẫu mô với tế bào T dương tính với CD3 ≥ 7/mm2)
Không được mô tả liên quan đến chấn thương |
Đặc trưng mô học bởi thâm nhiễm tế bào viêm.
Không có tổn thương tế bào cơ tim (thoái hóa/hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim). Giai đoạn chuyển tiếp giữa viêm cơ tim cấp và bệnh cơ tim viêm mãn tính |
||
| Bệnh cơ tim do viêm mãn tính | Không xác định | Không xác định | Viêm cơ tim kéo dài ≥30 ngày sau khi khởi phát | |
| Rối loạn vận động vùng
Về mặt mô học: xơ hóa kèm theo bất thường tế bào cơ tim (thay đổi kích thước tế bào cơ tim) và thâm nhiễm tế bào viêm (bạch cầu ≥14 / mm2 mẫu mô với tế bào T dương tính CD3 ≥7/mm2) Không có tổn thương tế bào cơ tim (thoái hóa/hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim) |
||||
| Bệnh cơ tim giãn do viêm | Không xác định | Phân nhóm của bệnh cơ tim giãn nở
Đặc trưng mô học bởi thâm nhiễm tế bào viêm Không có tổn thương tế bào cơ tim (thoái hóa/hoại tử kèm theo sự xâm lấn của các tế bào viêm ở chu vi tế bào cơ tim) |
||
4. Chẩn đoán viêm cơ tim
Từ năm 2013, Hiệp hội tim mạch Châu Âu đã đưa ra hướng dẫn các tiêu chuẩn chẩn đoán viêm cơ tim từ biểu hiện lâm sàng, triệu chứng phụ và cận lâm sàng.
Bảng 6.1 Chẩn đoán viêm cơ tim theo ESC 2013[8]
5. Bệnh cảnh lâm sàng viêm cơ tim[8]
Bệnh cảnh lâm sàng viêm cơ tim không đặc hiệu từ tác nhân vi-rút hoặc tác nhân nhiễm trùng và cũng có thể xảy ra với tác nhân độc chất, dị ứng hoặc các dạng tổn thương cơ tim khác. Các bất thường mô liên quan, chẳng hạn như giãn mạch, phù, thâm nhiễm bạch huyết và hoại tử tế bào cơ, là những phản ứng không đặc hiệu của hệ thống miễn dịch. Do đó, phát hiện CMR là tín hiệu hình ảnh phản ánh các quá trình này nhưng không đặc hiệu đối với một tác nhân cụ thể và kết quả cần được diễn giải trong bối cảnh lâm sàng [8].
Tùy thuộc vào mức độ nghiêm trọng và mức độ viêm và tổn thương cơ tim, biểu hiện lâm sàng của viêm cơ tim cấp tính có thể rất khác nhau, trải rộng từ thể bán cấp không triệu chứng đến thể tối cấp cần hỗ trợ tuần hoàn cơ học, thậm chí dẫn đến đột tử do loạn nhịp tim. Các triệu chứng thường gặp bao gồm đau ngực hoặc thường bao gồm tiền sử bệnh nhiễm vi-rút gần đây hoặc tiêm vắc-xin, dị ứng hoặc các dạng viêm hoặc nhiễm trùng toàn thân khác [8].
Theo Hội Tim mạch Châu Âu (ESC) trong đồng thuận về chẩn đoán và điều trị viêm cơ tim năm 2013, sau loại trừ nguyên nhân bệnh mạch vành và các nguyên nhân khác gây suy tim, có bốn thể lâm sàng chính của viêm cơ tim bao gồm: đau ngực kiểu hội chứng mạch vành cấp; suy tim mới xuất hiện hay tiến triển, suy tim mạn; tình trạng đe dọa tính mạng (rối loạn nhịp, đột tử).
Bảng 7.1 Các bệnh cảnh lâm sàng viêm cơ tim cấp [8]
| 1. Đau ngực kiểu hội chứng vành cấp
(a) Đau ngực cấp tính – Thường bắt đầu trong vòng 1-4 tuần sau khi bị nhiễm trùng đường hô hấp hoặc đường tiêu hóa – Thường liên quan đến các triệu chứng nặng và tái phát – Không có bệnh động mạch vành (b) Thay đổi sóng ST / T – ST chênh lên hoặc chênh xuống – Sóng T âm (c) Kèm hoặc không kèm rối loạn chức năng thất trái (LV) và/hoặc thất phải (RV) khu trú hoặc toàn bộ phát hiện trên siêu âm hoặc cộng hưởng từ (CMR) (d) Có/không tăng men tim TnT/TnI diễn biến thời gian tương tự như nhồi máu cơ tim cấp tính hoặc tăng kéo dài trong vài tuần hoặc vài tháng |
| 2. Suy tim mới xuất hiện hay tiến triển
(a) Suy tim mới xuất hiện hay tiến triển trong vòng 2 tuần đến 3 tháng, gồm các triệu chứng: khó thở, phù ngoại biên, khó chịu ở ngực, mệt mỏi (b) Giảm chức năng tâm thu thất trái LV và/ hoặc thất phải, kèm tăng/không tăng bề dày thành tim; dãn/không dãn thất trái/thất phải trên siêu âm hoặc cộng hưởng từ (c) Các triệu chứng bắt đầu sau khi nhiễm trùng đường hô hấp hoặc đường tiêu hóa, hoặc trong giai đoạn chu sinh; (d) Bất thường ECG không đặc hiệu: blốc nhánh, Blốc nhĩ thất, loạn nhịp thất |
| 3. Suy tim mạn tính (trong trường hợp không có bệnh mạch vành và các nguyên nhân đã biết của suy tim)
(a) Các triệu chứng suy tim (với đợt kịch phát tái phát) kéo dài trên 3 tháng (b) Mệt mỏi, đánh trống ngực, khó thở, đau ngực không điển hình, rối loạn nhịp tim ở bệnh nhân cấp cứu (c) Giảm chức năng tâm thu thất trái và/hoặc thất phải trên siêu âm tim hoặc CMR gợi ý hoặc bệnh cơ tim không thiếu máu cục bộ (d) Bất thường ECG không đặc hiệu: blốc nhánh, Blốc nhĩ thất, loạn nhịp thất |
| 4. Tình trạng đe dọa tính mạng (trong trường hợp không có bệnh mạch vành và các nguyên nhân đã biết của suy tim)
(a) Rối loạn nhịp tim đe dọa tính mạng và đột tử cứu sống (b) Sốc tim (c) Suy giảm chức năng thất trái nghiêm trọng |
6. Phương tiện chẩn đoán trong chẩn đoán viêm cơ tim
Siêu âm tim vẫn là một phương thức chẩn đoán hình ảnh thiết yếu và đầu tay khi nghi ngờ viêm cơ tim, giúp loại trừ các nguyên nhân khác gây suy tim, đánh giá bệnh lý van tim cũng như đánh giá hiện diện của huyết khối trong tim. Siêu âm tim đánh giá rối loạn chức năng tâm thu và tâm trương của tâm thất trái. Ở bệnh nhân viêm cơ tim cấp, siêu âm tim có thể cho thấy dày thành thất trái dày tình trạng do phù cơ tim kẽ, rối loạn vận động vùng khu trú hoặc toàn thể không phân theo chi phối mạch vành và thường gặp giảm động thành dưới và thành bên [15]. Vùng cơ tim dày do phù nề thường thoáng qua và chỉ kéo dài trong giai đoạn cấp tính của bệnh [13]. Ngoài việc đánh giá chức năng thất trái, điều quan trọng là phải đánh giá chức năng tâm thất phải (đánh giá kích thước, TAPSE). Giảm chức năng thất phải là một yếu tố dự báo mạnh mẽ về tử vong và nhu cầu ghép tim ở những bệnh nhân bị viêm cơ tim[13]. Giảm chức năng thất trái ở thời điểm siêu âm tim kiểm tra lần đầu tiên có ý nghĩa tiên lượng và dự đoán kết cục xấu[16] Theo nghiên cứu của tác giả Meindl C. và cs ở bênh nhân viêm cơ tim giai đoạn cấp và bán cấp cho thấy độ biến dạng cơ tim theo trục dọc toàn thể ( LV- GLS) giúp tiên lượng tốt hơn so với chức năng tâm thu thất trái (p < 0,05) [17]. Chẩn đoán phân biệt giữa viêm cơ tim cấp và nhồi máu cơ tim cấp vẫn là một thách thức lớn, việc áp dụng các kỹ thuật siêu âm tim mới, đặc biệt là siêu âm đánh dấu mô (speackle tracking), không những gia tăng chính xác không chỉ trong chẩn đoán rối loạn chức năng tâm thu và tâm trương của tâm thất trái, mà còn có thể phân biệt hai bệnh này và có giá trị theo dõi và tiên lượng bệnh [18].
Tuy nhiên, siêu âm có độ nhạy không cao để xác định viêm cơ tim trong các trường hợp không có rối loạn chức năng thất trái, và độ đặc hiệu thấp trong việc phân biệt cấp tính với mãn tính, cũng như không phân biệt viêm cơ tim với các bệnh cơ tim không do thiếu máu cục bộ khác[19, 20]. Trước đây, hình ảnh y học hạt nhân với 67-gallium và 111-indium hữu ích trong chẩn đoán viêm cơ tim cấp tính, nhưng hiếm khi sử dụng trong thực hành lâm sàng. So sánh FDG-PET và CMR ghi nhận FDG-PET chẩn đoán giá trị chẩn đoán tương đương nhưng nhiễm tia xạ và độ phân giải không gian tương đối kém.
Do tính chất xâm lấn của EMB, nên các phương pháp không xâm lấn để đánh giá viêm cơ tim đóng một vai trò thiết yếu trong chẩn đoán nghi ngờ viêm cơ tim, mặc dù EMB vẫn là tiêu chuẩn vàng để phân loại nguyên nhân [21]. Trong các khuyến cáo của ESC, CMR được chỉ định ở những bệnh nhân ổn định về mặt lâm sàng và huyết động [22].
Bảng 8.1 Khuyến cáo ESC về chỉ định cộng hưởng từ tim[22]
| Khuyến cáo | Phân độ (Class) | Mức độ (Level) |
| Cộng hưởng từ được khuyến cáo chỉ định đánh giá cấu trúc và chức năng tim trong trường hợp của sổ siêu âm tim hạn chế | I | C |
| Cộng hưởng từ được khuyến cáo chỉ định đánh giá đặc tính mô cơ tim như: bệnh cơ tim thâm nhiễm, bệnh Fabry, Viêm cơ tim, bệnh cơ tim tăng sinh cơ bè, amyloid, sarcoidosis, và bệnh cơ tim do quá tải sắt | I | C |
CMR không thể phân biệt giữa sự tồn tại của virus và viêm tự miễn và do đó không thể thay thế EMB cho việc ra quyết định điều trị. Do đó, trong trường hợp suy tim cấp tính hoặc các biểu hiện đe dọa tính mạng khác, EMB không nên bị trì hoãn bởi bất kỳ thủ tục chẩn đoán nào khác[8].
Bảng 8.2 So sánh chỉ định của cộng hưởng từ (CMR) và sinh thiết nội mạc cơ tim (EMB) trong chẩn đoán và điều trị viêm cơ tim [23]
| CMR | EMB | |
| Sốc tim | – | + |
| Viêm cơ tim cấp không biến chứng | + | – |
| Viêm cơ tim cấp biến chứng loạn nhịp | – | + |
| Bệnh cơ tim dãn do viêm (> 3 tháng) | + (kết quả âm tính không loại trừ do ngưỡng viêm thấp) | ++ (quyết định liệu pháp điều trị) |
| Đánh giá đáp ứng điều trị | + | thất bại/ không đáp ứng điều trị |
7. Cộng hưởng từ trong đánh giá viêm cơ tim
Khoảng hơn 2 thập kỉ nay, với sự tiến bộ về các kĩ thuật chẩn đoán hình ảnh, cộng hưởng từ ngày càng đóng vai trò quan trọng, góp phần trong việc chẩn đoán và theo dõi viêm cơ tim. Cộng hưởng từ có thể phát hiện các thay đổi trong quá trình viêm cơ tim, độc lập với tác nhân gây bệnh, do đó có thể giúp đưa ra quyết định lâm sàng cho bệnh nhân. Ưu việt lớn nhất của cộng hưởng từ là phương pháp hình ảnh không xâm lấn duy nhất có thể đánh giá bản chất mô cơ tim, đông thời khảo sát các thông số thay đổi trong thể tích dịch ngoại bào (ECV) để hình dung quá trình diễn tiến viêm. Các đặc điểm của viêm cơ tim trên CMR bao gồm: phù, sung huyết, thoát dịch mao mạch, hoại tử và cuối cùng là xơ hóa cơ tim thông qua các chuỗi xung T2-W, EGE và LGE. Năm 2009, đồng thuận các chuyên gia đưa ra tiêu chuẩn Lake – Louise sử dụng kết hợp 2/3 đặc điểm mô để tăng độ tin cậy trong chẩn đoán viêm cơ tim (Hình 9.1) [24].
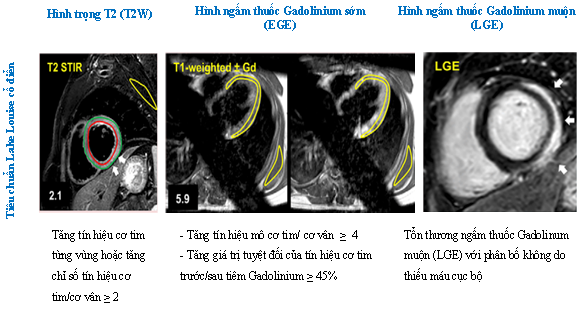
Hình 9.1 Tiêu chuẩn Lake Louise 2009 trong chẩn đoán viêm cơ tim [24]
Hiện nay, các kĩ thuật mới của cộng hưởng từ như bản đồ T1, T2 và ECV được chứng minh rất hữu ích trong đánh giá mô bệnh học cơ tim. Những kĩ thuật tiến bộ này khắc phục được các hạn chế của tiêu chuẩn Lake Louise cũ, và giúp gia tăng độ nhạy và độ đặc hiệu trong chẩn đoán. Do đó năm 2018, đồng thuận các chuyên gia đã đưa ra tiêu chuẩn Lake Louise cải tiến: khác với tiêu chuẩn năm 2009, hiện nay chẩn đoán viêm cơ tim khi có 1 tiêu chuẩn trên hình T1 và 1 tiêu chuẩn trên hình T2 và các tiêu chuẩn hỗ trợ không thay đổi so với tiêu chuẩn Lake Louise cổ điển (Hình 9.2).
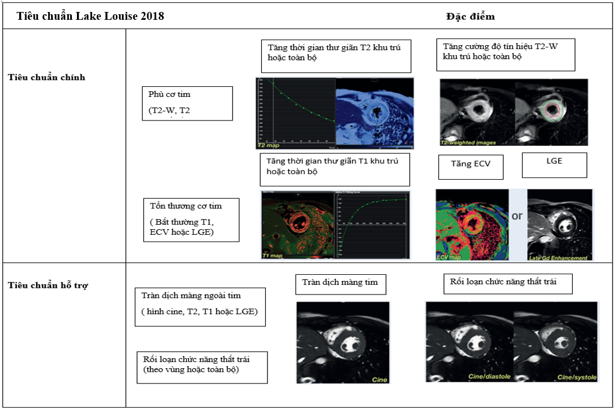
Hình 9.2 Tiêu chuẩn Lake Louise cải tiến [25]
Tiêu chuẩn Lake Louise cổ điển đã được áp dụng rộng rãi trong lâm sàng và trong các nghiên cứu. Theo phân tích gộp của Lagan và công sự độ nhạy, độ đặc hiệu và độ chính xác của tiêu chuẩn Lake Louise cổ điển lần lượt là 77%, 81% và 79%[26]. Một phân tích gộp của tác giả Kotanisis và cộng sự ghi nhận độ nhạy và độ đặc hiệu của tiêu chuẩn LLC cổ điểm là 78% và 88%[27]. Hơn nữa, cả hai phân tích gộp đều chứng minh tiềm năng góp phần gia tăng chẩn đoán của kĩ thuật mapping ở bệnh nhân nghi ngờ viêm cơ tim.
Bảng 9.1 Giá trị chẩn đoán của cộng hưởng từ trong chẩn đoán viêm cơ tim [25]
| Đặc điểm trên MRI | Giá trị chẩn đoán
(diện tích dưới đường cong AUC) |
Số lượng nghiên cứu | Tổng số bệnh nhân |
| Từng tiêu chuẩn độc lập | |||
| Hình T2W | 73 (58-100) | 13 | 981 |
| EGE | 73 (62 – 93) | 10 | 711 |
| LGE | 83 (53 – 96) | 14 | 1073 |
| Bản đồ T1 | 89 (71 – 99) | 9 | 682 |
| Bản đồ T2 | 80 (73 – 86) | 6 | 499 |
| ECV | 74 (54 – 82) | 7 | 555 |
| Phối hợp các tiêu chuẩn | |||
| Tiêu chuẩn Lake Louise cổ điển | 84 (57 – 90) | 8 | 630 |
| Hình T2W + EGE | 76 (71 – 89) | 3 | 191 |
| Hình T2W + LGE | 75 | 1 | 45 |
| EGE + LGE | 70 | 1 | 45 |
| Bản đồ T2 + LGE | 80 (83 – 97) | 2 | 120 |
| Bản đồ T1 + T2 | 86 | 1 | 36 |
| Hình T2W + bản đồ T1 | 84 (73 – 95) | 2 | 176 |
| Bản đồ T1 + LGE | 96 (82 – 97) | 5 | 350 |
Trong phân tích gộp nhiều nghiên cứu, khi so sánh giá trị chẩn đoán viêm cơ tim của tiêu chuẩn Lake Louise cổ điển với các tiêu chuẩn cập nhật mới, cho thấy giá trị chẩn đoán tăng từ 84% lên đến 96%[25]. Nhờ đó, hiện nay các đồng thuận của hội tim mạch Châu Âu năm 2021 đã cho thấy vai trò của CMR trong chẩn đoán: từ gợi ý chẩn đoán ở bệnh nhân nghi ngờ viêm cơ tim đến khẳng định chẩn đoán (Hình 9.3) [22].
Hình 9.3 Bước tiến của CMR trong chẩn đoán viêm cơ tim [22]
Mức độ và cường độ của các đặc điểm mô cơ tim phụ thuộc vào độ nặng của tình trạng viêm cơ tim, cũng như thời điểm thực hiện CMR liên quan đến diễn tiến tự nhiên của bệnh từ giai đoạn cấp tính, bán cấp, đến giai đoạn lành hoặc tổn thương mạn tính. Những biểu hiện tiến trình viêm thay đổi theo thời gian, và thường chỉ kéo dài vài ngày đến vài tuần, do đó một trong những hạn chế của các phương pháp hình ảnh nói chung là chỉ nhạy trong vài tuần đầu kể từ lúc khởi phát. Vì vậy, CMR nên được chỉ định càng sớm càng tốt, tốt nhất ở giai đoạn sớm của bệnh, hoặc lúc khởi phát các triệc chứng như đau ngực, suy tim, hoặc rối loạn nhịp (Bảng 9.2).
Bảng 9.2 Các đặc điểm của cộng hường từ đánh giá giai đoạn viêm cơ tim [28]
| Đặc điểm | Phù | Sung huyết / thoát mạch | Hoại tử | Xơ hóa |
| Giai đoạn cấp | ↑ T2
(T2 STIR/T2 mapping) ↑T1 (native T1/ ECV) |
T1 ↑
(native T1/ ECV) EGE – hoặc + |
LGE – hoặc + | – |
| Giai đoạn bán cấp | T2 – hoặc ↑
(T2 STIR/T2 mapping) T1 – hoặc ↑ (native T1/ ECV) |
T1 ↑
(native T1 / ECV) EGE – hoặc + |
LGE – hoặc + | LGE – hoặc +
T 1 – hoặc ↑ (native T1 / ECV) |
| Giai đoạn mạn | – | – | – | LGE – hoặc +
T1 – hoặc ↑ (native T1/ECV) |
Mặc dù không phân lập được tác nhân gây bệnh, tuy nhiên trong một số thể viêm cơ tim, CMR cũng có thể giúp hỗ trợ chẩn đoán như: viêm cơ tim trong sarcoidosis, viêm cơ tim do tăng tế bào Eosinophilin, viêm cơ tim tế bào khổng lồ. Tác giả Polter và cs, đã đưa ra các tiêu chuẩn lâm sàng và hình ảnh trong phân biệt một số thể viêm cơ tim đặc biệt. (Bảng 9.3)
Bảng 9.3 Đặc điểm một số thể viêm cơ tim [28]
| Đặc điểm | VCT do vi rút | Sarcoidosis | VCT tế bào khổng lồ | VCT tăng Eosinophilin |
| Dịch tễ | – Trung niên
– 2 giới |
– Trung niên
– 2 giới |
– < 40 tuổi
– 2 giới |
|
| Bệnh cảnh lâm sàng | Lâm sàng hội chứng vành cấp kèm tiền triệu nhiễm siêu vi | Lâm sàng rối loạn nhịp thất, block dẫn truyền tim, suy tim tiến triển. Thường kèm sarcoidosis ngoài tim | Rối loạn nhịp thất, suy tim tiến triển | Biểu hiện giống hội chứng vành cấp, kèm sốt và khó thở |
| Đặc điểm lâm sàng | Biểu hiện đa dạng từ không triệu chứng đến VCT thể tối cấp | Biểu hiện đa dạng từ không triệu chứng đến VCT thể tối cấp | Thường VCT thể tối cấp | Biểu hiện lâm sàng cấp tính |
| Đặc điểm LGE | Tổn thương dạng dưới thượng mạc và giữa thành, ưu thế đáy vách đến giữa thành bên và thành dưới bên. | LGE đa dạng (có thể tổn thương toàn bộ các lớp cơ tim), tổn thương bao gồm cả 2 thất và ranh giới vách liên thất tiếp giáp thất phải – thất trái | LGE rộng, có thể tổn thương toàn bộ các lớp cơ tim, tổn thương bao gồm cả 2 thất và ranh giới tiếp giáp thất phải – thất trái | Tổn thương lan tỏa dưới nội mạc cơ tim (sub-endo) với tín hiệu cao |
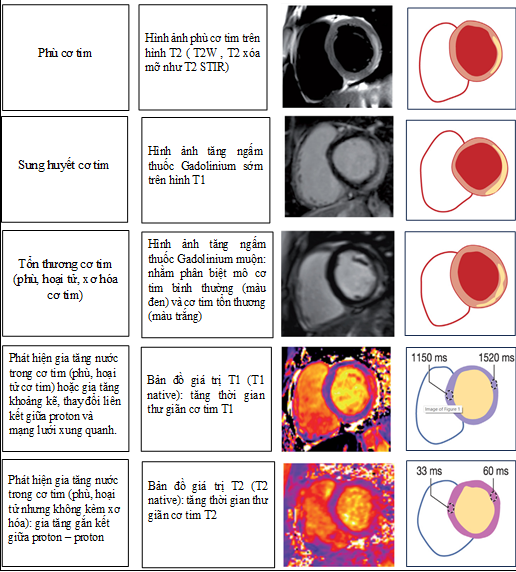
Tóm tại, chúng tôi xin tóm tắt một số đặc điểm tổn thương trên cộng hưởng từ tóm tắt theo bảng sau (Bảng 9.4):
Bảng 9.4 Tóm tắt các đặc điểm tổn thương viêm cơ tim trên cộng hưởng từ
8. Điều trị
Mục tiêu điều trị viêm cơ tim cấp là phục hồi chức năng cơ tim, theo dõi và phòng ngừa các biến chứng. Hiện nay, viêm cơ tim cấp do virút là thường gặp, chủ yếu điều trị triệu chứng và chưa có hướng dẫn về lựa chọn điều trị chuyên biệt cụ thể. Tuy nhiên, viêm cơ tim tự miễn (viêm cơ tim tế bào khổng lồ) được điều trị bằng liệu pháp ức chế miễn dịch. Một số ít bệnh nhân cần hỗ trợ tuần hoàn cơ học hoặc ghép tim trong vòng một năm. Tiên lượng của bệnh nhân được điều trị viêm cơ tim là khác nhau, với tỷ lệ sống sót sau năm năm là 60-90% [29].
8.1. Bệnh nhân ổn định huyết động:
Bệnh nhân bị viêm cơ tim và giảm chức năng thất trái tuân theo các hướng dẫn hiện hành trong điều trị suy tim [22]. Tình trạng suy tim do viêm cơ tim nhưng huyết động ổn định cần được điều trị bằng bốn nhóm thuốc điều trị chính trong suy tim theo hướng dẫn ESC 2021 gồm: thuốc lợi tiểu, thuốc ức chế men chuyển, hoặc thuốc chẹn thụ thể angiotensine, thuốc chẹn beta giao cảm và thuốc SGLT2 [30]. Theo các khuyến cáo hướng dẫn cần tiếp tục duy trì điều trị ít nhất sáu tháng ở những bệnh nhân bị LVEF giảm, ngay cả khi LVEF cải thiện (>50%). Thuốc chống viêm không steroid, đặc biệt là axit acetylsalicylic, không nên được sử dụng trong viêm cơ tim kèm suy tim vì làm gia tăng tỷ lệ tử vong [8]. Ở một số bệnh nhân viêm cơ tim kèm viêm màng ngoài tim, có chỉ định kháng viêm không steroid liều thấp. Các nghiên cứu bệnh chứng gần đây cho thấy sử dụng kháng viêm không steroid không đúng chỉ định sẽ làm tăng tỷ lệ tử vong ở bệnh nhân viêm cơ tim [31, 32].
| Mức độ khuyến cáo | Mức độ chứng cứ | |
| Nên nhập viện và theo dõi trong ít nhất 48 giờ ở bệnh nhân suy tim huyết động ổn không có triệu chứng suy tim | IIa | C |
| Cân nhắc sử dụng ức chế Phosphodiesterase III trong trường hợp suy bơm hoặc sung huyết phổi | IIa | C |
| Cân nhắc sử dung Noradrenaline trong trường hợp sốc tim | IIa | B |
| Cân nhắc sử dung Dopamine trong trường hợp sốc tim | IIb | B |
8.2. Bệnh nhân huyết động không ổn định
Bệnh nhân suy tim cấp huyết động không ổn định với nên được điều trị trong các đơn vị chăm sóc đặc biệt. Trong các trường hợp bệnh cấp tính/tối cấp với sốc tim và rối loạn chức năng tâm thất nặng, cần dùng các thuốc vận mạch.
Bảng 10.1 Sử dụng thuốc vận mạch trong viêm cơ tim cấp/ tối cấp theo JCS 2023 [13]
| Mức độ khuyến cáo | Mức độ chứng cứ | |
| Cân nhắc sử dụng Dobutamine trong trường hợp suy bơm hoặc sung huyết phổi | IIa | C |
| Cân nhắc sử dụng ức chế Phosphodiesterase III trong trường hợp suy bơm hoặc sung huyết phổi | IIa | C |
| Cân nhắc sử dung Noradrenaline trong trường hợp sốc tim | IIa | B |
| Cân nhắc sử dung Dopamine trong trường hợp sốc tim | IIb | B |
Các trường hợp sốc kháng trị với vận mạch, khuyến cáo sử dụng hỗ trợ tuần hoàn cơ học với mục đích chờ đợi cơ tim hồi phục hoặc ghét tim [33]. Ghép tim nên được hoãn lại trong giai đoạn cấp tính do cơ tim có thể hồi phục, nhưng nên được xem xét ở những bệnh nhân huyết động không ổn định với viêm cơ tim tế bào khổng lồ [33].
Bảng 10.2 Chỉ định hỗ trợ tuần hoàn cơ học trong trường hợp suy tim tối cấp theo JCS 2023 [13]
| Mức độ khuyến cáo | Mức độ chứng cứ | |
| Chỉ định VA-ECMO trong trường hợp sốc tim hoặc rối loạn nhịp đe dọa tính mạng | I | C |
| Cân nhắc sử dụng IMPELLA trong trường hợp sốc tim | IIa | C |
| Cân nhắc sử dụng IABP trong trường hợp sốc tim | IIa | C |
| Cân nhắc phối hợp IABP hoặc IMPELLA với VA-ECMO trong trường hợp sốc tim | IIa | C |
| Không sử dụng IABP hoặc IMPELLA đơn độc không được khuyến cáo trong trường hợp rối loạn nhịp nguy hiểm, suy tim phải, hoặc suy hô hấp | III | C |
VA-ECMO: oxy hóa máu qua màng ngoài cơ thể tĩnh mạch- động mạch, IMPELLA (intracardiac pump catheter for circulatory support): thiết bị bơm trong tim hỗ trợ tuần hoàn, IABP: bóng đối xung động mạch chủ
8.3. Rối loạn nhịp tim
Không có khuyến cáo đặc biệt điều trị rối loạn nhịp tim trong viêm cơ tim, vì vậy việc điều trị nên theo các khuyến cáo hiện tại [34]. Trường hợp loạn nhịp ác tính nên được điều trị bằng thuốc chống loạn nhịp. Cấy máy khử rung tim cấy ghép nên trì hoãn trong một đợt viêm cơ tim cấp tính và nên được xem xét từ ba đến sáu tháng sau giai đoạn cấp tính. Bệnh nhân bị viêm cơ tim tế bào khổng lồ kèm loạn nhịp ác tính có kỳ vọng sống hơn 1 năm mà không kèm ghép tim nên được cấy ICD [8, 35]. Blốc nhĩ thất hoàn toàn có thể cần đặt máy tạo nhịp tim tạm thời [36]. Tuy nhiên, đa phần các blốc nhĩ thất thường thoáng qua, và hồi phục trong vòng khoảng một tuần sau khi bắt đầu điều trị . Liệu pháp ức chế miễn dịch với steroid có thể thúc đẩy phục hồi dẫn truyền nút nhĩ thất[8]. Tuy nhiên, ở một số bệnh nhân, blốc nhĩ thất hoàn toàn tồn tại kéo dài sau giai đoạn cấp tính, cần phải cấy máy tạo nhịp tim vĩnh viễn [37]. Các khuyến cáo nhấn mạnh cân nhắc các chỉ định cấy ICD và máy khử rung tim tái đồng bộ tim (CRT-D) trong giai đoạn mạn tính của bệnh để ngăn ngừa đột tử do tim, ngay cả ở những bệnh nhân đang hồi phục, nếu rối loạn nhịp thất tồn tại dai dẳng [38]. Phòng ngừa ban đầu đột tử do tim dựa trên các tiêu chí nghiên cứu SCD-Heft: suy tim mạn tính, NYHA > II và phân suất tống máu thất trái (LVEF) < 35% [39].
8.4. Tránh các hoạt động thể chất chuyên sâu
Trong giai đoạn cấp tính của viêm cơ tim, khuyến cáo ngưng các hoạt động thể chất cường độ cao cho đến viêm cơ tim khỏi hoàn toàn (ít nhất sáu tháng). Các vận động viên nên tạm thời bị loại khỏi hoạt động thể thao chuyên nghiệp bất kể tuổi tác, giới tính, mức độ nghiêm trọng của các triệu chứng hoặc chế độ điều trị [40].
9. Tiên lượng
Viêm cơ tim cấp tự khỏi ở nhiều bệnh nhân và tiên lượng phụ thuộc vào tình trạng suy tim và rối loạn nhịp. Theo nghiên cứu tại Châu Âu, ở bệnh nhân viêm cơ tim, tình trạng sốc tim chiếm 8,6% trường hợp và tỷ lệ tử vong nội viện chiếm 2,7% trường hợp[5]. Khi theo dõi dài hạn và tình trang tử vong hoặc ghép tim sau 30 ngày lần lượt ở 10,4% và 14,7% ở bệnh nhân LVEF <50%, rối loạn nhịp thất kéo dài hoặc hội chứng cung lượng tim thấp [5]. Các nghiên cứu đã chỉ ra rằng tỷ lệ tử vong do viêm cơ tim cấp tính (không gồm thể tối cấp) là khoảng 8-12%[8]. Các yếu tố dự báo tỷ lệ tử vong ở những bệnh nhân này đã được chứng minh là: giảm chức năng thất trái, ngất, rối loạn chức năng thất phải, tăng áp phổi và thời gian phức bộ QRS kéo dài hơn 120ms, giảm độ biến dạng cơ tim trục dọc toàn thể (GLS). Riêng đối với cộng hưởng từ hiện nay cũng áp dụng trong theo dõi và tiên lượng viêm cơ tim. Dựa trên kết quả cộng hưởng từ tim, chức năng co bóp thất trái tốt (LVEF > 55%), không rối loạn vận động vùng và không kèm tổn thương cơ tim ngấm thuốc gadolinium muộn (LGE) sẽ có tiên lượng tốt [41, 42]. Trong một phân tích gộp của tác giả Georgiopoulos và cs trên 11 nghiên cứu và 2328 bệnh nhân cho thấy tổn thương LGE là một yếu tố độc lập trong tiên lượng bệnh nhân viêm cơ tim [43]. Tổn thương LGE làm tăng nguy cơ biến cố loạn nhịp, suy tim và tử vong lên 3.28 lần so với nhóm không có LGE (KTC 95%, 1.69–6.39], p<0.001). Khi phân tích 5 nghiên cứu, ghi nhận các trường hợp tổn thương LGE lan tỏa (gồm > 2 phân vùng/17 phân vùng theo AHA, tỉ lệ LGE > 10% tổng khối cơ thất trái hoặc khối lượng tổn thương LGE > 17gram) làm tăng nguy cơ tử vong và các biến cố tim mạch chính (MACE) lên 1.96 lần so với nhóm còn lại (KTC 95%, 1.08–3.56], P=0.027). Khi đánh giá vị trí tổn thương LGE, các tác giả ghi nhận, nếu LGE ở thành trước sẽ làm tăng nguy cơ biến cố chính lên 2.58 lần (KTC95%, 1.64–4.06], P=0.004) [43].
10. Kết luận
Ngày nay, chẩn đoán chính xác và kịp thời viêm cơ tim vẫn còn nhiều thách thức do nhiều tác nhân gây bệnh từ siêu vi đến độc chất. Tuy nhiên, hiện nay sự phát triển của các phương thức chẩn đoán hình ảnh đưa ra khả năng chẩn đoán sớm, không xâm lấn cũng như theo dõi đầy đủ bệnh lý này. Ở những bệnh nhân ổn định huyết động, cộng hưởng từ là phương tiện giúp xác nhận chẩn đoán, và khuyến khích sử dụng trong thực hành lâm sàng. Ngược lại, sinh thiết mô cơ là tiêu chuẩn vàng trong chẩn đoán tuy nhiên đa phần chỉ định ở thể bệnh tối cấp hoặc đánh giá điều trị. Trong thực hành lâm sàng, cần phân tầng nguy cơ sớm ở bệnh nhân viêm cơ tim và chọn ra nhóm bệnh nhân dễ bị tổn thương nhất để ngăn ngừa các biến chứng giúp theo dõi và điều trị tích cực. Suy giảm chức năng thất trái, xuất hiện rối loạn nhịp thất ác tính kèm theo trụy tuần hoàn là những yếu tố dự báo đáng kể tiên lượng xấu ở bệnh nhân viêm cơ tim.
TÀI LIỆU THAM KHẢO:
- Pesudovs, K., Y.A. Melaku, and G.B.o.D.S.C.J. Lancet, Global, regional, and national incidence, prevalence, and years lived with disability for 301 acute and chronic diseases and injuries in 188 countries, 1990–2013 diseases and injuries in 188 countries, 1990-2013: A systematic analysis for the Global Burden of Disease Study 2013. 2015. 386(9995): p. 743-800.
- Roth, G., et al., NHLBI-JACC Global Burden of Cardiovascular Diseases Writing Group. 2020. 1990. 2019: p. 2982-3021.
- Pahuja, M., et al., Trends in the incidence of in-hospital mortality, cardiogenic shock, and utilization of mechanical circulatory support devices in myocarditis (analysis of national inpatient sample data, 2005–2014). 2019. 25(6): p. 457-467.
- OKADA, R., S. KAWAI, and H.J.J.C.J. KASYUYA, Nonspecific Myocarditis: A Statistical and Clinicopathological Study of Autopsy Cases: SYMPOSIUM ON SEVERAL ASPECTS OF MYOCARDITIS. 1989. 53(1): p. 40-48.
- Ammirati, E., et al., Management of acute myocarditis and chronic inflammatory cardiomyopathy: an expert consensus document. 2020. 13(11): p. e007405.
- Tsukada, B., et al., High prevalence of chronic myocarditis in dilated cardiomyopathy referred for left ventriculoplasty: expression of tenascin C as a possible marker for inflammation. 2009. 40(7): p. 1015-1022.
- Cai, C., et al., A comprehensive analysis of the efficacy and safety of COVID-19 vaccines. 2021. 29(9): p. 2794-2805.
- Caforio, A.L.P., et al., Current state of knowledge on aetiology, diagnosis, management, and therapy of myocarditis: a position statement of the European Society of Cardiology Working Group on Myocardial and Pericardial Diseases. European Heart Journal, 2013. 34(33): p. 2636-2648.
- Basso, C., et al., Classification and histological, immunohistochemical, and molecular diagnosis of inflammatory myocardial disease. 2013. 18: p. 673-681.
- Aretz, H.T.J.H.p., Myocarditis: the Dallas criteria. 1987. 18(6): p. 619-624.
- Leone, O., et al., 2011 consensus statement on endomyocardial biopsy from the Association for European Cardiovascular Pathology and the Society for Cardiovascular Pathology. 2012. 21(4): p. 245-274.
- Lampejo, T., et al., Acute myocarditis: aetiology, diagnosis and management. 2021. 21(5): p. e505.
- Nagai, T., et al., JCS 2023 Guideline on the Diagnosis and Treatment of Myocarditis. 2023. 87(5): p. 674-754.
- Journal, J.J.W.G.J.C., Guidelines for Diagnosis and Treatment of Myocarditis (JCS 2009)–Digest Version–. 2011. 75(3): p. 734-743.
- Adeboye, A., et al., A review of the role of imaging modalities in the evaluation of viral myocarditis with a special focus on COVID-19-related myocarditis. 2022. 12(2): p. 549.
- Lasica, R., et al., Update on Myocarditis: From Etiology and Clinical Picture to Modern Diagnostics and Methods of Treatment. 2023. 13(19): p. 3073.
- Meindl, C., et al., Patients with acute myocarditis and preserved systolic left ventricular function: comparison of global and regional longitudinal strain imaging by echocardiography with quantification of late gadolinium enhancement by CMR. 2021. 110(11): p. 1792-1800.
- Tünnemann-Tarr, A., et al., Speckle tracking echocardiography in a patient with viral myocarditis and acute myocardial infarction. 2020. 22(4): p. 184-191.
- Hsiao, J.-F., et al., Speckle tracking echocardiography in acute myocarditis. 2013. 29: p. 275-284.
- Nensa, F., et al., Feasibility of FDG-PET in myocarditis: comparison to CMR using integrated PET/MRI. 2018. 25: p. 785-794.
- Bami, K., et al., Noninvasive imaging in acute myocarditis. 2016. 31(2): p. 217-223.
- McDonagh, T.A., et al., 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) With the special contribution of the Heart Failure Association (HFA) of the ESC. European Heart Journal, 2021. 42(36): p. 3599-3726.
- Tschöpe, C., et al., Management of myocarditis-related cardiomyopathy in adults. 2019. 124(11): p. 1568-1583.
- Friedrich, M.G., et al., Cardiovascular magnetic resonance in myocarditis: a JACC white paper. 2009. 53(17): p. 1475-1487.
- Ferreira, V.M., et al., Cardiovascular magnetic resonance in nonischemic myocardial inflammation: expert recommendations. 2018. 72(24): p. 3158-3176.
- Lagan, J., M. Schmitt, and C.A.J.T.I.J.o.C.I. Miller, Clinical applications of multi-parametric CMR in myocarditis and systemic inflammatory diseases. 2018. 34: p. 35-54.
- Kotanidis, C.P., et al., Diagnostic accuracy of cardiovascular magnetic resonance in acute myocarditis: a systematic review and meta-analysis. 2018. 11(11): p. 1583-1590.
- Polte, C.L., et al., Cardiovascular magnetic resonance in myocarditis. 2022. 12(2): p. 399.
- Rapezzi, C., et al., Diagnostic work-up in cardiomyopathies: bridging the gap between clinical phenotypes and final diagnosis. A position statement from the ESC Working Group on Myocardial and Pericardial Diseases. 2013. 34(19): p. 1448-1458.
- McDonagh, T.A., et al., 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: Developed by the Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) With the special contribution of the Heart Failure Association (HFA) of the ESC. 2021. 42(36): p. 3599-3726.
- Berg, J., et al., Non-steroidal anti-inflammatory drug use in acute myopericarditis: 12-month clinical follow-up. 2019. 6(1): p. e000990.
- Mirna, M., et al., Treatment with non-steroidal anti-inflammatory drugs (NSAIDs) does not affect outcome in patients with acute myocarditis or myopericarditis. 2022. 9(2): p. 32.
- Maron, B.J., et al., Council on Clinical Cardiology. p. 1807-1816.
- Zeppenfeld, K., et al., 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death: Developed by the task force for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death of the European Society of Cardiology (ESC) Endorsed by the Association for European Paediatric and Congenital Cardiology (AEPC). 2022. 43(40): p. 3997-4126.
- Bang, V., et al., Management of patients with giant cell myocarditis: JACC review topic of the week. 2021. 77(8): p. 1122-1134.
- Wang, D., et al., C. Section of Precision Medicine Group of Chinese Society of, C. Editorial Board of Chinese Journal of, M. Working Group of Adult Fulminant Chinese society of cardiology expert consensus statement on the diagnosis and treatment of adult fulminant myocarditis. 2019. 62(2): p. 187-202.
- Maury, P., et al., Complete atrioventricular block persisting after regression of infectious myocarditis. 2008. 41(6): p. 665-667.
- Pelargonio, G., et al., Long-term arrhythmic risk assessment in biopsy-proven myocarditis. 2020. 6(5): p. 574-582.
- Bardy, G.H.J.N.E.J.M., Sudden Cardiac Death in Heart Failure Trial (SCD-HeFT) Investigators. Amiodarone or an implantable cardioverter-defibrillator for congestive heart failure. 2005. 352: p. 225-237.
- Pelliccia, A., et al., Recommendations for participation in competitive and leisure time sport in athletes with cardiomyopathies, myocarditis, and pericarditis: position statement of the Sport Cardiology Section of the European Association of Preventive Cardiology (EAPC). 2019. 40(1): p. 19-33.
- Grün, S., et al., Long-term follow-up of biopsy-proven viral myocarditis: predictors of mortality and incomplete recovery. 2012. 59(18): p. 1604-1615.
- Schumm, J., et al., Cardiovascular magnetic resonance risk stratification in patients with clinically suspected myocarditis. 2014. 16(1): p. 1-12.
- Georgiopoulos, G., et al., Prognostic impact of late gadolinium enhancement by cardiovascular magnetic resonance in myocarditis: a systematic review and meta-analysis. 2021. 14(1): p. e011492.







