ThS. TRẦN THỊ NGỌC HIẾU
TS. TRẦN VIẾT THẮNG
Khoa Nội tiết BV Đại học Y Dược TPHCM
Mở đầu:
Cường aldosterone nguyên phát (CANP) là bệnh lý do tăng sản xuất aldosterone quá mức từ một hoặc cả hai tuyến thượng thận, là nguyên nhân phổ biến gây tăng huyết áp (THA) thứ phát. So với THA nguyên phát, CANP làm tăng nguy cơ biến chứng tim mạch. Mặc dù CANP là nguyên nhân nội tiết thường gặp nhất gây THA thứ phát và có các phương pháp điều trị đặc hiệu hiệu quả, nhưng hiện nay bệnh vẫn chưa được quan tâm chẩn đoán sớm và điều trị tối ưu trong thực hành lâm sàng. Mới đây Hội Nội tiết Hoa Kỳ vừa đưa ra khuyến cáo về tầm soát và chẩn đoán CANP nhằm cải thiện tỷ lệ chẩn đoán và điều trị đặc hiệu bệnh lý này. Trong bài này, chúng tôi xin lược dịch tóm tắt các khuyến cáo nêu trên.
Phân nhóm và mức độ chứng cứ của khuyến cáo:
Các khuyến cáo này sử dụng hệ thống GRADE (Grading of Recommendations, Assessment, Development, and Evaluation: phân loại mức độ Khuyến cáo, Đánh giá, Xây dựng và Thẩm định bằng chứng) , bao gồm phân loại mức độ mạnh của khuyến cáo và độ tin cậy bằng chứng.
Mức độ mạnh của khuyến cáo (Strength of recommendation) được phân loại là 1 (mạnh) hoặc 2 (có điều kiện). Tất cả các khuyến cáo được tóm tắt dưới đây đều là khuyến cáo có điều kiện (2), nghĩa là các kết quả mong muốn có thể vượt trội hơn hậu quả không mong muốn trong hầu hết các trường hợp, nhưng cần cân nhắc các lựa chọn khác nhau tùy thuộc vào bối cảnh cụ thể, lựa chọn của bệnh nhân..
Độ tin cậy của bằng chứng (Certainty of evidence) được biểu thị bằng các biểu tượng ⊕, với ⊕⊕⊕⊕ là cao, ⊕⊕⊕O là trung bình, ⊕⊕OO là thấp, và ⊕OOO là rất thấp.
KHUYẾN CÁO 1: Nên xét nghiệm (XN) tầm soát CANP ở TẤT CẢ bệnh nhân THA (2 | ⊕⊕OO)
Đây là khuyến cáo có điều kiện. Việc triển khai tầm soát CANP phụ thuộc vào nguồn lực, chuyên môn địa phương và năng lực của hệ thống y tế. Những yếu tố này có thể ảnh hưởng đến tính khả thi và mức độ ưu tiên của việc tầm soát.
Lý do và Lợi ích:
- Mức độ phổ biến bệnh cao: CANP là nguyên nhân nội tiết thường gặp nhất gây THA thứ phát, chiếm 5–14% ở bệnh nhân THA tại phòng khám tuyến cơ sở và 30% tại bệnh viện chuyên sâu.
- Tăng nguy cơ các biến cố bất lợi: So với bệnh nhân THA nguyên phát, bệnh nhân CANP có nguy cơ mắc các biến cố tim mạch cao hơn đáng kể, bao gồm: đột quỵ (odds ratio, OR: 2,58), bệnh động mạch vành (OR: 1,77), rung nhĩ (OR: 3,52) và suy tim (OR: 2,05). Nguy cơ tổn thương thận (biểu hiện qua chỉ số albumin niệu và protein niệu) cũng cao hơn, cùng với giảm chất lượng cuộc sống.
- Mặc dù CANP khá phố biến, tỷ lệ bệnh nhân THA được tầm soát CANP hiện RẤT THẤP, dẫn đến bỏ lỡ chẩn đoán hoặc chẩn đoán muộn (khi bệnh nhân đã gặp các biến cố tim mạch – mạch máu – tổn thương thận). Ngay cả ở bệnh nhân được chẩn đoán CANP, việc điều trị và theo dõi bệnh cũng chưa được tối ưu. Việc này làm tăng đáng kể gánh nặng chi phí y tế liên quan đến THA và các biến chứng của THA.
- Tùy vào chẩn đoán phân loại CANP, bệnh có thể được điều trị bằng phẫu thuật nội soi cắt tuyến thượng thận một bên (đối với CANP do tăng tiết aldosterone một bên tuyến thượng thận) hoặc điều trị nội khoa với thuốc đối kháng thụ thể mineralocorticoid (MRA) (đối với CANP do tăng tiết aldosterone ở cả hai tuyến thượng thận). Các phương pháp này được chứng minh giúp kiểm soát hiệu quả huyết áp, điều chỉnh hạ kali máu và giảm nguy cơ tim mạch. Tầm soát sớm CANP đã được chứng minh hiệu quả về chi phí trong các nghiên cứu tại Nhật Bản, Trung Quốc và Úc.
- XN tầm soát ít gây rủi ro. Tầm soát CANP có thể thực hiện bằng XN máu và biện luận kết quả mà không nhất thiết ngưng thuốc hạ áp hoặc chỉ ngưng ở mức tối thiểu (Hình 1). Ngay cả khi nếu kết quả dương tính giả, điều trị bằng MRA vẫn có lợi cho bệnh nhân THA có nồng độ renin thấp.
KHUYẾN CÁO 2: Ở bệnh nhân THA và CANP, nên sử dụng các biện pháp điều trị đặc hiệu cho CANP (nội khoa hoặc phẫu thuật) (2 | ⊕⊕OO)
Lý do và Lợi ích:
- CANP là nguyên nhân nội tiết phổ biến nhất gây THA thứ phát và làm tăng nguy cơ biến chứng tim mạch đáng kể so với THA nguyên phát. Nguy cơ đột quỵ, bệnh động mạch vành, rung nhĩ và suy tim đều tăng cao ở bệnh nhân CANP không được điều trị đặc hiệu.
- Điều trị đặc hiệu (nội khoa hoặc phẫu thuật) giúp kiểm soát huyết áp đáng kể và giảm các biến cố tim mạch, mạch máu não và thận liên quan đến CANP.
- Phẫu thuật cắt một bên tuyến thượng thận khi xác định nguồn tăng tiết một bên có thể chữa khỏi CANP hoàn toàn (xem khuyến cáo 6 về việc phân loại CANP và xác định nguồn tăng tiết).
- Với bệnh nhân CANP do tăng tiết hai bên, không thể hay không mong muốn phẫu thuật, điều trị bằng MRA (spironolactone, eplerenone) là lựa chọn ưu tiên.
KHUYẾN CÁO 3: TẤT CẢ bệnh nhân THA nên được tầm soát CANP bằng cách đo nồng độ aldosterone trong huyết thanh/huyết tương và renin trong huyết tương (nồng độ hoặc hoạt tính) (2 | ⊕⊕OO)
Kỹ thuật tầm soát:
- XN nên thực hiện vào buổi sáng khi bệnh nhân ở tư thế ngồi.
- Không cần hạn chế muối trong chế độ ăn trước ngày thực hiện XN.
- XN kali đồng thời với renin và aldosterone để hỗ trợ biện luận kết quả XN, vì nồng độ kali thấp có thể gây nồng độ aldosterone thấp giả.
Lý do và Lợi ích:
- XN aldosterone, renin và lập tỷ số aldosterone:renin (ARR), có độ nhạy cao trong tầm soát CANP, kể cả khi kali máu bình thường hay thấp.
- Tầm soát CANP trên tất cả bệnh nhân THA giúp phát hiện sớm CANP, điều trị bệnh kịp thời và giảm nguy cơ tim mạch.
Thách thức và Lưu ý:
- XN aldosterone và renin có thể bị ảnh hưởng bởi thuốc (ví dụ: thuốc chẹn beta giao cảm, thuốc lợi tiểu), chế độ ăn muối và điều kiện lấy mẫu, gây dương tính giả hoặc âm tính giả.
- Kết quả dương tính giả có thể dẫn đến việc thực hiện các XN chuyên sâu hơn không cần thiết. Tuy nhiên ngay cả trong trường hợp dương tính giả, điều trị bằng MRA trên bệnh nhân THA có renin thấp vẫn có lợi.
- Kết quả âm tính giả có thể gặp trong CANP thể nhẹ hoặc do sự dao động nồng độ aldosterone.
- Ngưng các loại thuốc có thể gây nhiễu kết quả trước khi XN có thể không an toàn hoặc không khả thi cho tất cả bệnh nhân. Khuyến cáo khuyến khích tầm soát với việc ngừng thuốc hạ áp tối thiểu hoặc không cần ngừng thuốc hạ áp giúp tăng tính khả thi của tầm soát.
- Cần tầm soát lại nếu bệnh nhân có THA nặng hơn hoặc THA kháng trị không rõ nguyên nhân, hạ kali máu mới phát hiện hoặc rung nhĩ không rõ nguyên nhân.

Hình 1: Tầm soát CANP ở bệnh nhân THA.
Với những bệnh nhân có kết quả tầm soát gợi ý CANP, các bước tiếp theo được thể hiện chi tiết trong hình 2. XN: xét nghiệm; UCMC/UCTT: ức chế men chuyển/ ức chế thụ thể; PP: phương pháp; DRC: direct renin concentration, nồng độ renin huyết tương; PRA: plama renin activity, hoạt tính renin huyết tương. * XN máu cần thực hiện vào buổi sáng ở tư thế ngồi; tránh tình trạng ứ máu tĩnh mạch (tháo garô sau khi đâm kim vào tĩnh mạch và đợi ít nhất 5 giây trước khi lấy máu) nhằm tránh tăng kali máu giả. ** Các giá trị aldosterone, renin và ARR trong Hình 1 và Bảng 1 có tính chất tham khảo. *** Cân nhắc khả năng dương tính giả do sử dụng thuốc chẹn beta giao cảm khi aldosterone <15 ng/dL (<415 pmol/L) bằng PP miễn dịch. # Drospirenone trong các thuốc tránh thai uống là một thuốc kháng thụ thể mineralocorticoid. ## Amiloride và Triamterene là các thuốc ức chế kênh natri biểu mô (ENaC).
Bảng 1: Tầm soát CANP – Các ngưỡng giá trị ARR theo phương pháp XN aldosterone và renin, cùng các đơn vị đo lường tương ứng.
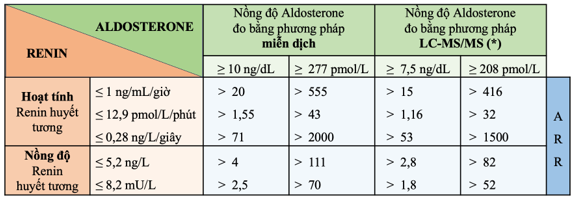
ARR: Aldosterone-Renin Ratio, tỷ số aldosterone-renin; LC-MS/MS: liquid chromatography–tandem mass spectrometry, sắc ký lỏng ghép khối phổ kép. Hiện tại ở Việt Nam chỉ đo được nồng độ renin huyết tương và nồng độ aldosterone đo bằng phương pháp miễn dịch. Lưu ý đơn vị sử dụng để chọn điểm cắt ARR tương ứng. Các giá trị aldosterone, renin và ARR có tính chất tham khảo. Độ nhạy và độ đặc hiệu của XN tầm soát phụ thuộc vào ngưỡng giá trị lựa chọn (không có ngưỡng tối ưu, vì mỗi ngưỡng lựa chọn đi kèm sự đánh đổi giữa tỷ lệ dương tính giả và âm tính giả). Nồng độ aldosterone và renin cũng bị ảnh hưởng bởi sự dao động cá nhân, phương pháp XN tại phòng XN địa phương và nhiều yếu tố khác. Kết quả cần được diễn giải dựa trên xác suất mắc CANP trước XN, các thuốc hoặc các tình trạng bệnh lý có thể gây nhiễu kết quả.
KHUYẾN CÁO 4: Đối với bệnh nhân có kết quả tầm soát CANP dương tính, thực hiện nghiệm pháp ức chế (NPUC) aldosterone trong các tình huống mà dự đoán khả năng CANP tăng tiết MỘT BÊN ở mức trung bình và bệnh nhân mong muốn phẫu thuật (2 | ⊕OOO)
Lý do và Lợi ích:
- Một số nghiên cứu cho thấy kết quả NPUC aldosterone có thể dự đoán khả năng CANP tăng tiết một bên (khả năng ức chế aldosterone càng kém thì khả năng CANP càng cao), giúp tối ưu hóa việc sử dụng các XN chẩn đoán hình ảnh tốn kém và xâm lấn hơn như AVS (adrenal vein sampling: lấy máu tĩnh mạch thượng thận) hay điều trị nội khoa.
- Nếu kết quả NPUC aldosterone cho thấy không có CANP (âm tính), điều trị bằng thuốc MRA vẫn có hiệu quả đối với bệnh nhân có THA với renin thấp.
Thách thức và Lưu ý:
- Nhiều nghiên cứu cho thấy các NPUC aldosterone trong việc xác nhận CANP có kết quả âm tính giả nhiều hơn dương tính giả. Nguy cơ âm tính giả cũng có thể xảy ra ở bệnh nhân có đặc điểm CANP rõ (ví dụ: THA kháng trị, hạ kali máu), dẫn đến việc bỏ lỡ chẩn đoán chính xác.
- Hiện có nhiều NPUC aldosterone với phương pháp thực hiện và giá trị ngưỡng cắt để biện luận kết quả khác nhau, dẫn đến thiếu chuẩn hóa và khó khăn trong việc giải thích kết quả.
Các tình huống KHÔNG cần NPUC aldosterone:
- Bệnh nhân THA kháng trị hoặc THA kèm hạ kali máu với bằng chứng sinh hóa rõ ràng của tăng tiết aldosterone không phụ thuộc renin (renin rất thấp và aldosterone rất cao), vì nguy cơ âm tính giả cao hơn nguy cơ dương tính giả.
- Bệnh nhân không muốn hoặc không thể thực hiện AVS hoặc/và phẫu thuật có thể điều trị bằng MRA dựa trên kết quả tầm soát, không cần NPUC.
- Bệnh nhân có tiền sử gia đình đột biến di truyền liên quan đến tăng aldosterone gia đình.
- Khả năng CANP do tăng tiết một bên thấp (kali máu bình thường, aldosterone thấp).
KHUYẾN CÁO 5: Đối với bệnh nhân CANP, lựa chọn điều trị nội khoa đặc hiệu hoặc phẫu thuật, tùy thuộc vào CANP là do tăng tiết hai bên hay một bên và khả năng bệnh nhân có thể phẫu thuật được hay không (2 | ⊕OOO)
Lý do và Lợi ích:
- Phẫu thuật cắt tuyến thượng thận một bên được chỉ định khi xác định chính xác CANP do tăng tiết một bên và bệnh nhân lựa chọn phẫu thuật có thể chữa khỏi (hoặc cải thiện) THA.
- Điều trị nội khoa suốt đời với MRA đối với CANP do tăng tiết hai bên, hoặc không rõ tăng tiết một bên hay hai bên, hoặc bệnh nhân không thể phẫu thuật hay từ chối phẫu thuật.
- Các nghiên cứu quan sát cho thấy phẫu thuật có hiệu quả lâu dài tốt hơn trong việc kiểm soát huyết áp và giảm số lượng/liều lượng thuốc hạ áp so với điều trị nội khoa. Phẫu thuật giúp làm giảm nguy cơ đột quỵ, các biến cố tim mạch lớn, suy tim và tử vong do mọi nguyên nhân so với điều trị nội khoa.
Thách thức và Lưu ý:
- Lưu ý một số tác dụng phụ có thể gặp với điều trị nội khoa (xem khuyến cáo 9).
- Điều trị nội khoa dù chi phí ban đầu thấp hơn nhưng có thể tốn kém hơn về lâu dài so với phẫu thuật ở bệnh nhân có thời gian sống còn lại lâu.
- Việc lựa chọn điều trị nên dựa trên đánh giá về khả năng phẫu thuật, mức độ bệnh và lựa chọn của bệnh nhân.
- Bệnh nhân CANP nhẹ hoặc có nhiều bệnh nền có thể điều trị nội khoa đặc hiệu mà không cần AVS.
KHUYẾN CÁO 6: Đối với bệnh nhân CANP đang cân nhắc phẫu thuật, khuyến cáo đánh giá vị trí tăng tiết bằng cả chụp cắt lớp vi tính (CT) và lấy máu tĩnh mạch thượng thận (AVS) trước khi quyết định phương pháp điều trị (nội khoa hoặc phẫu thuật). (2 | ⊕⊕OO)
Lý do và Lợi ích:
- CT/MRI có vai trò hạn chế trong đánh giá chức năng của tuyến thượng thận, gây chẩn đoán sai lệch vị trí tăng tiết của CANP (tăng tiết một bên hoặc hai bên) đến 38% trường hợp. Các khối u nhỏ có thể không nhìn thấy trên CT, và các khối u lớn có thể không có chức năng.
- AVS là tiêu chuẩn vàng để phân biệt chính xác CANP do tăng tiết một bên hay hai bên, là yếu tố quan trọng để quyết định có nên phẫu thuật cắt bỏ một bên tuyến thượng thận hay không.
- Lựa chọn phẫu thuật dựa trên kết quả AVS giúp tăng tỷ lệ chữa khỏi bệnh với bệnh nhân CANP một bên (đánh giá dựa vào XN sinh hóa sau phẫu thuật) cao hơn so với dựa trên kết quả CT.
Thách thức và Lưu ý:
- AVS là thủ thuật xâm lấn, cần các bác sĩ chẩn đoán hình ảnh can thiệp có chuyên môn cao, điều này hạn chế việc áp dụng thủ thuật, đặc biệt ở trung tâm không chuyên sâu hoặc thiếu nguồn lực.
- AVS là thủ thuật an toàn nhưng có thể gặp biến chứng hiếm (rách tĩnh mạch thượng thận: 0,61%).
- Chi phí AVS cao hơn nhiều so với CT.
Các trường hợp KHÔNG CẦN thực hiện AVS:
- Bệnh nhân < 35 tuổi có CANP rõ rệt (hạ kali máu, aldosterone rất cao và renin bị ức chế) và CT có u tuyến thượng thận một bên >1cm với đặc điểm phù hợp với u vỏ tuyến thượng thận.
- Bệnh nhân có u tuyến thượng thận một bên lớn (>1cm) có đồng tiết cả aldosterone và cortisol rõ trên lâm sàng. Trong trường hợp này nguồn tiết cortisol rõ trên lâm sàng là từ u thượng thận một bên và không cần thực hiện AVS.
- Bệnh nhân CANP có tính gia đình (loại I-IV) vì đây là các rối loạn hai bên và không cần AVS.
- Bệnh nhân có tăng sản vỏ thượng thận đa nốt hai bên nguyên phát (PBMAH) tiết cả cortisol và aldosterone quá mức, vì cả hai tuyến thượng thận đều tăng tiết nên không cần AVS.
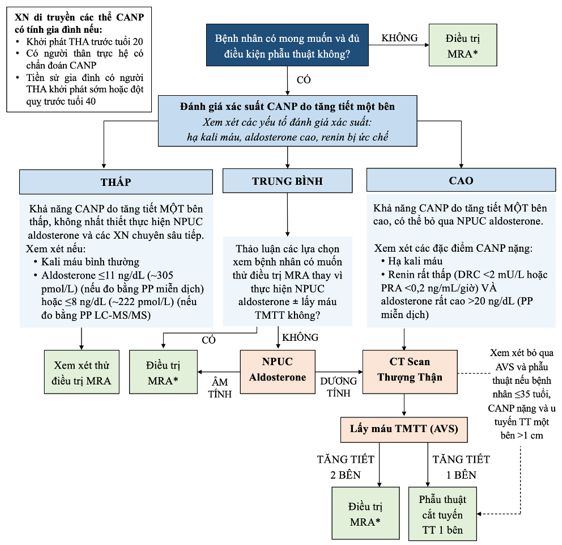
Hình 2: Sơ đồ xử trí bệnh nhân THA có khả năng CANP.
XN: xét nghiệm; PP: phương pháp; DRC: direct renin concentration, nồng độ renin huyết tương; PRA: plama renin activity, hoạt tính renin huyết tương; NPUC: nghiệm pháp ức chế; AVS: adrenal vein sampling, lấy máu tĩnh mạch thượng thận; TMTT: tĩnh mạch thượng thận.
Bảng 2. Các chỉ số quan trọng và ngưỡng giá trị trong giải thích kết quả lấy máu tĩnh mạch thượng thận.
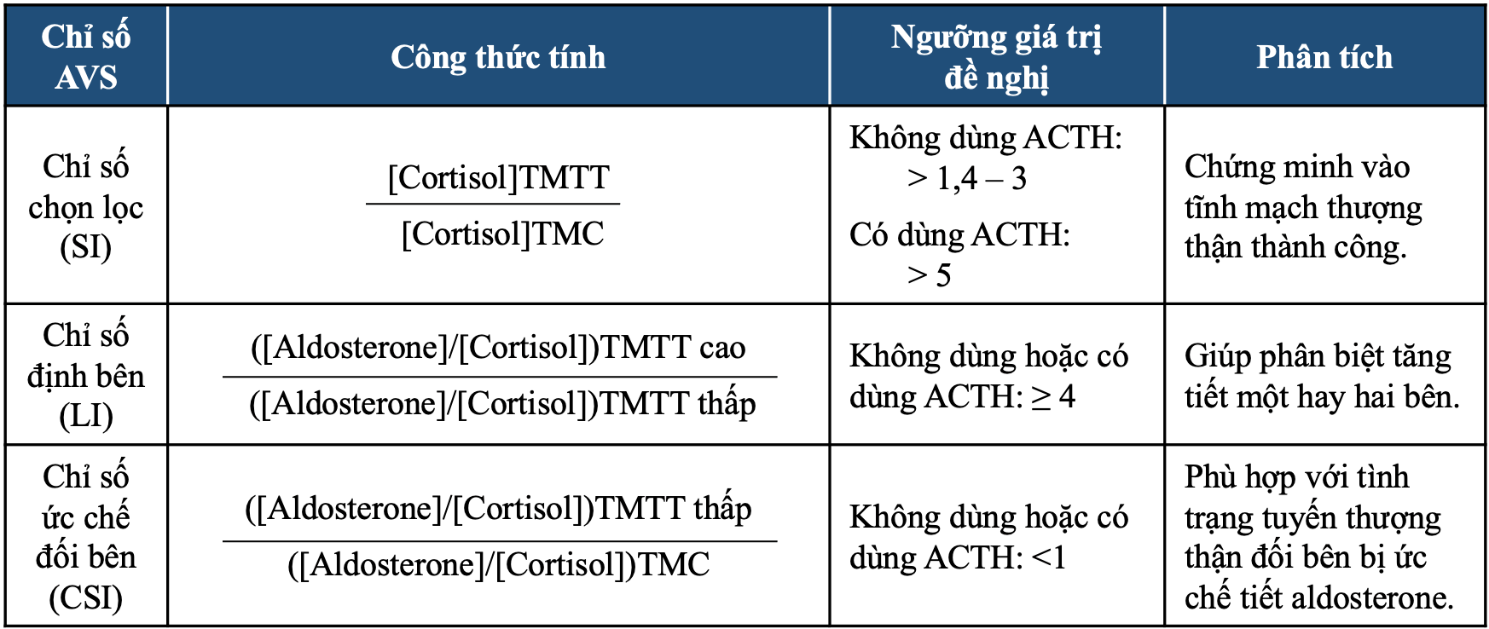
AVS: adrenal vein sampling, lấy máu tĩnh mạch thượng thận; TMTT: tĩnh mạch thượng thận; TMC: tĩnh mạch chủ; SI: selectivity index, chỉ số chọn lọc; LI: lateralization index, chỉ số định bên; CSI: contralateral suppression index; chỉ số ức chế đối bên; ACTH: adrenocorticotropic hormone, thường là Synacthen là thuốc dùng để kích thích sản xuất hormone tuyến thượng thận trong quá trình AVS.
KHUYẾN CÁO 7: Ở bệnh nhân CANP đang điều trị nội khoa đặc hiệu nhưng huyết áp chưa được kiểm soát và renin còn bị ức chế, khuyến cáo tăng liều thuốc điều trị đặc hiệu để làm tăng renin (2 | ⊕OOO).
Lý do và Lợi ích:
- CANP được chẩn đoán dựa trên tăng tiết aldosterone mặc dù renin bị ức chế. Do đó, điều trị nội khoa đặc hiệu làm tăng renin giúp đảo ngược cơ chế bệnh sinh của CANP.
- Các nghiên cứu quan sát cho thấy nồng độ renin bị ức chế liên tục trong quá trình điều trị có liên quan đến tăng nguy cơ tử vong, đột quỵ, rung nhĩ và hạ kali máu.
- Điều trị đặc hiệu với MRA nhằm làm tăng renin đã được chứng minh là có thể giảm các biến cố tim mạch và thận.
- Theo dõi renin có thể giúp điều chỉnh liều MRA và giảm liều thuốc hạ áp không phải MRA.
Thách thức và Lưu ý:
- Không có ngưỡng renin mục tiêu cụ thể nào được quy định, chỉ khuyến cáo điều trị làm tăng renin so với mức ban đầu trước điều trị.
- Theo dõi nồng độ renin làm tăng chi phí điều trị và có thể là yếu tố hạn chế ở một số nơi.
- Tăng liều MRA để đạt được mục tiêu tăng renin có thể gây ra nhiều tác dụng phụ hơn.
- Nồng độ renin có thể bị ảnh hưởng bởi các loại thuốc đồng thời khác (ví dụ: thuốc chẹn beta giao cảm làm giảm renin, thuốc ức chế RAAS làm tăng renin).
- Mục tiêu lâm sàng là kiểm soát huyết áp với số lượng thuốc ít nhất và kali máu bình thường.
- Ở bệnh nhân có bệnh thận mạn giai đoạn 3 trở lên, việc tăng renin có thể khó khăn và mục tiêu này có thể không khả thi do giảm sản xuất renin và nguy cơ tăng kali máu.
Hình 3: Khởi trị và theo dõi điều trị bằng thuốc kháng thụ thể mineralocorticoid (MRA).
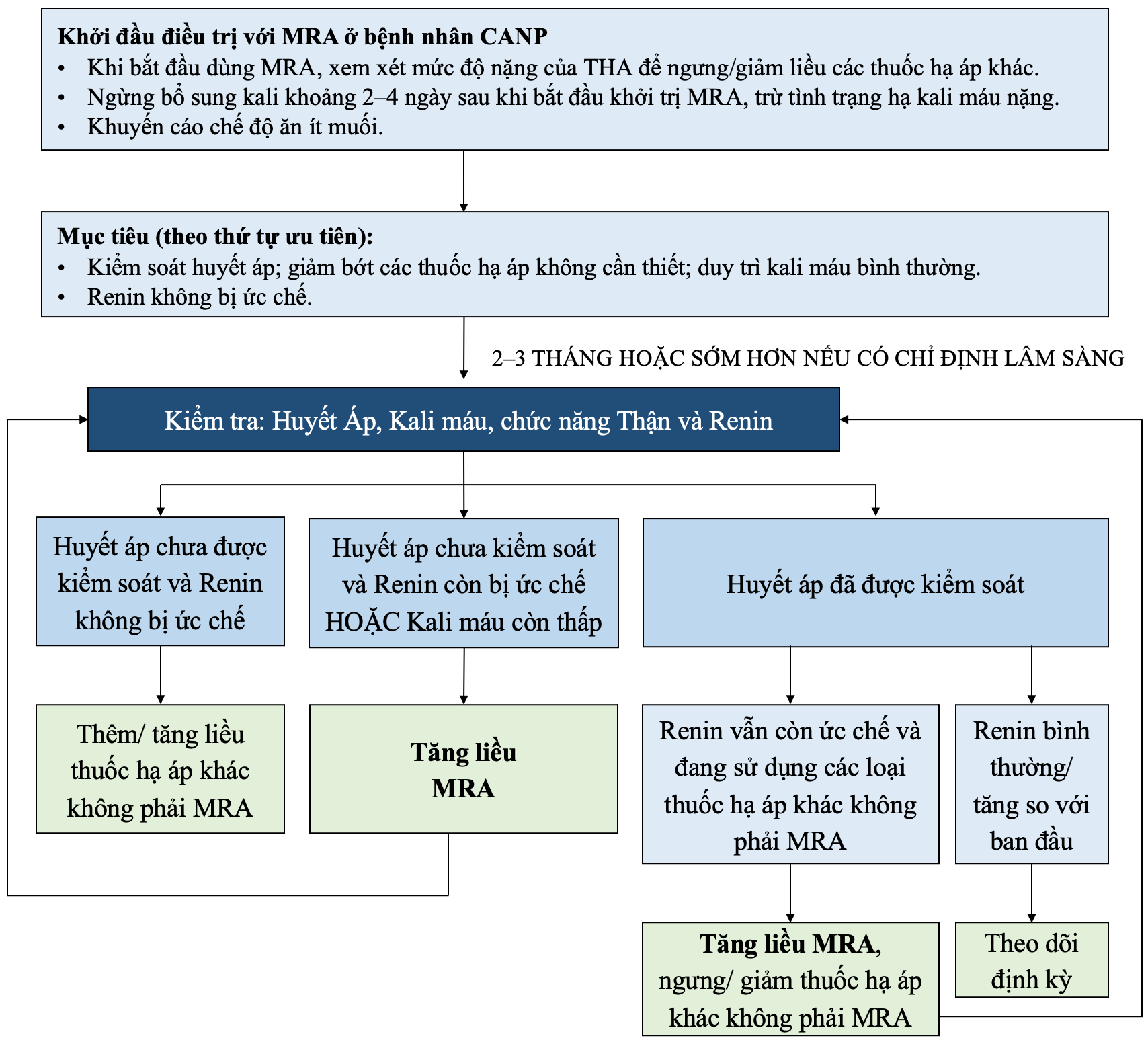
Đây là hướng dẫn chung, đáp ứng với MRA ở các bệnh nhân có thể rất khác. Quá trình khởi trị và chỉnh liều MRA gồm nhiều bước; mỗi lần chỉnh liều MRA đều đánh giá lại huyết áp và đáp ứng sinh hóa rồi tiếp tục theo phác đồ điều trị. Mục tiêu điều trị (theo thứ tự ưu tiên): (1) kiểm soát huyết áp, (2) kali bình thường. XN renin giúp đánh giá mức độ phong tỏa thụ thể mineralocorticoid, từ đó điều chỉnh liều MRA nhằm đạt các mục tiêu và ngưng/ giảm các thuốc hạ áp khác không phải MRA.
1. Khởi đầu điều trị với MRA: bắt đầu bằng liều thấp: Spironolactone 12,5–25 mg/ngày hay Eplerenone 25 mg/ngày (có thể chia 2 lần/ngày).
– Bệnh nhân già yếu, nhiều bệnh lý phối hợp, hoặc có tương tác thuốc (như đang dùng thuốc UCMC/UCTT) cần theo dõi sát.
– Bệnh nhân CANP nặng, đặc biệt khi có hạ kali máu nặng, có thể khởi đầu liều cao hơn: spironolactone 50 mg/ngày hay eplerenone 50 mg x 2 lần/ngày.
2. Theo dõi sau khi bắt đầu MRA
– Kiểm tra định kỳ điện giải đồ, chức năng thận, renin sau 2–3 tháng điều trị bằng MRA, cần theo dõi thường xuyên hơn nếu có hạ kali máu nặng hoặc suy giảm chức năng thận.
– Hỏi kỹ bệnh nhân về chế độ ăn muối hoặc đo natri niệu 24 giờ lúc ban đầu và định kỳ sau đó nhằm theo dõi chế độ ăn hạn chế muối. Khuyến cáo lượng natri <85,5 mmol/ngày (tương đương <5g muối/ngày).
3. Điều chỉnh liều MRA
– Chỉnh liều MRA để kiểm soát huyết áp thường thực hiện mỗi 8–12 tuần. Hiệu quả tối đa của thuốc có thể cần tới 3 tháng ở những trường hợp CANP nặng.
– Liều thuốc thường dùng để “khôi phục tình trạng ức chế renin” có thể thay đổi đáng kể, và thường cao hơn so với liều MRA trong điều trị THA kháng trị thông thường. Hầu hết bệnh nhân có renin không còn bị ức chế với liều spironolactone (hoặc tương đương) từ 50–100 mg/ngày.
– Spironolactone có thể tăng mỗi lần 25–50 mg/ngày; eplerenone tăng mỗi lần 25–100 mg/ngày.
– Sau mỗi lần điều chỉnh liều MRA, cần kiểm tra lại điện giải, chức năng thận, renin sau 2–3 tháng. Cân nhắc giảm liều hoặc ngưng các thuốc hạ áp khác không phải MRA nếu được.
– Khi renin không còn bị ức chế nhưng huyết áp chưa kiểm soát, nên cân nhắc thêm hoặc tăng liều các thuốc hạ áp khác không phải MRA. Nếu huyết áp đã kiểm soát tốt chỉ với MRA đơn trị, không đủ bằng chứng để khuyến cáo tiếp tục tăng liều MRA nếu chỉ dựa trên mức renin thấp.
4. Theo dõi và điều chỉnh kali máu
– Kali máu thường trở về bình thường trong vòng 3–5 ngày đầu điều trị, ngay cả khi dùng liều thấp MRA. Có thể ngưng hoặc giảm liều bổ sung kali vào ngày thứ 2–4 sau khi bắt đầu MRA, ngoại trừ các trường hợp hạ kali máu rất nặng.
– Bệnh nhân cần được hướng dẫn giảm lượng muối ăn vào. Chế độ ăn nhiều muối là nguyên nhân phổ biến gây đáp ứng kém với điều trị MRA.
5. Theo dõi mức lọc cầu thận (GFR)
– GFR có thể giảm khi bắt đầu điều trị hoặc khi tăng liều MRA. Tình trạng này có thể diễn ra trong vài ngày tới vài tuần đầu tiên và phần lớn là do hiệu quả điều trị, không phải là tác dụng phụ.
– Theo diễn tiến tự nhiên, GFR giảm do điều trị thích hợp sẽ ổn định và có tác dụng bảo vệ thận. Nếu chức năng thận tiếp tục giảm, cần hội chẩn chuyên khoa thận và cân nhắc ngưng thuốc UCMC/UCTT.
6. Theo dõi tác dụng phụ vú to ở nam giới
– Vú to nam giới do spironolactone có liên quan đến liều, có thể xuất hiện sớm từ 1–2 tháng nhưng thường gặp hơn sau ≥ 6 tháng điều trị.
– Một số trường hợp (đặc biệt nam giới trẻ), giảm liều spironolactone xuống ≤50 mg/ngày có thể cải thiện tình trạng vú to. Nếu tình trạng không cải thiện, có thể đổi sang các MRA chọn lọc hơn (như eplerenone hoặc các MRA thế hệ mới khác); amiloride là một lựa chọn thay thế .
7. Theo dõi định kỳ dài hạn sau khi tối ưu liều MRA
– Bao gồm kiểm soát huyết áp và XN kali máu, chức năng thận hàng năm.
– Bệnh nhân có bệnh thận mạn tính hoặc nguy cơ cao rối loạn điện giải/suy thận (như đang dùng phối hợp MRA với thuốc UCMC/UCTT) cần được theo dõi XN thường xuyên hơn.
– Không cần XN renin thường xuyên trừ khi cần điều chỉnh lại liều MRA do huyết áp hoặc kali máu chưa được kiểm soát hoàn toàn.
KHUYẾN CÁO 8: Nên thực hiện nghiệm pháp ức chế dexamethasone qua đêm 1 mg ở bệnh nhân CANP và có adenoma tuyến thượng thận. (2 | ⊕OOO)
Cách thực hiện nghiệm pháp ức chế dexamethasone qua đêm 1mg
- Uống 1 mg dexamethasone vào lúc 23:00 – 24:00.
- Đo nồng độ cortisol huyết thanh vào lúc 08:00 – 09:00 sáng hôm sau.
- Nồng độ cortisol huyết thanh >1,8 μg/dL (50 nmol/L) gợi ý có tăng tiết cortisol tự chủ.
Lý do và Lợi ích:
- Tăng tiết cortisol tự chủ mức độ nhẹ (MACS) gặp ở 5-27% bệnh nhân CANP có u tuyến thượng thận.
- Đồng tiết cortisol có thể gây ra các biến chứng tim mạch – chuyển hóa – thận nghiêm trọng hơn: tăng nguy cơ đột quỵ, bệnh động mạch vành, rung nhĩ, suy tim, bệnh thận, đái tháo đường, loãng xương và giảm chất lượng cuộc sống.
- Đồng tiết cortisol có thể ảnh hưởng kết quả AVS, dẫn đến chẩn đoán sai vị trí tiết aldosterone.
- Bệnh nhân CANP có đồng tiết cortisol tự chủ có thể bị suy thượng thận sau phẫu thuật cắt tuyến thượng thận một bên.
- Nghiệm pháp ức chế dexamethasone là XN đơn giản, chi phí thấp và được chấp nhận rộng rãi.
Thách thức và Lưu ý:
- Kết quả dương tính giả có thể gặp do sử dụng thuốc, béo phì, trầm cảm nặng hoặc sử dụng estrogen uống, dẫn đến việc thực hiện các XN chuyên sâu hơn không cần thiết để chẩn đoán hội chứng Cushing, dù các XN tiếp theo không xâm lấn và tương đối dễ thực hiện.
KHUYẾN CÁO 9: Đối với các bệnh nhân CANP đang điều trị nội khoa đặc hiệu, khuyến cáo sử dụng spironolactone hơn các thuốc đối kháng thụ thể mineralocorticoid (MRA) khác do chi phí thấp và sự sẵn có rộng rãi. (2 | ⊕OOO)
Lý do và Lợi ích:
- Spironolactone là MRA có chi phí thấp và phổ biến, nên được ưu tiên cho hầu hết bệnh nhân.
- Dù nghiên cứu trực tiếp so sánh spironolactone với các MRA khác không nhiều, nhưng trong điều trị CANP, tất cả MRA khi được chỉnh liều tương đương có hiệu quả như nhau.
- Spironolactone hiệu quả trong việc kiểm soát huyết áp và điều chỉnh hạ kali máu.
Thách thức và Lưu ý:
- Spironolactone có tác dụng phụ liên quan đến tác động lên các thụ thể androgen/ progesterone (vú to nam giới, rối loạn chức năng tình dục ở nam giới và rối loạn kinh nguyệt ở nữ giới), có thể ảnh hưởng tuân thủ điều trị.
- Các MRA mới hơn như eplerenone và finerenone có tính chọn lọc cao hơn với thụ thể mineralocorticoid và ít tác dụng phụ liên quan đến androgen/ progesterone, có thể được ưu tiên trong một số trường hợp, đặc biệt nếu spironolactone không được dung nạp. Tuy nhiên chúng có chi phí cao hơn.
- Chọn MRA nên cân bằng giữa hiệu quả, tác dụng phụ, chi phí và lựa chọn của bệnh nhân.
- Cần theo dõi kali, chức năng thận, renin và đáp ứng huyết áp để điều chỉnh liều MRA.
- Bệnh nhân CANP nặng hoặc có hạ kali máu nặng có thể cần liều khởi đầu cao hơn.
- Chế độ ăn hạn chế muối giúp tăng đáp ứng với điều trị MRA.
TÀI LIỆU THAM KHẢO
Gail K Adler, Michael Stowasser, Ricardo R Correa, Nadia Khan, Gregory Kline, Michael J McGowan, Paolo Mulatero, M Hassan Murad, Rhian M Touyz, Anand Vaidya, Tracy A Williams, Jun Yang, William F Young, Maria-Christina Zennaro, Juan P Brito, Primary Aldosteronism: An Endocrine Society Clinical Practice Guideline, The Journal of Clinical Endocrinology & Metabolism, 2025; https://doi.org/10.1210/clinem/dgaf284.







