BỆNH THẬN ĐÁI THÁO ĐƯỜNG: DIỄN TIẾN TỰ NHIÊN VÀ DỰ HẬU
Bệnh thận đái tháo đường (diabetic nephropathy) xảy ra ở 20-40% bệnh nhân đái tháo đường (ĐTĐ) 1. Bài xuất albumin trong nước tiểu dai dẳng ở mức 30-299 mg/mg creatinin hoặc 30-299 mg/24 giờ
TS Hồ Huỳnh Quang Trí
Viện Tim TP HCM
BỆNH THẬN ĐÁI THÁO ĐƯỜNG: DIỄN TIẾN TỰ NHIÊN VÀ DỰ HẬU
Bệnh thận đái tháo đường (diabetic nephropathy) xảy ra ở 20-40% bệnh nhân đái tháo đường (ĐTĐ) 1. Bài xuất albumin trong nước tiểu dai dẳng ở mức 30-299 mg/mg creatinin hoặc 30-299 mg/24 giờ (albumin niệu vi lượng) là giai đoạn sớm nhất của bệnh thận trong ĐTĐ týp 1 và là một chỉ điểm của bệnh thận trong ĐTĐ týp 2. Nếu không được điều trị, 80-100% bệnh nhân ĐTĐ týp 1 và 20-40% bệnh nhân ĐTĐ týp 2 có albumin niệu vi lượng sẽ tiến triển đến đạm niệu lâm sàng (albumin trong nước tiểu > 300 mg/mg creatinin hoặc > 300 mg/24 giờ). Một khi đã có đạm niệu lâm sàng, mức lọc cầu thận sẽ giảm nhanh, khoảng 10-12 ml/phút mỗi năm 1. Hiện nay bệnh thận ĐTĐ là nguyên nhân hàng đầu của bệnh thận giai đoạn cuối (phải chạy thận nhân tạo, thẩm phân phúc mạc dài hạn hoặc ghép thận) ở nhiều quốc gia 1-3. So với người bệnh thận mạn giai đoạn cuối không do ĐTĐ, người bệnh thận mạn giai đoạn cuối do ĐTĐ tiêu thụ nhiều nguồn lực về chăm sóc y tế hơn và có dự hậu xấu hơn một cách đáng kể 3. Hiện nay các chuyên gia đều thống nhất xem việc ngăn chặn tiến triển của tổn thương thận là một trong những mục tiêu chính khi điều trị bệnh nhân ĐTĐ 1.
ẢNH HƯỞNG CỦA LIỆU PHÁP HẠ HUYẾT ÁP TRÊN CHỨC NĂNG THẬN CỦA NGƯỜI BỆNH THẬN MẠN
Trong bệnh thận ĐTĐ (và cả trong bệnh thận không do ĐTĐ), tăng huyết áp là một yếu tố thúc đẩy tổn thương thận tiến triển nhanh hơn. Nghiên cứu MDRD (Modification of Diet in Renal Disease) trên những người bệnh thận do nhiều nguyên nhân khác nhau cho thấy những bệnh nhân có huyết áp được kiểm soát tích cực có mức lọc cầu thận giảm chậm hơn so với những bệnh nhân có huyết áp được giữ ở mức thông thường 4. Khi tổng hợp số liệu của 9 thử nghiệm lam sàng đánh giá ảnh hưởng của điều trị hạ huyết áp trên chức năng thận, Bakris và cộng sự nhận thấy những người bệnh thận mạn có huyết áp không được kiểm soát (> 140/90 mm Hg) có mức giảm độ lọc cầu thận hơn 12 ml/phút/năm, ngược lại những người bệnh thận mạn có huyết áp được kiểm soát dưới 130/85 mm Hg có mức giảm độ lọc cầu thận chỉ khoảng 2 ml/phút/năm (tương đương với mức giảm sinh lý) 5.
Khi khởi trị người bệnh thận mạn có tăng huyết áp bằng thuốc hạ huyết áp, có thể gặp hiện tượng giảm độ lọc cầu thận trong thời gian đầu. Để hiểu điều này chúng ta cần nhớ lại cơ chế tự điều hòa ở thận (renal autoregulation). Bình thường ở thận có sự tự điều hòa giữ cho tưới máu thận và áp lực trong cầu thận ổn định khi huyết áp trung bình thay đổi trong một khoảng khá rộng từ 80 đến 160 mm Hg. Cơ chế thứ nhất của sự tự điều hòa là phản xạ vận mạch của tiểu động mạch đến (afferent arteriole): Khi huyết áp trung bình giảm, tiểu động mạch đến dãn ra, ngược lại khi huyết áp trung bình tăng, tiểu động mạch đến co lại 6. Cơ chế thứ 2 của tự điều hòa là hiện tượng phản hồi ống thận – cầu thận (tubuloglomerular feedback), tức là thay đổi trương lực của tiểu động mạch đến đáp ứng với nồng độ NaCl ở ống thận xa 6. Ngoài ra, sự co tiểu động mạch đi (efferent arteriole) qua trung gian angiotensin II cũng góp phần duy trì áp lực trong cầu thận khi áp lực tưới máu thận giảm. Ở bệnh nhân tăng huyết áp mạn, do có rối loạn chức năng nội mô và biến đổi cấu trúc các tiểu động mạch thận, áp lực trong cầu thận bắt đầu giảm ở một mức cao hơn 80 mm Hg và bắt đầu tăng ở một mức cao hơn 160 mm Hg. Nếu biểu diễn sự thay đổi áp lực trong cầu thận theo thay đổi của huyết áp trung bình trên một biểu đồ, ta có thể thấy ở người tăng huyết áp mạn có hiện tượng đường biểu diễn “lệch phải” (hình 1). Riêng ở bệnh nhân tăng huyết áp mạn kèm tổn thương thận, sự tự điều hòa bị rối loạn do hệ tiểu động mạch trước cầu thận mất khả năng co dãn. Ở những người này áp lực trong cầu thận thay đổi gần như song song với huyết áp trung bình (hình 1).
Hình 1: Đường biểu diễn sự tự điều hòa áp lực trong cầu thận của người bình thường (normal), người tăng huyết áp mạn có chức năng thận bình thường (chronic hypertension with normal renal function) và người tăng huyết áp mạn kèm bệnh thận mạn (chronic hypertension with chronic renal disease) 6.
Khi khởi đầu điều trị một bệnh nhân tăng huyết áp mạn bằng thuốc hạ huyết áp, áp lực trong cầu thận sẽ bắt đầu giảm ở một mức huyết áp cao hơn so với người bình thường (do đường biểu diễn tự điều hòa lệch phải). Hệ quả tức thì của giảm áp lực trong cầu thận là giảm độ lọc cầu thận, biểu hiện là tăng creatinin huyết thanh. Tăng creatinin huyết thanh đặc biệt thường gặp ở bệnh nhân tăng huyết áp kèm bệnh thận mạn 6. Sự giảm độ lọc cầu thận này mang tính chất huyết động chứ không phản ánh tổn thương thực thể của thận và thường là thoáng qua. Sau một thời gian độ lọc cầu thận sẽ phục hồi và cải thiện vì kiểm soát tốt huyết áp giúp cải thiện cấu trúc và chức năng các tiểu động mạch ở thận và chuyển dịch đường biểu diễn tự điều hòa về vị trí bình thường 7.
ẢNH HƯỞNG CỦA CÁC THUỐC ỨC CHẾ HỆ RENIN-ANGIOTENSIN TRÊN CHỨC NĂNG THẬN VÀ VẤN ĐỀ KHỞI TRỊ VÀ THEO DÕI THÍCH HỢP
Khi khởi trị bằng thuốc ức chế hệ renin-angiotensin (ức chế men chuyển hoặc chẹn thụ thể angiotensin) cho bệnh nhân tăng huyết áp mạn, độ lọc cầu thận rất thường giảm vì ngoài tác dụng hạ huyết áp thuốc ức chế hệ renin-angiotensin còn gây dãn tiểu động mạch đi, làm áp lực trong cầu thận hạ nhiều hơn. Cũng như với các thuốc hạ huyết áp khác, sự giảm độ lọc cầu thận khi khởi trị bằng thuốc ức chế hệ renin-angiotensin mang tính chất thoáng qua, sau một thời gian độ lọc cầu thận thường phục hồi lại và tăng lên, phản ánh lợi ích về dài hạn của việc giảm áp lực trong cầu thận (dẫn đến giảm lọc albumin ở cầu thận) bởi thuốc ức chế hệ renin-angiotensin. Ngoài tác động thuận lợi trên huyết động trong thận, thuốc ức chế hệ renin-angiotensin còn bảo tồn chức năng thận thông qua nhiều cơ chế ở mức mô-tế bào: cải thiện chức năng nội mô mạch máu thận, ngăn ngừa các tổn thương ở cầu thận và mô kẽ ống thận (ngăn hoạt hóa gian mô, tổn thương tế bào podocyte và thấm nhuận các tế bào viêm) 8,9.
Khi khởi trị bằng thuốc ức chế hệ renin-angiotensin cho người có bệnh thận mạn nên khởi đầu bằng liều thấp và tăng liều từ từ 8. Mức tăng creatinin huyết thanh khi khởi đầu dùng thuốc thường không quá 20% 8. Nếu creatinin huyết thanh tăng hơn 30% ở lần kiểm tra đầu (1 tuần sau khi bắt đầu dùng thuốc) hoặc tăng tiến triển theo thời gian nên tạm ngưng thuốc và tìm xem bệnh nhân có các yếu tố nguy cơ của suy thận cấp liên quan với ức chế hệ renin-angiotensin hay không (bảng 1). Trong quá trình điều trị cần theo dõi định kỳ creatinin huyết thanh (từ đó ước tính độ lọc cầu thận) và nồng độ K/máu. Nếu độ lọc cầu thận khởi điểm < 60 ml/phút/1,73 m2 hoặc K/máu khởi điểm > 4,5 mmol/l, nên kiểm tra lại creatinin huyết thanh và K/máu sau thời gian không quá 4 tuần mỗi khi tăng liều thuốc 10. Khi huyết áp đã đạt mục tiêu và liều thuốc đã ổn định, cũng nên kiểm tra lại creatinin huyết thanh và K/máu mỗi 1-6 tháng nếu độ lọc cầu thận khởi điểm < 60 ml/phút/1,73 m2 hoặc độ lọc cầu thận giảm ≥ 4 ml/phút/1,73 m2 hoặc bệnh nhân có những tình trạng kèm theo có thể gây suy thận tiến triển nhanh: dùng thuốc độc thận (kháng viêm không steroid kể cả ức chế chọn lọc COX-2, aminoglycoside, amphotericin B, thuốc cản quang tiêm tĩnh mạch có chứa iode, cyclosporine, tacrolimus), giảm thể tích tuần hoàn, béo phì, ngưng thở khi ngủ, nghiện thuốc lá, uống rượu nhiều và bệnh tim mạch trên lâm sàng (bệnh mạch máu não, bệnh mạch vành, bệnh động mạch ngoại vi) 10.
Bảng 1: Các yếu tố nguy cơ của suy thận cấp liên quan với ức chế hệ renin-angiotensin 8.
|
– Hẹp động mạch thận 2 bên hoặc hẹp động mạch thận ở người có một thận độc nhất – Bệnh thận đa nang – Giảm thể tích tuần hoàn (quá liều lợi tiểu, tiêu chảy, ói mửa nhiều …) – Huyết áp quá thấp không đảm bảo tưới máu thận một cách thích ứng (giảm cung lượng tim nặng, giảm sức cản mạch hệ thống) – Dùng thuốc kháng viêm không steroid hoặc ức chế COX-2 – Dùng cyclosporine hay tacrolimus |
CHỨNG CỨ VỀ LỢI ÍCH CỦA CÁC THUỐC ỨC CHẾ HỆ RENIN-ANGIOTENSIN TRONG BỆNH THẬN ĐÁI THÁO ĐƯỜNG
Hiệu lực bảo vệ thận của các thuốc ức chế hệ renin-angiotensin ở người bệnh thận đái tháo đường đã được chứng minh trong cả 2 tình huống là albumin niệu vi lượng và đạm niệu lâm sàng.
Trong tình huống albumin niệu vi lượng, các nghiên cứu EUCLID (EURODIAB Controlled trial of Linsinopril in Insulin dependent Diabetes) trên bệnh nhân ĐTĐ týp 1 và BRILLIANT (Blood pressure, Renal effects, Insulin control, Lipids, Lisinopril And Nifedipine Trial) trên bệnh nhân ĐTĐ týp 2 cho thấy thuốc ức chế men chuyển có tác dụng giảm mức bài xuất albumin trong nước tiểu 11,12. Cũng trong tình huống này, các nghiên cứu IRMA 2 (Irbesartan in patients with type 2 diabetes and Microalbuminuria study), INNOVATION (Incipient to Overt: Angiotensin II Blocker, Telmisartan, Investigation on Type 2 Diabetic Nephropathy) và MARVAL (MicroAlbuminuria Reduction with VALsartan) chứng tỏ thuốc chẹn thụ thể angiotensin cũng có tác dụng giảm mức bài xuất albumin trong nước tiểu và ngăn tiến triển đến đạm niệu lâm sàng 13-15. Riêng đối với losartan, các nghiên cứu của Lozano và Agha cho thấy thuốc này giảm có ý nghĩa mức bài xuất albumin trong nước tiểu cả ở người có tăng huyết áp lẫn ở người có huyết áp bình thường 16,17. Bảng 2 tóm tắt các nghiên cứu này.
Bảng 2: Các nghiên cứu chứng minh hiệu quả bảo vệ thận của thuốc ức chế hệ renin-angiotensin ở bệnh nhân đái tháo đường có albumin niệu vi lượng.
|
Nghiên cứu |
Bệnh nhân |
Thuốc |
Kết quả |
|
EUCLID 11 |
Bệnh nhân ĐTĐ týp 1, tuổi trung vị 33, HA tâm trương 75-90 mm Hg và tâm thu ≤ 155 mm Hg |
Lisinopril vs placebo |
Lisinopril giảm bài xuất albumin trong nước tiểu nhiều hơn 38,5 mg/phút (p = 0,001) so với placebo |
|
BRILLIANT 12 |
335 bệnh nhân ĐTĐ týp 2, tuổi trung bình 59, HA tâm trương 90-100 mm Hg, creatinin < 200 mmol/l |
Lisinopril vs nifedipine |
Lisinopril giảm bài xuất albumin trong nước tiểu nhiều hơn 20 mg/phút (p = 0,0006) so với nifedipine |
|
IRMA 2 13 |
590 bệnh nhân ĐTĐ týp 2, tuổi trung bình 58, HA > 135/85 mm Hg, creatinin < 1,5 mg/dl (nam) và < 1,1 mg/dl (nữ) |
Irbesartan vs placebo |
Irbesartan 300 mg giảm 70% nguy cơ mắc đạm niệu lâm sàng; Irbesartan 150 mg giảm 39% nguy cơ mắc đạm niệu lâm sàng |
|
INNOVATION 14 |
527 bệnh nhân ĐTĐ týp 2, tuổi trung bình 61, HA < 180/100 mm Hg, creatinin < 1,5 mg/dl (nam) và < 1,3 mg/dl (nữ) |
Telmisartan vs placebo |
Telmisartan 80 mg giảm 66% nguy cơ mắc đạm niệu lâm sàng; Telmisartan 40 mg giảm 55% nguy cơ mắc đạm niệu lâm sàng |
|
MARVAL 15 |
332 bệnh nhân ĐTĐ týp 2, tuổi trung bình 59, HA < 180/105 mm Hg, creatinin bình thường |
Valsartan vs amlodipine |
Valsartan giảm bài xuất albumin trong nước tiểu nhiều hơn có ý nghĩa (p < 0,001) so với amlodipine |
|
Lozano 16 |
422 bệnh nhân ĐTĐ týp 2, HA > 140/90 mm Hg, creatinin < 2 mg/dl |
Losartan (± HCTZ) |
Bài xuất albumin trong nước tiểu giảm từ 115 mg/24 g xuống 66 mg/24 g (p < 0,0001) |
|
Agha 17 |
361 bệnh nhân ĐTĐ týp 2, HA < 140/90 mm Hg, creatinin < 1,5 mg/dl |
Losartan vs vitamin B12 |
Losartan giảm bài xuất albumin trong nước tiểu nhiều hơn có ý nghĩa (p < 0,0001) so với chứng |
Trong tình huống đạm niệu lâm sàng có 3 nghiên cứu quan trọng chứng minh hiệu lực bảo vệ thận của các thuốc ức chế hệ renin-angiotensin là nghiên cứu của Lewis và cộng sự, nghiên cứu IDNT (Irbesartan Diabetic Nephropathy Trial) và nghiên cứu RENAAL (Reduction of Endpoints in NIDDM with the Angiotensin II Antagonist Losartan). Trong nghiên cứu của Lewis trên 409 bệnh nhân ĐTĐ týp 1 có đạm niệu lâm sàng và creatinin huyết thanh ≤ 2,5 mg/dl, thuốc ức chế men chuyển captopril giảm có ý nghĩa nguy cơ creatinin huyết thanh tăng gấp đôi so với ban đầu cũng như nguy cơ chết, phải chạy thận nhân tạo hoặc ghép thận 18. Cùng với IDNT, RENAAL đã chứng minh là thuốc chẹn thụ thể angiotensin có hiệu quả bảo vệ thận ở bệnh nhân ĐTĐ týp 2 có tăng huyết áp và đạm niệu lâm sàng 19,20.
RENAAL là một thử nghiệm lâm sàng phân nhóm ngẫu nhiên, mù đôi, thực hiện tại 250 trung tâm thuộc 28 quốc gia (có 4 quốc gia-lãnh thổ ở châu Á tham gia là Nhật, Hongkong, Malaysia và Singapore). Mục tiêu nghiên cứu là đánh giá hiệu quả của thuốc chẹn thụ thể angiotensin losartan trong việc ngăn chặn sự tiến triển của tổn thương thận ở bệnh nhân ĐTĐ týp 2 có bệnh thận toàn phát. Tiêu chuẩn chọn bệnh là: tuổi 31-70, có bệnh ĐTĐ týp 2, đạm niệu lâm sàng (tỉ số albumin/creatinin nước tiểu > 300 mg/g hoặc đạm niệu 24 giờ > 0,5 g) và creatinin huyết thanh 1,3-3,0 mg/dl. Trong giai đoạn tầm soát kéo dài 6 tuần, bệnh nhân có tăng huyết áp được tiếp tục dùng thuốc hạ huyết áp, tuy nhiên nếu đang dùng thuốc ức chế men chuyển hoặc chẹn thụ thể angiotensin thì các thuốc này được thay thế bằng những thuốc nhóm khác (lợi tiểu, chẹn canxi, chẹn alpha, chẹn bêta, thuốc tác dụng trung ương hoặc phối hợp các thuốc này với nhau). Sau đó bệnh nhân được phân ngẫu nhiên cho dùng losartan (liều khởi đầu 50 mg/ngày, sau 4 tuần tăng lên 100 mg/ngày) hoặc placebo. Ở nhóm losartan lẫn nhóm placebo bác sĩ điều trị có thể thêm thuốc hạ huyết áp (trừ ức chế men chuyển và chẹn thụ thể angiotensin) để đạt mục tiêu huyết áp < 140/90 mm Hg. Tiêu chí đánh giá chính là phối hợp các biến cố creatinin huyết thanh tăng gấp 2 so với ban đầu, mắc bệnh thận giai đoạn cuối (phải chạy thận nhân tạo dài hạn hoặc ghép thận) và chết.
Tổng cộng có 1513 bệnh nhân được tuyển vào nghiên cứu. Bệnh nhân có tuổi trung bình 60, nam giới chiếm tỉ lệ 63%, có 93% bệnh nhân được điều trị bằng thuốc hạ huyết áp lúc được tuyển vào nghiên cứu. Creatinin huyết thanh trung bình là 1,9 mg/dl và HbA1c trung bình là 8,4%. Huyết áp của 2 nhóm tương đương nhau lúc ban đầu (nhóm losartan: 152/82 mm Hg, nhóm placebo: 153/82 mm Hg) và vào cuối nghiên cứu (nhóm losartan: 140/74 mm Hg, nhóm placebo: 142/74 mm Hg).
Sau thời gian theo dõi trung bình 3,4 năm, các nhà nghiên cứu nhận thấy điều trị bằng losartan giảm rất có ý nghĩa các biến cố thuộc tiêu chí đánh giá chính. Hai thành phần thuộc tiêu chí đánh giá chính là creatinin huyết thanh tăng gấp 2 so với ban đầu và mắc bệnh thận giai đoạn cuối đều giảm rõ rệt ở nhóm losartan. Bảng 3 tóm tắt các kết quả chính của nghiên cứu và hình 2 biểu diễn tần suất dồn mắc bệnh thận giai đoạn cuối của nhóm losartan và nhóm placebo. Các nhà nghiên cứu cũng ghi nhận điều trị bằng losartan giảm 32% (p = 0,005) nguy cơ nhập viện vì suy tim so với placebo. Có thể nói RENAAL là một nghiên cứu bản lề giúp khẳng định vị trí của thuốc chẹn thụ thể angiotensin losartan trong điều trị bệnh thận toàn phát ở bệnh nhân ĐTĐ týp 2.
Nói tóm lại, các chứng cứ hiện có cho thấy ức chế hệ renin-angiotensin (bằng thuốc ức chế men chuyển hoặc chẹn thụ thể angiotensin) là nền tảng để ngăn sự tiến triển của tổn thương thận ở bệnh nhân ĐTĐ. Bên cạnh tác dụng hạ huyết áp, các thuốc ức chế men chuyển và chẹn thụ thể angiotensin còn có nhiều tác động đặc hiệu ở mức mô-tế bào giúp bảo vệ thận. Riêng ở bệnh nhân ĐTĐ týp 2 có bệnh thận toàn phát, chẹn thụ thể angiotensin là liệu pháp được lựa chọn hàng đầu nhằm ngăn sự tiến triển đến bệnh thận giai đoạn cuối.
Bảng 3: Kết quả của nghiên cứu RENAAL 18.
|
|
Nhóm losartan (n = 751) |
Nhóm placebo (n = 762) |
Trị số p |
|
Phối hợp biến cố thuộc tiêu chí đánh giá chính |
327 (43,5%) |
359 (47,1%) |
0,02 |
|
Creatinin huyết thanh tăng gấp 2 |
162 (21,6%) |
198 (26,0%) |
0,006 |
|
Mắc bệnh thận giai đoạn cuối |
147 (19,6%) |
194 (25,5%) |
0,002 |
|
Chết |
158 (21,0%) |
155 (20,3%) |
0,88 |
|
Mắc bệnh thận giai đoạn cuối hoặc chết |
255 (34,0%) |
300 (39,4%) |
0,01 |
|
Creatinin huyết thanh tăng gấp 2 hoặc mắc bệnh thận giai đoạn cuối |
226 (30,1%) |
263 (34,5%) |
0,01 |
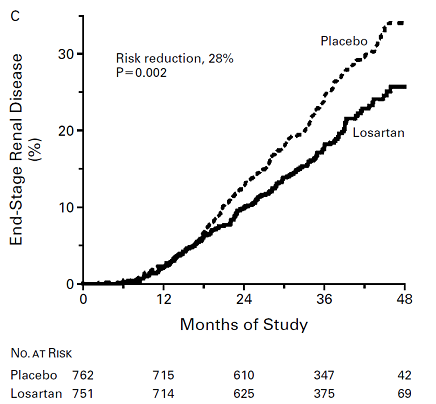
Hình 2: Tần suất dồn mắc bệnh thận giai đoạn cuối ở nhóm placebo (đường biểu diễn trên) và nhóm losartan (đường biểu diễn dưới) trong nghiên cứu RENAAL 18.
TÀI LIỆU THAM KHẢO
1) American Diabetes Association. Standards of medical care in diabetes – 2012. Diabetes Care 2012;35(suppl 1):S11-S63.
2) US Renal Data System: USRDS 2003 Annual Data Report : Atlas of end-stage renal disease in the United States. Bethesda, MD, National Institute of Health, National Institute of Diabetes and Digestive and Kidney Diseases, 2003.
3) Ritz E, Rychlik I, Locatelli F, Halimi S. End-stage renal failure in type 2 diabetes: A medical catastrophe of worldwide dimension. Am J Kidney Dis 1999;34:795-808.
4) Samak MJ, Greene T, Wang X, et al. The effect of a lower target blood pressure on the progression of kidney disease: Long term follow up of the Modification of Diet in Renal Disease Study. Ann Intern Med 2005;142:342-351.
5) Bakris GL, Williams M, Dworkin L, et al, for the National Kidney Foundation Hypertension and Diabetes Executive Committees Working Group. Preserving renal function in adults with hypertension and diabetes: a consensus approach. Am J Kidney Dis 2000;36:646-661.
6) Palmer BF. Renal dysfunction complicating the treatment of hypertension. N Engl J Med 2002;347:1256-1261.
7) Apperloo AJ, de Zeeuw D, de Jong PE. A short-term antihypertensive treatment-induced fall in glomerular filtration rate predicts long-term stability of renal function. Kidney Int 1997;51:793-797.
8) Schoolwerth AC, Sica DA, Ballermann BJ, Wilcox CS. Renal considerations in angiotensin-converting enzyme inhibitor therapy. A statement for healthcare professionals from the Council on the Kidney in Cardiovascular disease and the Council for High Blood Pressure Research of the American Heart Association. Circulation 2001;104:1985-1991.
9) Izuhara Y, Nangaku M, Inagi R, et al. Renoprotective properties of angiotensin receptor blockers beyond blood pressure lowering. J Am Soc Nephrol 2005;16:3631-3641.
10) National Kidney Foundation. KDOQI Clinical Practice Guidelines and Clinical Practice Recommendations for Diabetes and Chronic Kidney Disease. Am J Kidney Dis 2007;49 (suppl 2):S1-S180.
11) The EUCLID Study Group. Randomised placebo-controlled trial of lisinopril in normotensive patients with insulin-dependent diabetes and normoalbuminuria or microalbuminuria. Lancet 1997;349:1787-1792.
12) Agardh CD, Garcia-Puig J, Charbonnel B, Angelkort , Barnett AH. Greater reduction of urinary albumin excretion in hypertensive type 2 diabetic patients with incipient nephropathy by lisinopril than by nifedipine. J Hum Hypertens 1996;10:185-192.
13) Parving HH, Lehnert H, Brochner-Mortensen J, et al, for the Irbesartan in Patients with Type 2 Diabetes and Microalbuminuria Study Group. The effect of irbesartan on the development of diabetic nephropathy in patients with type 2 diabetes. N Engl J Med 2001;345:870-878.
14) Makino H, Haneda M, Babazono T, et al, for the INNOVATION Study Group. Prevention of transition from incipient to overt nephropathy with telmisartan in patients with type 2 diabetes. Diabetes Care 2007;30:1577-1578.
15) Viberti G, Wheeldon NM, for the MicroAlbuminuria Reduction with VALsartan (MARVAL) Study Investigators. Microalbuminuria reduction with valsartan in patients with type 2 diabetes mellitus: a blood pressure independent effect. Circulation 2002;106:672-678.
16) Lozano JV, Llisterri JL, Aznar J, Redon J on behalf of a Spanish Working Group. Losartan reduces microalbuminuria in hypertensive microalbuminuric type 2 diabetics. Nephrol Dial Transplant 2001;16 (suppl 1):85-89.
17) Agha A, Amer W, Anwar E, Bashir K. Reduction of microalbuminuria by using losartan in normotensive patients with type 2 diabetes mellitus: a randomized controlled trial. Saudi J Kidney Dis Transplant 2009;20:429-435.
18) Lewis EJ, Hunsicker LG, Bain RP, Rohde RD, for the Collaborative Study Group. The effect of angiotensin-converting-enzyme inhibition on diabetic nephropathy. N Engl J Med 1993;329:1456-1462.
19) Lewis EJ, Hunsicker LG, Clarke WR, et al, for the Collaborative Study Group. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes. N Engl J Med 2001;345:851-860.
Brenner BM, Cooper ME, de Zeeuw D, et al, for the RENAAL Study Investigators. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Engl J Med 2001;345:861-869.









