Tóm tắt
Hệ rennin angiotensin aldosterone (RAAS) giữ vai trò trung tâm trong sinh lý bệnh của tăng huyết áp và bệnh lý mạch máu.
Martin H. Strauss, Alistair S. Hall
Người dịch: BS Bàng Ái Viên – BV Chợ Rẫy
Các thuốc ức chế men chuyển angiotensin (UCMC) làm giảm nồng độ của angiotensin II (AT II), trong khi đó các thuốc ức chế thụ thể angiotensin (UCTT) ngăn chặn sự gắn kết của AT II với thụ thể AT1.Cả UCMC và UCTT đều là những thuốc hạ áp có hiệu quả và có khả năng như nhau về làm giảm nguy cơ đột quỵ – một bệnh lý bị ảnh hưởng bởi huyết áp. UCMC cũng làm giảm nguy cơ nhồi máu cơ tim và tử vong trên những bệnh nhân tăng huyết áp có nguy cơ cao cũng như những bệnh nhân đái tháo đường, cao tuổi, bệnh lý mạch máu và suy tim sung huyết. Ngược lại UCTT không làm giảm nguy cơ nhồi máu cơ tim hay tử vong trong các thử nghiệm lâm sàng so sánh với các thuốc hạ áp khác hay thậm chí với giả dược. Các tổng quan y văn về UCTT bao gồm phân tích gộp hay phân tích gộp hồi quy khẳng định rằng UCTT thiếu những hiệu quả bảo vệ tim mạch như của UCMC, một yếu tố độc lập với hiệu quả hạ áp. Các khuyến cáo lâm sàng, đặc biệt là trên những bệnh nhân tăng huyết áp nguy cơ cao, nên thể hiện rõ hiệu quả khác biệt trên tim mạch của UCMC và UCTT – UCMC giảm tử vong trong khi UCTT thì không. UCMC nên là thuốc ức chế hệ RAAS được ưu tiên lựa chọn trên những bệnh nhân nguy cơ cao.
UCMC và UCTT (ức chế thụ thể AT 1) là các thuốc hạ áp tác động đến hệ RAAS thông qua tác dụng lên angiotensin II với mỗi thuốc có 1 kiểu tác động riêng. UCMC ức chế sự hình thành AT II trong khi UCTT ngăn chặn sự kích thích thụ thể AT1 của AT II, do đó chúng được xếp 2 nhóm riêng biệt. Cả 2 nhóm thuốc này đều có hiệu quả hạ áp tương tự nhau và có lợi ích trên những bệnh nhân đột quỵ1, bệnh thận do đái tháo đường2, có triệu chứng suy tim sung huyết3 và ít nhất là trong các phân tích của các thử nghiệm lâm sàng lớn cho thấy làm giảm tần suất mới mắc đái tháo đường và rung nhĩ4. Hiệu quả chung này đã đưa đến nhiều khuyến cáo lâm sàng kết luận rằng UCMC và UCTT tương đương nhau, có thể thay thế nhau và chỉ lựa chọn 1 trong 2; có lẽ được xem như là 1 nhóm dược lý duy nhất – thuốc ức chế hệ RASS,6. Tuy nhiên kết luận về hiệu quả chung này không đúng trong tất cả trường hợp.
Trong khuyến cáo mới nhất của Hiệp Hội Châu Âu về Tăng Huyết Áp (ESH)7, phần 5.1.2.4 nói rằng “UCTT có thể có hiệu quả thấp hơn UCMC trong phòng ngừa nhồi máu cơ tim hay tử vong do mọi nguyên nhân”. Phát biểu này còn nhiều tranh cãi. Tuy nhiên, nếu hiệu quả làm giảm huyết áp của UCTT không dẫn đến làm giảm các biến cố tim mạch “nặng” giống như UCMC thì UCMC nên là thuốc ức chế hệ RAAS được lựa chọn đầu tiên trên những bệnh nhân nguy cơ cao. Có những bằng chứng mạnh mẽ và thuyết phục ủng hộ cho kết luận này như một nghiên cứu lâm sàng với khoảng 3 000 000 bệnh nhân. Kết quả vẫn hằng định bất kể là từ các nghiên cứu riêng biệt có so sánh với giả dược hay thuốc khác cho đến các phân tích gộp hay phân tích gộp hồi quy có hiệu chỉnh theo trị số huyết áp1,11 : UCMC làm giảm nguy cơ nhồi máu cơ tim và tử vong dựa trên và “độc lập” với hiệu quả hạ áp; trong khi UCTT thì không.
Bài báo này sẽ tập trung vào các biến cố tim mạch “nặng” của các nghiên cứu về UCMC và UCTT – nhồi máu cơ tim và tử vong – trong bối cảnh là đã biết ảnh hưởng của chính hiệu quả hạ áp trên các biến cố này. Đồng thời, các dữ liệu nghiên cứu sẽ được đánh giá trên khía cạnh về thiết kế và phương pháp phân tích thống kê được sử dụng – tiền cứu so với hồi cứu, mù đôi so với mở nhãn, có đối chứng với thuốc khác hoặc giả dược, các phân tích thống kê “vượt trội hơn” hoặc “không thua kém” – với bất kỳ kết luận về hiệu quả điều trị được xác định trên độ mạnh và hạn chế của phân tích thống kê được sử dụng.
Nghịch lý về NMCT của thuốc UCTT – bằng chứng từ 2004
Một bài báo của ban biên tập tờ British Medical Journal năm 200415 (với đồng tác giả là Martin H. Strauss) là tài liệu tham khảo đầu tiên trong y văn gợi ý rằng UCTT không có hiệu quả bảo vệ tim mạch tương tự như UCMC. Những nghiên cứu đầu tiên về thuốc UCTT cho thấy nó không giảm nguy cơ nhồi máu cơ tim hay tử vong mặc dù chứng minh được có hiệu quả hạ áp và có tính dung nạp tốt15. Nghiên cứu VALUE16 trên dân số lớn bệnh nhân tăng huyết áp đã ghi nhận rằng nhóm bệnh nhân điều trị với Valsartan có tỷ lệ nhồi máu cơ tim cao hơn có ý nghĩa thống kê là 19% so với nhóm bệnh nhân điều trị với thuốc chẹn kênh canxi Amlodipin. Những nghiên cứu khác về thuốc UCTT cũng cho thấy làm tăng nhẹ nguy cơ nhồi máu cơ tim4 – và tăng nguy cơ nhồi máu cơ tim này có ý nghĩa thống kê trong nghiên cứu CHARM-Alternative1. Có tính hợp lý về sinh học để giải thích hiện tượng này – được thảo luận dưới đây – và được gọi bằng nhóm từ “nghịch lý về nhồi máu cơ tim của thuốc UCTT”.
Bài báo của ban biên tập BMJ15 gây ra sự tranh cãi dữ dội và được giải quyết 6 tháng sau đó tại hội nghị năm 2005 tại Milan của Hiệp Hội Tăng Huyết Áp Châu Âu. The Blood Pressure Lowering Treatment Trialists Collaboration (BPLTTC)1 đã đưa ra một phân tích gộp hồi cứu song song về thuốc UCMC và UCTT để phân tích sự khác biệt về huyết áp trên nguy cơ nhồi máu cơ tim và tử vong – BMV. Cả UCMC và UCTT đều có hiệu quả giống nhau trên việc giảm nguy cơ BMV “phụ thuộc” vào hạ HA. Tuy nhiên, đối với bất kỳ mức độ hạ áp, thuốc UCMC còn làm giảm thêm nguy cơ bệnh mạch vành 9% (p=0,002) và lợi ích này “độc lập” với hiệu quả hạ áp với giảm nguy cơ tương đối BMV 9% ngay cả khi không có bất kỳ hiệu quả hạ áp nào (hình 1)1 – hiện tượng này cũng được khẳng định trong các nghiên cứu khác 11,18. Ngược lại, thuốc UCTT không có lợi ích trên BMV “độc lập” với hiệu quả hạ áp mà còn làm tăng nhẹ nhưng không có ý nghĩa thống kê nguy cơ BMV 7% (95% CI: 24% – 7%, p=NS) (hình 1). Với bất kỳ mức độ hạ áp thì UCMC giảm thêm 15% nguy cơ nhồi máu cơ tim và tử vong (p=0,0001) so với UCTT và lợi ích này “độc lập” với hiệu quả hạ áp (Hình 1). Ngược lại, lợi ích giảm nguy cơ đột quỵ và suy tim của UCMC và UCTT thì tương đồng nhau và chỉ phụ thuộc vào hiệu quả hạ áp. Phân tích gộp hồi quy của BPLTTC1 xác nhận giả thuyết được đưa ra trong bài báo của ban biên tập BMJ15 – UCTT thiếu lợi ích bảo vệ tim như của UCMC trên BMV – do đó khẳng định “nghịch lý về nhồi máu cơ tim của UCTT”.
Những hiệu quả khác nhau của UCMC và UCTT trên tim mạch đã được chứng minh trong một phân tích gộp song song CIRCULATION năm 2006 của nhiều nghiên cứu về UCMC và UCTT4 (đồng tác giả với các tác giả trên). So sánh có đối chứng với giả dược và các thuốc hạ áp khác (34 nghiên cứu, n=154 943), UCMC so sánh làm giảm nguy cơ tương đối của tử vong chung 9% (p<0,0001) và nhồi máu cơ tim 14% (p<0,001); trong khi đó UCTT (11 nghiên cứu; n=55 050) không những không làm giảm tử vong (OR=1,01; 95% 0,96 – 1,06; p=0,8) mà còn làm tăng nguy cơ nhồi máu cơ tim (OR 1,08; 95%CI 1,01 – 1,16, p=0,03) (hình 2). Ngược lại, lợi ích làm giảm nguy cơ các biến cố mạch máu não là như nhau giữa 2 nhóm thuốc và phụ thuộc vào hiệu quả hạ áp. Đồng thời, nguy cơ của tử vong chung, nhồi máu cơ tim và đột quỵ giữa các nhánh so sánh trong phân tích gộp song song về UCMC và UCTT là như nhau (lần lượt là 13% vs 14%; 5,8% vs 6,3%; 4,2% vs 4,4%). Mặc dù các phân tích gộp khác về UCTT không chứng minh được UCTT làm tăng nguy cơ nhồi máu cơ tim có ý nghĩa thống kê9,19,20, nhưng quan trọng hơn là những phân tích này chứng minh được UCTT không làm giảm nhồi máu cơ tim và tử vong – điều này làm bối rối các nhà phân tích.
Angiotensin II (AT II), bradykinin, thụ thể AT1, AT2 – chúng liên kết với nhau như thế nào?
Lợi ích “độc lập” với hiệu quả hạ áp duy nhất của UCMC có cơ chế sinh học hợp lý4. UCMC làm giảm angiotensin II – angiotensin II không chỉ đóng vai trò chính trong sinh bệnh của tăng huyết áp thông qua co mạch và giữ nước mà còn có độc tính trực tiếp lên mô ở mạch máu, tim, não và thận. AT II gây ra tổn thương hệ tim mạch do duy trì tăng trưởng tế bào, viêm và xơ hóa; tác động trực tiếp lên sự di chuyển của tế bào cơ trơn, phì đại mạch máu và hình thành lớp phức hợp ngoại bào dẫn đến tái cấu trúc mạch máu và làm rối loạn chức năng tế bào nội mạc21. Hiệu quả làm giảm nồng độ AT II của UCMC có thể làm giảm tác hại độc mô trực tiếp của AT II độc lập với hiệu quả hạ áp. UCMC cũng ngăn cản phá vỡ bradykinin, là một chất trung gian quan trọng của tiền thích nghi thiếu máu cục bộ, chức năng nội mô và ly giải fibrin – những yếu tố quan trọng trong bảo vệ tim mạch4.
Ngược lại với UCMC, UCTT không làm tăng bradykinin do đó thiếu hiệu quả bảo vệ tim mạch4. UCTT không làm giảm nồng độ AT II như UCMC mà chỉ ức chế chọn lọc thụ thể AT1 – nên cả hai nhóm thuốc đều làm giảm tác dụng của AT II nhưng với cơ chế khác nhau. UCTT ức chế thụ thể AT1 làm ức chế vòng phản hồi ngược âm tính dẫn đến làm tăng nồng độ AT II gấp 200% – 300% so với bình thường và gây độc trực tiếp tế bào. Cũng có giả thuyết là việc tăng nồng độ AT II đóng vai trò có lợi thông qua kích thích thụ thể AT2 – cho tác dụng ngược lại với kích thích thụ thể AT1 – gây giãn mạch ngoại biên cũng như hạn chế tăng trưởng tế bào và kháng viêm21. Thụ thể AT2 ít được biết tới do ít biểu hiện trên người lớn, hoạt động của nó lấn át bởi sự hoạt hóa thụ thể AT1 với đặc tính đối kháng21. Kích hoạt các thụ thể AT2 trên những mạch vành bị bệnh được cho là dẫn đến vỡ mảng xơ vữa, nhồi máu cơ tim, tái cấu trúc mạch máu22. Điều này rõ ràng không làm hạn chế hay loại bỏ lợi ích bảo vệ tim mạch thông qua hiệu quả hạ áp khi ức chế thụ thể AT1 của UCTT.
UCMC và UCTT khi so sánh với giả dược
Những nghiên cứu lâm sàng so sánh với giả dược có những lợi thế riêng biệt hơn khi so sánh với các thuốc khác. Những nghiên cứu có đối chứng với giả dược đánh giá chính xác nhất hiệu quả và tác hại của điều trị, cho phép thử nghiệm các điều kiện điều trị riêng biệt tối đa, nên tăng khả năng phát hiện lợi ích cũng như tác hại; từ đó có thể “thêm vào” điều trị chuẩn23. Gần đây có 3 phân tích gộp các thử nghiệm của UCTT so sánh với giả dược, giúp đánh giá sâu về hiệu quả điều trị cũng như những thiếu sót.
Trong một phân tích gộp song song các nghiên cứu về UCMC và UCTT có so sánh với giả dược trên bệnh nhân có nguy cơ cao đã loại trừ bệnh nhân suy tim (26 thử nghiệm, n=108212) (Savarese8), UCMC (13 nghiên cứu, n=53791) làm giảm nguy cơ nhồi máu cơ tim 17,7% (p<0,001) và tử vong do mọi nguyên nhân 8,3% (p=0,008). Ngược lại, UCTT (13 nghiên cứu, n=54,421) không làm giảm có ý nghĩa thống kê nguy cơ nhồi máu cơ tim hay tử vong do mọi nguyên nhân (OR=1,006; 95CI 0,941 – 1,08; p=0,866). UCMC và UCTT có hiệu quả tương đương nhau về giảm đột quỵ có ý nghĩa thống kê – lợi ích này chỉ phụ thuộc vào hiệu quả hạ áp – gợi ý UCMC và UCTT có hiệu quả hạ áp tương tự nhau. Một phân tích gộp các nghiên cứu về UCTT có đối chứng với giả dược khác cũng cho kết quả tương tự (17 nghiên cứu, n=67374)(Bangalore9), UCTT không làm giảm tỷ lệ nhồi máu cơ tim và tử vong do mọi nguyên nhân (lần lượt OR 0,93; CI 0,81 – 1,07; OR 0,99 CI 0,95 – 1,03; p=0,98). Một phân tích gộp giới hạn những bệnh nhân >65 tuổi (8 nghiên cứu, n=50521) (Elgendy10) cũng không tìm thấy sự giảm nguy cơ nhồi máu cơ tim hay tử vong (HR 1,03; CI 0,88 – 1,21; HR 1,03 CI 0,98 – 1,08). Tương tự phân tích gộp Savarese, trong phân tích gộp Bangalore và Elgendy, nguy cơ đột quỵ cũng giảm có ý nghĩa thống kê (lần lượt là OR 0,91; CI 0,87 – 0,98; HR 0,93 CI 0,86 – 1,0).
Kết quả từ 3 phân tích gộp có đối chứng với giả dược trên là đều giống nhau: UCTT làm giảm có ý nghĩa thống kê nguy cơ đột quỵ, một lợi ích tim mạch có liên quan trực tiếp từ hiệu quả hạ áp. Tuy nhiên, UCTT không có giảm nguy cơ phụ thuộc huyết áp trên nhồi máu cơ tim hay tử vong mà mức tối thiểu cần phải có là một nửa mức giảm nguy cơ đột quỵ trên12,13. Điều này gợi ý rằng UCTT có thể có tác động gây hại trực tiếp trên tim mạch, có lẽ thứ phát qua việc điều hòa tăng nồng độ AT II và có thể làm giảm lợi ích của hiệu quả hạ áp.
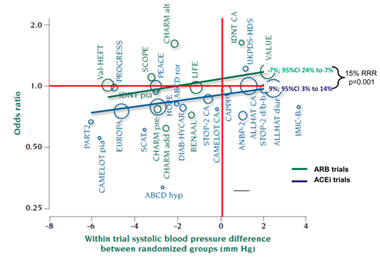
Hình 1 – Phân tích gộp hồi quy song song các nghiên cứu về thuốc UCMC và thuốc UCTT trên nguy cơ nhồi máu cơ tim và tử vong do nguyên nhân tim mạch đã được điều chỉnh theo hiệu quả hạ áp. Giảm 15% nguy cơ nhồi máu cơ tim và tử vong do nguyên nhân tim mạch giữa các nghiên cứu UCMC (vòng màu xanh dương) và nghiên cứu UCTT (vòng xanh lá). Turbull et al. J Hypertens. 2007; 25(5):951-958.
Các nghiên cứu so sánh UCMC với UCTT
Một số tác giả cho rằng các nghiên cứu so sánh đối đầu trực tiếp UCMC và UCTT là cách tối ưu nhất để đánh giá hiệu quả bảo vệ tim mạch tương đối của chúng. Có 4 nghiên cứu lớn như vậy và mặc dù không có nghiên cứu nào chứng minh được giả thuyết UCTT tốt hơn có ý nghĩa thống kê, chúng đưa ra một cách nhìn độc đáo. Nghiên cứu ELITE25 trên bệnh nhân suy tim mạn (n=3152, theo dõi 18 tháng) so sánh Losartan 50mg với Captopril 50mg 3 lần mỗi ngày; nhóm điều trị với losartan có tỷ lệ tử vong chung cao hơn 13% so với nhóm điều trị captopril nhưng không có ý nghĩa thống kê (280 vs 250 bệnh nhân, p=ns)
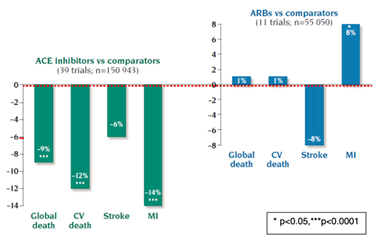
Hình 2 – Phân tích gộp song song các nghiên cứu về UCMC và UCTT : UCMC giảm nguy cơ tương đối của tử vong chung 9% (p<0,0001) và của nhồi máu cơ tim 14% (p<0,0001) trong khi UCTT (11 nghiên cứu, n=55 050) không làm giảm tử vong chung (OR=1,01; 95CI 0,96 – 1,06) và tăng nguy cơ nhồi máu cơ (OR 1,08; 95%CI 1,01 – 1,16; p=0,03). Strauss and Hall. Circulation. 2006: 114(8):838-854.
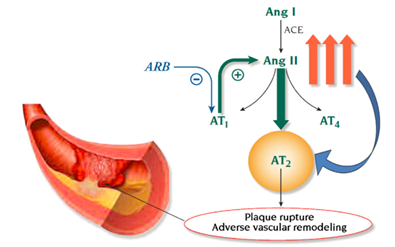
Hình 3 – Vỡ mảng xơ vữa trên động mạch vành với UCTT. Ức chế thụ thể AT1 do thuốc UCTT gây ức chế vòng phản hồi âm tính làm tăng nồng độ Angiotensin II gấp 2 – 3 lần, dẫn tới tăng kích thích thụ thể AT2 và vỡ mảng xơ vữa mạch vành. Strauss và Hall. Circulation. 2006; 114(8):838-854.
Một thuốc điều trị “không thua kém hơn” về mặt thống kê thì không có cách nào để xác định được thuốc này là một phương pháp điều trị tương đương với tiêu chuẩn vàng – chứ không phải là tốt nhất, điều trị “không thua kém hơn” về mặt thống kê là phương pháp điều trị đứng hàng thứ 2 đặc biệt là khi nó gắn liền với các kết cục tim mạch chính. Điều giải thích “không thua kém hơn” về mặt thống kê này trong bối cảnh kết quả của nghiên cứu ONTARGET29 được xác nhận bằng khuyến cáo của FDA và the Health Protection Branch of Canada – cả hai tổ chức đều công nhận Telmisartan là thuốc lựa chọn thứ hai trên bệnh nhân nguy cơ cao, khi không dung nạp được UCMC. Mặc dù các cơ quan thẩm quyền đã khuyến cáo rõ ràng nhưng giới bác sĩ vẫn còn nhầm lẫn khi hiểu từ “không thua kém hơn” về mặt thống kê. Sự nhầm lẫn này là dễ hiểu do dịch nghĩa đen từ “không thua kém hơn” thành “tương đương” hay “thay thế” – đó chắc chắn không phải là điều thuật ngữ thống kê “không thua tkém hơn” chứng minh.
Những kết luận trên cũng phù hợp EMA với phân tích nghiên cứu ONTARGET29 của EMA (the European Medicines Agency) trong “Bảng báo cáo đánh giá Micardis” (London, 2009 #EMA/CHMP/768468/2009). Báo cáo này kết luận rằng “dữ liệu nghiên cứu không cho phép kết luận rằng hiệu quả tương đương với Ramipril. Thậm chí tính ưu việt của Telmisartan so với giả dược cũng không được chứng minh khi so sánh với giả dược giả định như trong ONTARGET cũng như khi so sánh trực tiếp với giả dược như trong TRANSCEND và pRoFESS”. Điều thật sự gây bối rối và đi ngược lại việc thực hành dựa trên y học chứng cứ là mặc dù EMA kết luận Telmisartan thậm chí còn không vượt trội so với giả dược nhưng Telmisartan lại được chấp thuận là thuốc lựa chọn đầu tiên trên những bệnh nhân nguy cơ cao như Ramipril và vì thế có thể được ưu tiên kê toa nhiều hơn UCMC.
Tăng huyết áp – UCMC và UCTT – các hiệu quả độc lập với huyết áp
Một phân tích gộp gần đây cộng dồn các nghiên cứu về UCMC và UCTT với bất kỳ thuốc so sánh, bao gồm 20 nghiên cứu với 158 998 bệnh nhân (7 nghiên cứu UCMC, n=76,615 và 13 nghiên cứu UCTT, n= 82,383 bn)14 và bệnh nhân tăng huyết áp chiếm tỷ lệ cao. Các nghiên cứu này được thực hiện cùng thời điểm và được công bố từ năm 2000 – nên những bệnh nhân trong nghiên cứu tương đương nhau về tỷ lệ bệnh đi kèm và các thuốc điều trị nền tảng… Thời gian theo dõi trung bình 4,3 năm với HATT trung bình ban đầu là 153 mmHg và ít nhất 2/3 bệnh nhân đã được chẩn đoán tăng huyết áp. Kết quả cho thấy nguy cơ tương đối của tử vong do mọi nguyên nhân giảm rõ rệt tới 5% (p=0,05) cho nhóm bệnh nhân dùng UCMC hay UCTT. Khi phân tích riêng các nghiên cứu về UCMC và UCTT – các thuốc UCMC làm giảm tử vong do mọi nguyên nhân là 10% (p=0,004) trong khi đó các thuốc UCTT cho kết quả trung tính (HR: 0,99; p=0,683). Vì vậy, giảm nguy cơ tử vong do mọi nguyên nhân khi phân tích gộp chung cả hai thuốc UCMC và UCTT là do ảnh hưởng của các nghiên cứu về UCMC. Số bệnh nhân cần phải điều trị với UCMC để phòng ngừa 1 trường hợp tử vong (NNT) là 67 (HR 0,84 – 0,97) – số liệu có ý nghĩa lâm sàng quan trọng – trong khi đó NNT của UCTT là 335 (p=ns)31. Mặc dù kết quả này có thể thứ phát do mức giảm huyết áp nhiều hơn trong các thử nghiệm UCMC so với UCTT, nhưng thật sự không phải như thế. Trong các nghiên cứu về UCMC, chỉ có 19% bệnh nhân được so sánh với giả dược, trong khi các nghiên cứu về UCTT có đến 51% bệnh nhân được so sánh với giả dược. Mức độ hạ huyết áp sẽ cao nhất trong các nghiên cứu so sánh với giả dược chứ không phải trong các nghiên cứu so sánh với thuốc hạ áp khác, do đó các nghiên cứu về UCTT sẽ thuận lợi hơn khi cho kết quả giảm tỷ lệ tử vong khi hạ áp.
Phân tích gộp này có vài hạn chế như có sự khác biệt giữa các dân số nghiên cứu, dữ liệu lấy từ nghiên cứu không phải trực tiếp từ bệnh nhân và giả định rằng có hiệu quả nhóm giữa các thuốc UCMC và UCTT khác nhau. Dựa trên độ mạnh của các chứng cứ trong tăng huyết áp có thể nói rằng UCMC nên là thuốc ức chế hệ RAAS ưu tiên lựa chọn và không thể được thay thế bởi UCTT như trong khuyến cáo 127 năm 2011 của UK National Institute for Health and Clinical Excellence (NICE) (www.nice.org.uk/guidance/CG127) và của Canadian Hypertension Education Program (CHEP)5.
Đái tháo đường
Trong những nghiên cứu có so sánh với giả dược33, UCMC (11 nghiên cứu, n=21 997) làm giảm 11% tử vong do mọi nguyên nhân (HR 0,89, 95% CI 0,89 – 0,99; p=0,03), trong khi UCTT (8 nghiên cứu, n = 13 304) không làm giảm tử vong do mọi nguyên nhân (HR 1,03; 95% CI 0,89 – 1,18). Đáng chú ý, trong một nghiên cứu lớn nhất về UCMC có đối chứng với giả dược trên bệnh nhân đái tháo đường là nghiên cứu ADVANCE34 (n=11140), dùng phối hợp perindopril-indapamide làm giảm được huyết áp 5,6/2,2 mmHg trong thời gian theo dõi 4,3 năm và giảm nguy cơ tử vong do mọi nguyên nhân là 14% (p=0,25). Ngược lại, trong nghiên cứu lớn nhất về UCTT có đối chứng với giả dược trên bệnh nhân đái tháo đường là nghiên cứu ROADMAP35 (n=4447), Olmesartan giảm được huyết áp 3,1/1,9 mmHg trong thời gian theo dõi 3,2 năm và làm tăng có ý nghĩa thống kê tử vong do nguyên nhân tim mạch (HR 4,94; CI 1,47 – 17,06; p=0,01).
Bệnh thận – độ lọc cầu thận thấp hay có albunin niệu – là bệnh lý thường gặp bệnh nhân đái tháo đường và là yếu tố tiên lượng độc lập cho bệnh thận giai đoạn cuối và tử vong tim mạch36. UCMC và UCTT cho tác dụng bảo vệ cầu thận2,37 tương tự nhau và không có sự khác biệt về mặt bệnh lý thận. Tuy nhiên, tử vong thường gặp hơn nguy cơ bệnh thận giai đoạn cuối gấp 5 – 10 lần ở bệnh nhận trên những bệnh nguy cơ cao như đái tháo đường với tỷ lệ tử vong tuyệt đối cao nhất khi độ lọc cầu thận dưới 60 ml/phút và tiểu albumin đại thể36 – và chỉ thuốc UCMC làm giảm tử vong và thuốc UCTT thì không nên UCMC nên được ưu tiên lựa chọn33.
Mặc dù những hiệu quả khác nhau trên tim mạch của UCMC và UCTT đã được chứng minh rõ ràng trong các nghiên cứu ngẫu nhiên, nhưng các nghiên cứu ngẫu nhiên với nhóm bệnh nhân chọn lọc cao có thể không phản ánh được toàn bộ dân số nguy cơ. Một số tác giả cho rằng các nghiên cứu “hồi cứu dựa vào dân số thuần tập” bao gồm hơn, nhận phổ bệnh nhân rộng hơn, có thể phản ánh “kinh nghiệm điều trị trên dân số thật” và vì vậy có giá trị đánh giá hiệu quả điều trị như thử nghiệm mù đôi. Giả định này không hoàn toàn chính xác. Lấy ví dụ, trong nghiên cứu thuần tập hồi cứu trên 87 472 bệnh nhân đái tháo đường điều trị với UCMC hay UCTT, cho kết luận rằng UCTT làm giảm nguy cơ nhập viện và tử so với UCMC38 và vì vậy “ủng hộ sử dụng UCTT có thể thay thế UCMC”. Kết luận này không đáng tin cậy bởi các yếu tố sau: kết cục chính của nghiên cứu chiếm ưu thế là tỷ lệ nhập viện chứ không phải là tử vong, thời gian theo dõi dưới 1 năm là quá ngắn để thấy được lợi ích “phụ thuộc thời gian” của UCMC, biến cố tử vong ít nên không thể hiệu chỉnh theo các yếu tố có khả năng khác và nó là nghiên cứu hồi cứu. Dữ liệu hồi cứu cung cấp thông tin về tỷ lệ các biến cố, thuốc sử dụng, bệnh lý đi kèm trong dân số, phương pháp điều trị hiện hành – nhưng khi có liên quan đến việc đánh giá hiệu quả của điều trị của những thuốc không được phân ngẫu nhiên, nó là phương pháp tốt nhất để đưa ra giả thuyết chứ không phải để bác bỏ với bằng chứng từ các nghiên cứu ngẫu nhiên mù đôi.
Thuốc UCMC và UCTT trong suy tim – các nghiên cứu có đối chứng với giả dược
Kết quả từ các nghiên cứu đối đầu giữa UCMC và UCTT trên suy tim như ELITE II25, OPTIMAAL26 và VALIANT3 cũng đã ủng hộ cho kết luận rằng UCMC ưu thế hơn được rút ra từ các nghiên cứu có so sánh với giả dược. Trong nghiên cứu CONSENSUS – 1 (n=253, theo dõi 188 ngày), những bệnh nhân suy tim nặng (NYHA 4) được phân ngẫu nhiên vào nhóm dùng thuốc UCMC enalapril hoặc nhóm dùng giả dược – tỷ lệ tử vong sau 1 năm giảm 31% (36% vs 52%, p=0,001)39, từ đó bắt đầu thay đổi mô hình tiếp cận điều trị suy tim từ “huyết động” sang “thần kinh thể dịch”. Trong một phân tích gộp của 5 nghiên cứu dài hạn về UCMC có so sánh với giả dược trên những bệnh nhân có có rối loạn chức năng thất trái và suy tim có triệu chứng với huyết áp bình thường (n=12 763 theo dõi 35 tháng), nhóm UCMC có tỷ lệ thấp hơn về tử vong (23% vs 26,8%; OR 0,8; 0,74 – 0,87), tái nhồi máu (8,9% vs 11%; OR 0,79; 0,7 – 0,89) tái nhập viện do suy tim (13,7% vs 18,9%; OR 0,67; 0,61 – 0,74)40. Những lợi ích này được nhận thấy từ giai đoạn sớm khi bắt đầu điều trị và tồn tại lâu dài. Trong 5 nghiên cứu, có 3 nghiên cứu đánh giá sau nhồi máu cơ tim (SAVE, AIRE và TRACE). 3 nghiên cứu này cho thấy nhóm UCMC có tỷ lệ tử vong thấp hơn nhóm giả dược (23,4% vs. 29.1%; OR 0,74; 0,66–0,83), tương tự với tỷ lệ tái nhập viện do suy tim (11,9% vs. 15,5%; OR 0,73; 0,63–0,85), và tái nhồi máu cơ tim (10,8% vs. 13,2%; OR 0,80, 0,69–0,94).
Nghiên cứu Val-Heft41 (n=5010, theo dõi 23 tháng) so sánh UCTT Valsartan liều 160mg 2 lần mỗi ngày với giả dược cho thấy không làm giảm tỷ lệ tử vong chung (khoảng 20% ở cả 2 nhóm) nhưng làm giảm có ý nghĩa thống kê tỷ lệ tái nhập viện do suy tim (18,2% vs. 13,8% p<0,001) và cũng cải thiện có ý nghĩa phân độ suy tim theo NYHA, phân suất tống máu thất trái và chất lượng cuộc sống so với giả dược (p<0,01)41. Lợi ích của Valsartan trên chất lượng cuộc sống là rõ ràng mặc dù 93% bệnh nhân có điều trị nền UCMC.
Chương trình CHARM42 (n=7599) bao gồm 3 nghiên cứu song song có đối chứng với giả dược để đánh giá hiệu quả Candesartan 32mg ở bệnh nhân suy tim có triệu chứng. Candesartan giảm tử vong do mọi nguyên nhân (HR 0,91; 95% CI 0,83–1,0, P = 0,055) nhưng tất cả lợi ích chỉ hiện diện trong năm đầu tiên điều trị. Trích dẫn từ báo cáo của các nhà nghiên cứu là “sự khác biệt về tử vong do nguyên nhân tim mạch của điều trị này chỉ nổi bật trong năm đầu tiên mà không có sự khác biệt khác thêm vào trong năm kế tiếp”, điều này gợi ý rằng Candesartan có lợi ích về huyết động ngay lập tức nhưng còn hạn chế và có khoảng 40% bệnh nhân có điều trị nền cùng lúc với UCMC. Điều thú vị cần lưu ý rằng các nhà nghiên cứu của CHARM kết luận tỷ lệ tử vong ở bệnh nhân nhóm tuân thủ điều trị với giả dược không khác biệt với nhóm bệnh nhân tuân thủ điều trị với Candesartan, điều này có thể đưa đến kết luận trong nghiên cứu CHARM, sự tuân thủ điều trị chứ không phải là do Candesartan làm giảm tần suất tử vong.43
UCMC và UCTT trong bệnh lý mạch máu
Có 3 nghiên cứu lớn về UCMC có đối chứng với giả dược của trên những bệnh nhân nguy cơ cao với huyết áp bình thường (133/78 – 139/79 mmHg) và có bệnh lý mạch máu hoặc đái tháo đường, và không triệu chứng suy tim hoặc rối loạn chức năng thất trái là HOPE44, EUROPA45 và PEACE46. Trong 1 phân tích gộp của 3 nghiên cứu này (n= 29 805, theo dõi trung bình 4,5 năm), UCMC làm giảm tỷ lệ tử vong mọi nguyên nhân (7,8 vs. 8,9%, p = 0,0004), tử vong do nguyên nhân tim mạch (4,3 vs. 5,2%, p = 0,0002) và nhồi máu cơ tim không tử vong (5,3 vs. 6,4%, p = 0,0001), với chỉ làm giảm huyết áp rất ít (3/1–4/1 mmHg)47. Trong nghiên cứu TRANSCEND48 (n=5926, theo dõi 56 tháng), UCTT Telmisartan được so sánh với giả dược trên bệnh nhân có nguy cơ tương tự như HOPE/EUROPA/PEACE có bệnh lý mạch máu hay đái tháo đường – tất cả những bệnh nhân này đều không dung nạp với UCMC trước đó. Telmisartan không giảm tỷ lệ tử vong do nguyên nhân tim mạch (7,7% vs. 7,5%, p = 0,78) mặc dù có tác dụng hạ HATT tới 3,2mmHg48 và không có sự khác biệt về tỷ lệ tử vong do nguyên nhân tim mạch của nhóm giả dược so với nhóm giả dược trong nghiên cứu HOPE (7,5% vs. 8,1%)44. Trong nghiên cứu PRoFESS trên những bệnh nhân sau đột quỵ (n=20 232, theo dõi 30 tháng), khi so sánh với giả dược, Telmisartan cũng không làm giảm nguy cơ tử vong tim mạch (13,5% vs. 14,4%, P = 0,11) mặc dù có hiệu quả hạ huyến áp tâm thu 3,8mmHg49.
Khuyến cáo gần đây nhất của AHA/ACCF về Phòng Ngừa Thứ Phát Và Điều Trị Giảm Nguy Cơ Trên Bệnh Nhân Bệnh Mạch Vành Và Bệnh Lý Xơ Vữa Mạch Máu Khác50 khuyên rằng : “UCMC nên được khởi đầu và duy trì không hạn định trên tất cả bệnh nhân có phân suất tống máu thất trái < 40% và những bệnh nhân có tăng huyết áp, đái tháo đường, bệnh thận mạn, trừ khi có chống chỉ định (mức độ bằng chứng A) và hợp lý khi sử dụng UCMC trên tất cả bệnh nhân khác (mức độ bằng chứng B). Sử dụng UCTT được khuyến cáo trên những bệnh nhân có suy tim hay nhồi máu cơ tim với phân suất tống máu thất trái < 40% và không dung nạp với UCMC (mức độ bằng chứng A)”. Ít nhất là trên bệnh nhân suy tim và bệnh mạch máu, các khuyến cáo đã phân biệt rõ ràng được lợi ích của UCMC ưu thế hơn UCTT.
Bảng 1 – Phân tích gộp song song thử nghiệm UCMC và UCTT so sánh với các thuốc khác trên bệnh nhân đái tháo đường.
|
Bảng 1 – Phân tích gộp song song thử nghiệm UCMC và UCTT so sánh với các thuốc khác trên bệnh nhân đái tháo đường. |
||
|
|
UCMC 23 thử nghiệm N = 32 827 Giảm nguy cơ tương đối |
UCTT 13 thử nghiệm N = 23 867 Giảm nguy cơ tương đối |
|
Tử vong do mọi nguyên nhân |
13% 0,87:95% CI 0,78–0,98 |
NS 0,94:95% CI 0,82–1,08 |
|
Tử vong do nguyên nhân tim mạch |
17% 0,83:95% CI 0,7–0,99 |
NS 1,21:95% CI 0,81–1,8 |
|
Biến cố tim mạch chính |
14% 0,86:95% CI 0,77–0,95 |
NS 0,94:95% CI 0,85–1,01 |
|
Nhồi máu cơ tim |
21% 0,79:95% CI 0,65–0,95 |
NS 0,89:95% CI 0,74–1,07 |
|
Suy tim |
19% 0,81:95% CI 0,71–0,93 |
30% 0,70:95% CI 0,59–0,82 |
|
Đột quỵ |
NS 0,95:95% CI 0,81–1,04 |
NS 1,0:95% CI 0,89–1,12 |
|
Chang et al. JAMA Intern Med. 2014;174(5):773-785 |
||
Thiết kế các nghiên cứu về UCTT
Một thiết kế nghiên cứu thường gặp trong các nghiên cứu về UCTT là nghiên cứu PROBE (Prospective Randomized Open-label Blinded Endpoint) – với cả bệnh nhân và bác sĩ đều biết về điều trị ngẫu nhiên. Nghiên cứu nhãn mở được giới thiệu năm 1992 như là nguồn thay thế tiềm năng của chứng cứ khách quan51. Tính toàn vẹn thống kê của “thử nghiệm nhãn mở” dựa trên tiền đề là các phân tích chính được thực hiện bằng các tiêu chí khách quan nghiêm ngặt như tử vong do mọi nguyên nhân. Do đó, người ta chấp nhận nó rộng rãi nếu nó được thiết kế và chọn mẫu cẩn thận, kết quả sẽ không phải chịu sai số hệ thống mặc dù thiếu đối chứng mù đôi. Nguy cơ sai số tiềm tàng ở 1 nghiên cứu nhãn mở được đánh giá trong một phân tích gộp của tất cả các nghiên cứu về UCTT ở bệnh nhân nguy cơ cao (37 thử nghiệm, n= 147 202 bệnh nhân) mà phân tích độ nhạy so sánh các tiêu chí tim mạch trong “nghiên cứu nhãn mở” như so sánh trong nghiên cứu mù đôi9.
Có 12 nghiên cứu trong 37 nghiên cứu về UCTT là nhãn mở (17 323 trong tổng số 147 020 bệnh nhân) và cho thấy giảm nhẹ tỷ lệ tử vong chung, tử vong do nguyên nhân tim mạch và nhồi máu cơ tim giảm nhưng không có ý nghĩa thống kê và giảm có ý nghĩa thống kê về cơn đau thắt ngực, đột quỵ, suy tim và đái tháo đường mới khởi phát (p<0,05). Ngược lại, 25 nghiên cứu mù đôi (129 697 trong tổng số 147 020 bệnh nhân) cho thấy không có giảm tử vong chung, tử vong tim mạch hay nhồi máu cơ tim với tăng không ý nghĩa thống kê cơn đau thắt ngực và giảm không ý nghĩa thống kê các biến cố mạch máu não và giảm có ý nghĩa thống kê nhưng ít rõ rệt hơn về tỷ lệ suy tim và đái tháo đường mới khởi phát (p<0,05). Các phép thử về mối liên quan của đau thắt ngực, đột quỵ, suy tim có ý nghĩa thống kê cho thấy có sự không tương hợp giữa các nghiên cứu nhãn mở và ngẫu nhiên mù đôi. (hình 4)
Các nghiên cứu “nhãn mở” về UCTT – mặc dù chỉ đóng góp 12% bệnh nhân cho phân tích gộp – nhưng đã chứng minh được lợi ích có ý nghĩa thống kê hay khuynh hướng có lợi. Ngược lại, trong các nghiên cứu ngẫu nhiên mù đôi tiến cứu – đo lường hiệu quả thật sự của thuốc và được xem là tiêu chuẩn vàng phương pháp học không bị hạn chế bởi các sai số52 – lợi ích tim mạch hầu như biến mất hoặc giảm đi rõ rệt. Đây là một bằng chứng rõ ràng cho thấy các nghiên cứu nhãn mở có khả năng sai số cao – ngay cả sử dụng các tiêu chí chính như tử vong – như nhóm Cochrane đã nêu ra 53. Thay vì góp phần cho “dựa trên bằng chứng” thì nghiên cứu nhãn mở lại góp phần cho “sai lệch bằng chứng”. Những sai số có nhiều nguyên nhân (i) vai trò của thay đổi ngẫu nhiên (ii) hiệu quả tiềm tàng khác nhau trên từng nhóm chủng tộc khi chọn vào nghiên cứu nhãn mở so với nghiên cứu mù đôi (iii) những khác biệt tinh tế trong các điều trị đi cùng hay nghiên cứu viên thường xảy ra trong nghiên cứu nhãn mở (iv) phương pháp thống kê yếu hơn khi xác định khác biệt, báo cáo, chấp thuận, tính toán tiêu chí chính của nghiên cứu – trong đó nguyên nhân (iii) & (iv) thường xảy ra nhất. Vì liên quan đến khả năng sai lệch trong các nghiên cứu nhãn mở nên nghiên cứu JIKEI-Heart 55 bị rút lại do “dữ liệu HA không đáng tin cậy” và nghiên cứu KYOTO cũng vậy khi “có vấn đề quan trọng với một số dữ liệu báo cáo”56 – cả hai nghiên cứu này đều thực hiện với UCTT Valsartan.
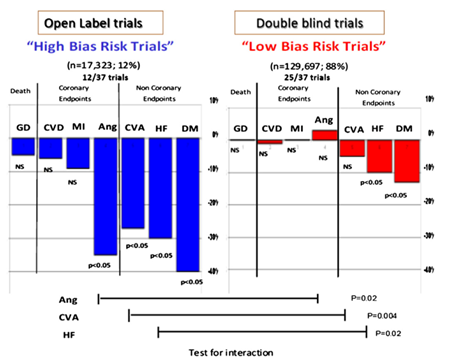
Hình 4 – Nguy cơ tương đối của tử vong chung, tử vong do nguyên nhân tim mạch, nhồi máu cơ tim, đau thắt ngực, biến cố mạch máu não, suy tim và đái tháo đường trong nhóm UCTT so với các thuốc khác trong các nghiên cứu “nguy cơ sai số cao”so với các nghiên cứu “nguy cơ sai số thấp” (theo Bangalore và cs. BMJ 2011;342:d2234). Nghiên cứu nhãn mở: Ecost, Ecost R, HJ-Create, I-Preserve, Jikei, Kondo, Kyoto, Moses, Rass, Road, Suzuki, Takahushi; Double Blind trials: Case J, Charm, Elite, Gissi AF, IDNT, Irma-2, Life,Navigator, Ontarget, Optimal, Profess, Renaal, Scope, Transcend, Val-Heft, Valiant, Value.
Kết luận
Các phân tích gộp song song về UCMC và UCTT có đối chứng với giả dược hay các thuốc khác và các phân tích gộp hồi cứu có hiệu chỉnh với huyết áp đã chứng minh rõ ràng và hằng định được rằng UCMC giảm nguy cơ nhồi máu cơ tim và tử vong dựa trên và độc lập với hiệu quả hạ áp, trong khi UCTT thì không – điều này gọi là “nghịch lý về nhồi máu cơ tim của thuốc UCTT”. Lợi ích này hằng định trong các dân số nguy cơ cao khác nhau như tăng huyết áp, đái tháo đường, bệnh lý mạch máu và suy tim. Sự thật này bị che lấp bởi những nghiên cứu nhãn mở có nguy cơ sai số cao, những nghiên cứu với thiết kế thống kê kiểu “không thua kém hơn” dễ bị hiểu lầm là “tương đương” và các nghiên cứu “hồi cứu trên dân số thuần tập” lại được giới thiệu như “kinh nghiệm cuộc sống thật” mà có thể bác bỏ những phát hiện từ thử nghiệm ngẫu nhiên mù đôi.
Nếu các khuyến cáo lâm sàng nhận thấy được lợi ích bảo vệ tim mạch duy nhất của thuốc UCMC và thuốc ức chế hệ RAAS nên ưu tiên lựa chọn là UCMC hơn là UCTT thì hiệu quả “cứu mạng” sẽ đạt được nhiều hơn.
TÀI LIỆU THAM KHẢO
1. Blood pressure-dependent and independent effects of agents that inhibit the renin–angiotensin system. J Hypertens. 2007;25(5):951-958.
2. Sarafidis PA, Stafylas PC, Kanaki AI, Lasaridis AN. Effects of renin–angiotensin system blockers on renal outcomes and all-cause mortality in patients with diabetic nephropathy: an updated meta-analysis. Am J Hypertens. 2008;21(8):922-929.
3. Pfeffer MA, McMurray JJ, Velazquez EJ, et al. Valsartan, captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both.
N Engl J Med. 2003;349(20):1893-1906.
4. Strauss MH, Hall AS. Angiotensin receptor blockers may increase risk of myocardial infarction: unraveling the ARB-MI paradox. Circulation. 2006;114(8):838-854.
5. Daskalopoulou SS, Khan NA, Quinn RR, et al. The 2012 Canadian hypertension education program recommendations for the management of hypertension: blood pressure measurement, diagnosis, assessment of risk, and therapy. Can J Cardiol. 2012;28(3):270-287.
6. American Diabetes Association. Standards of medical care — 2013. Diabetes Care. 2013:S11-S56.
7. Mancia G, Fagard R, Narkiewicz K, et al. 2013 ESH/ESC guidelines for the management of arterial hypertension: the Task Force for the Management of Arterial Hypertension of the European Society of Hypertension (ESH) and of the
European Society of Cardiology (ESC). Eur Heart J. 2013;34(28): 2159-2219.
8. Savarese G, Costanzo P, Cleland JG, et al. A meta-analysis reporting effects of angiotensin-converting enzyme inhibitors and angiotensin receptor blockers in patients without heart failure. J Am Coll Cardiol. 2013;61(2):131-142.
9. Bangalore S, Kumar S, Wetterslev J, Messerli FH. Angiotensin receptor blockers and risk of myocardial infarction: meta-analyses and trial sequential analyses of 147 020 patients from randomised trials. BMJ. 2011;342:d2234.
10. ElgendyIY,HuoT,ChikV,PepineCJ,BavryAA.Efficacyandsafety of angiotensin receptor blockers in older patients: a meta-analysis of randomized trials. Am J Hypertens. 2015;28(5):576-585.
11. Verdecchia P, Reboldi G, Angeli F, et al. Angiotensin-converting enzyme inhibitors and calcium channel blockers for coronary heart disease and stroke prevention. Hypertension. 2005;46(2):386-392.
12. Lewington S, Clarke R, Qizilbash N, Peto R, Collins R. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet. 2002;360(9349):1903-1913.
13. Law MR, Morris JK, Wald NJ. Use of blood pressure lowering drugs in the prevention of cardiovascular disease: meta-analysis of 147 randomised trials in the context of expectations from prospective epidemiological studies. BMJ. 2009;338:b1665.
14. van Vark LC, Bertrand M, Akkerhuis KM, et al. Angiotensin-converting enzyme inhibitors reduce mortality in hypertension: a meta-analysis of randomized clinical trials of renin–angiotensin–aldosterone system inhibitors involving 158 998 patients. Eur Heart J. 2012;33(16):2088-2097.
15. Verma S, Strauss M. Angiotensin receptor blockers and myocardial infarction. BMJ. 2004;329(7477):1248-1249.
16. Julius S, Kjeldsen SE, Weber M, et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial. Lancet. 2004;363(9426):2022-2031.
17. Granger CB, McMurray JJ, Yusuf S, et al. Effects of candesartan in patients with chronic heart failure and reduced left-ventricular systolic function intolerant to angiotensin-converting-enzyme inhibitors: the CHARM-Alternative trial. Lancet. 2003;362(9386):772-776.
18. Sever PS, Poulter NR, Elliott WJ, et al. Blood pressure reduction is not the only determinant of outcome. Circulation. 2006;113(23):2754-2772.
19. Tsuyuki RT, McDonald MA. Angiotensin receptor blockers do not increase risk of myocardial infarction. Circulation. 2006;114(8):855-860.
20. Volpe M, Tocci G, Sciarretta S, Verdecchia P, Trimarco B, Mancia G. Angiotensin II receptor blockers and myocardial infarction: an updated analysis of randomized clinical trials. J Hypertens. 2009;27(5):941-946.
21. Macia-Heras M, Castillo-Rodrigues N, Gonzalez J. The renin– angiotensin–aldosterone system in renal and cardiovascular disease and the effects of its pharmacological blockade. J Diabetes Metab 12 A.D.; 3(1).
22. Levy BI. Can angiotensin II type 2 receptors have deleterious effects in cardiovascular disease? Implications for therapeutic blockade of the renin–angiotensin system. Circulation. 2004;109(1):8-13.
23. Castro M. Placebo versus best-available-therapy control group in clinical trials for pharmacologic therapies: which is better? Proc Am Thorac Soc. 2007;4(7):570-573.
24. Strauss MH, Hall A. Angiotensin receptor blockers should be regarded as first-line drugs for stroke prevention in both primary and secondary prevention settings: no. Stroke. 2009;40(9):3161-3162.
25. Pitt B, Poole-Wilson PA, Segal R, et al. Effect of losartan compared with captopril on mortality in patients with symptomatic heart failure: randomised trial—the Losartan Heart Failure Survival Study ELITE II. Lancet. 2000;355(9215): 1582-1587.
26. Dickstein K, Kjekshus J. Effects of losartan and captopril on mortality and morbidity in high-risk patients after acute myocardial infarction: the OPTIMAAL randomised trial. Optimal Trial in Myocardial Infarction with Angiotensin II Antagonist Losartan. Lancet. 2002;360(9335):752-760.
27. Pfeffer MA, Braunwald E, Moye LA, et al. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction. Results of the survival and ventricular enlargement trial. The SAVE Investigators.
N Engl J Med. 1992;327(10):669-677.
28. Indications for ACE inhibitors in the early treatment of acute
myocardial infarction: systematic overview of individual data from 100,000 patients in randomized trials. ACE Inhibitor Myocardial Infarction Collaborative Group. Circulation. 1998;97(22):2202-2212.
29. Yusuf S, Teo KK, Pogue J, et al. Telmisartan, ramipril, or both in patients at high risk for vascular events. N Engl J Med. 2008;358(15):1547-1559.
30. Kaul S, Diamond GA. Good enough: a primer on the analysis and interpretation of noninferiority trials. Ann Intern Med. 2006;145(1):62-69.
31. Brugts JJ, van Vark L, Akkerhuis M, et al. Impact of renin–angiotensin system inhibitors on mortality and major cardiovascular endpoints in hypertension: a number-needed-to-treat analysis. Int J Cardiol. 2015;181:425-429.
32. Ryden L, Grant PJ, Anker SD, et al. ESC guidelines on diabetes, pre-diabetes, and cardiovascular diseases developed in collaboration with the EASD: the Task Force on diabetes, pre-diabetes, and cardiovascular diseases of the European Society of Cardiology (ESC) and developed in collaboration with the European Association for the Study of Diabetes (EASD). Eur Heart J. 2013;34(39):3035-3087.
33. Cheng J, Zhang W, Zhang X, et al. Effect of angiotensin-converting enzyme inhibitors and angiotensin II receptor blockers on all-cause mortality, cardiovascular deaths, and cardiovascular events in patients with diabetes mellitus: a meta-analysis. JAMA Intern Med. 2014;174(5):773-785.
34. Patel A, MacMahon S, Chalmers J, et al. Effects of a fixed combination of perindopril and indapamide on macrovascular and microvascular outcomes in patients with type 2 diabetes mellitus (the ADVANCE trial): a randomised controlled trial. Lancet. 2007;370(9590):829-840.
35. Haller H, Ito S, Izzo Jr JL, et al. Olmesartan for the delay or prevention of microalbuminuria in type 2 diabetes. N Engl J Med. 2011;364(10):907-917.
36. Tobe SW, Clase CM, Gao P, et al. Cardiovascular and renal outcomes with telmisartan, ramipril, or both in people at high renal risk: results from the ONTARGET and TRANSCEND studies. Circulation. 2011;123(10):1098-1107.
37. Vejakama P, Thakkinstian A, Lertrattananon D, Ingsathit A, Ngarmukos C, Attia J. Reno-protective effects of renin–angiotensin system blockade in type 2 diabetic patients: a systematic review and network meta-analysis. Diabetologia. 2012;55(3):566-578.
38. Padwal R, Lin M, Eurich DT. The comparative effectiveness of angiotensin-converting enzyme inhibitors and angiotensin II receptor blockers in patients with diabetes. J Clin Hypertens (Greenwich). 2015:1-7.
39. Effects of enalapril on mortality in severe congestive heart failure. Results of the Cooperative North Scandinavian Enalapril Survival Study (CONSENSUS). The CONSENSUS Trial Study Group. N Engl J Med. 1987;316(23):1429-1435.
40. Flather MD, Yusuf S, Kober L, et al. Long-term ACE-inhibitor therapy in patients with heart failure or left-ventricular
dysfunction: a systematic overview of data from individual patients. ACE-Inhibitor Myocardial Infarction Collaborative Group. Lancet. 2000;355(9215):1575-1581.
41. Cohn JN, Tognoni G. A randomized trial of the angiotensin-receptor blocker valsartan in chronic heart failure. N Engl J Med. 2001;345(23):1667-1675.
42. Pfeffer MA, Swedberg K, Granger CB, et al. Effects of candesartan on mortality and morbidity in patients with chronic heart failure: the CHARM-Overall programme. Lancet. 2003;362(9386):759-766.
43. Granger BB, Swedberg K, Ekman I, et al. Adherence to candesartan and placebo and outcomes in chronic heart failure in the CHARM programme: double-blind, randomised, controlled clinical trial. Lancet. 2005;366(9502):2005-2011.
44. Yusuf S, Sleight P, Pogue J, Bosch J, Davies R, Dagenais G. Effects of an angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients. The Heart Outcomes Prevention Evaluation Study Investigators. N Engl J Med. 2000;342(3):145-153.
45. Fox KM. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study). Lancet. 2003;362(9386):782-788.
46. Braunwald E, Domanski MJ, Fowler SE, et al. Angiotensin-converting-enzyme inhibition in stable coronary artery disease. N Engl J Med. 2004;351(20):2058-2068.
47. Dagenais GR, Pogue J, Fox K, Simoons ML, Yusuf S. Angiotensin-converting-enzyme inhibitors in stable vascular disease without left ventricular systolic dysfunction or heart failure: a combined analysis of three trials. Lancet. 2006;368(9535):581-588.
48. Yusuf S, Teo K, Anderson C, et al. Effects of the angiotensin-receptor blocker telmisartan on cardiovascular events in high-risk patients intolerant to angiotensin-converting enzyme inhibitors: a randomised controlled trial. Lancet. 2008;372(9644):1174-1183.
49. Yusuf S, Diener HC, Sacco RL, et al. Telmisartan to prevent recurrent stroke and cardiovascular events. N Engl J Med. 2008;359:1225-1237.
50. Smith Jr SC, Benjamin EJ, Bonow RO, et al. AHA/ACCF secondary prevention and risk reduction therapy for patients with coronary and other atherosclerotic vascular disease: 2011 update: a guideline from the American Heart Association and American College of Cardiology Foundation. Circulation. 2011;124(22):2458-2473.
51. Hansson L, Hedner T, Dahlof B. Prospective randomized open blinded end-point (PROBE) study. A novel design for intervention trials. Prospective Randomized Open Blinded End-Point. Blood Press. 1992;1(2):113-119.
52. Kaul S, Diamond GA. Trial and error. How to avoid commonly encountered limitations of published clinical trials. J Am Coll Cardiol. 2010;55(5):415-427.
53. Higgins JP, Altman DG, Gotzsche PC, et al. The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. BMJ. 2011;343:d5928.
54. Kohro T, Yamazaki T. Cardiovascular clinical trials in Japan and controversies regarding prospective randomized open-label blinded end-point design. Hypertens Res. 2009;32(2):109-114.
55. Retraction—Valsartan in a Japanese population with hypertension and other cardiovascular disease (Jikei Heart Study): a randomised, open-label, blinded endpoint morbidity–mortality study. Lancet. 2013;382(9895):843.
56. Sawada T, Yamada H, Dahlof B, Matsubara H. Retraction of: Effects of valsartan on morbidity and mortality in uncontrolled hypertensive patients with high cardiovascular risks: KYOTO HEART Study [Eur Heart J (2009) 30:2461–2469, doi: 10.1093/eurheartj/ehp363]. Eur Heart J. 2013;30:2461-2469.








