TÓM TẮT
Tổng quan
Mức huyết áp tâm thu (HATT) lý tưởng cần đạt nhằm giảm biến chứng và tử vong do bệnh lý tim mạch trên bệnh nhân (BN) không có đái tháo đường (ĐTĐ) hiện nay vẫn chưa rõ.
Người dịch: BS. CAO THỊ LAN HƯƠNG
Phương pháp
Nghiên cứu lâm sàng phân nhóm ngẫu nhiên, gồm 9361 BN có nguy cơ tim mạch cao nhưng không có ĐTĐ với HATT ≥ 130 mmHg; chia làm 2 nhóm, điều trị tích cực hạ HATT xuống dưới 120 mmHg và điều trị chuẩn hạ HATT xuống dưới 140 mmHg.
Tiêu chí đánh giá chính gồm nhồi máu cơ tim, hội chứng mạch vành cấp, đột quỵ, suy tim hoặc tử vong do nguyên nhân tim mạch.
Kết quả
Sau 1 năm, HATT trung bình là 121.4 mmHg ở nhóm điều trị tích cực và 136.2 mmHg ở nhóm điều trị chuẩn. Nghiên cứu kết thúc sớm hơn dự kiến với thời gian theo dõi trung bình 3.26 năm do kết quả ban đầu cho thấy tần suất các biến cố tim mạch chính ở nhóm điều trị tích cực giảm ngoạn mục so với nhóm điều trị chuẩn (1.65% mỗi năm so với 2.19% mỗi năm; tỷ suất rủi ro (HR) cho điều trị tích cực là 0.75; khoảng tin cậy (CI) 95%, 0.64 – 0.89; p<0.001). Tần suất tử vong do mọi nguyên nhân cũng giảm đáng kể ở nhóm điều trị tích cực (HR 0.73; CI 95%, 0.60 – 0.90; p=0.003). Tần suất các biến cố không mong đợi cao hơn ở nhóm điều trị tích cực bao gồm tụt huyết áp, ngất, rối loạn điện giải, tổn thương thận cấp, không bao gồm té ngã gây thương tích.
Kết luận
Chiến lược kiểm soát huyết áp tích cực – hạ HATT xuống dưới 120 mmHg – ở BN có nguy cơ tim mạch cao nhưng không có ĐTĐ, giúp giảm tỷ lệ tử vong do tim mạch, biến cố tim mạch nặng không tử vong và tử vong do mọi nguyên nhân, mặc dù có sự tăng đáng kể tần suất một vài biến cố không mong đợi ở nhóm điều trị tích cực.
ĐẶT VẤN ĐỀ
Tăng huyết áp (THA) ảnh hưởng đến khoảng 1 tỷ người trưởng thành trên toàn thế giới. [1, 2] Đối với người trên 50 tuổi, THA tâm thu đơn thuần là thường gặp nhất. [3, 4] Huyết áp tâm thu quan trọng hơn huyết áp tâm trương và là yếu tố nguy cơ độc lập đối với bệnh mạch vành, đột quỵ, suy tim, và bệnh thận mạn giai đoạn cuối (ESRD). [5-13]
Các thử nghiệm lâm sàng nhận thấy điều trị hạ áp giúp giảm biến cố tim mạch, bao gồm đột quỵ (35-40%), nhồi máu cơ tim (15-25%), và suy tim (lên đến 64%). [5, 15, 16] Tuy nhiên, mục tiêu HATT vẫn chưa được xác định rõ. Nhiều nghiên cứu quan sát cho thấy nguy cơ tim mạch tăng dần khi HATT tăng trên 115 mmHg, [10] nhưng bằng chứng từ các thử nghiệm lâm sàng ngẫu nhiên có đối chứng trên BN có THA trong dân số chung chỉ ghi lại lợi ích của việc hạ HATT xuống dưới 150 mmHg, với dữ liệu hạn chế về mục tiêu huyết áp. [11, 17-21] Trong một nghiên cứu trên BN có ĐTĐ type 2, tần suất các biến cố tim mạch chính tương đương nhau giữa mục tiêu HATT dưới 120 mmHg và HATT dưới 140 mmHg, mặc dù tần suất đột quỵ thấp hơn ở nhóm có HATT dưới 120 mmHg. [22] Một nghiên cứu gần đây trên BN có tiền căn đột quỵ được hạ HATT xuống dưới 130 mmHg so với việc chỉ hạ HATT xuống dưới 150 mmHg, ghi nhận không có lợi ích đáng kể của việc hạ thấp mục tiêu huyết áp trên các rủi ro tổng thể khác của đột quỵ nhưng lại có lợi ích đáng kể lên các nguy cơ của đột quỵ xuất huyết. [23]
Năm 2007, Ban khoa học của Viện Tim – Phổi – Máu Quốc gia đưa ra giả thuyết rằng hạ thấp mục tiêu huyết áp (vd, < 120 mmHg) sẽ giúp giảm các biến cố lâm sàng nhiều hơn so với mục tiêu HATT chuẩn ở những BN THA không kèm ĐTĐ. [24] Bài viết này trình bày các kết quả chính của nghiên cứu SPRINT, so sánh lợi ích của việc hạ HATT xuống dưới 120 mmHg so với mục tiêu cũ là dưới 140 mmHg.
QUY TRÌNH THỰC HIỆN NGHIÊN CỨU
Thiết kế nghiên cứu và quy trình giám sát
SPRINT là thử nghiệm lâm sàng phân nhóm ngẫu nhiên, có đối chứng, nhãn mở được tiến hành tại 102 trung tâm lâm sàng (tổ chức thành 5 mạng lưới trung tâm chính) ở Hoa Kỳ và Puerto Rico. Một trung tâm điều phối phụ trách phân tích dữ liệu và giám sát các phòng thí nghiệm, trung tâm đọc điện tâm đồ, trung tâm đọc hình ảnh cộng hưởng từ, và trung tâm phân phối thuốc. Cơ sở lý luận và quy trình thực hiện của nghiên cứu được công bố công khai, [25, 26] tại trang web NEJM.org.
SPRINT được tài trợ bởi Viện Tim – Phổi – Máu Quốc gia, và đồng tài trợ bởi Viện Đái tháo đường – Tiêu hóa – Thận Quốc gia, Viện Rối loạn thần kinh – Đột quỵ Quốc gia, và Viện Lão khoa Quốc gia. Dữ liệu và kết quả của nghiên cứu được phân tích và giám sát hoàn toàn độc lập. Mỗi trung tâm lâm sàng tham gia nghiên cứu đều được sự chấp thuận của hội đồng xét duyệt. Ban chỉ đạo thiết kế nghiên cứu, thu thập dữ liệu (hợp tác với ban điều tra ở các đơn vị nghiên cứu khác) nộp bản thảo xuất bản và chứng từ xác minh tính trung thực của quy trình thực hiện nghiên cứu. Ban biên tập viết bản thảo và chứng từ xác minh sự chuẩn xác và đầy đủ của bộ dữ liệu và bộ phân tích dữ liệu. Các trung tâm điều phối chịu trách nghiệm phân tích dữ liệu. Các nhà khoa học ở Viện Sức khỏe Quốc gia tham gia thiết kế nghiên cứu và có một phiếu biểu quyết trong hội đồng điều hành nghiên cứu.
Dân số nghiên cứu
Tiêu chuẩn chọn mẫu (đáp ứng tất cả các tiêu chí): ≥ 50 tuổi, HATT từ 130 đến 180 mmHg, có nguy cơ tim mạch cao. Nguy cơ tim mạch cao khi BN có ít nhất 1 trong các yếu tố sau: có bệnh lý tim mạch trên lâm sàng hay dưới lâm sàng ngoài đột quỵ; bệnh thận mạn, ngoại trừ bệnh thận đa nang, độ lọc cầu thận ước tính (eGFR) từ 20 đến dưới 60 ml/phút/1.73 m2, tính theo công thức MDRD; nguy cơ tim mạch 10 năm theo Framingham ≥ 15%; hoặc BN ≥ 75 tuổi. BN có ĐTĐ hay tiền căn đột quỵ được loại trừ.
Cách thức tiến hành phân bố ngẫu nhiên và can thiệp
BN đáp ứng đủ tiêu chí chọn mẫu được phân ngẫu nhiên vào 2 nhóm, nhóm có mục tiêu hạ áp xuống dưới 140 mmHg (nhóm điều trị chuẩn) và nhóm có mục tiêu hạ áp xuống dưới 120 mmHg (nhóm điều trị tích cực). Cách phân nhóm ngẫu nhiên tùy vào mỗi trung tâm lâm sàng. BN và bác sĩ biết được thiết kế trong nhóm nguyên cứu nhưng người xử lý kết quả thì không.
Sau khi phân nhóm ngẫu nhiên BN, phác đồ điều trị được áp dụng tương tự như nghiên cứu ACCORD. [22] Tất cả các nhóm thuốc hạ áp đều được đưa vào danh mục thuốc và cấp miễn phí cho BN. Các bác sĩ có thể kê thuốc hạ áp ngoài danh mục thuốc của nghiên cứu. Nghiên cứu khuyến khích sử dụng các nhóm thuốc có bằng chứng mạnh mẽ giảm biến cố tim mạch, bao gồm lợi tiểu Thiazide (lựa chọn hàng đầu), lợi tiểu quai (BN có bệnh thận mạn tiến triển), và chẹn β (BN có bệnh mạch vành). [5, 27] Trong nhóm Thiazide, Chlorthalidone được khuyến khích dùng và Amlodipine được ưu tiên trong nhóm ức chế Canxi. [28, 29] Azilsartan và Azilsartan phối hợp Chlorthalidone được tài trợ bởi Hãng dược Quốc tế Takeda và Arbor; cả 2 công ty đều không có bất cứ vai trò gì trong nghiên cứu.
BN được theo dõi mỗi tháng trong 3 tháng đầu và mỗi 3 tháng sau đó. Ở nhóm điều trị tích cực, BN được điều chỉnh thuốc mỗi tháng để đạt HATT dưới 120 mmHg. Với nhóm điều trị chuẩn, thuốc được điều chỉnh để duy trì HATT từ 135 đến 139 mmHg, và giảm liều nếu HATT dưới 130 mmHg trong 1 lần tái khám, hoặc HATT dưới 135 mmHg ở 2 lần tái khám liên tiếp. Liều điều chỉnh dựa vào HATT trung bình sau 3 lần đo huyết áp ở tư thế ngồi và BN được nghỉ 5 phút; dụng cụ đo là máy đo huyết áp tự động (Đời 907, hãng Omron Healthcare). Điều chỉnh lối sống luôn được khuyến khích và là một phần của chiến lược điều trị. Việc duy trì tham gia nghiên cứu và tuân thủ điều trị luôn được kiểm tra định kỳ. [26]
Phương pháp thu thập số liệu
Dữ liệu nhân khẩu học được thu thập tại thời điểm tham gia nghiên cứu. Dữ liệu lâm sàng và cận lâm sàng được thu thập lúc bắt đầu tham gia nghiên cứu và mỗi 3 tháng sau đó. Phỏng vấn theo mẫu được sử dụng trong cả 2 nhóm mỗi 3 tháng để báo cáo các biến cố bệnh lý tim mạch. Mặc dù người phỏng vấn biết được thiết kế nghiên cứu của nhóm, họ vẫn sử dụng cùng một mẫu phỏng vấn cho cả 2 nhóm để giảm sai số. Hồ sơ bệnh án và điện tâm đồ được ghi lại khi có biến cố. Bất cứ khi nào có trường hợp tử vong, một quy trình chuẩn sẽ được sử dụng để thu thập thông tin của biến cố này.
Các biến cố nguy hiểm gồm tử vong hay đe dọa tính mạng, tàn tật nặng hay vĩnh viễn, cần nằm viện dài ngày, hay cần can thiệp phẫu thuật. [30, 31] Các tình trạng lâm sàng được đánh giá khi BN nhập khoa cấp cứu cũng được xếp vào biến cố nặng gồm: tụt huyết áp, ngất, té ngã gây thương tích, rối loạn điện giải, và nhịp chậm. Sự xuất hiện của tổn thương thận cấp cũng được ghi nhận tại thời điểm nhập viện hoặc trong thời gian nằm viện và trong chẩn đoán xuất viện. Ban an toàn nghiên cứu sẽ xem xét có điều trị can thiệp tiếp tục ở mỗi biến cố nguy hiểm hay không.
Tiêu chí đánh giá
Tiêu chí đánh giá chính bao gồm nhồi máu cơ tim, hội chứng vành cấp không dẫn đến nhồi máu cơ tim, đột quỵ, suy tim cấp mất bù, hay tử vong do nguyên nhân tim mạch. Tiêu chí đánh giá phụ bao gồm các tiêu chí chính và tần suất tử vong do mọi nguyên nhân, tần suất cộng dồn của tiêu chí chính và tử vong do mọi nguyên nhân.
SPRINT cũng đánh giá biến cố trên thận và sử dụng định nghĩa khác nhau cho BN đã có bệnh thận mạn (eGFR < 60 ml/phút/1.73 m2) và những BN không có bệnh thận mạn tại thời điểm bắt đầu tham gia nghiên cứu. Biến cố trên thận ở BN có tiền căn bệnh thận mạn bao gồm sự sụt giảm eGFR trên 50% (dựa vào xét nghiệm creatinine máu) hoặc tiến triển đến ESRD cần lọc thận dài hạn hay ghép thận. Ở những BN không có bệnh thận mạn trước đó, biến cố trên thận được xác định khi có sự sụt giảm eGFR trên 30% hoặc eGFR giảm dưới 60 ml/phút/1.73 m2. Xuất hiện albumine niệu được xác định khi tăng gấp đôi tỷ số albumin niệu (mg)/creatinine niệu (g) từ giá trị dưới 10 ở thời điểm ban đầu lên trên 10 trong thời gian theo dõi đối với tất cả BN tham gia nghiên cứu, cũng được xếp vào biến cố thận.
Phân tích phân nhóm bao gồm có/không bệnh lý tim mạch tại thời điểm tham gia nghiên cứu, có/không bệnh thận mạn tại thời điểm tham gia nghiên cứu, giới tính, chủng tộc (da đen/da trắng), tuổi (< 75 và ≥ 75), HATT tại thời điểm tham gia nghiên cứu với 3 mức độ (≤ 132 mm Hg, > 132 đến < 145 mmHg, và ≥ 145 mmHg). SPRINT cũng so sánh hiệu quả hạ áp trên chứng mất trí nhớ, thay đổi nhận thức, và bệnh lý mạch máu nhỏ ở não.
KẾT QUẢ NGHIÊN CỨU
Dân số nghiên cứu
Tổng cộng nghiên cứu tuyển vào 9361 BN từ tháng 10/2010 đến tháng 03/2013 với các đặc điểm được trình bày ở bảng 1. Ngày 20 tháng 8 năm 2015, ban điều hành NHLBI quyết định ngừng nghiên cứu trước thời hạn, sau khi có kết quả phân tích các tiêu chí chính tại 2 thời điểm liên tiếp cho thấy sự giảm ngoạn mục các biến cố tim mạch ở nhóm điều trị tích cực. Tính đến ngày 20 tháng 8/2015 thì thời gian theo dõi trung bình là 3.26 năm, thay vì 5 năm như hoạch định.
|
Bảng 1: Đặc điểm cơ bản của dân số nghiên cứu * |
||
|
ĐẶC ĐIỂM |
ĐIỀU TRỊ TÍCH CỰC (N = 4678) |
ĐIỀU TRỊ CHUẨN (N = 4683) |
|
Tiêu chuẩn xếp loại nguy cơ cao tim mạch – n (%) † |
||
|
Tuổi ≥ 75 |
1317 (28.2) |
1319 (28.2) |
|
Bệnh thận mạn ‡ |
1330 (28.4) |
1316 (28.1) |
|
Bệnh tim mạch |
940 (20.1) |
937 (20.0) |
|
Lâm sàng |
779 (16.7) |
783 (16.7) |
|
Dưới lâm sàng |
247 (5.3) |
246 (5.3) |
|
Nguy cơ tim mạch 10 năm theo Framingham ≥ 15% |
2870 (36.0) |
2867 (61.2) |
|
Giới nữ – n (%) |
1684 (36.0) |
1648 (35.2) |
|
Tuổi (năm) |
|
|
|
Tổng thể |
67.9 ± 9.4 |
67.9 ± 9.5 |
|
≥ 75 tuổi |
79.8 ± 3.9 |
79.9 ± 4.1 |
|
Chủng tộc hay sắc tộc – n (%) |
|
|
|
Người da đen không phải gốc Tây Ban Nha |
1379 (29.5) |
1423 (30.4) |
|
Người Tây Ban Nha gốc |
503 (10.8) |
481 (10.3) |
|
Người da trắng không phải gốc Tây Ban Nha |
2698 (57.7) |
2701 (57.7) |
|
Khác |
98 (2.1) |
78 (1.7) |
|
Người da đen § |
1454 (31.1) |
1493 (31.9) |
|
Huyết áp lúc tham gia nghiên cứu – mmHg |
|
|
|
Huyết áp tâm thu (HATT) |
139.7 ± 15.8 |
139.7 ± 15.4 |
|
Huyết áp tâm trương (HATTr) |
78.2 ± 11.9 |
78.0 ± 12.0 |
|
Sự phân bố HATT – n (%) |
|
|
|
≤ 132 mmHg |
1583 (33.8) |
1553 (33.2) |
|
> 132 mmHg đến < 145 mmHg |
1489 (31.8) |
1489 (31.8) |
|
≥ 145 mmHg |
1606 (34.3) |
1581 (33.8) |
|
Creatinine huyết thanh – mg/dL |
1.07 ± 0.34 |
1.08 ± 0.34 |
|
eGFR – ml/phút/1.73 m2 |
|
|
|
Toàn bộ BN |
71.8 ± 20.7 |
71.7 ± 20.5 |
|
BN có eGFR ≥ 60 ml/phút/1.73 m2 |
81.3 ± 15.5 |
81.1 ± 15.5 |
|
BN có eGFR < 60 ml/phút/1.73 m2 |
47.8 ± 9.5 |
47.9 ± 9.5 |
|
Tỷ số albumin niệu (mg) / creatinine niệu (g) |
44.1 ± 178.7 |
41.1 ± 152.9 |
|
Cholesterol toàn phần — mg/dl |
190.2 ± 41.4 |
190.0 ± 40.9 |
|
HDL cholesterol — mg/dl |
52.9 ± 14.3 |
52.8 ± 14.6 |
|
Triglycerides — mg/dl |
124.8 ± 85.8 |
127.1 ± 95.0 |
|
Đường huyết đói – mg/dl |
98.8 ± 13.7 |
98.8 ± 13.4 |
|
Có sử dụng statin – n/N (%) |
1978/4645 (42.6) |
2076/4640 (44.7) |
|
Có sử dụng aspirin – n/N (%) |
2406/4661 (51.6) |
2350/4666 (50.4) |
|
Hút thuốc lá – n (%) |
|
|
|
Chưa bao giờ hút |
2050 (43.8) |
2072 (44.2) |
|
Đã từng hút |
1977 (42.3) |
1996 (42.6) |
|
Đang hút |
639 (13.7) |
601 (12.8) |
|
Mất dữ liệu |
12 (0.3) |
14 (0.3) |
|
Nguy cơ tim mạch 10 năm theo Framingham – % |
20.1 ± 10.9 |
20.1 ± 10.8 |
|
BMI ‖ |
29.9 ± 5.8 |
29.8 ± 5.7 |
|
Số thuốc hạ áp – n/BN |
1.8 ± 1.0 |
1.8 ± 1.0 |
|
Không dùng thuốc hạ áp – n (%) |
432 (9.2) |
450 (9.6) |
|
* Không có sự khác biệt có ý nghĩa (p<0.05) giữa 2 nhóm, ngoại trừ việc sử dụng statin (p=0.04). Để chuyển đổi đơn vị của creatinine sang µmol/L thì nhân với 88.4. Để chuyển đổi đơn vị của cholesterol sang mmol/L thì nhân với 0.01129. Để chuyển đổi đơn vị của đường huyết sang mmol/L thì nhân với 0.05551. GFR là độ lọc cầu thận. † Nguy cơ tim mạch cao là một trong những tiêu chí tuyển vào nghiên cứu. ‡ Bệnh thận mạn được định nghĩa là khi eGFR < 60 ml/phút/1.73 m2 § Sắc tộc da đen bao gồm người da đen gốc Tây Ban Nha và cả người da đen đa chủng tộc khác. ‖ Chỉ số khối cơ thể (BMI) được tính bằng cân nặng (kg) chia cho chiều cao (m) bình phương. |
||
Huyết áp
Sau 1 năm, HATT trung bình là 121.4 mmHg ở nhóm điều trị tích cực và 136.2 mmHg ở nhóm điều trị chuẩn, khác biệt trung bình là 14.8 mmHg. Huyết áp tâm trương (HATTr) trung bình sau 1 năm là 68.7 mmHg ở nhóm điều trị tích cực và 76.3 mmHg ở nhóm điều trị chuẩn (Hình 1).
Sau 3.26 năm theo dõi, HATT trung bình là 121.5 mmHg ở nhóm điều trị tích cực và 134.6 mmHg ở nhóm điều trị chuẩn, và số thuốc hạ áp trung bình được sử dụng cho 2 nhóm lần lượt là 2.8 và 1.8. Sự phân bố các nhóm thuốc hạ áp tương đối giống nhau ở 2 nhóm, mặc dù xét trên từng nhóm thì số thuốc dùng trong nhóm điều trị tích cực là nhiều hơn (Hình 1).
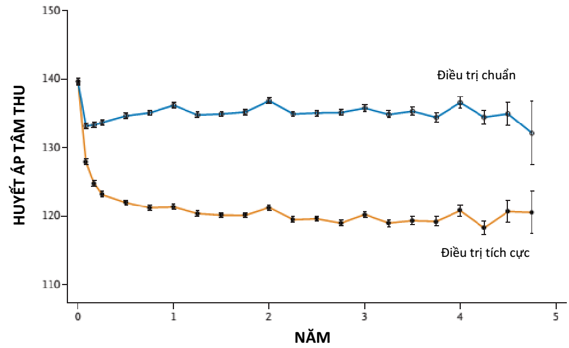
Hình 1. Huyết áp tâm thu giữa 2 nhóm điều trị trong SPRINT
Kết quả lâm sàng
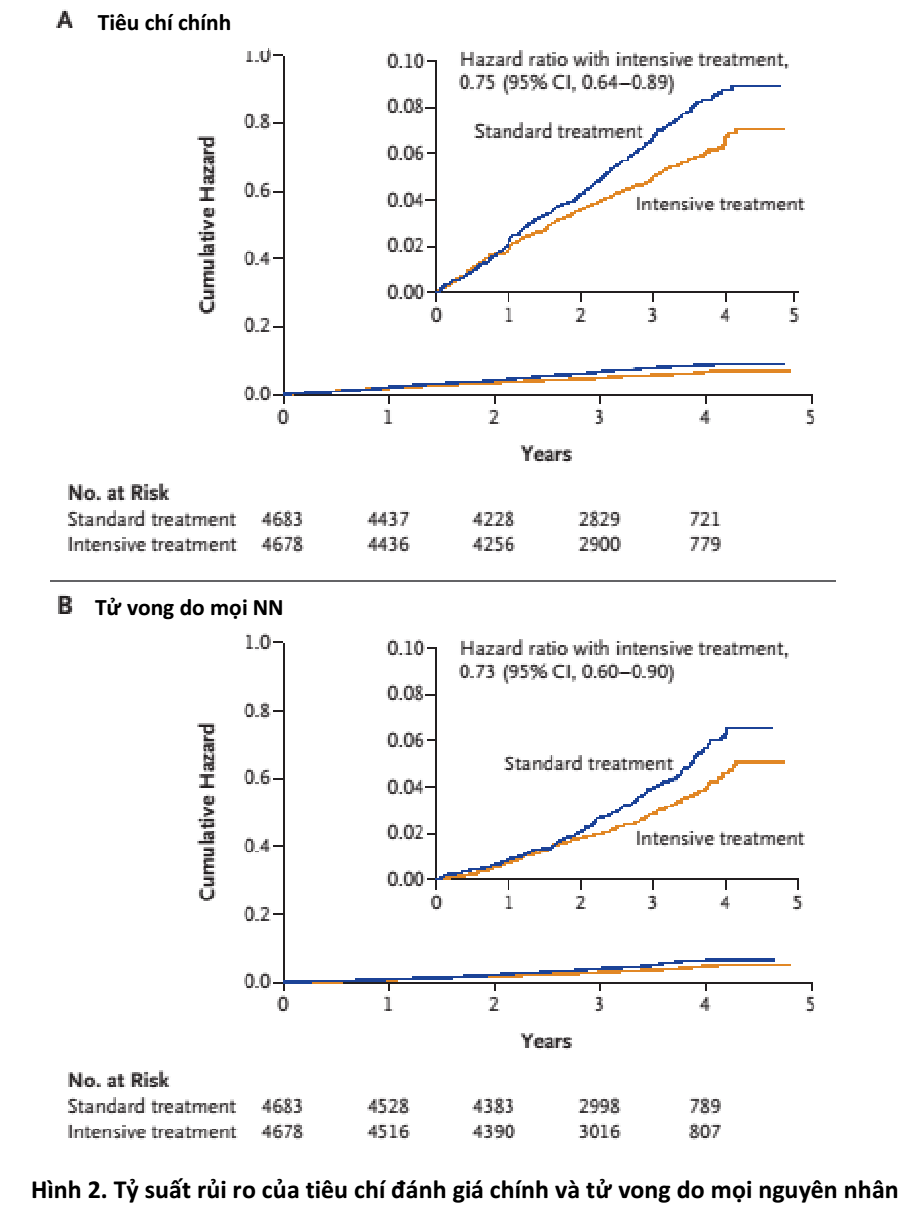
Biến cố tim mạch chính xảy ra trên 562 BN – 243 người (1.65%/năm) ở nhóm điều trị tích cực và 319 người (2.19%/năm) ở nhóm điều trị chuẩn (tỷ suất rủi ro (HR) cho điều trị tích cực là 0.75; khoảng tin cậy (CI) 95%, 0.64 – 0.89; p<0.001) (Bảng 2). Sự tách biệt rõ ràng giữa 2 nhóm ở thời điểm 1 năm (Hình 2A). Các tiêu chí chính khác và các tiêu chí phụ cũng khác biệt rõ giữa 2 nhóm.
Tổng cộng có 365 trường hợp tử vong – 155 ở nhóm điều trị tích cực và 210 ở nhóm điều trị chuẩn (HR 0.73; CI 95%, 0.60 – 0.90; p=0.003). Sự tách biệt rõ ràng giữa 2 nhóm ở thời điểm 2 năm (Hình 2B). Nguy cơ tử vong tương đối do nguyên nhân tim mạch là 43% thấp hơn ở nhóm điều trị tích cực so với nhóm điều trị chuẩn (p=0.005) (Bảng 2).
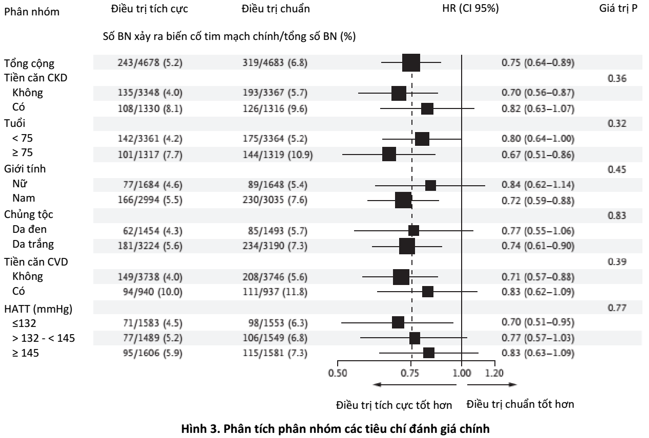
Số người cần điều trị để giảm 1 biến cố chính, tử vong do mọi nguyên nhân và tử vong do nguyên nhân tim mạch trong thời gian theo dõi 3.26 năm là 61, 90 và 172. Hiệu quả của điều trị tích cực trên tần suất các biến cố chính và tần suất tử vong do mọi nguyên nhân bền vững trong phân tích phân nhóm và không có tương quan có ý nghĩa giữa các phân nhóm trong cùng 1 nhóm (Hình 3). Khi tử vong được xét là yếu tố cạnh tranh trong mô hình Fine-Gray, kết quả của các tiêu chí chính nhìn chung là không khác biệt (HR 0.76; CI 95%, 0.64 – 0.89).
Ở những BN đã có bệnh thận mạn khi tuyển vào nghiên cứu, không có sự khác biệt có ý nghĩa về mức giảm eGFR trên 50% hay tiến tiến đến ESRD, mặc dù con số này khá nhỏ (Bảng 2). Ở những BN không có bệnh thận mạn khi tham gia nghiên cứu, tần suất xảy ra biến cố thận (eGFR giảm trên 30% hay giảm xuống dưới 60 ml/phút/1.73 m2) cao hơn ở nhóm điều trị tích cực so với nhóm điều trị chuẩn (1.21%/năm so với 0.35%/năm; HR 3.49; CI 95%, 2.44 – 5.10; p<0.001).
|
Bảng 2. Các tiêu chí đánh giá chính, phụ và biến cố trên thận |
||||||
|
Kết quả |
Điều trị tích cực |
Điều trị chuẩn |
HR (CI 95%) |
P |
||
|
|
Số BN (%) |
%/năm |
Số BN (%) |
%/năm |
|
|
|
Dân số nghiên cứu |
(N=4678) |
(N=4683) |
|
|
||
|
Tiêu chí chính † |
243 (5.2) |
1.65 |
319 (6.8) |
2.19 |
0.75 (0.64–0.89) |
<0.001 |
|
Tiêu chí phụ |
|
|
|
|
|
|
|
Nhồi máu cơ tim |
97 (2.1) |
0.65 |
116 (2.5) |
0.78 |
0.83 (0.64–1.09) |
0.19 |
|
Hội chứng vành cấp |
40 (0.9) |
0.27 |
40 (0.9) |
0.27 |
1.00 (0.64–1.55) |
0.99 |
|
Đột quỵ |
62 (1.3) |
0.41 |
70 (1.5) |
0.47 |
0.89 (0.63–1.25) |
0.50 |
|
Suy tim |
62 (1.3) |
0.41 |
100 (2.1) |
0.67 |
0.62 (0.45–0.84) |
0.002 |
|
Tử vong do nguyên nhân tim mạch |
37 (0.8) |
0.25 |
65 (1.4) |
0.43 |
0.57 (0.38–0.85) |
0.005 |
|
Tử vong do mọi nguyên nhân |
155 (3.3) |
1.03 |
210 (4.5) |
1.40 |
0.73 (0.60–0.90) |
0.003 |
|
Tiêu chí chính hay tử vong |
332 (7.1) |
2.25 |
423 (9.0) |
2.90 |
0.78 (0.67–0.90) |
<0.001 |
|
BN đã có bệnh thận mạn lúc tuyển vào nghiên cứu |
(N=1330) |
(N=1316) |
|
|
||
|
Biến cố cộng dồn ở thận ‡ |
14 (1.1) |
0.33 |
15 (1.1) |
0.36 |
0.89 (0.42–1.87) |
0.76 |
|
eGFR giảm ≥ 50% § |
10 (0.8) |
0.23 |
11 (0.8) |
0.26 |
0.87 (0.36–2.07) |
0.75 |
|
Lọc thận dài hạn |
6 (0.5) |
0.14 |
10 (0.8) |
0.24 |
0.57 (0.19–1.54) |
0.27 |
|
Ghép thận |
0 |
|
0 |
|
|
|
|
Tiểu Albumin ¶ |
49/526 (9.3) |
3.02 |
59/500 (11.8) |
3.90 |
0.72 (0.48–1.07) |
0.11 |
|
BN không có bệnh thận mạn lúc tuyển vào nghiên cứu ‖ |
(N=3332) |
(N=3345) |
|
|
||
|
eGFR giảm ≥ 30% hay < 60 ml/phút/1.73 m2 § |
127 (3.8) |
1.21 |
37 (1.1) |
0.35 |
3.49 (2.44–5.10) |
<0.001 |
|
Tiểu Albumin ¶ |
110/1769 (6.2) |
2.00 |
135/1831 (7.4) |
2.41 |
0.81 (0.63–1.04) |
0.10 |
|
† Tiêu chí chính bao gồm nhồi máu cơ tim, hội chứng vành cấp, đột quỵ, suy tim, hoặc tử vong do nguyên nhân tim mạch. ‡ Biến cố cộng dồn ở thậnở những BN đã có bệnh thận mạn lúc tuyển vào nghiên cứu được tính khi eGFR giảm trên 50% hay tiến triển đến cần lọc thận dài hạn hay ghép thận § Độ giảm eGFR được xác định dựa vào đánh giá eGFR lần 2 ít nhất 90 ngày sau đó. ¶ Tiểu albumine được xác định khi tăng gấp đôi tỷ số albumine niệu (mg)/creatinine niệu (g) từ giá trị dưới 10 ở thời điểm ban đầu tăng lên trên 10 trong thời gian theo dõi. Mẫu số chính là số BN không có đạm niệu lúc tuyển vào nghiên cứu ‖ Ở những BN không có bệnh thận mạn lúc tuyển vào nghiên cứu không ghi nhận trường hợp nào cần lọc thận dài hạn hay cần ghép thận |
||||||
Các biến cố nặng không mong đợi xảy ra ở 1793 người trong nhóm điều trị tích cực (38.3%) và 1736 người trong nhóm điều trị chuẩn (37.1%) (HR của điều trị tích cực là 1.04; p=0.25) (Bảng 3). Các biến cố nặng không mong đợi xảy ra thường hơn ở nhóm điều trị tích cực so với nhóm điều trị chuẩn bao gồm tụt huyết áp, ngất, rối loạn điện giải, tổn thương thận cấp hay suy thận cấp, hay nhịp chậm, không bao gồm té ngã gây thương tích. Tụt huyết áp tư thế được đánh giá trong suốt những lần tái khám lại giảm có ý nghĩa ở nhóm điều trị tích cực. Tổng cộng có 220 người trong nhóm điều trị tích cực (4.7%) và 118 người trong nhóm điều trị chuẩn (2.5%) xảy ra biến cố không mong đợi và được phân thành có khả năng hoặc chắc chắn là do hạ áp tích cực (HR 1.88; p<0.001). Đặc điểm và độ nặng của các biến cố xảy ra giữa 2 nhóm ≥ 75 tuổi và < 75 tuổi là tương tự nhau.
|
Bảng 3. Biến cố không mong đợi |
||||
|
Biến số |
Điều trị tích cực (N = 4678) |
Điều trị chuẩn (N = 4683) |
HR (CI 95%) |
P |
|
|
Số BN (%) |
|
|
|
|
Biến cố nguy hiểm * |
1793 (38.3) |
1736 (37.1) |
1.04 |
0.25 |
|
Tình trạng lâm sàng được đánh giá khi BN nhập khoa cấp cứu |
||||
|
Chỉ xét biến cố nguy hiểm |
||||
|
Tụt huyết áp |
110 (2.4) |
66 (1.4) |
1.67 |
0.001 |
|
Ngất |
107 (2.3) |
80 (1.7) |
1.33 |
0.05 |
|
Nhịp tim chậm |
87 (1.9) |
73 (1.6) |
1.19 |
0.28 |
|
Rối loạn điện giải |
144 (3.1) |
107 (2.3) |
1.35 |
0.02 |
|
Té ngã gây thương tích † |
105 (2.2) |
110 (2.3) |
0.95 |
0.71 |
|
Tổn thương thận cấp ‡ |
193 (4.1) |
117 (2.5) |
1.66 |
<0.001 |
|
Tình trạng lâm sàng được đánh giá khi BN nhập khoa cấp cứu hoặc xảy ra biến cố nguy hiểm |
||||
|
Tụt huyết áp |
158 (3.4) |
93 (2.0) |
1.7 |
<0.001 |
|
Ngất |
163 (3.5) |
113 (2.4) |
1.44 |
0.003 |
|
Nhịp tim chậm |
104 (2.2) |
83 (1.8) |
1.25 |
0.13 |
|
Rối loạn điện giải |
177 (3.8) |
129 (2.8) |
1.38 |
0.006 |
|
Té ngã gây thương tích † |
334 (7.1) |
332 (7.1) |
1.00 |
0.97 |
|
Tổn thương thận cấp ‡ |
204 (4.4) |
120 (2.6) |
1.71 |
<0.001 |
|
Biến cố lâm sàng theo dõi định kỳ |
||||
|
Rối loạn điện giải § |
||||
|
Na máu < 130 mmol/L |
180 (3.8) |
100 (2.1) |
1.76 |
<0.001 |
|
Na máu > 150 mmol/L |
6 (0.1) |
0 |
|
0.02 |
|
K máu < 3.5 mmol/L |
114 (2.4) |
74 (1.6) |
1.50 |
0.006 |
|
K máu > 5.5 mmol/L |
176 (3.8) |
171 (3.7) |
1.00 |
0.97 |
|
Tụt huyết áp tư thế ¶ |
||||
|
Không triệu chứng |
777 (16.6) |
857 (18.3) |
0.88 |
0.01 |
|
Kèm hoa mắt |
62 (1.3) |
71 (1.5) |
0.85 |
0.35 |
|
* Các biến cố nguy hiểm gồm tử vong hay đe dọa tính mạng, tàn tật nặng hay vĩnh viễn, cần nằm viện dài ngày, hay cần can thiệp phẫu thuật. † Té ngã gây thương tích được xác định khi BN nhập khoa cấp cứu hay nhập viện điều trị vì té ngã. ‡ Tổn thương thận cấp hay suy thận cấp được ghi nhận trong chẩn đoán lúc xuất viện và là 1 trong 3 nguyên nhân hàng đầu khiến BN nhập viện và nằm viện kéo dài. Một vài trường hợp tổn thương thận cấp ghi nhận ở khoa cấp cứu khi BN nhập viện vì các lý do khác trong nhóm biến cố lâm sàng quan tâm. § Rối loạn điện giải được phát hiện qua kiểm tra định kỳ hay đột xuất; xét nghiệm cận lâm sàng thường quy được thực hiện mỗi tháng, sau đó hàng quý trong năm đầu, sau đó mỗi 6 tháng. ¶ Tụt huyết áp tư thế được định nghĩa là là tình trạng HATT giảm ít nhất 20 mmHg hoặc HATTr giảm ít nhất 10 mmHg khi đứng trong vòng 1 phút. Tầm soát tụt huyết áp tư thế được thực hiện lúc nhận vào nghiên cứu, 1 tháng, 6 tháng, 12 tháng, và mỗi năm sau đó. BN được hỏi có kèm hoa mắt không mỗi khi đo huyết áp tư thế đứng. |
||||
BÀN LUẬN
Nghiên cứu SPRINT cho thấy ở những BN THA nhưng không có ĐTĐ thì việc hạ HATT xuống dưới 120 mmHg, so với mức hạ áp chuẩn trước đây là dưới 140 mmHg, giúp giảm đáng kể tỷ lệ tử vong do tim mạch, biến cố tim mạch nặng không tử vong và tử vong do mọi nguyên nhân. Nguy cơ tương đối (RR) của các tiêu chí đánh giá chính trong nhóm điều trị tích cực thấp hơn 25% so với nhóm điều trị chuẩn; thêm vào đó, nhóm điều trị tích cực có tỷ lệ xảy ra các biến cố quan trọng khác thấp hơn, bao gồm suy tim (RR 38%), tử vong do mọi nguyên nhân (RR 27%). Trong suốt thời gian theo dõi của nghiên cứu (trung bình là 3.26 năm), số người cần điều trị để ngừa 1 trường hợp xảy ra biến cố chính trong nhóm điều trị tích cực là 61, và số người cần điều trị để ngừa 1 trường hợp tử vong do mọi nguyên nhân là 90. Những lợi ích này tương tự trong các phân tích phân nhóm, kể cả nhóm trên 75 tuổi.
Một phần vì mức giảm eGFR thấp hơn mong đợi và một phần vì nghiên cứu kết thúc sớm, nên số biến cố trên thận khá nhỏ. Xét trên những BN đã có bệnh thận mạn từ trước, số BN giảm eGFR trên 50% hay tiến triển đến ESRD trong quá trình theo dõi không có khác biệt có ý nghĩa giữa 2 nhóm. Xét trên những BN không có bệnh thận mạn trước đó, sự sụt giảm eGFR trên 30% hay eGFR giảm xuống dưới 60 ml/phút/1.73 m2 thường xảy ra hơn ở nhóm điều trị tích cực so với nhóm điều trị chuẩn (1.21%/năm so với 0.35%/năm). Xét trên tất cả những người tham gia nghiên cứu, tổn thương thận cấp thường xảy ra hơn ở nhóm điều trị tích cực so với nhóm điều trị chuẩn (Bảng 3). Sự khác biệt trên biến cố ở thận có thể liên quan đến cơ chế điều hòa ngược đối với huyết động học tại thận khi áp lực dòng máu tưới thận giảm mạnh và tác dụng của thuốc lợi tiểu, ức chế men chuyển và chẹn thụ thể angiotensin ở nhóm điều trị tích cực. [35, 36] Với các dữ liệu hiện có, không có bằng chứng tổn thương thận đáng kể về lâu dài liên quan đến mục tiêu hạ áp; tuy nhiên, khả năng này cũng không thể loại trừ. Cần tiếp tục theo dõi dài hơn và phân tích sâu hơn các kết quả lâm sàng.
Kết quả của SPRINT bổ sung mạnh mẽ bằng chứng về lợi ích của việc hạ áp thấp hơn, đặc biệt ở người lớn tuổi bị THA. Những nghiên cứu tương tự như “Systolic Hypertension in the Elderly Program”, [17] “Systolic Hypertension in Europe”, [11] và “Hypertension in the Very Elderly” [18] cũng cho thấy lợi ích của việc hạ áp xuống dưới 150 mmHg. Tuy nhiên, các thử nghiệm đánh giá lợi ích của mục tiêu HATT thấp hơn mức trên lại không đủ mạnh [19-21] hay không nêu ra mức HATT cụ thể. [37] Một vài quan điểm gây tranh cãi về việc lựa chọn mức HATT lý tưởng bắt nguồn từ những dữ liệu không đầy đủ về cán cân nguy cơ và lợi ích của việc hạ áp dưới 150 mmHg. [11, 17-21, 37] Hiện nay SPRINT cung cấp bằng chứng về lợi ích của việc hạ thấp HATT hơn mức khuyến cáo hiện tại ở hầu hết các đối tượng bị tăng huyết áp.
So sánh giữa SPRINT và ACCORD 22 là không thể tránh khỏi, bởi vì cả 2 đều xem xét các mục tiêu huyết áp giống nhau (< 120 mmHg so với < 140 mmHg). Nhưng ngược lại với phát hiện của SPRINT, các lợi ích trên tim mạch và tử vong quan sát thấy trong ACCORD lại không có ý nghĩa thống kê và sự khác biệt cũng nhỏ. Một số khác biệt quan trọng giữa 2 nghiên cứu này cần được chú ý. ACCORD chỉ tuyển BN THA có kèm ĐTĐ, trong khi SPRINT loại trừ các BN có ĐTĐ; thêm vào đó, cỡ mẫu của ACCORD chỉ bằng phân nửa so với SPRINT (4733 so với 9361). Đối tượng nghiên cứu của SPRINT già hơn (tuổi trung bình là 68, so với 62 trong nghiên cứu ACCORD), với 28% người trên 75 tuổi, và cũng bao gồm người có bệnh thận mạn. ACCORD cho thấy các biến cố tim mạch chính giảm 12% (không có ý nghĩa), với khoảng tin cậy 95%, trong đó có khả năng giảm đến 27%, phù hợp với lợi ích tim mạch quan sát thấy ở SPRINT. ACCORD cũng thiết kế nghiên cứu dư thừa khi gộp cả so sánh giữa điều trị chuẩn và điều trị tích cực trên mục tiêu đường huyết và mỡ máu trong cùng 1 nghiên cứu. Phân tích phân nhóm các kết quả của ACCORD cho thấy, khi so sánh với việc phối hợp kiểm soát đường huyết và huyết áp chuẩn, thì chỉ riêng việc hạ áp tích cực giúp giảm 26% biến cố tim mạch chính mà không có lợi ích thêm vào từ việc phối hợp vừa kiểm soát huyết áp tích cực vừa kiểm soát đường huyết tích cực. [38] Vì vậy, sự khác biệt trong kết quả của 2 nghiên cứu có thể bắt nguồn từ sự khác biệt trong thiết kế nghiên cứu, tương tác điều trị, hay ngẫu nhiên. Lợi ích trên tim mạch của việc hạ áp tích cực giữa dân số có ĐTĐ và dân số không có ĐTĐ có vẻ như chưa rõ nhưng cũng không thể loại trừ.
Trong nghiên cứu “Secondary Prevention of Small Subcortical Strokes” (mục tiêu HATT < 130 mmHg) [23] và trong nghiên cứu ACCORD (mục tiêu HATT < 120 mmHg), mức huyết áp thấp hơn có liên quan đến sự giảm không có ý nghĩa 19% tần suất đột quỵ (p=0.08) và giảm có ý nghĩa 41% tần suất đột quỵ, so với mục tiêu huyết áp cao hơn. Nhóm điều trị tích cực trong SPRINT có sự giảm không có ý nghĩa 11% tần suất đột quỵ, mặc dù SPRINT đã không nhận vào nghiên cứu những BN có tiền căn đột quỵ hay cơn thoáng thiếu máu não thoáng qua.
Trong nghiên cứu SPRINT, có sự khác biệt có ý nghĩa giữa 2 nhóm trên một vài biến cố không mong muốn do can thiệp điều trị. Tụt huyết áp tư thế được đánh giá trong mỗi lần tái khám (Bảng 3) và kết quả cho thấy nhóm điều trị chuẩn thường có tụt huyết áp tư thế hơn (p=0.01), nhưng ngất thường gặp ở nhóm điều trị tích cực hơn (3.5% so với 2.4$, p=0.003), cũng như tụt huyết áp (3.4% so với 2.0%, p<0.001). Không có sự khác biệt giữa 2 nhóm trong biến cố té ngã gây thương tích (HR 1.00; p=0.97). Nhóm điều trị tích cực cũng có tần suất tổn thương thận cấp cao hơn, như đã trình bày ở trên. Đây chính là những biến cố không mong đợi cần phải được cân nhắc so với lợi ích giảm biến cố tim mạch và tử vong ở nhóm hạ áp tích cực.
Điểm mạnh của SPRINT bao gồm cỡ mẫu lớn, sự đa dạng trong dân số nghiên cứu (bao gồm tỷ lệ BN trên 75 tuổi cao), và thành công trên việc đạt được sự tách biệt HATT ở 2 nhóm trong suốt thời gian nghiên cứu. SPRINT thiếu sự khái quát hóa trong dân số, vì BN có ĐTĐ, tiền căn đột quỵ trước đây và người dưới 50 tuổi không được đưa vào nghiên cứu. Và cũng đáng chú ý là SPRINT không tuyển vào những BN lớn tuổi điều trị nội trú trong viện điều dưỡng hay cần chăm sóc hỗ trợ. Ngoài ra, hiệu quả của việc hạ huyết áp thấp hơn trên hệ thần kinh trung ương và thận không thể giải thích một cách hợp lý khi dựa trên phân tích dữ liệu khi nghiên cứu kết thúc.
Các kết quả của SPRINT cung cấp một vài vấn đề quan trọng trong thực hành lâm sàng. Chỉ khoảng 50% dân số chung ở Mỹ đạt mức kiểm soát huyết áp dưới 140/90 mmHg, điều này cho thấy việc kiểm soát huyết áp là một thử thách. [39] SPRINT loại trừ những BN có THA nặng, và kiểm soát HATT xuống dưới 120 mmHg, và trung bình BN cần thêm 1 thuốc hạ áp. Thêm vào đó, HATT trung bình ở nhóm điều trị tích cực chỉ vừa trên 120 mmHg, cho thấy hơn phân nửa BN tham gia nghiên cứu có HATT trên 120 mmHg. Những quan sát cho thấy việc đạt mục tiêu HATT dưới 120 mmHg trên toàn thể dân số bị tăng huyết áp đòi hỏi nhiều yêu cầu và thời gian của cả bác sĩ lẫn BN hơn so với chỉ cần đạt mục tiêu 140 mmHg, và sẽ đòi hỏi tăng chi phí thuốc và số lần tái khám.
Tóm lại, kiểm soát HATT dưới 120 mmHg, so với mức dưới 140 mmHg, ở BN có nguy cơ tim mạch cao nhưng không có ĐTĐ, giúp giảm tỷ lệ tử vong do tim mạch, biến cố tim mạch nặng không tử vong và tử vong do mọi nguyên nhân. Tuy nhiên, một vài biến cố không mong đợi xảy ra nhiều hơn một cách có ý nghĩa khi đạt mức huyết áp mục tiêu thấp hơn.
TÀI LIỆU THAM KHẢO
1. Kearney PM, Whelton M, Reynolds K, Muntner P, Whelton PK, He J. Global burden of hypertension: analysis of worldwide data. Lancet 2005;365:217-23.
2. Go AS, Mozaffarian D, Roger VL, et al. Heart disease and stroke statistics — 2014 update: a report from the American Heart Association. Circulation 2014; 129(3):e28-292.
3. Franklin SS. Cardiovascular risks related to increased diastolic, systolic and pulse pressure: an epidemiologists point of view. Pathol Biol (Paris) 1999;47:594-603.
4. Franklin SS, Jacobs MJ, Wong ND, LItalien GJ, Lapuerta P. Predominance of isolated systolic hypertension among middle-aged and elderly US hypertensives: analysis based on National Health and Nutrition Examination Survey (NHANES) III. Hypertension 2001;37:869-74.
5. Chobanian AV, Bakris GL, Black HR, et al. The seventh report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure: the JNC 7 Report. JAMA 2003;289:2560-72.
6. Collins R, Peto R, MacMahon S, et al. Blood pressure, stroke, and coronary heart disease. 2. Short-term reductions in blood pressure: overview of randomised drug trials in their epidemiological context. Lancet 1990;335:827-38.
7. Hsu CY, McCulloch CE, Darbinian J, Go AS, Iribarren C. Elevated blood pressure and risk of end-stage renal disease in subjects without baseline kidney disease. Arch Intern Med 2005;165:923-8.
8. Levy D, Larson MG, Vasan RS, Kannel WB, Ho KK. The progression from hypertension to congestive heart failure. JAMA 1996;275:1557-62.
9. MacMahon S, Peto R, Cutler J, et al. Blood pressure, stroke, and coronary heart disease. Part 1: prolonged differences in blood pressure: prospective observational studies corrected for the regression dilution bias. Lancet 1990;335:765-74.
10. Lewington S, Clarke R, Qizilbash N, Peto R, Collins R. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet 2002;360:1903-13.
11. Staessen JA, Fagard R, Thijs L, et al. Randomised double-blind comparison of placebo and active treatment for older patients with isolated systolic hypertension. Lancet 1997;350:757-64.
12. Vasan RS, Larson MG, Leip EP, et al. Impact of high-normal blood pressure on the risk of cardiovascular disease. N Engl J Med 2001;345:1291-7.
13. Sundström J, Arima H, Jackson R, et al. Effects of blood pressure reduction in mild hypertension: a systematic review and meta-analysis. Ann Intern Med 2015; 162:184-91.
14. Lim SS, Vos T, Flaxman AD, et al. A comparative risk assessment of burden of disease and injury attributable to 67 risk factors and risk factor clusters in 21 regions, 1990-2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 2012;380:2224-60.
15. Neal B, MacMahon S, Chapman N. Effects of ACE inhibitors, calcium antagonists, and other blood-pressure-lowering drugs: results of prospectively designed overviews of randomised trials. Lancet 2000;356:1955-64.
16. Psaty BM, Smith NL, Siscovick DS, et al. Health outcomes associated with antihypertensive therapies used as first-line agents: asystematic review and metaanalysis. JAMA 1997;277:739-45.
17. SHEP Cooperative Research Group. Prevention of stroke by antihypertensive drug treatment in older persons with isolated systolic hypertension: final results of the Systolic Hypertension in the Elderly Program (SHEP). JAMA 1991;265:3255-64.
18. Beckett NS, Peters R, Fletcher AE, et al. Treatment of hypertension in patients 80 years of age or older. N Engl J Med 2008;358:1887-98.
19. JATOS Study Group. Principal results of the Japanese trial to assess optimal systolic blood pressure in elderly hypertensive patients (JATOS). Hypertens Res 2008;31:2115-27.
20. Ogihara T, Saruta T, Rakugi H, et al. Target blood pressure for treatment of isolated systolic hypertension in the elderly: Valsartan in Elderly Isolated Systolic Hypertension study. Hypertension 2010;56:196-202.
21. Verdecchia P, Staessen JA, Angeli F, et al. Usual versus tight control of systolic blood pressure in non-diabetic patients with hypertension (Cardio-Sis): an openlabel randomised trial. Lancet 2009;374:525-33.
22. Cushman WC, Evans GW, Byington RP, et al. Effects of intensive blood-pressure control in type 2 diabetes mellitus. N Engl J Med 2010;362:1575-85.
23. Benavente OR, Coffey CS, Conwit R, et al. Blood-pressure targets in patients with recent lacunar stroke: the SPS3 randomised trial. Lancet 2013;382:507-15.
24. Working group report: Expert Panel on a Hypertension Treatment Trial Initiative meeting summary, 2007. Bethesda, MD, National Heart Lung and Blood Institute (http://www.nhlbi.nih.gov/sites/www.nhlbi.nih.gov/files/hypertsnsion-full.pdf).
25. Systolic Blood Pressure Intervention Trial (SPRINT) protocol. November 1, 2012 (https://www.sprinttrial.org/public/Protocol_Current.pdf).
26. Ambrosius WT, Sink KM, Foy CG, et al. The design and rationale of a multicenter clinical trial comparing two strategies for control of systolic blood pressure: the Systolic Blood Pressure Intervention Trial (SPRINT). Clin Trials 2014;11:532-46.
27. Lindholm LH, Carlberg B, Samuelsson O. Should beta blockers remain first choice in the treatment of primary hypertension? A meta-analysis. Lancet 2005;366:1545-53.
28. ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group. Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: the Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT). JAMA 2002;288:2981-97.
29. Ernst ME, Carter BL, Goerdt CJ, et al. Comparative antihypertensive effects of hydrochlorothiazide and chlorthalidone on ambulatory and office blood pressure. Hypertension 2006;47:352-8.
30. Office for Human Research Protections. OHRP guidance on unanticipated problems and adverse events. 2007 (http://www.hhs.gov/ohrp/policy/advevntguid.html).
31. Food and Drug Administration. Code of Federal Regulations. Title 21CFR312.32a, 2013 (http://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/cfrsearch.cfm?fr=312.32).
32. Hommel G. A stagewise rejective multiple test procedure based on a modified Bonferroni test. Biometrika 1988;75:383-86.
33. Proschan MA, Lan KKG, Wittes JT. Statistical monitoring of clinical trials: a unified approach. New York: Springer,2006.
34. Fine JP, Gray RJ. A proportional hazards model for the subdistribution of a competing risk. J Am Stat Assoc 1999;94:496-509.
35. Bakris GL, Weir MR. Angiotensinconverting enzyme inhibitor-associated elevations in serum creatinine: is this a cause for concern? Arch Intern Med 2000;160:685-93.
36. Apperloo AJ, de Zeeuw D, de Jong PE. A short-term antihypertensive treatmentinduced fall in glomerular filtration rate predicts long-term stability of renal function. Kidney Int 1997;51:793-7.
37. Liu L, Zhang Y, Liu G, Li W, Zhang X, Zanchetti A. The Felodipine Event Reduction (FEVER) Study: a randomized longterm placebo-controlled trial in Chinese hypertensive patients. J Hypertens 2005;23:2157-72.
38. Margolis KL, OConnor PJ, Morgan TM, et al. Outcomes of combined cardiovascular risk factor management strategies in type 2 diabetes: the ACCORD randomized trial. Diabetes Care 2014;37:1721-8.
39. Nwankwo T, Yoon SS, Burt V, Gu Q. Hypertension among adults in the United States: National Health and Nutrition Examination Survey, 2011–2012. NCHS Data Brief 2013;133:1-8.








