Tóm tắt:
Mục tiêu nghiên cứu:
Đánh giá hiệu quả và tính an tòan lâu dài của linagliptin khi điều trị thêm vào ở những bệnh nhân Châu á mắc bệnh đái tháo đường type 2, chưa kiểm sóat đường huyết đạt mục tiêu với điều trị insulin nền có/không kết hợp với các thuốc đường huyết uống khác.
Wayne H-H Sheu, Sung Woo Park, Yan Gong, Sabine Pinnetti, Sudipta
Bhattacharya, Sanjay Patel, Thomas Seck, Hans-Juergen Woerle
Tổng hợp: Ths.Bs Vũ Thị Tuyết Mai
Khoa Nội Tim Mạch BV Chợ rẫy
Thiết kế và phương pháp nghiên cứu:
Đây là phân tích hậu kiểm(post hoc analysis) trên những bệnh nhân Châu á từ một nghiên cứu toàn cầu kéo dài trên 52 tuần, trong đó những bệnh nhân đang được điều trị với insulin nền được phân nhóm ngẫu nhiên(1:1), mù đôi để điều trị với linagliptin hoặc giả dược. Liều insulin nền vẫn giữ ổn định trong 24 tuần đầu, sau đó nó có thể được điều chỉnh theo quyết định của điều tra viên để cải thiện kiểm sóat đường huyết. Tiêu chí chính là sự thay đổi của nồng độ trung bình HbA1c sau 24 tuần điều trị so với lúc ban đầu.
Kết quả:
Dữ liệu thu thập từ 154 bệnh nhân Châu á (80 linagliptin, 74 placebo). HbA1c ban đầu(độ lệch chuẩn[SD]) là 8.6 (0.9)% (70[10]mmol/mol). Mức thay đổi HbA1c trung bình có hiệu chỉnh với giả dược( sai biệt chuẩn standard error[SE]) của HbA1c so với mức ban đầu là –0.9 (0.1)% (–10 [1] mmol/mol) ( khoảng tin cậy 95% [CI]: –1.2, –0.7; p<0.0001) ở tuần thứ 24, và –0.9 (0.1)% (–10 [1] mmol/mol) (95% CI: –1.1, –0.6; p<0.0001) ở tuần 52. Tần suất các tác dụng phụ (linagliptin 81.3%, placebo 91.9%) và hạ đường huyết (tuần thứ 24: linagliptin 25.0%, placebo 25.7%; kết thúc điều trị: linagliptin 28.8%, placebo 35.1%) giống nhau giữa 2 nhóm. Vào tuần thứ 52, sự thay đổi cân nặng trung bình [SE] cũng giống nhau ở cả 2 nhóm (linagliptin –0.67 [0.26] kg, placebo –0.38 [0.25] kg).
Kết luận:
Nghiên cứu này bị giới hạn bởi bản chất của phân tích hậu kiểm và số lượng bệnh nhân nhỏ. Tuy nhiên kết quả cho thấy rằng linagliptin cải thiện đáng kể việc kiểm soát đường huyết ở bệnh nhân Châu á mắc đái tháo đường type 2 chưa kiểm soát tốt đường huyết bằng insulin nền, mà không làm tăng nguy cơ hạ đường huyết hoặc tăng cân.
Giới thiệu:
Các khu vực địa lý bao gồm Đông Nam Á và Tây Thái Bình Dương chiếm hơn một phân nửa của tổng số bệnh nhân được chẩn đoán đái tháo đường1. Trong những thập kỷ gần đây, Châu Á đã trải qua sự phát triển kinh tế xã hội rất lớn, có những thay đổi trong chế độ ăn uống, giảm họat động thể lực, tăng tình trạng béo phì cũng như là việc đưa vào các chương trình tầm soát quốc gia hay cộng đồng2. Do đó tỷ lệ mắc và phát hiện đái tháo đường type 2 ở Châu Á tăng lên nhanh chóng. Dữ liệu dịch tễ học cho thấy sự khởi phát đái tháo đường type 2 ở bệnh nhân Châu Á tương đối trẻ và có chỉ số BMI thấp hơn so với các bệnh nhân ở Phương Tây3. Sinh lý bệnh tiềm ẩn trong sự phát triển đái tháo đường type 2 ở những bệnh nhân Châu Á được cho là do sự suy thóai chức năng của tế bào β ở cả những bệnh nhân béo phì và không béo phì2,4-6, nó có thể liên quan đến việc tăng đường huyết sau ăn7,8.Ở những bệnh nhân Châu Á, bệnh đái tháo đường type 2 cũng liên quan đến biến chứng nhiều hơn. Bệnh thận mạn, có thể tiến triển đến bệnh thận giai đọan cuối, được xem là biến chứng nghiêm trọng, nó có thể ảnh hưởng đến các phản ứng dược lý của các thuốc điều trị đái tháo đường đường uống (OADs) thường được sử dụng9,10. Hơn nữa, tần suất hạ đường huyết đã được chứng minh là khá cao ở các bệnh nhân thuộc khu vực Châu Á-Thái Bình Dương, một nghiên cứu đã cho thấy rằng, 35,8% các bệnh nhân đang điều trị OADs đã từng trải qua các triệu chứng hạ đường huyết11. Lo lắng về nguy cơ hạ đường huyết thường ngăn cản các bệnh nhân đái tháo đường type 2 và các bác sĩ khởi đầu điều trị hoặc tăng dần liều insulin nền, dẫn đến những bệnh nhân tăng đường huyết chưa kiểm soát được vẫn giữ đường huyết ở mức trên mục tiêu. Tóm lại, điều này cho thấy việc xác định tính hiệu quả và an tòan của các thuốc OADs thế hệ mới trong điều trị kết hợp với insulin là rất cần thiết trong thực hành lâm sàng. Trong đó, linagliptin và các thuốc ức chế DPP-4 khác có thể bổ sung vào liệu pháp insulin nền. Vì chúng đặc biệt nhắm đến đường huyết sau ăn, theo cách thức phụ thuộc vào đường huyết, mặc dù việc kiểm sóat đường huyết đói cũng cải thiện12. Do đó các thuốc nhóm DPP-4 ít có nguy cơ gây hạ đường huyết khi sử dụng trong đơn trị liệu hoặc khi kết hợp với các thuốc đường uống khác, vì bản thân chúng không làm tăng nguy cơ hạ đường huyết hoặc tăng cân13, đây cũng chính là những hạn chế lớn của các OADs khác. Linagliptin là thuốc ức chế DPP-4 đường uống hiện nay được cho phép sử dụng ở nhiều quốc gia, trong đó có nhiều nước Châu Á, để điều trị đái tháo đường type 2 với phác đồ một lần mỗi ngày. Ở những bệnh nhân suy thận, linagliptin là thuốc duy nhất không cần chỉnh liều vì nó được bài tiết chủ yếu qua mật và ruột10,14. Trong những thử nghiệm lâm sàng pha III đa quốc gia, trong đó có một số lượng bệnh nhân từ các nước Châu Á, linagliptin được dung nạp tốt và đạt được những cải thiện có ý nghĩa về mặt lâm sàng trong kiểm soát đường huyết khi điều trị đơn trị liệu15,16, khi kết hợp với metformin17 hoặc pioglitazone 18, khi điều trị thêm vào ở bệnh nhân đang điều trị phối hợp metformin và sulfonylnurea19,hoặc khi điều trị thêm vào với một số thuốc OADs khác bao gồm biguanide, glinide, glitazone, sulfonylurea, hoặc nhóm ức chế men α-glucosidase20. Khi điều trị với linagliptin nguy cơ hạ đường huyết thấp, trừ khi kết hợp với sulfonylurea, và không ảnh hưởng đến cân nặng. Trong một nghiên cứu phase III thêm, dựa trên phân tích dướinhóm hiện tại, linagliptin được điều trị thêm vào ở những bệnh nhân đang điều trị insulin nền mà chưa kiểm sóat được đường huyết, cho thấy mức giảm HbA1c có ý nghĩa lâm sàng và được dung nạp tốt, cũng như không làm tăng nguy cơ hạ đường huyết khi so sánh với giả dược21.
Trong nghiên cứu này, hiệu quả và tính an toàn của linagliptin khi điều trị thêm vào liệu pháp insulin nền một mình, hoặc khi kết hợp với metformin và/ hoặc pioglitazone được đánh giá ở nhóm bệnh nhân Châu Á mắc đái tháo đường type 2 từ nghiên cứu đánh giá linagliptin khi điều trị thêm vào insulin nền trên tòan cầu21
Các bệnh nhân và phương pháp:
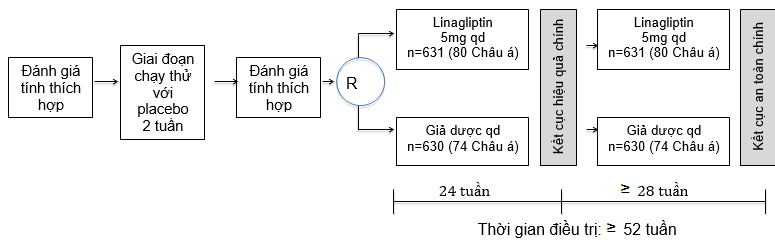
Đây là một phân tích hậu kiểm của một thử nghiệm lâm sàng pha III ở những bệnh nhân chưa kiểm soát đường huyết đầy đủ, những bệnh nhân này được chọn ngẫu nhiên để được điều trị mù đôi với linagliptin 5mg hoặc giả dược kéo dài ≥ 52 tuần, được thêm vào insulin nền có hoặc không kết hợp thêm với metformin và/hoặc pioglitazone (ClinicalTrials.gov identifier NCT00954447)21. Liều cơ bản của insulin nền được giữ ổn định trong suốt 24 tuần đầu điều trị, sau đó có thể điều chỉnh theo điều tiết của điều tra viên, để cải thiện kiểm soát đường huyết( Hình 1). Liều cơ bản của các OADs vẫn được giữ ổn định trong suốt nghiên cứu. Thiết kế và phương pháp nghiên cứu đã được mô tả chi tiết phía trên21
Hình 1. Thiết kế nghiên cứu
FPG, đường huyết đói; qd, một lần mỗi ngày; R, phân nhóm ngẫu nhiên.
Đề cương nghiên cứu được tiến hành dựa trên các nguyên lý của tuyên ngôn Helsinki và khuyến cáo của ICH (International Conference on Harmonization) về thực hành lâm sàng tốt – GCP (Good Clinical Practice). Đề cương nghiên cứu đã được xem xét và thông qua bởi các uỷ ban y đức và hội đồng y đức độc lập của tất cả các trung tâm tham gia nghiên cứu.
Phân tích này bao gồm dữ liệu của tất cả bệnh nhân chủng tộc châu Á. Cũng như trong nghiên cứu gốc, tiêu chí hiệu quả chính là sự thay đổi HbA1c trung bình sau 24 tuần điều trịso vớilúc ban đầu. Các tiêu chí phụ bao gồm sự thay đổi HbA1c so với giá trị ban đầu, tỷ lệ bệnh nhân đạt HbA1c < 7.0% (53 mmol/mol) và tỷ lệ bệnh nhân giảm HbA1c 0.5% (6 mmol/mol), đường huyết đói theo thời gian (FPG over time), và mức thay đổi đường huyết đói sau 52 tuầnso vớiban đầu. Các kết cục khác bao gồm mức thay đổi liều insulin nền trung bình theo thời gian so với liều ban đầu và sau 52 tuần điều trị, việc sử dụng trị liệu hạ đường huyết nhanh (rescue therapy), thay đổi cân nặng so với lúc ban đầu khi kết thúc nghiên cứu.
Việc đánh giá tính an toàn và dung nạp bao gồm tần suất và độ nặng các tác dụng phụ (AEs), như hạ đường huyết, các dấu hiệu thăm khám lâm sàng mới xuất hiện hay nặng hơn, điện tâm đồ 12 chuyển đạo, sinh hiệu, các thông số mỡ trong máu, và các xét nghiệm cận lâm sàng. Các tiêu chí an toàn chính khác bao gồm các biến cố tử vong liên quan điều trị,các biến cố nghi ngờ đột qụy hay thiếu máu cơ tim (bao gồm nhồi máu cơ tim), nhập viện vì suy tim, huyết khối trong stent, các thủ thuật tái thông mạch máu, được đánh giá bởi uỷ ban biến cố lâm sàng độc lậpbên ngoài.
Các tiêu chí về tính hiệu quả đã được đánh giá bằng cách sử dụng nhóm được phân tích đầy đủ, được định nghĩa là tất cả bệnh nhân được chọn ngẫu nhiên điều trị với >=1 liều thuốc nghiên cứu, có HbA1c nền và>=1 lần đo HbA1c trong vòng 24 tuần điều trị. Dữ liệu liên tục được phân tích bằng cách sử dụng các giá trị cuối cùng quan sát được (LOCF – last observation carried forward) hay các ca quan sát được, trong khi các dữ liệu phân loại (phần trăm bệnh nhân đạt HbA1c < 7.0% hay có giảm HbA1c >=0.5% tại tuần thứ 24 và 52) được phân tích với cách tiếp cận xem những người không hoàn thành là không đạt( những bệnh nhân không hoàn thành 24 tuần hay 52 tuần điều trị được đếm là không đạt HbA1c < 7% hay không có giảm HbA1c >=0.5% ). Mức thay đổi giá trị HbA1c trung bình so với mức ban đầu ở tuần 24 được so sánh giữa 2 nhóm linagliptin và giả dược bằng mô hình phân tích hiệp phương sai ANCOVA với mức α=0.025 (1 đuôi). Các tiêu chí thứ phát cũng được phân tích bằng mô hình ANCOVA. Việc ảnh hưởng của điều trị lên sự xuất hiện biến cố hạ đường huyết được khảo sát bằng hồi qui logistic và phân tích Kaplan – Meier. Các tiêu chí an toàn được tóm tắt bằng cách sử dụng thống kê mô tả.
KẾT QUẢ:
Sự sắp xếp bệnh nhân, nhân khẩu học, các đặc tính lâm sàng ban đầu của bệnh nhân
Trong số 1261 bệnh nhân được phân nhóm ngẫu nhiên trong nghiên cứu gốc21,có 154 bệnh nhân là người Châu Á (linagliptin n=80, giả dược n=74). Trong đó, 15 bệnh nhân trong nhóm linagliptin và 12 bệnh nhân trong nhóm giả dược kết thúc sớm điều trị. Các đặc tính nhân khẩu học và lâm sàng trong phân nhóm Châu átương đồng giữa 2 nhóm linagliptin và giả dược (Bảng 1). Hầu hết bệnh nhân có chức năng thận bình thường (50%) hay giảm nhẹ (44.2%), và đã được chẩn đoán đái tháo đường > 5 năm (84.3%). Tất cả bệnh nhân đã được điều trị insulin nền tại lúc đi vào nghiên cứu và phần lớn bệnh nhân được điều trị metformin (81.5%). Khoảng 4% bệnh nhân được điều trị kết hợp metformin và pioglitazone thêm vào với insulin. Không có bệnh nhân nào trong nghiên cứu này được điều trị pioglitazone thêm vào insulin.
Bảng 1. Đặc tính nhân chủng học và các đặc điểm lâm sàng ban đầu
|
|
Linagliptin |
Giả dược |
|
Đặc điểm nhân chủng học |
|
|
|
Bệnh nhân (nhóm điều trị*), n |
80 |
74 |
|
Nam, n% |
40 (50.0) |
33 (44.6) |
|
Tuổi, năm, trung bình (SD) |
57.5 (10.1) |
56.7 (9.6) |
|
Nhóm tuổi, n% |
|
|
|
< 65 tuổi |
57 (71.3) |
61 (82.4) |
|
>= 65 tuổi |
23 (28.8) |
13 (17.6) |
|
Chỉ số khối cơ thể, kg/m2, trung bình (SD) |
25.6 (3.6) |
26.2 (3.4) |
|
Chức năng thận (eGFR) theo MDRD, n% |
|
|
|
Bình thường (>= 90 mL/ph) |
40 (50.0) |
37 (50.0) |
|
Giảm nhẹ ( 60 đến < 90 mL/ph) |
33 (41.3) |
35 (47.3) |
|
Giảm trung bình ( 30 đến < 60 mL/ph ) |
6 (7.5) |
1 (1.4) |
|
Giảm nặng – giai đoạn cuối ( < 30 mL/ph) |
1 (1.3) |
1 (1.4) |
|
Đặc tính lâm sàng |
|
|
|
Bệnh nhân (nhóm phân tích toàn bộ+), n |
79 |
74 |
|
HbA1c, %, trung bình (SD) |
8.5 (0.9) |
8.6 (0.9) |
|
HbA1c, mmol/mol, trung bình (SD) |
69 (10) |
70 (10) |
|
FPG, mmol/L, trung bình (SD) |
7.3 (2.3) |
7.5 (2.2) |
|
Thời gian kể từ lúc chẩn đoán ĐTĐ, trung bình (SD) |
|
|
|
>=1 năm, n (%) |
4 (5.1) |
4 (5.4) |
|
> 1 đến >=5 năm, n (%) |
12 (15.2) |
4 (5.4) |
|
> 5 năm, n (%) |
63 (79.7) |
66 (89.2) |
|
Loại insulin nền, n (%) |
|
|
|
Insulin glargine |
46 (58.2) |
51 (68.9) |
|
Insulin detemir |
15 (19.0) |
15 (20.3) |
|
NPH |
18 (22.8) |
8 (10.8) |
|
OADs đi kèm, n (%) |
|
|
|
Không |
7 (8.9) |
15 (20.3) |
|
Chỉ metformin |
69 (87.3) |
56 (75.7) |
|
Chỉ pioglitazone |
0 (0.0) |
0 (0.0) |
|
Metformin + pioglitazone |
3 (3.8) |
3 (4.1) |
*Tất cả bệnh nhân được điều trị >=1 liều thuốc nghiên cứu
+Tất cả bệnh nhân có HbA1c nền tảng và có >=1 lần đo HbA1c trong quá trình điều trị
eGFR, độ lọc cầu thận ước đoán; FPG, đường huyết đói; HbA1c, hemoglobin glycated hoá; MDRD, điều chỉnh chế độ ăn trong bệnh thận; NPH, protamine Hagedorn trung tính; OADs, thuốc hạ đường huyết uống; SD, độ lệch chuẩn.
Các kết quả đạt được
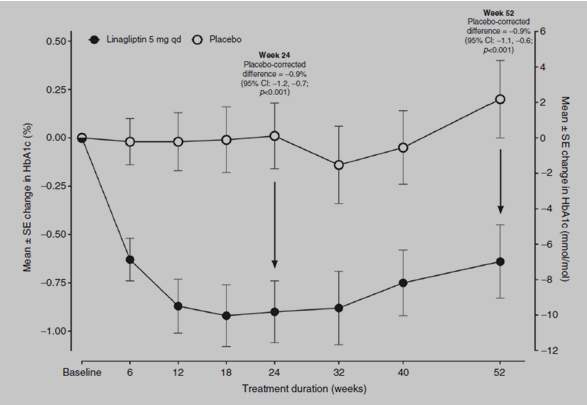
Điều trị với linagliptin dẫn đến cải thiện đáng kể có ý nghĩa thống kê HbA1c, với mức thay đổi trung bình đã được hiệu chỉnh với giả dược (sai số chuẩn (SE) – 0.9 (0.1)% – (-10 [1] mmol/mol) ở tuần 24 (Bảng 2 và Hình 2). Hiệu quả điều trị được duy trì cho đến tuần 52. Số bệnh nhân ở nhóm linagliptin đạt HbA1c mục tiêu < 7.0% (53 mmol/mol) nhiều hơn ở nhóm giả dược ở cả tuần thứ 24 và 52 (Bảng 3). So với nhóm giả dược, bệnh nhân ở nhóm linagliptin cũng đạt được mức giảm HbA1c >=0.5% (6mmol/mol) nhiều hơn sau 24 tuần và 52 tuần điều trị (Bảng 3).
Hình 2. Thay đổi HbA1c trung bình được hiệu chỉnh so với giá trị ban đầu theo thời gian cho đến tuần 52 (FAS; LOCF). CI, khoảng tin cậy; FAS, nhóm phân tích toàn bộ (full analysis set); HbA1c, hemoglobin glycated hoá; LOCF, kết quả cuối cùng quan sát được; qd, một lần mỗi ngày; SE, sai số chuẩn.
Bảng 2. Thay đổi HbA1c hiệu chỉnh so với giá trị ban đầu tại tuần thứ 24 và 52
|
|
Linagliptin |
Giả dược |
|
Tuần thứ 24 |
|
|
|
Bệnh nhân*, n |
79 |
74 |
|
Trung bình lúc đầu, %(SE) (mmol/mol [SE]) |
8.5 (0.1) (69[1]) |
8.6 (0.1)(70[1]) |
|
Thay đổi so với lúc đầu, % (SE) (mmol/mol [SE]) |
|
|
|
Trung bình được hiệu chỉnh+ |
-0.9 (0.2) (-10 [2]) |
0.0 (0.2)(0[2]) |
|
Khác biệt so với giả dược |
|
|
|
Trung bình được hiệu chỉnh+, % (SE) (mmol/mol [SE]) |
-0.9 (0.1)(-10 [1]) |
|
|
CI 95% |
-1.2, -0.7 |
|
|
Giá trị P |
< 0.001 |
|
|
Tuần thứ 52 |
|
|
|
Thay đổi so với lúc đầu, % (SE) (mmol/mol [SE]) |
|
|
|
Trung bình được hiệu chỉnh+ |
-0.6 (0.2)(7[2]) |
0.2 (0.2)(2[2]) |
|
Khác biệt so với giả dược |
|
|
|
Trung bình được hiệu chỉnh+, % (SE) (mmol/mol [SE]) |
-0.9 (0.1)(-10[1]) |
|
|
CI 95% |
-1.1, -0.6 |
|
|
Giá trị P |
<0.001 |
|
*Nhóm phân tích toàn bộ – tất cả bệnh nhân có 1 HbA1c nền tảng và có >=1 lần đo HbA1c trong quá trình điều trị
+Mô hình hiệu chỉnh bao gồm điều trị, HbA1c ban đầu, phân nhóm theo suy chức năng thận, và các thuốc hạ đường huyết uống kèm theo.
Phân tích kết quả cuối cùng quan sát được
CI, khoảng tin cậy; HbA1c, hemoglobin glycated hoá; SE, sai số chuẩn.
Ghi chú: Dựa trên số ca quan sát được (bệnh nhân hoàn thành 24 và 52 tuần điều trị), giá trị HbA1c trung bình là 7.48 (n=67) (linagliptin) và 8.52 (n=68) (giả dược) tại tuần 24, và 7.52 (n=55) (linagliptin) và 8.40 (n=49) (giả dược) tại tuần 52.
Bảng 3. Đánh giá các tiêu chí thứ phát
|
|
Linagliptin (n=79) |
Giả dược (n=74) |
|
HbA1c < 7.0% (53 mmol/mol)* (NCF), n (%) |
|
|
|
Tuần 24 |
14 (17.9) |
4 (5.6) |
|
Tuần 52 |
13 (16.7) |
5 (6.9 ) |
|
Giảm HbA1c >= 0.5% (6 mmol/mol)* |
|
|
|
(NCF), n (%) |
|
|
|
Tuần 24 |
48 (60.8) |
16 (21.6) |
|
Tuần 52 |
39 (49.4) |
20 (27.0) |
|
Thay đổi liều insulin* (LOCF), IU (SE) |
|
|
|
Tuần 52 |
|
|
|
Ban đầu (chưa hiệu chỉnh) |
32.2 (2.8) |
34.1 (2.0) |
|
Thay đổi so với ban đầu (hiệu chỉnh+) |
0.3 (1.5) |
0.6 (1.6) |
|
Khác biệt so với giả dược (hiệu chỉnh+) |
-0.3 (1.1) |
|
|
CI 95% |
-2.5, 1.9 |
|
|
Giá trị P |
0.772 |
|
|
Thay đổi cân nặng* (OC) |
|
|
|
Ban đầu, kg (SD) |
67.0 (11.6) |
69.0 (12.6) |
|
Thay đổi so với ban đầu ở tuần 24, kg (SE) |
-0.3 (0.2) |
0.1 (0.3) |
|
Thay đổi so với ban đầu ở tuần 52, kg (SE) |
-0.7 (0.3) |
-0.4 (0.3) |
*Nhóm phân tích toàn bộ – tất cả bệnh nhân có 1 HbA1c nền tảng và có >=1 lần đo HbA1c trong quá trình điều trị
+Mô hình hiệu chỉnh bao gồm điều trị, HbA1c ban đầu, phân nhóm theo suy chức năng thận, và các thuốc hạ đường huyết uống kèm theo.
HbA1c, hemoglobin glycated hoá; LOCF, kết quả cuối cùng quan sát được; NCF, người tham gia không hoàn thành xem như thất bại; OC, các ca được quan sát; SD, độ lệch chuẩn; SE, sai số chuẩn.
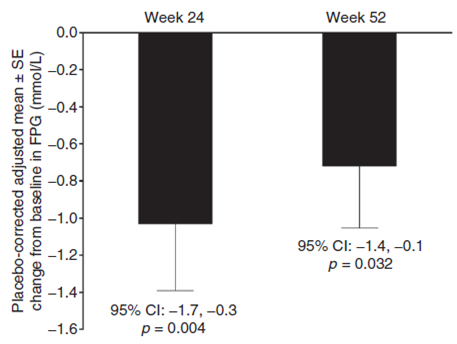
Tại tuần 24, sau giai đoạn insulin nền ổn định, chỉ có nhóm linagliptin cho thấy có giảm giá trị đường huyết đói (FPG) trung bình có hiệu chỉnh so với giá trị ban đầu, tạo ra sự khác biệt có ý nghĩa được hiệu chỉnh với giả dược (Hình 3). Tại tuần 52 (khi điều chỉnh liều insulin nền được cho phép ở cả 2 nhóm), nồng độ FPG không thấp hơn giá trị ban đầu ở cả 2 nhóm. Tuy nhiên, giống như ở tuần 24, sự thay đổi FPG ở tuần 52 được hiệu chỉnh với giả dược khi so với giá trị ban đầu cũng có khác biệt có ý nghĩa thống kê.
Hình 3. Thay đổi trung bình đường huyết đói (FPG) được hiệu chỉnh với placebo so với ban đầu tại thời điểm 24 và 52 tuần (FAS; LOCF).
CI, khoảng tin cậy; FAS, nhóm phân tích toàn bộ (full analysis set); FPG, đường huyết đói; LOCF, kết quả cuối cùng quan sát được; qd, một lần mỗi ngày; SE, sai số chuẩn.
Thay đổi điều trị insulin ban đầu
Trong suốt giai đoạn insulin nền ổn định (khi liều insulin được duy trì trong khoảng ± 10% so với ban đầu), sự thay đổi trung bình (SE) liều insulin nền cho đến tuần 24 là -0.1 (0.5) IU đối với linagliptin và -0.3 (0.3) đối với placebo. Mức thay đổi trung vị (tổi thiểu, tối đa) liều insulin nền cho tới tuần 24 là 0 (-10,30) IU đối với linagliptin và 0 (-12,7) IU đối với placebo. Mặc dù liều insulin nền trung bình tăng nhiều hơn ở nhóm giả dược so với nhóm linagliptin tại tuần 52, nhưng sự thay đổi này không đạt ý nghĩa thống kê (linagliptin 0.3 (1.5) IU, giả dược 0.6 (1.6) IU; độ tin cậy (CI) 95%: -2.5, 1.9, p=0.772).
Phân tích phân nhóm sự thay đổi HbA1c so với giá trị ban đầu
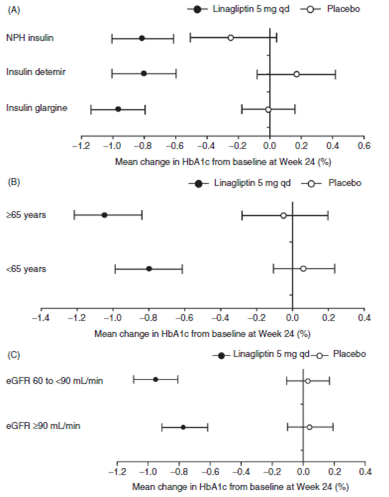
Sự thay đổi HbA1c với điều trị linagliptin không có mối liên quan với loại insulin nền điều trị ban đầu (Hình 4A). Sự thay đổi trung bình HbA1c được hiệu chỉnh với giả dược so với giá trị ban đầu ở tuần 24 là -1.0% (-11 mmol/mol) ở bệnh nhân dùng insulin glargine, -0.9% (-10 mmol/mol) ở bệnh nhân dùng insulin detemir, và -0.6% (-6 mmol/mol) ở bệnh nhân dùng insulin protamine Hagedorn trung tính (NPH). Sự thay đổi HbA1c cũng có vẻ không liên quan với tuổi và giống nhau ở bệnh nhân không suy chức năng thận và suy chức năng thận nhẹ (không có kết quả ở nhóm suy chức năng thận trung bình và nặng do số lượng bệnh nhân ở 2 nhóm này ít) (Hình 4B-C). Sự thay đổi trung bình HbA1c có hiệu chỉnh với giả dược so với giá trị ban đầu ở tuần 24 là -0.9% (-9 mmol/mol) đối với bệnh nhân < 65 tuổi và -1.0% (-11 mmol/mol) đối với bệnh nhân >=65 tuổi. Đối với tình trạng suy thận, HbA1c ban đầu là 8.6% (70 mmol/mol) ở nhóm không suy thận (n=77) (độ lọc cầu thận ước đoán eGFR >=90 mL/ph), và 8.6% (70 mmol/mol) ở nhóm suy thận nhẹ (n=67) (eGFR từ 60 đến < 90 mL/ph). Sự thay đổi trung bình HbA1c có hiệu chỉnh với giả dược so với giá trị ban đầu là -0.8% (-9 mmol/mol) ở bệnh nhân không suy thận và -1.0% (-11 mmol/mol) ở bệnh nhân suy thận nhẹ.
Hình 4. Thay đổi HbA1c trung bình so với lúc đầu tại thời điểm tuần thứ 24 theo loại insulin nền được sử dụng (A), theo tuổi (B), và theo giai đoạn suy thận (C) (FAS; LOCF).
eGFR, độ lọc cầu thận ước đoán; FAS, gói phân tích toàn bộ (full analysis set); HbA1c, hemoglobin glycated hoá; LOCF, kết quả cuối cùng quan sát được; NPH: protamine Hagedorn trung tính; qd, một lần mỗi ngày.
Tính an toàn và dung nạp
Suất độ chung bệnh nhân phản ánh các tác dụng ngoại ý tương đương giữa nhóm linagliptin và giả dược (Bảng 4). Tác dụng phụ nghiêm trọng được báo cáo là 16.3% ở nhóm bệnh nhân dùng linagliptin và 16.2% bệnh nhân dùng giả dược. Các tác dụng phụ liên quan đến thuốc xảy ra ở 25% trong nhóm linagliptin và 21.6% trong nhóm giả dược. Các tác dụng phụ dẫn đến ngưng điều trị không xảy ra trên cả 2 nhóm bệnh nhân.
Bảng 4. Tóm tắt tổng quát các tác dụng ngoại ý cho đến tuần 52 và các biến cố hạ đường huyết được xác định bởi nghiên cứu viên tại tuần 24 và lúc kết thúc điều trị.*
|
|
Linagliptin |
Giả dược |
|
Các tác dụng ngoại ý cho đến tuần 52 |
|
|
|
Bệnh nhân, n |
80 |
74 |
|
Thời gian điều trị nghiên cứu trung bình,ngày |
434 |
458 |
|
Bất cứ tác dụng ngoại ý nào, n (%) |
65 (81.3) |
68 (91.9) |
|
Tác dụng ngoại ý nặng, n (%) |
7 (8.8) |
3 (4.1) |
|
Tác dụng ngoại ý liên quan đến thuốc, n (%) |
20 (25.0) |
16 (21.6) |
|
Các tác dụng ngoại ý đáng kể khác (dựa trên ICH E3), n (%) |
0 (0.0) |
0 (0.0) |
|
Các tác dụng ngoại ý gây ngưng điều trị thử nghiệm, n (%) |
0 (0.0) |
0 (0.0) |
|
Tác dụng ngoại ý trầm trọng, n (%) |
13 (16.3) |
12 (16.2) |
|
Tử vong |
0 (0.0) |
0 (0.0) |
|
Đe doạ tính mạng tức thời |
0 (0.0) |
0 (0.0) |
|
Gây di chứng |
0 (0.0) |
0 (0.0) |
|
Cần nhập viện |
13 (16.3) |
12 (16.2) |
|
Kéo dài thời gian nằm viện |
1 (1.3) |
0 (0.0) |
|
Dị tật bẩm sinh |
0 (0.0) |
0 (0.0) |
|
Khác |
1 (1.3) |
1 (1.4) |
|
Các biến cố hạ đường huyết |
|
|
|
Bệnh nhân, n |
80 |
74 |
|
Tuần 24 |
|
|
|
Tác dụng ngoại ý hạ đường huyết, n (%) |
20 (25.0) |
19 (25.7) |
|
Bất cứ hạ đường huyết có triệu chứng được ghi nhận+ và đo đường huyết >= 70 mg/dL |
14 (17.5) |
13 (17.6) |
|
Bất cứ hạ đường huyết có triệu chứng được ghi nhận‡và đo đường huyết >= 54 mg/dL |
2 (2.5) |
7 (9.5) |
|
Bất cứ giai đoạn hạ đường huyết nặng§ |
0 (0.0) |
0 (0.0) |
|
Kết thúc điều trị |
|
|
|
Tác dụng ngoại ý hạ đường huyết, n (%) |
23 (28.8) |
26 (35.1) |
|
Bất cứ hạ đường huyết có triệu chứng được ghi nhận+ và đo đường huyết >= 70 mg/dL |
15 (18.8) |
17 (23.0) |
|
Bất cứ hạ đường huyết có triệu chứng được ghi nhận‡ và đo đường huyết >= 54 mg/dL |
3 (3.8) |
10 (13.5) |
|
Bất cứ giai đoạn hạ đường huyết nặng§ |
1 (1.4) |
0 (0.0) |
*Nhóm tất cả bệnh nhân được điều trị, được điều trị >= 1 liều thuốc nghiên cứu
+Đi kèm các triệu chứng điển hình hạ đường huyết
‡Đi kèm các triệu chứng điển hình hạ đường huyết nhưng không cần hỗ trợ bên ngoài
§Cần hỗ trợ từ người khác để dùng carbohydrate chủ động, glucagon, hay các hành động hồi sức khác.
AE, biến cố ngoại ý; ICH, International Conference on Harmonization.
Tỷ lệ bệnh nhân bị hạ đường huyết tương đương ở 2 nhóm linagliptin và giả dược tại tuần thứ 24 và tại thời điểm kết thúc điều trị (Bảng 4). Phần lớn bệnh nhân trong nhóm linagliptin từng bị hạ đường huyết đều chỉ bị 1 lần (55%) tại thời điểm tuần thứ 24. Tuy nhiên, có 6 bệnh nhân (30.0%) có >=4 cơn hạ đường huyết.Ở nhóm sử dụng giả dược, cũng tương tự, 36,8% trải qua ≥ 4 cơn hạ đường huyết. Hạ đường huyết chủ yếu xảy ra ở mức độ nhẹ; hạ đường huyết nặng, được định nghĩa là cần hỗ trợ chủ động, chỉ được báo cáo ở 1 bệnh nhân trong nhóm linagliptin.
Trọng lượng trung bình (SE) không có sự khác biệt đáng kể ở tuần 24 so với ban đầu (linagliptin -0.29 (0.19) kg, giả dược +0.08 (0.32)kg ), và đến tuần thứ 52 (linagliptin -0.67 (0.26) kg, giả dược -0.38 (0.25) kg ) (Bảng 3).
Thay đổi trung bình (SE) chức năng thận, được đo lường bằng eGFR, so với ban đầu tại tuần thứ 52, là -4,47 (3.02) mL/ph/1.73 m2 đối với linagliptin và -5.00 (2.96) mL/ph/1.73 m2 đối với giả dược. Sự thay đổi chức năng thận trung bình hiệu chỉnh với giả dược là 0.53 mL/ph/1.73 m2 (95% CI: -4.87 -5.93; p=0.846).
Các biến cố tim mạch được xem xét xảy ra trên 4 bệnh nhân nhóm linagliptin (5.0%) và 4 bệnh nhân nhóm giả dược (5.4%); hai bệnh nhân trong mỗi nhóm có đau thắt ngực không ổn định phải nhập viện và hai bệnh nhân trong mỗi nhóm có đau thắt ngực không ổn định không nhập viện. Không có biến cố tim mạch khác hay tử vong do tim mạch được ghi nhận ở cả 2 nhóm.
BÀN LUẬN:
Phân tích hiện tại chứng minh rằng điều trị với linagliptin 5mg một lần trong ngày dẫn đến sự cải thiện có ý nghĩa lâm sàng về kiểm soát đường huyết trên bệnh nhân Châu á có đường huyết chưa kiểm soát tốt đang được điều trị kết hợp bằng: insulin nền, bổ sung vào trước đólà metformin và/hoặc pioglitazone. Không những linagliptin làm cải thiện đáng kể nồng độ HbA1c, mà còn không làm tăng nguy hơ hạ đường huyết và tăng cân. Sự cải thiện kiểm soát đường huyết được chứng minh độc lập với loại insulin nền được sử dụng (insulin NPH, insulin detemir, insulin glargine) và tuổi tác, cũng như tương đương trên nhóm bệnh nhân không suy thận và suy thận nhẹ, mặc dù kết quả này nên được xem xét cẩn thận vì số lượng bệnh nhân ít và đặc tính phân tích hậu kiểmdưới nhóm.
Tại tuần thứ 24, mức độ cải thiện đường huyết được quan sát ở những bệnh nhân Châu á trong phân tích này tương đương với kết quả quan sát được trong dân số chung ở nghiên cứu gốc 21. Sự giảm đáng kể nồng độ HbA1c cũng tương đồng với kết quả quan sát được trong một phân tích dưới nhóm được công bố gần đây, trên những bệnh nhân Châu á tham gia một nghiên cứu 24 tuần về việc kết hợp vildagliptin với insulin có hay không kèm metformin 22. Trong phân tích này, sự thay đổi trung bình HbA1c hiệu chỉnh với giả dược là -0.8% (-9 mmol/mol) với vildagliptin, so với nồng độ HbA1c ban đầu là 8.9%. Điều đáng ngạc nhiên là nồng độ FPG không giảm so với trị số ban đầu trong cả nhóm vildagliptin và giả dược, trong khi so sánh với dân số chung nghiên cứu thì thay đổi FPG trung bình hiệu chỉnh với giả dược là -0.6 mmol/L23. Những nghiên cứu trước đây cho thấy linagliptin có thể làm giảm đáng kể HbA1c mà không làm tăng nguy cơ hạ đường huyết khi được dùng đơn trị liệu trên bệnh nhân Nhật Bản16,24, hay được dùng kết hợp với các OADs thông dụng tại Nhật20, cũng như kết hợp với metformin và sulfonylurea trên bệnh nhân Trung Quốc25, hay đơn trị liệu hoặc phối hợp với những OADs thông thường khác trên bệnh nhân Châu á26. Những kết quả này tương đồng với những nghiên cứu trước đây về các thuốc ức chế DPP-4 khác trên bệnh nhân Châu á27-32.
Điều hiển nhiên là bệnh nhân thường không muốn tăng liều insulin vì điều trị bằng insulin nền thường làm tăng nguy cơ hạ đường huyết và tăng cân33. Trong nghiên cứu hiện tại, điều quan trọng sau giai đoạn insulin nền ổn định là liều insulin có thể được điều chỉnh theo quyết định lâm sàng của nghiên cứu viên với mục tiêu FPG điều trị là 6.1 mmol/L. Mặc dù liều insulin được tăng ở cả 2 nhóm và hơi tăng nhiều hơn ở nhóm giả dược so với nhóm linagliptin, mức độ tăng này nhỏ hơn nhiều so với mong muốn và phần lớn bệnh nhân không đạt được FPG khuyến cáo. Trong suốt giai đoạn mở rộng này, tăng liều không được khuyến khích và cũng có thể các nghiên cứu viên cũng không muốn tăng liều insulin vì sợ hạ đường huyết, đặc biệt trên người lớn tuổi và bệnh nhân có suy thận. Mặc dù mục tiêu FPG không đạt được trong phần lớn bệnh nhân ở cả 2 nhóm, điều trị bằng linagliptin làm giảm có ý nghĩa mức HbA1c so với giả dược, có thể được cho là do cải thiện FPG, cũng như cải thiện mức đường huyết sau ăn theo cơ chế phụ thuộc glucose.
Điều nên được ghi nhận là việc thêm linagliptin vào insulin nền dẫn đến giảm có ý nghĩa HbA1c mà không làm tăng nguy cơ hạ đường huyết và tăng cân, ngay cả khi liều insulin nền không được điều chỉnh giảm thấp xuống tại thời điểm đi vào nghiên cứu. Kiểm soát đường huyết vì vậy vẫn có thể được cải thiện mà không cần giảm liều insulin nền trước khi bắt đầu thêm linagliptin.Cũng vì thế, việc tăng nhẹ liều insulin nền trong suốt nghiên cứu không đủ để bù trừ tăng đường huyết trầm trọng trong dân số này với đái tháo đường type 2 nặng.Những kết quả quan sát này củng cố tính dung nạp và hiệu quả của phối hợp linagliptin với insulin nền. Lý do chính xác tại sao linagliptin có thể không làm tăng nguy cơ hạ đường huyết khi phối hợp với insulin nền, mặc dù gây giảm có ý nghĩa HbA1c, vẫn chưa biết. Tuy nhiên, các thuốc ức chế DPP-4 như linagliptin được suy đoán rằng không chỉ gây kích thích tiết insulin bởi các tế bào beta và ức chế tiết glucagon sau ăn bởi tế bào alpha, mà còn làm tăng đáp ứng của tế bào alpha với mức đường huyết thấp, dẫn đến tiết glucagon trong những điều kiện này (gián tiếp một phần là do tăng nồng độ polypeptide ưa insulin phụ thuộc glucose bởi quá trình ức chế DPP-4)34-35. Những tác dụng này có thể giải thích khả năng làm cải thiện kiểm soát đường huyết mà không làm tăng nguy cơ hạ đường huyết của linagliptin.
Trên bệnh nhân Châu Á, cơ chế rối loạn tiết insulin có thể quan trọng hơn trong sinh bệnh học đái tháo đường type 2 so với người da trắng4-6. Dữ liệu từ nghiên cứu rối loạn chuyển hóa, đái tháo đường quốc gia ở Trung Quốc, cho phép ước lượng tần suất mắc bệnh đái tháo đường ở Trung Quốc, cho thấy tần suất rối loạn dung nạp đường đơn thuần cao hơn so với tần suất rối loạn đường huyết đói36. Kết quả này củng cố chứng cứ cho thấy trên bệnh nhân Châu Á, rối loạn điều hoà đường huyết sau ăn là vấn đề chính nên được nhắm đến7,8, bằng cách tăng mức độ điều trị insulin hay thêm một OAD với cơ chế hoạt động phụ thuộc glucose. Linagliptin kích thích tiết insulin bằng một cơ chế phụ thuộc glucose với nguy cơ hạ đường huyết thấp, và vì thế có thể là lựa chọn đặc biệt hiệu quả trên bệnh nhân Châu Á10. Ngoài ra, linagliptin không như hầu hết các thuốc ức chế DPP-4 khác, có đường thải trừ chủ yếu không qua thận và không cần chỉnh liều ngay cả khi bệnh nhân giảm chức năng thận14. Điều này có thể mang lại lợi ích, bởi vì nhiều bệnh nhân được điều trị bằng insulin có suy chức năng thận, đặc biệt quan trọng trên dân số Châu Á, nơi có suất độ giảm chức năng thận nhiều hơn9.
Những kết quả của nghiên cứu dưới nhóm trên bệnh nhân Châu á này cho thấy có sự cải thiện đường huyết ở mức độ nhẹ so với dân số chung. Tuy nhiên, việc suy rộng các kết quả này cho dân số lớn hơn có thể bị giới hạn bởi tính chất hậu kiểm (post-hoc) của nghiên cứu, và bởi số lượng bệnh nhân nhỏ ở dân số dưới nhóm.
KẾT LUẬN:
Các kết quả của phân tích dưới nhóm này cho thấy linagliptin là một lựa chọn điều trị hiệu quả và dung nạp tốt cho bệnh nhân đái tháo đường type 2 Châu á kiểm soát đường huyết chưa đạt mục tiêu bằng insulin nền. Điều trị với linagliptin không làm tăng nguy cơ hạ đường huyết cũng như thay đổi cân nặng khi so sánh với giả dược cho tới 52 tuần điều trị.
Tài liệu trích dẫn:
1. International Diabetes Federation. Diabetes Atlas, sixth edition. Available at: http://www.idf.org/sites/default/files/EN_6E_Atlas_Full_0.pdf [Last accessed 7 August 2014]
2. Chan JC, Malik V, Jia W, et al. Diabetes in Asia: epidemiology, risk factors, and pathophysiology. JAMA 2009;301:2129-40
3. Yoon KH, Lee JH, Kim JW, et al. Epidemic obesity and type 2 diabetes in Asia. Lancet 2006;368:1681-8
4. Kang HW, Kim DJ, Lee MS, et al. Pathophysiologic heterogeneity in the development of type 2 diabetes mellitus in Korean subjects. Diabetes Res Clin Pract 2005;69:180-7
5. Kim DJ, Lee MS, Kim KW, et al. Insulin secretory dysfunction and insulin resistance in the pathogenesis of korean type 2 diabetes mellitus. Metabolism 2001;50:590-3
6. Suzuki H, Fukushima M, Usami M, et al. Factors responsible for development from normal glucose tolerance to isolated postchallenge hyperglycemia. Diabetes Care 2003;26:1211-5
7. Wang JS, Tu ST, Lee IT, et al. Contribution of postprandial glucose to excess hyperglycaemia in Asian type 2 diabetic patients using continuous glucose monitoring. Diabetes Metab Res Rev 2011;27:79-84
8. Sheu WH, Rosman A, Mithal A, et al. Addressing the burden of type 2 diabetes and cardiovascular disease through the management of postprandial hyperglycaemia: an Asian-Pacific perspective and expert recommendations. Diabetes Res Clin Pract 2011;92:312-21
9. Luk A, Chan JC. Diabetic nephropathy–what are the unmet needs? Diabetes Res Clin Pract 2008;82 Suppl 1:S15-20
10. Mu YM, Misra A, Adam JM, et al. Managing diabetes in Asia: overcoming obstacles and the role of DPP-IV inhibitors. Diabetes Res Clin Pract 2012;95:179-88
11. Chan SP, Ji LN, Nitiyanant W, et al. Hypoglycemic symptoms in patients with type 2 diabetes in Asia-Pacific-Real-life effectiveness and care patterns of diabetes management: the RECAP-DM study. Diabetes Res Clin Pract 2010;89:e30-2
12. Rosenstock J, Aguilar-Salinas C, Klein E, et al. Effect of saxagliptin monotherapy in treatment-naive patients with type 2 diabetes. Curr Med Res Opin 2009;25:2401-11
13. Gallwitz B. Implications of postprandial glucose and weight control in people with type 2 diabetes: understanding and implementing the International Diabetes Federation guidelines. Diabetes Care 2009;32 Suppl 2:S322-5
14. Graefe-Mody U, Friedrich C, Port A, et al. Effect of renal impairment on the pharmacokinetics of the dipeptidyl peptidase-4 inhibitor linagliptin(*). Diabetes Obes Metab 2011;13:939-46
15. Del Prato S, Barnett AH, Huisman H, et al. Effect of linagliptin monotherapy on glycaemic control and markers of beta-cell function in patients with inadequately controlled type 2 diabetes: a randomized controlled trial. Diabetes Obes Metab 2011;13:258-67
16. Kawamori R, Inagaki N, Araki E, et al. Linagliptin monotherapy provides superior glycaemic control versus placebo or voglibose with comparable safety in Japanese patients with type 2 diabetes: a randomized, placebo and active comparator-controlled, double-blind study. Diabetes Obes Metab 2012;14:348-57
17. Taskinen MR, Rosenstock J, Tamminen I, et al. Safety and efficacy of linagliptin as add- on therapy to metformin in patients with type 2 diabetes: a randomized, double-blind, placebo-controlled study. Diabetes Obes Metab 2011;13:65-74
18. Gomis R, Espadero RM, Jones R, et al. Efficacy and safety of initial combination therapy with linagliptin and pioglitazone in patients with inadequately controlled type 2 diabetes: a randomized, double-blind, placebo-controlled study. Diabetes Obes Metab 2011;13:653-61
19. Owens DR, Swallow R, Dugi KA, et al. Efficacy and safety of linagliptin in persons with type 2 diabetes inadequately controlled by a combination of metformin and sulphonylurea: a 24-week randomized study. Diabet Med 2011;28:1352-61
20. Inagaki N, Watada H, Murai M, et al. Linagliptin provides effective, well-tolerated add- on therapy to pre-existing oral antidiabetic therapy over 1 year in Japanese patients with type 2 diabetes. Diabetes Obes Metab 2013;15:833-43
21. Yki-Järvinen H, Rosenstock J, Durán-Garcia S, et al. Effects of adding linagliptin to basal insulin regimen for inadequately controlled type 2 diabetes: a ≥52-week randomized, double-blind study. Diabetes Care 2013;36:3875-81
22. Kozlovski P, Foley J, Shao Q, et al. Vildagliptin-insulin combination improves glycemic control in Asians with type 2 diabetes. World J Diabetes 2013;4:151-6
23. Kothny W, Foley J, Kozlovski P, et al. Improved glycaemic control with vildagliptin added to insulin, with or without metformin, in patients with type 2 diabetes mellitus. Diabetes Obes Metab 2013;15:252-7
24. Araki E, Kawamori R, Inagaki N, et al. Long-term safety of linagliptin monotherapy in Japanese patients with type 2 diabetes. Diabetes Obes Metab 2013;15:364-71
25. Zeng Z, Yang J, Tong N, et al. Efficacy and safety of linagliptin added to metformin and sulphonylurea in Chinese patients with type 2 diabetes: a sub-analysis of data from a randomised clinical trial. Curr Med Res Opin 2013;29:921-9
26. Zeng Z, Choi DS, Mohan V, et al. Linagliptin is efficacious and well tolerated in Asian patients with inadequately controlled type 2 diabetes. Diabetes 2012;61:A300
27. Pan C, Yang W, Barona JP, et al. Comparison of vildagliptin and acarbose monotherapy in patients with Type 2 diabetes: a 24-week, double-blind, randomized trial. Diabet Med 2008;25:435-41
28. Pan C, Xing X, Han P, et al. Efficacy and tolerability of vildagliptin as add-on therapy to metformin in Chinese patients with type 2 diabetes mellitus. Diabetes Obes Metab 2012;14:737-44
29. Mohan V, Yang W, Son HY, et al. Efficacy and safety of sitagliptin in the treatment of patients with type 2 diabetes in China, India, and Korea. Diabetes Res Clin Pract 2009;83:106-16
30. Yang W, Guan Y, Shentu Y, et al. The addition of sitagliptin to ongoing metformin therapy significantly improves glycemic control in Chinese patients with type 2 diabetes. J Diabetes 2012;4:227-37
31. Pan CY, Yang W, Tou C, et al. Efficacy and safety of saxagliptin in drug-naive Asian patients with type 2 diabetes mellitus: a randomized controlled trial. Diabetes Metab Res Rev 2012;28:268-75
32. Yang W, Pan CY, Tou C, et al. Efficacy and safety of saxagliptin added to metformin in Asian people with type 2 diabetes mellitus: a randomized controlled trial. Diabetes Res Clin Pract 2011;94:217-24
33. Swinnen SG, Hoekstra JB, DeVries JH. Insulin therapy for type 2 diabetes. Diabetes Care 2009;32 Suppl 2:S253-9
34. Ahrén B, Schweizer A, Dejager S, et al. Vildagliptin enhances islet responsiveness to both hyper- and hypoglycemia in patients with type 2 diabetes. J Clin Endocrinol Metab 2009;94:1236-43
35. Barnett A. DPP-4 inhibitors and their potential role in the management of type 2 diabetes. Int J Clin Pract 2006;60:1454-70
36. Yang W, Lu J, Weng J, et al. Prevalence of diabetes among men and women in China. N Engl J Med 2010;362:1090-101








