Mở đầu: Kết quả lâu dài của phẫu thuật bắc cầu mạch vành ảnh hưởng rất nhiều bởi tiến triển xơ vữa, xơ hóa nội mạc của cầu nối tĩnh mạch hiển. Ở thời điểm 1 năm sau phẫu thuật bắc cầu, tỉ lệ tắc hoàn toàn ít nhất 1 cầu tĩnh mạch
BS. Hồ Minh Tuấn
Bác Sĩ khoa tim mạch can thiệp BV Tim Tâm Đức
PGS.TS. Phạm Nguyễn Vinh
PGS.TS, Giám Đốc Y khoa BV Tim Tâm Đức
Tóm tắt
Mở đầu: Kết quả lâu dài của phẫu thuật bắc cầu mạch vành ảnh hưởng rất nhiều bởi tiến triển xơ vữa, xơ hóa nội mạc của cầu nối tĩnh mạch hiển. Ở thời điểm 1 năm sau phẫu thuật bắc cầu, tỉ lệ tắc hoàn toàn ít nhất 1 cầu tĩnh mạch hiển là 19% đến 41% (bảng 1) (1-8). Tái phẫu thuật mổ bắc cầu có nguy cơ biến chứng và tử vong cao. Vì vậy, can thiệp mạch vành qua da đặt stent là phương pháp điều trị thích hợp và chiếm khoảng 5-10% các thủ thuật can thiệp mạch vành qua da (9-11).
Mục đích: Trong bài báo này, chúng tôi mô tả đặc điểm tiến triển của cầu nối tĩnh mạch hiển, nguy cơ biến chứng của can thiệp cầu nối tĩnh mạch hiển, chiến lược thuốc kháng đông tối ưu quanh thủ thuật can thiệp, lựa chọn stent và biện pháp để giảm nguy cơ thuyên tắc phần sau chỗ hẹp mạch vành lúc can thiệp mạch vành qua da.
Phương pháp: Chọn lọc tài liệu từ các nghiên cứu và bài báo trong nước và trên thế giới.
Kết luận: Tĩnh mạch hiển thường sử dụng để làm cầu nối mạch vành, tuy nhiên tỉ lệ hẹp cao sau phẫu thuật. So với can thiệp các nhánh mạch vành nguyên thủy, can thiệp cầu nối tĩnh mạch hiển có kết quả lâm sàng kém hơn bao gồm: tái hẹp, tái tưới máu mạch đích, nhồi máu cơ tim và tử vong. Sử dụng dụng cụ phòng ngừa thuyên tắc phần sau chỗ hẹp (distal embolic protecton) là chỉ định nhóm I theo hướng dẫn của hiệp hội tim mạch và trường môn tim mạch Hoa Kỳ để giảm thuyên tắc sau chỗ hẹp, không có dòng chảy và nhồi máu cơ tim. Một số nghiên cứu cho thấy stent phủ thuốc giảm tái hẹp so với stent không phủ thuốc. Tuy nhiên, nghiên cứu lớn, ngẫu nhiên là cần thiết để so sánh giữa 2 loại sent.
Abstract
Background: The long-term success of surgical coronary revascularization is limited by accelerated atherosclerosis and intimal fibrosis of the saphenous vein graft (SVG) after its use as a vascular conduit. At 1 year, the incidence of 1 or more total SVG occlusions has been reported to be as high as 19-41% after on-pump bypass surgery (Table 1) (1–8). Because of increased morbidity and mortality with repeat coronary artery bypass graft surgery, SVG intervention is considered by many to be the preferred revascularization modality in patients with diseased SVGs and accounts for approximately 5% to 10% of all percutaneous coronary interventions (PCI) (9–14).
Objective: In this review, we describe the characteristic of SVG, risk factors for complications after SVG intervention and discuss the optimal procedural treatment strategies regarding periprocedural anticoagulation, choice of stent, and measures to mitigate the risks of distal embolization.
Method Data Source: Manual review of bibliographies from selected articles and monographs.
Conclusion: Saphenous vein grafts are commonly used conduits for surgical revascularization of coronary arteries but are associated with poor long-term patency rates. Percutaneous revascularization of saphenous vein grafts is associated with worse clinical outcomes including higher rates of in-stent restenosis, target vessel revascularization, myocardial infarction, and death compared with percutaneous coronary intervention of native coronary arteries. Use of embolic protection devices is a Class I indication according to the American College of Cardiology/American Heart Association guidelines to decrease the risk of distal embolization, no-reflow, and periprocedural myocardial infarction. Most available evidence supports treatment with drug-eluting stents in this high-risk lesion subset to reduce angiographic and clinical restenosis, although large, randomized trials comparing drug-eluting stents and bare-metal stents are needed.
|
Bảng 1.Các nghiên cứu tỉ lệ hẹp, tắc cầu nối tĩnh mạch hiển |
|||
|
Tên nghiên cứu hoặc tác giả |
Thời điểm 1 năm (%) |
Thời điểm 5 năm (%) |
Thời điểm 10 năm (%) |
|
Prague-4(1) |
41 (mổ tim hở) 51 (mổ tim kín) |
|
|
|
Prevent IV (2) |
41.7 (trên số bệnh nhân) 26.6 (trên số cầu) |
|
|
|
Fitzgibbon et al.(3) |
19 (trên số cầu) |
25 (trên số cầu) |
40 (trên số cầu) |
|
RIGOR (4) |
31 (trên số bệnh nhân) 19 (trên số cầu) |
|
|
|
Halabi et al. (5) |
39.3 (trên số bệnh nhân) |
|
|
|
Khot et al. (6) |
30.1 (trên số cầu) |
|
|
|
ROOBY (7) |
28.7 (mổ tim hở) 36.5 (mổ tim kín) |
|
|
|
Goldman et al. (8) |
20 (trên số bệnh nhân) |
31 (trên số bệnh nhân) |
39 (trên số bệnh nhân) |
I.Đặc điểm của cầu nối tĩnh mạch hiển
Động mạch vú trong thường là cầu nối với động mạch liên thất trước. Trong khi tĩnh mạch hiển rất thường sử dụng cho bắc cầu các nhánh mạch vành khác, có nhiều lý do. Thứ nhất, vì kích thước lớn và tính chất thành tĩnh mạch nên kỹ thuật nối dễ hơn so với loại cầu động mạch; Thứ hai, hệ thống tĩnh mạch hiển rộng lớn thuận lợi việc lấy để làm cầu nối; Thứ ba, tĩnh mạch hiển có thể lấy được đoạn dài nên có thể sử dụng để nối bất kỳ nhánh nào của mạch vành; Thứ tư, tĩnh mạch hiển dễ lấy ra từ chi (15).
Tuy nhiên, bất lợi của cầu nối tĩnh mạch hiển là tỉ lệ hẹp cao sau mổ bắc cầu: khoảng 25% hẹp hoặc nghẽn ở thời điểm 1 năm sau mổ bắc cầu (16-18). Thêm vào đó, trong thời gian từ 1-5 năm sau mổ bắc cầu có thêm 1-2 % bệnh nhân bị hẹp mỗi năm, và thời gian từ 5-10 nằm có thêm 4-5% bệnh nhân hẹp mỗi năm. Vì vậy, ở thời điểm 10 năm sau mổ bắc cầu mạch vành chỉ có 50-60% cầu nối tĩnh mạch hiển là thông tốt (19).
Trong năm đầu tiên sau phẫu thuật bắc cầu mạch vành, cầu nối tĩnh mạch hiển hẹp là do: lỗi kỹ thuật, huyết khối, và tăng sinh nội mạc. Các cầu nối tĩnh mạch hiển bị tổn thương nội mạc do thủ thuật khi lấy ra từ chi, và chịu áp lực cao động mạch khi làm cầu nối. Những tổn thương nội mạc dẫn đến kết tập tiểu cầu và gây huyết khối, tắc cấp. Kết tập tiểu cầu cũng làm tăng sinh nội mạc: sau khi kết dính vào nội mạc, tiểu cầu phóng thích protein gây phân bào, protein này kích thích cơ trơn gây tăng sinh nội mạc (20-24). Sau 1 năm, xơ vữa mạch máu đóng vai trò thêm vào trong hẹp và tắc cầu nối tĩnh mạch hiển (25-26).
II.Quyết định can thiệp cầu nối tĩnh mạch hiển
Quyết định can thiệp cầu tĩnh mạch hiển dựa vào: triệu chứng bệnh nhân, mức độ hẹp của cầu nối tĩnh mạch hiển trên hình ảnh chụp mạch vành và bằng chứng thiếu máu cơ tim trên trắc nghiệm không xâm lấn (bảng 2). Các phương tiện xâm lấn hổ trợ như đo phân xuất dự trữ dòng máu mạch vành (FFR) và siêu âm trong lòng mạch (IVUS), đặc biệt đo phân xuất dự trữ dòng máu mạch vành rất hữu ích trong chẩn đoán hẹp có ý nghĩa: giá trị< 0.8. Đồng thời, bằng cách kéo lùi dây đo áp lực (pressure wire) có thể xác định vị trí hẹp khu trú có ý nghĩa trên đoạn hẹp lan tỏa. Tuy nhiên, đây là giá trị ngưỡng trên của hẹp nhánh mạch vành nguyên thủy có ý nghĩa, nghiên cứu lớn tiền cứu trên cầu nối tĩnh mạch hiển là cần thiết để xác định giá trị ngưỡng của hẹp có ý nghĩa.
|
Bảng 2. Chỉ định tái tưới máu đối với bệnh nhân hẹp cầu nối tĩnh mạch hiển(ACCF/SCAI/STS/AATS/AHA/ASNC/HFSA/SCCT; Appropriate Use Criteria for Coronary Revascularization 2012) |
|||
|
|
Không triệu chứng |
CCS I hoặc II |
CCS III hoặc IV |
|
Hẹp 1 hoặc nhiều cầu tĩnh mạch hiển Kết quả trắc nghiệm không xâm lấn nguy cơ thấp và chức năng thất trái tốt Chưa điều trị nội khoa tối ưu |
I(3) |
U(4) |
U(6) |
|
Hẹp 1 hoặc nhiều cầu tĩnh mạch hiển Kết quả trắc nghiệm không xâm lấn nguy cơ thấp và chức năng thất trái tốt Điều trị nội khoa tối ưu |
U(4) |
U(6) |
A(7) |
|
Hẹp 1 hoặc nhiều cầu tĩnh mạch hiển Kết quả trắc nghiệm không xâm lấn nguy cơ trung bình Chưa điều trị nội khoa tối ưu |
U(4) |
U(6) |
A(7) |
|
Hẹp 1 hoặc nhiều cầu tĩnh mạch hiển Kết quả trắc nghiệm không xâm lấn nguy cơ trung bình Điều trị nội khoa tối ưu |
U(4) |
A(7) |
A(8) |
|
Hẹp 1 hoặc nhiều cầu tĩnh mạch hiển Kết quả trắc nghiệm không xâm lấn nguy cơ cao Chưa điều trị nội khoa tối ưu |
U(6) |
A(7)
|
A(7) |
|
Hẹp 1 hoặc nhiều cầu tĩnh mạch hiển Kết quả trắc nghiệm không xâm lấn nguy cơ cao Điều trị nội khoa tối ưu |
A(7) |
A(8) |
A(9) |
|
A(7-9): chỉ định thích hợp; U(3-6): chỉ định có thể thích hợp cần thêm nghiên cứu lâm sàng và thông tin bệnh nhân; I(1-3): chỉ định không thích hợp |
|||
Các nghiên cứu đoàn hệ cho thấy kết quả sống còn trung hạn và dài hạn là tương đương nhau đối với nong mạch vành qua da và tái mổ bắc cầu mạch vành ở những bệnh nhân đã mổ bắc cầu mạch vành có chỉ định tái tưới máu (27-35).
Tỉ lệ can thiệp mạch vành qua da thành công tắc mạn tính hoàn toàn cầu nối tĩnh mạch hiển là 68%, theo dõi ở thời điểm 18 tháng tỉ lệ cần tái tưới máu tới 61% mặc dù tỉ lệ sử dụng stent phủ thuốc tới 95% (36). Vì vậy, cần xem xét ưu tiên can thiệp mạch vành nguyên thủy trước nếu tổn thương phù hợp trong trường hợp tắc hoàn toàn mạn tính cầu nối tĩnh mạch hiển.
III.Thuốc kháng đông và chống ngưng tập tiểu cầu
Phân tích sau nghiên cứu (post hoc) cho thấy sử dụng thuốc ức chế thụ thể GPIIbIIa kết hợp với dụng cụ phòng ngừa thuyên tắc sau chỗ hẹp làm tăng tỉ lệ thành công thủ thuật. Tuy nhiên, không cải thiện biến cố tim mạch chính ở thời điểm 30 ngày (37).
Trong phân tích phân nhóm của nghiên cứu ACUITY (38), tỉ lệ chảy máu thấp hơn trong nhóm dùng Bivaluridin đơn độc so với nhóm dùng kết hợp Heparine và ức chế thụ thể GPIIbIIIa. Vì vậy, Bivalurindin có thể là kháng đông ưu tiên dùng trong can thiệp cầu nối tĩnh mạch hiển.
IV.Chọn stent trong can thiệp cầu nối tĩnh mạch hiển
Có nhiều nghiên cứu so sánh giữa stent phủ thuốc, stent không phủ thuốc và stent được bao phủ lớp polytetrafluorethylene (covered stent) (liệt kê bảng 3). Đối với stent bao phủ lớp polytetrafluorethylene, cho thấy kết quả kém hơn về biến cố tim mạch chính, nhồi máu cơ tim và tử vong so với stent phủ thuốc và không phủ thuốc. Mặt khác, phân tích đa trung tâm gồm 172 bệnh nhân can thiệp cầu nối tĩnh mạch hiển (39) cho thấy không có sự khác biệt giữa stent không phủ thuốc và stent phủ thuốc thế hệ thứ nhất về tử vong và tái tưới máu mạch đích. Nghiên cứu đang thực hiện về thế hệ thứ 2 của stent phủ thuốc đối với can thiệp cầu nối tĩnh mạch hiển SOS-Xience V sẽ cho ta thêm thông tin về stent phủ thuốc đối với can thiệp cầu nối tĩnh mạch hiển.
|
Bảng 3.Các nghiên cứu lâm sàng so sánh các loại stent trong can thiệp cầu nối tĩnh mạch hiển |
||||||||||||||||||
|
|
SYMBIOT III |
BARRICADE |
RECOVERS |
SOS |
RRISC |
ISAR-CABG |
||||||||||||
|
|
PTFE |
BMS |
P |
PTFE |
BMS |
P |
PTFE |
BMS |
P |
PES |
BMS |
P |
SES |
BMS |
P |
DES |
BMS |
P |
|
Biến cố tim mạch chính |
||||||||||||||||||
|
1 năm |
30.6 |
26.6 |
0.43 |
39.2 |
28.0 |
0.07 |
23.1 |
15.9 |
0.15 |
37 |
49 |
0.20 |
15.8 |
29.7 |
0.15 |
15.4 |
22.1 |
0.03 |
|
3 năm |
|
|
|
60.2 |
37.0 |
0.001 |
|
|
|
54 |
77 |
0.49 |
58 |
41 |
0.13 |
|
|
|
|
5 năm |
|
|
|
68.3 |
51.8 |
0.007 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Tử vong |
||||||||||||||||||
|
1 năm |
20.6 |
4.7 |
0.29 |
7.0 |
5.0 |
0.51 |
24.6 |
2.8 |
0.92 |
12 |
5 |
0.27 |
2.6 |
0 |
0.99 |
5.2 |
4.7 |
0.82 |
|
3 năm |
|
|
|
18.8 |
11.2 |
0.13 |
|
|
|
24 |
13 |
0.19 |
29 |
0 |
<0.001 |
|
|
|
|
5 năm |
|
|
|
29.8 |
22.3 |
0.20 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Nhồi máu cơ tim |
||||||||||||||||||
|
1 năm |
9.2 |
10.9 |
0.61 |
14.2 |
11.3 |
0.53 |
14.1 |
5.5 |
0.02 |
15 |
31 |
0.10 |
2.6 |
0 |
0.99 |
4.2 |
6.0 |
0.27 |
|
3 năm |
|
|
|
21.0 |
14.1 |
0.21 |
|
|
|
17 |
46 |
0.01 |
18 |
5 |
0.15 |
|
|
|
|
5 năm |
|
|
|
26.2 |
17.4 |
0.16 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Tái tưới máu mạch đích |
||||||||||||||||||
|
1 năm |
23.5 |
15.6 |
0.06 |
28.2 |
21.1 |
0.46 |
9.6 |
8.3 |
0.84 |
5 |
28 |
0.003 |
5.3 |
21.6 |
0.05 |
7.2 |
13.1 |
0.02 |
|
3 năm |
|
|
|
37.4 |
21.8 |
0.02 |
|
|
|
10 |
41 |
0.004 |
24 |
30 |
0.55 |
|
|
|
|
5 năm |
|
|
|
43.9 |
29.6 |
0.04 |
|
|
|
|
|
|
|
|
|
|
|
|
|
– PTFE: stent có bao phủ lớp polytetrafluorethylene (covered stent); BMS: stent không phủ thuốc; DES: stent phủ thuốc; PES: stent phủ thuốc paclitaxel; SES: stent phủ thuốc sirolimus. – Ô trống:không có theo dõi |
||||||||||||||||||
V.Kỹ thuật can thiệp cầu nối tĩnh mạch hiển
Dụng cụ phòng ngừa thuyên tắc mạch vành
Có đến 91% các ca có huyết khối xuất hiện trong dụng cụ phòng ngừa thuyên tắc đoạn sau tổn thương trong can thiệp cầu nối tĩnh mạch hiển (40). Mặc dù, dụng cụ phòng ngừa thuyên tắc đoạn sau tổn thương trong can thiệp cầu nối tĩnh mạch hiển là chỉ định nhóm I theo hướng dẫn của hiệp hội tim mạch và trường môn tim mạch Hoa Kỳ năm 2011 (41). Tuy nhiên, tại Hoa Kỳ cũng chỉ có 23% các ca can thiệp cầu nối tĩnh mạch hiển có sử dụng dụng cụ phòng ngừa thuyên tắc đoạn sau tổn thương (10).
Tần xuất biến cố tim mạch chính gấp đôi trong can thiệp cầu nối tĩnh mạch hiển so với can thiệp mạch vành nguyên thủy (42). Nghiên cứu ngẫu nhiên cho thấy sử dụng dụng cụ phòng ngừa thuyên tắc đoạn sau chỗ hẹp làm giảm tử vong và biến cố tim mạch ở thời điểm 30 ngày (43), đồng thời kết quả các nghiên cứu cho thấy lợi điểm tương đương giữa dụng cụ phòng ngừa thuyên tắc đoạn sau tổn thương bằng lưới lọc và bằng bóng ở đoạn trước tổn thương (44-45).
Các dụng cụ phòng ngừa thuyên tắc liệt kê ở bảng 4 và hình 1, 2, 3.
|
Bảng 4. Ưu và nhược điểm của các dụng cụ phòng ngừa thuyên tắc mạch vành trong can thiệp cầu nối tĩnh mạch hiển |
|||
|
|
Lưới lọc sau chỗ hẹp ( Distal filter) |
Bóng gây nghẽn đoạn xa (Distal balloon occlusion) |
Bóng gây nghẽn đoạn gần (Proximal balloon occlusion) |
|
Tắc hoàn toàn |
Không |
Có |
Có |
|
Gây thiếu máu cơ tim lúc can thiệp |
Không |
Có |
Có |
|
Duy trì dòng lúc can thiệp |
Có |
Không |
Không |
|
Kích thước |
3.2 F |
2.7 F |
|
|
Sử dụng |
Đơn giản |
Phức tạp |
Phức tạp |
|
Lọc mảnh rất nhỏ |
Không |
Có |
Có |
|
Bắt được chất trung gian thần kinh gây nghẽn mạch |
Không |
Có |
Có |

Hình 1. Filter wire EZ: Lưới lọc sau chỗ hẹp (distal filter): lưới lọc đính vào dây dẫn 0.014 inch, kích thước lỗ của lưới lọc là 100 µm.
Trong thủ thuật, lưới lọc được đưa vào phần sau chỗ hẹp qua ống thông can thiệp; Kế đến nong và đặt stent đồng thời lưới lọc bắt huyết khối và mảnh vỡ mảng xơ vữa; Sau cùng, thu lại lưới lọc cùng với huyết khối, mảnh vỡ.
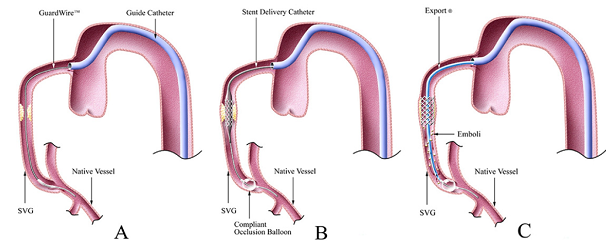
Hình 2. PercuSurge GuardWire Distal Protection System: Bóng gây nghẽn đoạn xa: A-Bóng đưa qua chỗ hẹp; B-Bóng được bơm lên và thủ thuật nong và đặt stent thực hiện dưới sự bảo vệ của bóng không cho huyết khối và mảnh xơ vữa đi xuống phần xa mạch vành; C- Dùng dụng cụ hút hết huyết khối và mảnh vỡ mảng xơ vữa sau đó xả bóng.
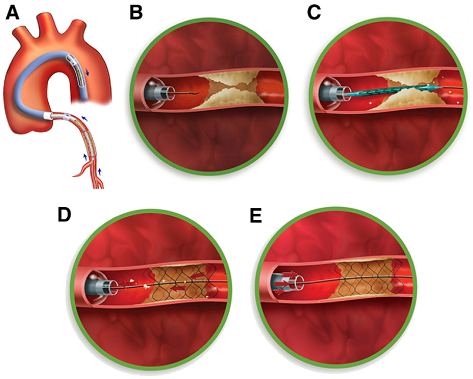
Hình 3. Proxis Proximal Embolic Protection Device:bóng gây nghẽn đoạn đầu: A-Hình tổng thể dụng cụ phòng ngừa huyết khối; B-Khi dụng cụ đưa vào ngay trước chỗ hẹp, bóng được bơm lên để gây mất dòng chảy; C- Đưa wire qua chỗ hẹp, nong và đặt stent, các mảnh vỡ và huyết khối vẫn còn quanh tổn thương vì không có dòng chảy; D- Hút huyết khối và mảnh vỡ mảng xơ vữa; E- Xả bóng phục hồi dòng chảy và lấy dụng cụ ra.
Các nghiên cứu lâm sàng về sử dụng dụng cụ phòng ngừa thuyên tắc mạch vành trong can thiệp cầu nối tĩnh mạch hiển liệt kê bảng 5.
|
Bảng 5. Kết quả lâm sàng ở thời điểm 30 ngày của dụng cụ phòng ngừa thuyên tắc mạch vành |
||||
|
Tên nghiên cứu |
Biến cố tim mạch chính |
Tử vong |
Nhồi máu cơ tim |
Không có dòng chảy sau can thiệp |
|
SAFER(20) |
||||
|
– Dụng cụ GuardWire |
9.6 |
1.0 |
8.6 |
3 |
|
– Nhóm không dùng dụng cụ phòng ngừa thuyên tắc |
16.5 |
2.3 |
14.7 |
9 |
|
– P |
0.004 |
0.17 |
0.008 |
0.001 |
|
FIRE(46) |
||||
|
– Dụng cụ FilterWire EX |
9.9 |
0.9 |
9 |
|
|
– Dụng cụ GuardWire |
11.6 |
0.9 |
10 |
|
|
– P |
0.53 |
0.99 |
0.69 |
|
|
BLAZE(47) |
||||
|
– Dụng cụ FilterWire EZ |
6.7 |
0 |
6.7 |
|
|
PRIDE(48) |
||||
|
– Dụng cụ TriActiv |
11.2 |
1.3 |
9.9 |
|
|
– Dụng cụ GuardWire/FilterWire EZ |
10.1 |
0.6 |
8.8 |
|
|
– P |
0.65 |
0.45 |
0.64 |
|
|
SPIDER(49) |
||||
|
– Dụng cụ Spider |
9.1 |
0.3 |
7.7 |
|
|
– Dụng cụ GuardWire/FilterWire EZ |
8.4 |
0.6 |
7.0 |
|
|
– P |
0.79 |
NS |
NS |
|
|
PROXIMAL(50) |
||||
|
– Dụng cụ Proxis |
9.2 |
0.7 |
6.4 |
|
|
– Nhóm không dùng dụng cụ phòng ngừa thuyên tắc |
10.0 |
1.0 |
7.9 |
|
|
– P |
0.78 |
1.0 |
0.52 |
|
|
Giá trị tính theo %; NS: không có ý nghĩa; ô trống: không có dữ liệu theo dõi. |
||||
VI.Kết luận
Tỉ lệ hẹp và tắc cầu nối tĩnh mạch hiển rất cao trong các nghiên cứu theo dõi sau phẫu thuật bắc cầu mạch vành. Dụng cụ phòng ngừa thuyên tắc mạch vành là cần thiết sử dụng trong can thiệp cầu nối tĩnh mạch hiển vì đã có nhiều nghiên cứu lâm sàng cho thấy nhiều lợi điểm và có khuyến cáo mạnh từ hiệp hội tim mạch Hoa Kỳ. Stent phủ thuốc có thể giảm tái hẹp sau can thiệp cầu nối tĩnh mạch hiển so với stent không phủ thuốc. Tuy nhiên, nghiên cứu lâm sàng lớn và ngẫu nhiên là cần thiết để chứng minh rõ ràng. Khi hẹp hoặc tắc cầu nối tĩnh mạch hiển có chỉ định can thiệp, chúng ta luôn xem xét mạch vành nguyên thủy có thể can thiệp được hay không trước khi quyết định can thiệp cầu nối tĩnh mạch hiển.
Tài liệu tham khảo
1. Widimsky P, Straka Z, Stros P, et al. One-year coronary bypass graft patency: a randomized comparison between off-pump and on-pump surgery angiographic results of the PRAGUE-4 trial. Circulation 2004;110:3418 –23.
2. Alexander JH, Hafley G, Harrington RA, et al., for the PREVENT IV Investigators. Efficacy and safety of edifoligide, an E2F transcription factor decoy, for prevention of vein graft failure following coronary artery bypass graft surgery: PREVENT IV: a randomized controlled trial. JAMA 2005;294:2446 –54.
3. Fitzgibbon GM, Kafka HP, Leach AJ, Keon WJ, Hooper GD, Burton JR. Coronary bypass graft fate and patient outcome: angiographic follow-up of 5,065 grafts related to survival and reoperation in 1,388 patients during 25 years. J Am Coll Cardiol 1996;28:616 –26.
4. Gluckman TJ, McLean RC, Schulman SP, et al. Effects of aspirin responsiveness and platelet reactivity on early vein graft thrombosis after coronary artery bypass graft surgery. J Am Coll Cardiol 2011;57: 1069–77.
5. Halabi AR, Alexander JH, Shaw LK, et al. Relation of early saphenous vein graft failure to outcomes following coronary artery bypass surgery. Am J Cardiol 2005;96:1254 –9.
6. Khot UN, Friedman DT, Pettersson G, Smedira NG, Li J, Ellis SG. Radial artery bypass grafts gave an increased occurrence of angiographically severe stenosis and occlusion compared with left internal mammary arteries and saphenous vein grafts. Circulation 2004;109:2086–91.
7. Shroyer AL, Grover FL, Hattler B, et al., for the ROOBY Study Group. On-pump versus off-pump coronary-artery bypass surgery. N Engl J Med 2009;361:1827–37.
8. Goldman S, Zadina K, Moritz T, et al., for the VA Cooperative Study Group #207/297/364. Long-term patency of saphenous vein and left internal mammary artery grafts after coronary artery bypass surgery: results from a Department of Veterans Affairs Cooperative Study. J Am Coll Cardiol 2004;44:2149 –56.
9. Brodie BR, Wilson H, Stuckey T, et al. Outcomes with drug-eluting versus bare-metal stents in saphenous vein graft intervention: results from the STENT (Strategic Transcatheter Evaluation of New Therapies) Group. J Am Coll Cardiol Intv 2009;2:1105–12.
10. Brilakis ES, Wang TY, Rao SV, et al. Frequency and predictors of drug-eluting stent use in saphenous vein bypass graft percutaneous coronary interventions: a report from the American College of Cardiology National Cardiovascular Data CathPCI Registry. J Am Coll Cardiol Intv 2010;3:1068 –73.
11. Morrison DA, Sethi G, Sacks J, et al., for the VA Cooperative Study Group #385. Percutaneous coronary intervention versus repeat bypass surgery for patients with medically refractory myocardial ischemia: AWESOME randomized trial and registry experience with post- CABG patients. J Am Coll Cardiol 2002;40:1951– 4.
12. Loop FD. A 20-year experience in coronary artery reoperations. Eur Heart J 1989;10 Suppl M:78–84.
13. Foster ED, Fisher LD, Kaiser GC, Myers WO. Comparison of operative mortality and morbidity for initial and repeat coronary artery bypass grafting: the Coronary Artery Surgery Study (CASS) registry experience. Ann Thorac Surg 1984;38:563–70.
14. Lytle BW, Loop FD, Cosgrove DM, et al. Fifteen hundred coronary reoperations: results and determinants of early and late survival. J Thorac Cardiovasc Surg 1987;93:847–59.
15. Joseph F. Sabik III, MD; Understanding Saphenous Vein Graft Patency; Circulation. 2011;124:273-275
16. Sabik JFI, Lytle BW, Blackstone EH, et al. Comparison of saphenous vein and internal thoracic artery graft patency by coronary system. Ann Thorac Surg. 2005;79:544 –51
17. FitzGibbon GM, Kafka HP, Leach AJ, et al. Coronary bypass graft fate and patient outcome: angiographic follow-up of 5065 grafts related to survival and reoperation in 1,388 patients during 25 years. J Am Coll Cardiol. 1996;28:616 –26.
18. Chesebro JH, Fuster V, Elveback LR, et al. Effect of dipyridamole and aspirin on late vein-graft patency after coronary bypass operations. N Engl J Med. 1984;310:209 –14.
19. Bourassa MG, Fisher LD, Campeau L, et al. Long-term fate of bypass grafts: the Coronary Artery Surgery Study (CASS) and Montreal Heart Institute experiences. Circulation. 1985;72:V71–8.
20. Unni KK, Kottke BA, Titus JL, Frye RL, Wallace RB, Brown AL. Pathologic changes in aortocoronary saphenous vein grafts. Am J Cardiol. 1974;34:526 –532.
21. Bulkley BH, Hutchins GM. Accelerated “atherosclerosis.” A morphologic study of 97 saphenous vein coronary artery bypass grafts. Circulation. 1977;55:163–169.
22. Barboriak JJ, Batayias GE, Pintar K, Tieu TM, Van Horn DL, Korns ME. Late lesions in aorta-coronary artery vein grafts. J Thorac Cardiovasc Surg. 1977;73:596–601.
23. Kern WH, Dermer GB, Lindesmith GG. The intimal proliferation in aortic-coronary saphenous vein grafts. Light and electron microscopic studies. Am Heart J. 1972;84:771–777.
24. Minick CR, Stemerman MB, Insull W Jr. Role of endothelium and hypercholesterolemia in intimal thickening and lipid accumulation. Am J Pathol. 1979;95:131–158.
25. Fuster V, Dewanjee MK, Kaye MP, Josa M, Metke MP, Chesebro JH. Noninvasive radioisotopic technique for detection of platelet deposition in coronary artery bypass grafts in dogs and its reduction with platelet inhibitors. Circulation. 1979;60:1508 –1512.
26. Chesebro JH, Clements IP, Fuster V, Elveback LR, Smith HC, Bardsley WT, Frye RL, Holmes DR Jr, Vlietstra RE, Pluth JR, Wallace RB, Puga FJ, Orszulak TA, Piehler JM, Schaff HV, Danielson GK. A platelet-inhibitor- drug trial in coronary-artery bypass operations: benefit of perioperative dipyridamole and aspirin therapy on early postoperative vein-graft patency. N Engl J Med. 1982;307:73–78.
27. Gurfinkel EP, Perez de la Hoz R, Brito VM, et al. Invasive vs noninvasive treatment in acute coronary syndromes and prior bypass surgery. Int J Cardiol. 2007;119:65–72.
28. Morrison DA, Sethi G, Sacks J, et al. Percutaneous coronary intervention versus coronary artery bypass graft surgery for patients with medically refractory myocardial ischemia and risk factors for adverse outcomes with bypass: a multicenter, randomized trial. Investigators of the Department of Veterans Affairs Cooperative Study #385, the Angina With Extremely Serious Operative Mortality Evaluation (AWESOME). J Am Coll Cardiol. 2001;38:143–9.
29. Subramanian S, Sabik JF, Houghtaling PL, et al. Decision-making for patients with patent left internal thoracic artery grafts to left anterior descending. Ann Thorac Surg. 2009;87:1392– 8.
30. Pfautsch P, Frantz E, Ellmer A, et al. [Long-term outcome of therapy of recurrent myocardial ischemia after surgical revascularization]. Z Kardiol. 1999;88:489 –97.
31. Weintraub WS, Jones EL, Morris DC, et al. Outcome of reoperative coronary bypass surgery versus coronary angioplasty after previous bypass surgery. Circulation. 1997;95:868 –77.
32. Brener SJ, Lytle BW, Casserly IP, et al. Predictors of revascularization method and long-term outcome of percutaneous coronary intervention or repeat coronary bypass surgery in patients with multivessel coronary disease and previous coronary bypass surgery. Eur Heart J. 2006;27: 413–8.
33. Lytle BW, Loop FD, Taylor PC, et al. The effect of coronary reoperation on the survival of patients with stenoses in saphenous vein bypass grafts to coronary arteries. J Thorac Cardiovasc Surg. 1993; 105:605–12.
34. Sergeant P, Blackstone E, Meyns B, et al. First cardiological or cardiosurgical reintervention for ischemic heart disease after primary coronary artery bypass grafting. Eur J Cardiothorac Surg. 1998;14: 480–7.
35. Stephan WJ, OKeefe JH Jr, Piehler JM, et al. Coronary angioplasty versus repeat coronary artery bypass grafting for patients with previous bypass surgery. J Am Coll Cardiol. 1996;28:1140–6.
36. Al-Lamee R, Ielasi A, Latib A, et al. Clinical and angiographic outcomes after percutaneous recanalization of chronic total saphenous vein graft occlusion using modern techniques. Am J Cardiol 2010;106:1721–7.
37. Jonas M, Stone GW, Mehran R, et al. Platelet glycoprotein IIb/IIIa receptor inhibition as adjunctive treatment during saphenous vein graft stenting: differential effects after randomization to occlusion or filterbased embolic protection. Eur Heart J 2006;27:920–8.
38. Kumar D, Dangas G, Mehran R, et al. Comparison of bivalirudin versus bivalirudin plus glycoprotein IIb/IIIa inhibitor versus heparin plus glycoprotein IIb/IIIa inhibitor in patients with acute coronary syndromes having percutaneous intervention for narrowed saphenous vein aorto-coronary grafts (the ACUITY Trial Investigators). Am J Cardiol 2010;106:941–5.
39. Lee MS, Hu PP, Aragon J, et al. Comparison of sirolimus-eluting stents with paclitaxel-eluting stents in saphenous vein graft intervention (from a multicenter Southern California Registry). Am J Cardiol 2010;106:337– 41
40. Grube E, Schofer J, Webb J, et al., for SAFE Trial Study Group. Evaluation of a balloon occlusion and aspiration system for protection from distal embolization during stenting and saphenous vein grafts. Am J Cardiol 2002;89:941–5.
41. Smith SC Jr., Feldman TE, Hirshfeld JW Jr., et al. ACC/AHA/SCAI 2011 guideline update for percutaneous coronary intervention— summary article: a report of the American College of Cardiology/ American Heart Association Task Force on Practice Guidelines (ACC/AHA/SCAI Writing Committee to Update the 2005 Guidelines for Percutaneous Coronary Intervention). J Am Coll Cardiol 2011;47:216 –35.
42. Hoffmann R, Hamm C, Nienaber CA, et al. Implantation of sirolimuseluting stents in saphenous vein grafts is associated with high clinical follow-up event rates compared with treatment of native vessels. Coron Artery Dis. 2007;18:559–64.
43. Baim DS, Wahr D, George B, et al. Randomized trial of a distal embolic protection device during percutaneous intervention of saphenous vein aorto-coronary bypass grafts. Circulation. 2002;105:1285–90.
44. Mauri L, Cox D, Hermiller J, et al. The PROXIMAL trial: proximal protection during saphenous vein graft intervention using the Proxis Embolic Protection System: a randomized, prospective, multicenter clinical trial. J Am Coll Cardiol. 2007;50:1442–9.
45. Stone GW, Rogers C, Hermiller J, et al. Randomized comparison of distal protection with a filter-based catheter and a balloon occlusion and aspiration system during percutaneous intervention of diseased saphenous vein aorto-coronary bypass grafts. Circulation. 2003;108: 548–53.
46. Stone GW, Rogers C, Hermiller J, et al., for the FilterWire EX Randomized Evaluation Investigators. Randomized comparison of distal protection with a filter-based catheter and a balloon occlusion and aspiration system during percutaneous intervention of diseased saphenous vein aortocoronary bypass grafts. Circulation 2003;108:548–53.
47. Cox D, Masud A, Myers F, et al. Stenting in saphenous vein grafts with distal protection using the second generation FilterWire EZ: the BLAZE registry (abstr). Am J Cardiol 2003;92 Suppl 6:33L.
48. Carrozza JP, Mumma M, Breall JA, et al., for the PRIDE Study Investigators. Randomized evaluation of the TriActiv balloonprotection flush and extraction system for the treatment of saphenous vein graft disease. J Am Coll Cardiol 2005;46:1677– 83.
49. Dixon SR. Saphenous vein graft protection in a distal embolic protection randomized trial. Paper presented at: Transcatheter Cardiovascular Therapeutics 2005; October 18, 2005; Washington, DC.
50. Mauri L, Cox D, Hermiller J, et al. The PROXIMAL trial: proximal protection during saphenous vein graft intervention using the Proxis Embolic Protection System: a randomized, prospective, multicenter clinical trial. J Am Coll Cardiol 2007;50:1442–9.








