I/ Đại cương
Gần đây, các vấn đề xử trí bệnh nhân (BN) đái tháo đường (ĐTĐ) có suy giảm chức năng thận đang ngày càng được chú ý, nhất là từ khi có sự xuất hiện của một số thuốc hạ đường huyết có thể sử dụng khi có suy giảm
PGS TS BS Phạm Văn Bùi
BV Nguyễn Tri Phương
GS Thỉnh giảng ĐH Liège, Bỉ
Abstract
In type2 diabetic patients with renal impairment, glucose-lowering therapies are quite complicated and require more frequent monitoring of both renal function and glycaemic control. Moderate renal impairment (glomerular filtration rate 30 – < 60 ml/min) requires consideration of dose reduction or treatment cessation for metformin, glucagon-like peptide-1 receptor agonists, some sulphonylureas and some dipeptidyl peptidase-4 inhibitors. At lower rates of glomerular filtration down to about 15 ml/min, it may be appropriate to use a meglitinide, pioglitazone or certain sulphonylureas with careful consideration of dose and co-morbidities. Dipeptidyl peptidase-4 inhibitors can be used at reduced dose in patients with very low rates of glomerular filtration, and linagliptin can be used without dose reduction, and has been used in patients on dialysis. Insulin can be used at any stage of renal impairment, but the regimen and the dose must be suitably adjusted and accompanied by adequate monitoring.
I/ Đại cương
Gần đây, các vấn đề xử trí bệnh nhân (BN) đái tháo đường (ĐTĐ) có suy giảm chức năng thận đang ngày càng được chú ý, nhất là từ khi có sự xuất hiện của một số thuốc hạ đường huyết có thể sử dụng khi có suy giảm chức năng thận từ vừa đến nặng. Dưới đây là tổng quan cập nhật chủ yếu về điều trị ĐTĐ týp 2 nơi BN có suy giảm chức năng thận.
II/ Suy giảm chức năng thận trong ĐTĐ týp 2
Chúng ta đã biết rằng độ lọc cầu thận (ĐLCT) sẽ giảm trung bình khoảng 0,75 ml/min/năm trong quá trình lão hóa, tiến trình suy sụp ĐLCT này có thể nhanh hơn khi có bệnh tim mạch, béo phì và ĐTĐ. Khi ĐTĐ tiến triển, chức năng thận sẽ suy sụp nhanh hơn và hầu như luôn luôn song hành với thời gian và độ nặng của tăng đường huyết[1-4] .
Mặc khác, mặc dầu không luôn luôn nhưng thường có sự song hành giữa suy giảm ĐLCT và sự xuất hiện cũng như sự gia tăng số lượng albumin trong nước tiểu[5-7]; và dù có kiểm soát chặc chẽ huyết áp, dường như 40% BN ĐTĐ cuối cùng sẽ bị suy giảm vừa phải ĐLCT(< 60/ml/phút) và khoảng 2-3% tiếp tục bị suy giảm nặng chức năng thận(ĐLCT< 30ml/phút)[ 8], khoảng 1% tiến đến suy thận giai đoạn cuối cần lọc máu hay ghép thận[9].
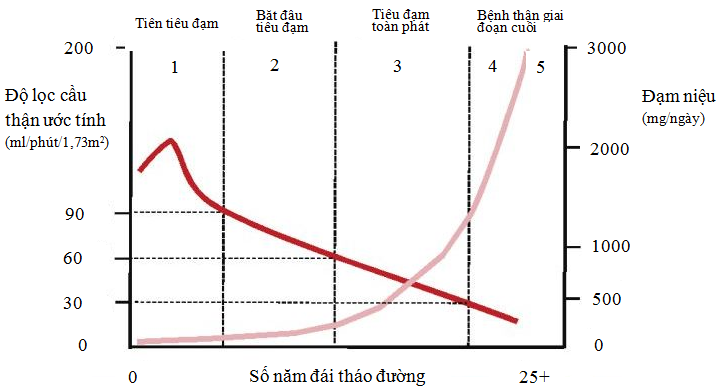
Hình 1: Tiến triển điển hình của bệnh thận mạn trong ĐTĐ týp 2 cho thấy giai đoạn tăng lọc khởi đầu theo sau là sự suy giảm dần dần ĐLCT với albumin niệu vi lượng tiến triển đến albumin niệu đại lượng [8].
Mặc dầu các bệnh mạch máu lớn và nhỏ đi kèm và có liên quan với ĐTĐ týp 2 nhưng lại thường được xem xét một cách riêng biệt. Sự suy giảm chức năng thận làm gia tăng các biến cố tim mạch và giảm ĐLCT làm nặng thêm bệnh tim mạch nơi BN ĐTĐ[10-13]. Tương tự, albumin niệu cũng tăng nguy cơ tim mạch[14]. Một số thử nghiệm lâm sàng đã chứng minh kiểm soát đường huyết tốt làm chậm sự xuất hiện và tiến triển bệnh thận trong ĐTĐ týp 2[15-17]. Như vậy, quan trọng là kiểm soát tốt đường huyết thật sớm ngay khi chẩn đoán và cần mọi cố gằng duy trì kiểm soát đường huyết khi suy thận xuất hiện[8].
III/ Các thuốc hạ đường huyết, chỉ định/chống chỉ định khi có suy giảm chức năng thận
Dưới đây là bảng tóm tắt về các thuốc hạ đường huyết, chỉ định/chống chỉ định khi có suy giảm chức năng thận. .
Bảng 1: Sử dụng các thuốc hạ đường huyết khi có suy giảm chức năng thận[8]
|
Thuốc |
Chất chuyển hóa |
Loại thải |
ĐLCT ước tính(ml/phút) |
|||
|
>60 |
60–30 |
<30 |
<15 |
|||
|
Metformin |
Không đổi |
~100 % qua nước tiểu |
✓ |
✓*?X |
X |
X |
|
Glimepiride |
Hoạt động |
~ 60 % qua nước tiểu |
✓ |
✓?* |
X |
X |
|
Glibenclamide |
Hoạt động |
<50 % qua nước tiểu |
✓ |
✓?* |
X |
X |
|
Glipizide |
Bất hoạt |
~ 70 % qua nước tiểu |
✓ |
✓ |
X |
X |
|
Gliclazide |
Bất hoạt |
~ 65 % qua nước tiểu |
✓ |
✓ |
?* |
X |
|
Tolbutamide |
Bất hoạt |
~100 % qua nước tiểu |
✓ |
✓?* |
✓* |
X |
|
Repaglinide |
Bất hoạt |
~ 90 % qua mật |
✓ |
✓ |
✓* |
X ? |
|
Nateglinide |
Bất hoạte |
~80 % qua nước tiểu |
✓ |
✓ |
✓ |
X ? |
|
Pioglitazone |
Hoạt động |
~ 55% qua mật |
✓ |
✓ |
X |
X |
|
Acarbose |
Trong ruộta |
~ 2 % qua nước tiểu |
✓ |
✓ |
X |
X |
|
Exenatide |
Lọc qua cầu thậnb |
Hầu hết qua nước tiểu |
✓ |
✓*?X |
X |
X |
|
Liraglutide |
Thoái biếnc |
Một phần qua nước tiểu |
✓ |
X |
X |
X |
|
Sitagliptin |
Không đổi |
~ 80 % qua nước tiểu |
✓ |
✓* |
✓* |
✓* |
|
Vildagliptin |
Bất hoạt |
~ 85 % qua nước tiểu |
✓ |
✓* |
✓* |
✓* |
|
Saxagliptin |
Hoạt động |
~ 60 % qua nước tiểu |
✓ |
✓* |
✓* |
✓*? |
|
Linagliptin |
Không đổid |
~ 80 % qua mật |
✓ |
✓ |
✓ |
✓ |
|
Insulin |
Thoái biếnc |
Một phần trong nước tiểu |
✓ |
✓* |
✓* |
✓* |
ĐLCT= độ lọc cầu thận; ✓= chỉ định ; ? = chỉ định thay đổi; X = chống chỉ định; * xem xét giảm liều, theo dõi thường xuyên và tình trạng sức khỏe tương ứng; a = chất chuyển hóa được hình thành trong ruột; b = hầu hết được loại thải thông qua lọc cầu thận; c = y thoái biến trong hệ tuần hoàn, gan và thận; d = hầu hết được loại thải không đổi qua mật; e = hầu hết được loại thải dưới dạng bất hoạt
Thuốc hạ đường huyết và suy giảm chức năng thận
Metformin
Metformin được loại thải qua thận hầu như hoàn toàn dưới dạng nguyên thủy, một phần qua lọc cầu thận và một phần qua bài tiết ống thận. Để tránh tích tụ thuốc quá mức có thể gây nguy cơ nhiễm toan lactic, thuốc được khuyên nên ngưng khi ĐLCT < 60ml/phút. Tuy nhiên, nhiều nghiên cứu như NICE (National Institute for Health and Clinical Excellence) ở Anh gợi ý không nên dùng metformin khi ĐLCT < 45 ml/phút. Nếu BN đã được kiểm soát tốt bằng metformin thì có thể tiếp tục đến khi ĐLCT < 30ml/phút với điều kiện BN phải được theo dõi chức năng thận thường xuyên và điều chỉnh liều khi cần thiết. Cũng cần xem xét, chú ý đến các mặt khác về sức khỏe của BN nhằm giảm thiểu nguy cơ vẫn sử dụng metformin khi có các chống chỉ định như bệnh cảnh giảm ôxy máu, hay giảm chức năng gan[18-19]. Phân tích chi tiết về dùng metformin trong suy thận từ nhẹ đến vừa phải gợi ý rằng khuyến cáo trong nghiên cứu NICE đã tạo cơ hội tăng số lượng BN ĐTĐ týp 2 có thể điều trị bằng metformin với nguy cơ tối thiểu bị tích tụ thuốc và các phản ứng phụ không mong muốn tương ứng[20]. Tuy nhiên, cần chú ý theo dõi chức năng thận thật chặt chẽ [8]
Sulphonylureas and Meglitinides
Các sulphonylureas (SU) khác nhau rất nhiều về phương diện chuyển hóa và đường loại thải thuốc [21]. Các thuốc có các chất chuyển hóa còn hoạt tính sẽ có tác dụng dược lực kéo dài, như glibenclamide và glimepiride chẳng hạn thì cần tránh sự tích tụ thuốc. Vì một phần các chất chuyển hóa của các thuốc này sẽ loại thải qua thận nên cần thận trọng và chỉnh liều khi có suy chức năng thận vừa phải, và glibenclamide , glimepiride không được khuyến cáo sử dụng khi suy thận nặng; điều này đặc biệt quan trọng ở người lớn tuổi và những người có lối sống hàng ngày rấy thay đổi, trong đó tụt đường huyết là vấn đề cần chú ý đặc biệt . Gliclazide có các chất chuyển hóa bất hoạt nên có thể xem xét sử dụng khi suy thận nhưng cần theo dõi và chỉnh liều. Tolbutamide là loại sulphonylurea có thời gian tác dụng ngắn và chất chuyển hóa bất hoạt được loại thải vào nước tiểu, cần theo dõi và chỉnh liều khi suy thận. Vì các sulfonylureas chuyển hoá ở gan nên cần chú ý chức năng gan và nguy cơ tương tác thuốc nhất là khi có suy giảm chức năng thận[21].
Với meglitinides, cần chú ý repaglinide hầu như được chuyển hóa ở gan thành chất bất hoạt và loại thải vào đường mật, và có thể sử dụng thận trọng cũng như phải chỉnh liều khi chức năng thận thấp. Nateglinide cũng được chuyển hóa nhanh ở gan thành chất có hoạt tính yếu loại thải vào nước tiểu nên khi chức năng gan còn tốt có thể sử dụng thận trọng và chỉnh liều khi chức năng thận giảm[8].
Pioglitazone
Pioglitazone là thuốc duy nhất thuộc nhóm thiazolidinedione(TZD) còn lưu hành, thuốc được chuyển hóa thành chất còn hoạt tính và loại thải một phần (< 45%) vào nước tiểu . Pioglitazone có thể dùng khi chức năng thận giảm nhưng cần chú ý các bệnh đi kèm và các thận trọng khác nhất là suy tim và suy gan; thuốc cũng gây giữ muối nước và nguy cơ gãy xương nên cần thận trọng trong suy thận và nguy cơ làm nặng thêm suy tim ứ huyết[8].
Acarbose
Acarbose có tác dụng ức chế sự hấp thu đường, hầu như được thoái hóa trong ruột và chất chuyển hóa bất hoạt có thể được hấp thu và hầu hết được loại thải vào nước tiểu[8]. Thuốc không được khuyến cáo sử dụng khi độ thanh thải creatinin < 25 ml/min/1.73 m2.
Chất đồng vận GLP-1.
Chất đồng vận GLP-1 exetinide hầu như được loại thải bởi lọc cầu thận và được thoái hóa trong thận[8]. Hậu quả là cần thận trọng khi suy thận vừa phải vớiđộ thanh thải creatinin 30-50ml/phút, nhất là khi tăng liều từ 5µg lên 10µg/ mũi tiêm. Exetinide không được khuyến cáo nếu độ thanh thải creatinin < 30ml/phút. Exetinide 2mg/tuần cũng không được khuyến cáo trong suy thận từ vừa đến nặng.
Liraglutide được chuyển hóa hầu hết ở mô và chỉ một phần nhỏ (< 15%) được chuyển hóa trong huyết tương, không được khuyến cáo khi độ thanh thải creatinin < 60ml/phút[8].
Ức chế DPP-4
Các thuốc ức chế DPP-4được chuyển hóa và loại thải qua nhiều đường khác nhau giúp chúng có thể sử dụng trong suy thận với những thận trọng khác nhau. Nhóm này có đặc điểm là không làm tăng cân và ít nguy cơ tụt đường huyết so với sulphonylureas hay insulin.
Sitagliptin hầu như được loại thải vào nước tiểu dưới dạng nguyên thủy nên phải chỉnh liều thích hợp khi chức năng thận suy giảm[8]. Liều bình thường là 100mg/ngày, cần phải giảm 50% (50mg/ngày) khi suy thận vừa phải (30ml/phút ≤ độ thanh thải creatinin < 50ml/phút). Trong suy thận nặng (độ thanh thải creatinin < 30ml/phút) hay suy thận giai đoạn cuối cần lọc máu, cần phải giảm liều hơn nữa xuống còn 25mg/ngày.
Vildagliptin được chuyển hóa hầu như tại thận thành chất bất hoạt được loại thải qua thận. Hiện tượng này độc lập với men CYP 450 và các men này không bị ức chế hay kích thích bởi vildagliptin. Nơi BN có suy thận từ vừa đến nặng, vildagliptin được khuyến cáo giảm còn 50% liều bình thường tức 50mg/ngày (liều bình thường 50mg, 2 lần/ngày). Cũng có thể dùng cho BN suy thận giai đoạn cuối hay lọc máu nhưng cần thận trọng và theo dõi chặc chẽ[8].
Saxagliptin được chuyển hóa chủ yếu ở gan thành chất còn hoạt tính loại thải vào nước tiểu[8]. Theo đó, liều bình thường (5mg/ngày) phải giảm xuống còn 2,5mg/ngày nơi BN có suy thận từ vừa đến nặng và không được sử dụng cho BN suy thận giai đoạn cuối cần chạy thận nhân tạo.
Linagliptin hầu như được loại thải phần lớn qua mật và rất ít bị chuyển hóa khiến cho thuốc này thích hợp và an toàn sử dụng cho bất cứ giai đoạn nào của suy thận mà không cần chỉnh liều[22]. Do thuốc chuyển hóa ít tại gan (<10%) và thành chất không hoạt tính, nên cũng có thể sử dụng cho BN co suy chức năng gan và cũng không chỉnh liều. Liều dùng 5mg/ngày cho mọi BN, chỉ khi dùng cho BN lọc máu thì cần thận trọng theo dõi, vì có < 5% thuốc được thải qua thận[8].
Nhằm đánh giá xem linagliptin có bảo vệ thận nơi BN ĐTĐ týp 2, Eynatten[23] đã thực hiện phân tích gộp 13 thử nghiệm lâm sàng, mù đôi, có kiểm chứng. Tổng cộng có 5.466 BN ĐTĐ týp 2 không được kiểm soát đường huyết tốt, chia ngẫu nhiên làm hai lô: Linagliptin (3505 BN) và giả dược (1961BN). Điều trị Linagliptin: trung bình 7 tháng (12 tuần-2 năm).
Hai nhóm tương thích tốt: quần thể, xét nghiệm, các thông số về ĐTĐ, bệnh sử tim mạch, thận và thuốc đang sử dụng.
Đánh giá tính an toàn trên thậnqua: đạm niệu vi thể mới xuất hiện, hoặc đạm niệu đại thể, hoặc creatinin tăng ≥ 2.83 mg/dL, hoặc bệnh thận mạn xấu đi với ĐLCT ước tính giảm > 50% so với trị số cơ bản, hoặc suy thận cấp, hoặc tử vong do mọi nguyên nhân.
Kết quả cho thấy BN dùng linagliptin: ¯16% biến chứng thận so với BN dùng giả dược (HR = 0.84; 95% CI, 0.72 – 0.97; P < .05). Tỷ lệ biến chứng thận mới mắc 266.8/1000 BN-năm/linagliptin so với 308.9/1000 BN-năm/giả dược.
Gần đây, trong một nghiên cứu về hiệu quả và tính an toàn của linagliptin nơi BN ĐTĐ týp 2 có nguy cơ tim mạch và thận cao, các tác giả[24] đã thực hiện phân tích gộp 6 thử nghiệm lâm sàng pha III. Trong 3.119 BN, 512 có đạm niệu vi lượng và tăng huyết áp (366 được điều trị linagliptin và 146 dùng giả dược). Các thông số ghi nhận giữa nhóm được điều trị linagliptin và nhóm dùng giả dược lần lượt là HbA1c 8.3 (0.9)% và 8.4 (0.9)%; đường huyết lúc đói 176(52) và 178(39)mg/dL ; tỷ số albumin/creatinin niệu 60 (30–292) mg/g và 64 (30–298) mg/g; huyết áp tâm thu 138 (15) mm Hg và 135 (16) mm Hg; huyết áp tâm trương 81 (10) mm Hg và 81 (10) mm Hg. Ngoài ra, hai nhóm tương thích nhau về chủng tộc, tuổi, giới tính, chỉ số khối lượng cơ thể (BMI-body mass index), thời gian từ lúc chẩn đoán bệnh đến nghiên cứu, các mức độ ĐLCT ước tính, thuốc điều trị ĐTĐ trước đó, thuốc hạ áp.
Ở BN có đạm niệu vi lượng và tăng huyết áp được điều trị với linagliptin, HbA1c giảm nhiều hơn một cách có ý nghĩa từ mức căn bản đến tuần 18 là −0.57 (0.06)% so với giả dược là 0.0 (0.08)% (95% CI: −0.75, −0.39; P < 0.0001). Ở tuần 24 HbA1c nhóm linagliptin là −0.65 (0.06)% và nhóm giả dược là −0.05 (0.09)%; tạo sự thay đổi trung bình từ trị số cơ bản hiệu chỉnh giả dược là -0.59% (95% CI: −0.80, −0.39; P < 0.0001).
Lignagliptin cũng giảm đường huyết lúc đói tốt hơn giả dược: thay đổi từ trị số cơ bản đến tuần 18 là −12.3 (2.3) mg/dl ở nhóm linagliptin và −1.6 (3.5) mg/dl ở nhóm giả dược, tạo sự thay đổi trung bình từ trị số cơ bản hiệu chỉnh giả dược là −10.6 mg/dl (95% CI: −18.4, −2.9; P = 0.0074). Ở tuần 24, đường huyết lúc đói thay đổi trung bình từ trị số cơ bản là −13.4 (2.9) mg/dl nhóm linagliptin và 7.9 (4.4) mg/d nhóm giả dược; tạo sự thay đổi trung bình từ trị số cơ bản hiệu chỉnh giả dược là −21.3 mg/dl (95% CI: −31.0, −11.6; P < 0.0001).
Thay đổi trung bìnhtỷ số albumin/creatinin niệu từ trị số cơ bản đến tuần 24 là −13.7 (−240.4 đến 695.7) mg/g với linagliptin và −4.9 (−234.3 to 2,263.9) mg/g với giả dược; tạo sự thay đổi trung bình từ trị số cơ bản hiệu chỉnh giả dược là −8.8 mg/g ở tuần 24 .
Các thay đổi về huyết áp tâm thu, huyết áp tâm trương, cholesterol và triglyceride không có khác biệt thống kê giữa hai nhóm.
Các loại phản ứng phụ không mong muốn giữa hai nhóm tương tự nhau 10,4% nhóm linagliptin và 8,2% nhóm giả dược. Các phản ứng phụ khiến phải ngưng thuốc là 1,4% ở nhóm linagliptin và 3,4% ở nhóm giả dược. Dưới 1% bị tụt đường huyết khi dùng linagliptin đơn trị hay kết hợp với metformin hay pioglitazone. Tuy nhiên khi linagliptin kết hợp với sulfonylurea, số lượng BN cảm nhận tụt đường huyết lớn hơn so với kết hợp với giả dược (linagliptin: 19.8% và giả dược: 5.9%).
Các tác giả kết luận ở BN ĐTĐ týp 2, có yếu tố nguy cơ tim mạch, thận thường gặp là tăng huyết áp và đạm niệu vi lượng, linagliptin 5mg/ngày dung nạp tốt và giúp cải thiện đường huyết. Linagliptin có thể giúp hỗ trợ các liệu pháp chiến lược dài hạn để điều trị các BN có nguy cơ cao bệnh thận và tim mạch.
Hiểu những tương đồng và khác biệt về hiệu quả và tính an toàn giữa các chất đồng vận GLP-1 và các chất ức chế DPP-4 góp phần quan trọng trong quyết định điều trị và tối ưu hóa liệu pháp thích hợp cho từng cá nhân. Chẳng hạn, các chất đồng vận GLP-1 sẽ thích hợp sử dụng cho người có béo phì hay tăng trọng và cho những người đang điều trị bằng SU, TZD hay insulin. Thật vậy, bổ sung chất đồng vận GLP-1 cho người không kiểm soát đường huyết tốt bằng insulin glargine đã cho thấy giảm được nguy cơ tụt đường huyết, giúp giảm cân lâu dài và cải thiện HbA1c một cách có ý nghĩa. Trong khi đó, các chất ức chế DPP-4 có thể được ưa thích hơn để bổ sung thêm cho những BN đang sử dụng thuốc hạ đường huyết mà không có tăng trọng, BN lớn tuổi, hay BN có các bệnh đi kèm như suy giảm chức năng thận hay có các vấn đề về tiêu hóa [25,26].
Insulin
Mặc dầu tất cả các mô nhạy cảm với insulin đều góp phần lấy đi và thoái hóa insulin lưu thông, gan và thận luôn là hai nơi chính loại thải insulin. Tại thận, một lượng insulin được lấy đi qua lọc cầu thận và có một phần của lượng này được ống thận tái hấp thu, hậu quả là khi thận giảm chức năng, insulin sẽ tồn tại lâu hơn trong huyết tương nên cần chỉnh liều[27].
IV/ Kết luận
Kiểm soát đường huyết không tốt sẽ tăng nhanh tiến triển bệnh thận nên cần duy trì kiểm soát đường huyết chặc chẽ khi chức năng thận bắt đầu suy giảm nhằm làm chậm hay phòng ngừa các hậu quả nguy hiểm. Giảm chức năng thận sẽ hạn chế sự chọn lựa thuốc hạ đường huyết và đòi hỏi các theo dõi đặc biệt tinh tế cả chức năng thận lẫn các thông số đường huyết. Tổn thương thận thường đi kèm các bệnh tim mạch và các bệnh lý khác ở BN lớn tuổi bị ĐTĐ týp 2 làm tăng tính phức tạp của điều trị, tăng nguy cơ tụt đường huyết nên cần chú ý đặc biệt đến liều lượng thuốc, sự tương tác cũng như sự chuyển hóa và loại thải của các thuốc hạ đường huyết. KDIGO, khuyến cáo đạt được HbA1c khoảng 7% sẽ giúp phòng ngừa hay làm chậm tiến triển các biến chứng vi mạch của ĐTĐ gồm cả bệnh thận do ĐTĐ[28].
Tài liệu tham khảo
- Pavkov ME, Knowler WC, Lemley KV et al. Early renal function decline in type 2 diabetes. Clin J Am Soc Nephrol 2012;7:78–84.
- American Diabetes Association. Standards of Medical Care in Diabetes: 2012. Diabetes Care 2012;35(suppl 1):S11-S63.
- Marshall SM, Flyvbjerg A. Diabetic nephropathy. In: Holt R, Cockram C, Flyvbjerg A, Goldstein B, (eds). Textbook of Diabetes, 4th edn. Chichester: Wiley-Blackwell, 2010:599–614.
- Girman CJ, Kou TD, Brodovicz K et al. Risk of acute renal failure in patients with type 2 diabetes mellitus. Diabet Med 2012;29:614–21.
- Lemley KV, Abdullah I, Myers BD et al. Evolution of incipient nephropathy in type 2 diabetes mellitus. Kidney Int 2000;58:1228–37.
- Myers BD, Nelson RG, Tan M et al. Progression of overt nephropathy in non-insulin-dependent diabetes. Kidney Int 1995;47:1781–9.
- Wright J, Vardhan A. The problem of diabetic nephropathy and practical prevention of its progression. Br J Diabetes Vasc Dis 2008;8:272–7.
- Bailey CJ , Day C . Diabetes Therapies in Renal Impairment. British Journal of Diabetes and Vascular Disease. 2012;12(4):167-171
- Abaterusso C, Lupo A, Ortalda V et al. Treating elderly people with diabetes and stages 3 and chronic kidney disease. Clin J Am Soc Nephrol 2008;3:1185–94.
- Foley RN, Murray AM, Li S et al. Chronic kidney disease and the risk for cardiovascular disease, renal replacement, and death in the United States Medicare population, 1998 to 1999. J Am Soc Nephrol 2005;16:489–95.
- Go AS, Chertow GM, Fan D et al. Chronic kidney disease and the risks of death, cardiovascular events and hospitalization. N Engl J Med 2004;351:1296–305.
- Sarnak MJ. Kidney disease as a risk factor for development of cardiovascular disease: a statement from the American Heart Association Councils. Circulation 2003;108:2154–69.
- Tonelli M, Muntner P, Lloyd A et al. Risk of coronary events in people with chronic kidney disease compared with those with diabetes: a population level cohort study. Lancet 2012:Doi 10.1016/S0140–6736(12)60572–8.
- Basi S, Fesler P, Mimran A, Lewis JB. Microalbuminuria in type 2 diabetes and hypertension A marker, treatment target, or innocent bystander? Diabetes Care 2008;31(suppl 2):S194–201.
- The action to control cardiovascular risk in diabetes study group. Effects of intensive glucose lowering in type 2 diabetes. N Engl J Med 2008;358:2545–59.
- The ADVANCE collaborative group. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. New Engl J Med 2008;358:2560–72.
- Duckworth W, Abraira C, Mortitz T et al. Glucose control and vcascular complications in veterans with type 2 diabetes. N Engl J Med 2009;360:129–39.
- Metformin. Summary of product characteristics. Revised 12 October 2010. www.medicines.org.uk/emc/medicine/1043/SPC/glucophage
- NICE clinical guideline 87. The management of type 2 diabetes. Revised May 2009. www.nice.org.uk/nicemedia/pdf/CG87QuickRefGuide.pdf
- Lipska KJ, Bailey CJ, Inzucchi SE. Use of metformin in the setting of mild-to-moderate renal insufficiency. Diabetes Care 2011;34:1431–7.
- Rendell M. The role of sulphonylureas in the management of type 2 diabetes mellitus.Drugs 2004;64:1339–58.
- Sloan L, Newman J, Sauce C et al. Safety and efficacy of linagiptin in type 2 diabetes patients with severe renal impairment. Diabetes 2011;60(suppl 1)Abs 413.
- von Eynatten Kidney Week 2012: American Society of Nephrology 45th Annual Meeting. Abstract TH-PO530. Presented November 1, 2012
- Maximilian von Eynatten, Yan Gong, Angela Emser, Hans-Juergen Woerle. Efficacy and Safety of Linagliptin in Type 2 Diabetes Subjects at High Risk for Renal and Cardiovascular Disease.A Pooled Analysis of Six Phase III Clinical Trials. Cardiovasc Diabetol. 2013;12(60)
- Handelsman Y, Blonde L, Fonseca V, James A. Shiffer, RPH. Focus On GLP-1 Receptor Agonists and Guideline-based Diabetes Care: Interlocking the Puzzle Pieces. Med Educ Diabetes & EndocrinologyCME 06/2013.
26. Richter B, Bandeira-Echtler E, Bergerhoff K, Lerch C. Emerging role of dipeptidyl peptidase-4 inhibitors in the management of type 2 diabetes. Vasc Health Risk Manag. 2008;4:753-768
- Duckworth WC, Bennett RG, Hamel FG. Insulin degradation: progress and potential.Endocr Rev 1998;19:608–24..
- KDIQO: KDIGO2012ClinicalPracticeGuidelinefortheEvaluationandManagementofChronicKidneyDisease. Kidney International, Suppl(1)2013: 76-77








