 Hội chứng chuyển hóa được định nghĩa là một nhóm các yếu tố nguy cơ về chuyển hóa tim mạch có liên quan đến sự đề kháng của insulin. Ngoài tầm quan trọng của mỗi yếu tố nguy cơ riêng biệt, thì sự hợp nhất của béo bụng
Hội chứng chuyển hóa được định nghĩa là một nhóm các yếu tố nguy cơ về chuyển hóa tim mạch có liên quan đến sự đề kháng của insulin. Ngoài tầm quan trọng của mỗi yếu tố nguy cơ riêng biệt, thì sự hợp nhất của béo bụng
Bộ Môn Lão khoa – Đại học Y dược TP.HCM
Tóm tắt
Hội chứng chuyển hóa được định nghĩa là một nhóm các yếu tố nguy cơ về chuyển hóa tim mạch có liên quan đến sự đề kháng của insulin. Ngoài tầm quan trọng của mỗi yếu tố nguy cơ riêng biệt, thì sự hợp nhất của béo bụng, giảm chuyển hóa glucose, rối loạn lipid máu và tăng huyết áp được gọi chung là hội chứng chuyển hóa, những cá nhân này có gia tăng rõ rệt nguy cơ mắc bệnh đái tháo đường típ 2 và bệnh tim mạch. Ở những nước phát triển, tần suất hội chứng chuyển hóa là 20% trong nhóm dân số trưởng thành, và tăng theo tuổi, chủ yếu là do tăng đáng kể số người thừa cân và béo phì ở người cao tuổi. Các dữ liệu hiện nay cho thấy rằng điều trị giảm cân cải thiện thể chất, chất lượng cuộc sống và các biến chứng về y tế có liên quan đến béo phì. Bản tổng kết này tóm tắt về dữ liệu dịch tễ học, tiêu chuẩn chẩn đoán và tầm quan trọng về mặt lâm sàng của hội chứng chuyển hóa, các cơ chế sinh bệnh học phức tạp liên quan đến sự đề kháng insulin ở người cao tuổi, và các lựa chọn điều trị khác nhau. Theo các dữ liệu này thì việc xác định và điều trị những bệnh nhân có hội chứng chuyển hóa là một cách tiếp cận quan trọng để làm giảm những khó chịu do bệnh gây ra và giảm sự suy yếu ở người cao tuổi.
GIỚI THIỆU
Ở những nước phát triển, tuổi thọ ngày càng tăng trong suốt những thập kỷ qua, song song với việc gia tăng những bệnh và tàn phế liên quan đến tuổi. Bên cạnh tuổi tác, tần suất cao của thừa cân, béo phì và các bệnh kèm theo có liên quan được xem là các vấn đề về y tế chủ yếu cũng ảnh hưởng đến nhóm dân số cao tuổi. Béo phì gây ra nhiều biến chứng nghiêm trọng về mặt y tế, bao gồm nhất là những bất thường về chuyển hóa, ung thư, tàn phế, hội chứng ngưng thở lúc ngủ do tắc nghẽn và tiểu không tự chủ. Đề kháng insulin, như là một rối loạn chính của các bệnh liên quan đến béo phì. Mức độ đề kháng insulin cho thấy gia tăng theo tuổi, và do vậy ở những người cao tuổi dễ hình thành các yếu tố nguy cơ chuyển hóa tim mạch hơn và được gọi chung là hội chứng chuyển hóa. Bên cạnh tầm quan trọng của mỗi yếu tố nguy cơ riêng lẻ, thì sự kết hợp của béo bụng, giảm chuyển hóa glucose, rối loạn lipid máu và tăng huyết áp dường như xác định ở những cá nhân có tăng rõ rệt nguy cơ mắc bệnh tim mạch và đái tháo đường típ 2. Nhiều bệnh nhân cao tuổi thường chưa nhận thức đúng đắn khi được chẩn đoán hội chứng chuyển hóa, vì vậy mà dễ dẫn tới bị tàn phế. Xét về khía cạnh việc gia tăng đáng kể của những vấn đề về sức khỏe này ở những người trên 65 tuổi, việc xác định và điều trị những bệnh nhân có hội chứng chuyển hóa là một cách tiếp cận quan trọng để làm giảm gánh nặng do bệnh gây ra và giảm sự suy yếu ở người cao tuổi.
ĐỊNH NGHĨA VÀ TẦN SUẤT CỦA HỘI CHỨNG CHUYỂN HÓA
Theo dịnh nghĩa gốc của Reaven, những thành phần chung nhất của hội chứng chuyển hóa là béo trung tâm, đề kháng insulin, tăng insulin trong máu và giảm dung nạp glucose, rối loạn lipid máu và tăng huyết áp. Các tình trạng về nội khoa như đông cầm máu, tiền viêm, bệnh gan nhiễm mỡ và hội chứng ngưng thở lúc ngủ do tắc nghẽn tiếp theo được định nghĩa như là những triệu chứng của hội chứng chuyển hóa. Nghiên cứu DECODE (the Eropean Diabetes Epidemiology Collabrotive survey analysis Of Diagnostic criteria in Europe) gần đây cho thấy rằng chẩn đoán hội chứng chuyển hóa dẫn đến việc gia tăng đáng kể tử vong do tim mạch và tất cả nguyên nhân, thậm chí ở những bệnh nhân không đái tháo đường [6]. Nhìn chung, nguy cơ xảy ra biến cố tim mạch tăng gấp đôi ở những bệnh nhân có hội chứng chuyển hóa so với những người không có hội chứng chuyển hóa; nguy cơ bị đái tháo đường típ 2 tăng gấp 5 lần. Hiện nay có nhiều định nghĩa về hội chứng chuyển hóa. Phần lớn các nghiên cứu về lâm sàng và dịch tễ học thực hiện việc đánh giá dựa theo tiêu chuẩn NCEP (National Cholesterol Education Program Adult Treament Panel) [10]. Trong những nghiên cứu này các bệnh nhân được xem là có hội chứng chuyển hóa khi có >= 3 trong 5 tiêu chuẩn (béo bụng, tăng triglyceride máu, giảm HDL cholesterol, tăng huyết áp hoặc đang sử dụng thuốc điều trị tăng huyết áp, đường huyết lúc đói cao hoặc đang sử dụng thuốc điều trị đái tháo đường). Theo định nghĩa của IDF (International Diabetes Federation) về hội chứng chuyển hóa, béo bụng được xem là tiêu chuẩn chẩn đoán cốt lõi [11] (bảng 1). Các khuyến cáo là nên đo vòng eo hơn là BMI (body mass index) ủng hộ cho tầm quan trọng của béo bụng trong hội chứng chuyển hóa.
Bảng 1. Tiêu chuẩn chẩn đoán hội chứng chuyển hóa trên lâm sàng
|
Các số đo lâm sàng |
NCEP, 2001 |
IDF, 2005 |
|
Chẩn đoán |
3 trong 5 đặc điểm sau |
Tăng vòng eo cộng với 2 trong các đặc điểm sau |
|
Cân nặng-vòng eo |
Vòng eo >= 102 ở nam hoặc >= 88 ở nữ |
Vòng eo >=94 ở nam hoặc >=80 ở nữ |
|
Các giá trị lipid |
Triglyceride >= 150 mg/dl; HDL-C <40 mg/dl ở nam hoặc <50 mg/dl ở nữ |
Triglycerides >=150 mg/dl HDL-C <40 mg/dl ở nam hoặc <50 mg/dl ở nữ |
|
Glucose |
Đường huyết đói >=110 mg/dl (bao gồm đái tháo đường) |
Đường huyết đói >= 100 mg/dl (bao gồm cả đái tháo đường) |
|
Huyết áp |
>=130 mmHg |
>=130/80 mm HG hoặc đang dùng thuốc hạ áp |
Cả hai định nghĩa về hội chứng chuyển hóa, tiêu chuẩn của NCEP-ATP hoặc IDF, thường được áp dụng trong thực hành lâm sàng và xác định những bệnh nhân có tăng nguy cơ bệnh tim mạch. Ứng dụng của tiêu chuẩn IDF ở những bệnh nhân đái tháo đường típ 2- so với định nghĩa theo NCEP- dẫn đến ước lượng tần suất hội chứng chuyển hóa cao hơn, nhưng không cải thiện về giá trị tiên lượng [13].
Trong một phân tích được xuất bản gần đây của một nghiên cứu cắt dọc ở người cao tuổi thì chẩn đoán hội chứng chuyển hóa theo tiêu chuẩn của IDF cho thấy nó không có sự liên quan đến nguy cơ nhồi máu cơ tim hoặc đột quị ở người cao tuổi [14]. Việc thiếu giá trị tiên đoán này ở nhóm dân số cao tuổi có thể được giải thích là do các định nghĩa về hội chứng chuyển hóa gần đây không xem xét đến tác động của tuổi lên các biến số giúp chẩn đoán. BMI, được tính bằng chiều cao (theo đơn vị m) chia cho cân nặng (theo đơn vị kg) bình phương được áp dụng như là một cách đơn giản để phân loại cân nặng. Không phụ thuộc vào tuổi, thừa cân được định nghĩa khi BMI từ 25-29.9 và béo phì khi BMI >=30 [15, 16]. Tuy nhiên, ở người cao tuổi, mối liên hệ giữa BMI và tỉ lệ lượng mỡ trong cơ thể bị thay đổi do kết quả của giảm chiều cao liên quan đến tuổi bởi xẹp thân đốt sống, và những thay đổi về thành phần cấu tạo trong cơ thể với việc giảm khối cơ và tăng khối mỡ [2]. Sự biến đổi chiều cao liên quan đến tuổi gây ra tăng BMI giả tạo đến 1.5 ở nam và 2.5 ở nữ. Thừa cân ở người cao tuổi được định nghĩa khi BMI >= 27 [17], BMI từ 25-27 không làm tăng tử vong do tim mạch và tất cả các nguyên nhân có thể được chứng minh [18].
Đa số cho rằng cân nặng có khuynh hướng gia tăng theo tuổi, đỉnh điểm từ 50-59, và sau đó giảm [19]. Giá trị của những dữ liệu quan sát này vẫn còn là một vấn đề đang tranh cãi liên quan đến những yếu tố gây nhiễu rằng những bệnh nhân béo phì có tỉ lệ tử vong lúc còn trẻ cao và có vòng đời ngắn, so với những bệnh nhân không béo phì có cơ hội sống thọ hơn rất nhiều [20]. Những kết quả từ các nghiên cứu đoàn hệ có thể cho thấy rằng cân nặng và BMI chỉ giảm nhẹ ở những người cao tuổi [21-23]. Hiện nay cũng có những dữ liệu đáng tin cậy hơn về những thay đổi trong thành phần cấu tạo của cơ thể liên quan đến tuổi. Khối cơ giảm đến 40% lúc 70 tuổi so với lúc 20 tuổi [2], khối lượng mỡ tăng chủ yếu tích tụ ở phần bụng [24], và tất cả những thay đổi liên quan đến tuổi này dẫn đến gia tăng tần suất hầu hết những bất thường về tim mạch và chuyển hóa được gọi chung là hội chứng chuyển hóa [2, 25]. Giá trị đường huyết lúc đói, nguy cơ đái tháo đường và tăng huyết áp tâm thu cho thấy có mối liên hệ chặt chẽ giữa tuổi và BMI [26].
SINH BỆNH HỌC
Sinh bệnh học của hội chứng chuyển hóa dường như phần lớn là do sự đề kháng insulin [5, 6]. Tuổi, gen và các yếu tố môi trường, như ăn thức ăn giàu calo và lối sống kém vận động làm tăng mức độ đề kháng insulin. Thừa cân, béo phì và đặc biệt là dạng tích tụ mỡ vùng trung tâm liên quan đến sự đề kháng insulin.
Béo phì là kết quả của sự cân bằng năng lượng dương trong thời gian dài dựa trên những tương tác phức tạp giữa các yếu tố môi trường và gen. Các nghiên cứu ở những gia đình có nhận người con nuôi và sinh đôi đã cho thấy tầm ảnh hưởng mạnh mẽ của gen [28, 29] và cho thấy rằng các giá trị BMI có liên quan giữa các thành viên trong gia đình dù được nuôi nấng riêng. Bên cạnh các dạng béo phì hiếm gặp do một gen gây ra, thì hơn 100 gen gây ra béo phì ở người đã được xác định cho đến thời điểm hiện tại [30]. Các gen có tính nhạy cảm này ảnh hưởng đến việc điều hòa cân nặng, sự biệt hóa các tế bào tạo mỡ và chuyển hóa. Dựa trên nền tảng về mặt di truyền này, các yếu tố môi trường gồm lối sống kém vận động, bữa ăn giàu năng lượng và các khía cạnh về mặt xã hội, làm gia tăng nguy cơ béo phì. Một kết quả được công bố gần đây của nghiên cứu Framingham đưa ra một lời giải thích thú vị về sự gia tăng tần suất béo phì trên toàn thế giới là một người sẽ dễ bị béo phì khi bạn, anh chị em hoặc người bạn đời của người đó bị béo phì [31]. Mạng lưới xã hội có thể là một yếu tố có liên quan đến sự bùng phát béo phì.
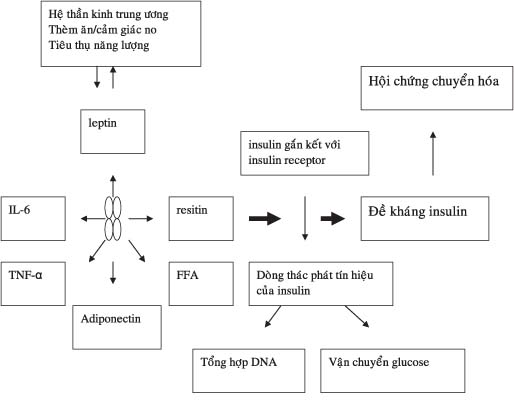
Béo phì làm tăng nguy cơ cho nhiều bệnh kèm theo, và những tiến bộ gần đây về sinh học mô mỡ cho một cái nhìn sâu hơn về các cơ chế sinh bệnh học phức tạp (hình 1). Các sản phẩm tiền viêm và nội tiết khác nhau từ mô mỡ nội tạng tương tác với dòng thác phát tín hiệu của insulin có thể được xác định [32]. Trong số những sản phẩm này, adiponectin giúp tránh sự đề kháng insulin và bệnh tim mạch [33], trong khi các acid béo tự do, leptin, resistin và các sản phẩm tiền viêm thúc đẩy dẫn đến đề kháng insulin [34]. Leptin, sản phẩm của gen gây béo phì, chủ yếu được sản xuất bởi mô mỡ, điều hòa sự hấp thu thức ăn và tiêu thụ năng lượng, sự chuyển hóa acid béo ở cơ vân và sản xuất glucose ở gan [35]. Hầu hết các dạng thường gặp của béo phì có đặc điểm là có nồng độ cao leptin lưu hành trong máu và sự đề kháng với leptin. Leptin có cấu trúc tương tự với các cytokine tiền viêm, như interleukin (IL)-6 mà IL này ảnh hưởng đến tác động của insulin. Các tế bào của phần mạch máu đệm trong mô mỡ, và đặc biệt là mỡ nội tạng, là những nguồn quan trọng sản xuất IL-6 [36]. Yếu tố hoại tử bướu alpha (TNF-a) là một adipocytokine khác được nghiên cứu nhiều và nó có thể có mối liên hệ với béo phì, viêm dưới mức l
âm sàng và đề kháng insulin. TNF-a làm giảm hoạt động của insulin bằng cách ức chế sự chuyến tiếp của adiponectin [37]. Các adipocytokines mới khác với những tác động lên độ nhậy cảm của insulin gần đây được phát hiện, gồm visfatin, mà nó làm gia tăng sản xuất IL-6 và TNF-a [38], protein-4 gắn kết với retinol, vaspin và omentin [39].
Hình 1. Sinh bệnh học của hội chứng chuyển hóa.

Bên cạnh các adipocytokines, sự tuôn ra ào ạt của các acid béo từ mô mỡ là nguyên nhân chính hình thành hội chứng chuyển hóa. Các acid béo tự do được phóng thích từ các triglycerides của mô mỡ thông qua hoạt động của men lipase nhạy cảm với hormone, và từ các lipoprotein giàu triglyceride thông qua ly giải mô mỡ bởi men lipoprotein lipase. Do cả hai cơ chế được điều hòa bởi insulin, nên sự đề kháng insulin dẫn đến việc tăng hơn nữa sự phóng thích các acid béo tự do từ các mô mỡ và làm giảm sự thanh thải các lipoprotein giàu triglyceride [40]. Tăng nồng dộ acid béo tự do trong huyết tương, liên quan với mức độ đề kháng insulin cao hơn, dẫn đến làm giảm tác động ức chế của insulin lên việc sản xuất glucose và tân tạo mỡ ở gan [40]. Kết quả là sự lắng đọng lipid ở các vị trí ngoại lai như gan, cơ vân và các đảo tụy, có thể xảy ra cùng với việc giảm chức năng của các cơ quan chuyên biệt (ngộ độc mỡ) [41]. Hơn nữa, có giả thuyết cho rằng một chế độ ăn giàu năng lượng – như là một sự kiện khởi đầu cho việc hình thành đề kháng insulin – làm quá tải mô mỡ, khả năng để dự trữ acid béo tự do trong các tế bào mỡ quá mức, và các lipid tích tụ ở các vị trí ngoại lai (giả thuyết chảy tràn ra) [42]. Xem xét sự đề kháng insulin liên quan đến tuổi, có thể dự đoán rằng tuổi của các tế bào mỡ với việc giảm khả năng dự trữ lipid liên quan đến các cơ chế phức tạp dẫn đến việc gia tăng tần suất hội chứng chuyển hóa ở người cao tuổi [43]. Những biến đổi liên quan đến tuổi trong thành phần cấu tạo cơ thể với việc giảm khối cơ và tăng khối mỡ làm tăng đề kháng insulin [6], và là kết quả của những thay đổi hormone phức tạp, gồm giảm hormone tăng trưởng và testosterone, và giảm đáp ứng với hormone tuyến giáp và leptin [2, 44-46]. Một lời giải thích thêm nữa cho việc tăng đề kháng insulin liên quan đến tuổi là việc nhận thấy rằng có sự giảm chức năng của ty thể và giảm cung cấp năng lượng cho tế bào ở người cao tuổi [47]. Những khiếm khuyết về sự phosphoryl oxi hóa trong ty thể được tìm thấy có mối liên hệ với sự tích tụ lipid ở cơ của người cao tuổi [48].
CÁC CHỌN LỰA ĐIỀU TRỊ
Các nghiên cứu lớn có thể cho thấy tính hiệu quả của thay đổi lối sống trong việc phòng béo phì và các bệnh kèm theo do béo phì [49]. Đặc biệt là nguy cơ bị đái tháo đường típ 2 cho thấy có mối liên hệ chặt chẽ với thừa cân và không hoạt động thể lực. Các nghiên cứu về phòng tránh đái tháo đường, như chương trình dự phòng đái tháo đường ở Phần Lan (Finnish Diabetes Prevention Program) [50] và chương trình dự phòng đái tháo đường ở Mỹ (US diabetes Prevetion Program) [51], khẳng định rằng việc giảm chút ít cân nặng và tăng hoạt động thể lực làm chậm tiến triển từ giảm dung nạp glucose đến đái tháo đường típ 2 thật sự. Trong một kết quả được công bố gần đây khi theo dõi liên tiếp 20 năm của nghiên cứu CHian Da Quing Prevetion, những người tham gia được can thiệp thay đổi lối sống cho thấy có xuất độ mắc đái tháo đường típ 2 thấp hơn 51% trong thời gian can thiệp tích cực và 43% trong suốt thời gian quan sát 20 năm [52]. Các kết quả khích lệ và lâu dài của việc thay đổi lối sống có tầm quan trọng rất lớn khi xét đến khía cạnh xuất hiện đái tháo đường típ 2 và vì vậy làm giảm nguy cơ tàn phế ở người cao tuổi. Điều trị giảm cân ở những người béo phì cao tuổi giúp cải thiện thể chất và chất lượng cuộc sống [2, 53].
Bên cạnh giảm cân và tăng hoạt động thể lực, metformin, glitazones, statins, các thuốc ức chế ACE và sartanes được tìm thấy có hiệu quả trong việc cải thiện độ nhậy của insulin ở những bệnh nhân nguy cơ cao [54, 55]. Giảm cân chút ít có chủ ý từ 5-15% cân nặng làm giảm đáng kể nguy cơ kèm theo ở những bệnh nhân thừa cân và béo phì [55]. Do đến nay chưa có những dữ liệu rõ ràng về tầm quan trọng của thừa cân và béo phì ở người cao tuổi (>=65 tuổi) về mặt tiên lượng, nên cần chú ý khi giảm cân. Chú ý này được hỗ trợ bởi những nghiên cứu cho thấy có tác dụng hữu ích của việc hơi thừa cân ở những người rất cao tuổi [56, 57]. Một phân tích tổng hợp được xuất bản gần đây, gồm 13 nghiên cúu, BMI từ 25-27, được định nghĩa là hơi thừa cân, có thể không được xem như là một yếu tố nguy cơ cho tử suất do tim mạch và tất cả nguyên nhân ở người cao tuổi [18]. Các chỉ số về béo nội tạng – như vòng eo – dường như là những chỉ điểm cho nguy cơ tim mạch tốt hơn BMI [44, 58]. Tăng khối mỡ ở bụng được cho là có liên quan độc lập với hội chứng chuyển hóa ở nam và nữ ở độ tuổi 70-79 [59].
Giảm cân bằng cách thực hiện chế độ ăn calorie thấp và ít chất béo và tăng hoạt động thể lực. Có thể tăng cường giảm cân bằng cách chống béo phì, hoặc, một thủ thuật hiếm được thực hiện ở người cao tuổi là phẫu thuật giảm thể tích dạ dày [55]. Do hầu hết các thử nghiệm lâm sàng loại những người cao tuổi ra [60, 62], nên biết rất ít về những lợi ích và những tai biến có thể xảy ra của việc giảm cân có chủ ý bằng các chương trình chế độ ăn hoặc dùng thuốc ở những bệnh nhân cao tuổi thừa cân và béo phì. Các phác đồ giảm cân làm giảm tối thiểu khả năng mất khối xương và cơ đặc biệt được khuyến cáo ở người cao tuổi, nhưng phải thay đổi phù hợp cho từng cá nhân. Nghiên cứu sức khỏe tim mạch Hoa Kỳ đánh giá vai trò của hoạt động thể lực ở một nhóm lớn nam và nữ có độ tuổi tử 65-100, và có thể cho thấy rằng tàn phế có liên quan chặt chẽ với khối mỡ [21]. Hoạt động thể lực đều đặn và trong thời gian dài giúp cải thiện tất cả các yếu tố nguy cơ dẫn đến hội chứng chuyển hóa [63], trong khi chỉ đi bộ nhẹ nhàng làm làm tăng khả năng mắc hội chứng chuyển hóa ở người cao tuổi [64]. Tập thể dục ngoài trời kích thích sinh tổng hợp của ty thể, các bài tập thể dục về độ bền làm tăng kích thước, số lượng, và hoạt động oxy h
óa của ty thể ở những bệnh nhân cao tuổi [65].
Hội chứng chuyển hóa và đái tháo đường típ 2
Hội chứng chuyển hóa gặp ở phần lớn bệnh nhân đái tháo đường típ 2 béo phì. Trong điều trị đái tháo đường típ 2, metformin và glitazones được xếp là những thuốc làm tăng độ nhậy insulin. Metformin được dùng trong chương trình phòng chống đái tháo đường [51], trong chương trình này có 648 trong số 3.2434 người tham gia > 60 utổi. Một kết quả được xuất bản gần đây của chương trình này cho thấy rằng những can thiệp về lối sống và metformin làm giảm mắc hội chứng chuyển hóa ở những bệnh nhân nguy cơ cao. [66]. Glitazones là những thuốc điều trị đái tháo đường giúp cải thiện độ nhạy insulin thông qua việc giảm thành phần lipid ở cơ và tái phân bố lipid vào các mô mỡ [67]. Cần thận trọng ở người cao tuổi vì có dữ liệu cho rằng khi điều trị với glitazones làm tăng tỉ lệ suy tim và gãy xương ở phụ nữ cao tuổi.
Các chiến thuật điều trị mới với hệ thống incretin. Glucagon-like peptide-1 (GLP-1) là một hormone dạ dày ruột được tiết bởi tế bào L của ruột sau khi ăn. GLP-1 kích thích tiết insulin ở tuyến tụy, ức chế sản xuất glucagons, kéo dài thời gian trống dạ dày và cảm giác no ở hệ thống thần kinh trung ương. Đặc biệt là làm giảm sự thèm ăn và vì vậy làm giảm cân nặng. GLP-1 có thời gian bán hủy rất ngắn do nó bị thoái biến bởi men dipeptidyl-peptidase IV có mặt hầu hết mọi nơi (DPP-IV). Incretin kháng DPP-IV tương tự extendin-4 và các thuốc ức chế DPP-IV gần đây đã được ứng dụng trên lâm sàng. Cần nghiên cứu rõ hơn về mức độ an toàn khi sử dụng lâu dài, và về những tác động của incretin.
Điều trị yếu tố nguy cơ tim mạch ở những bệnh nhân có hội chứng chuyển hóa
Những kết quả được xuất bản gần đây về statin cho thấy rằng giảm thấp LDL cholesterol một cách nghiêm ngặt giúp giảm đáng kể những gánh nặng và tử suất do tim mạch ở những bệnh nhân cao tuổi [69]. Đề kháng insulin liên quan đến kiểu hình lipoprotein gây xơ vữa với tăng triglyceride máu, tăng nồng độ apo-B chứa các lipoproteins trong huyết tương, giảm HDL cholesterol và các phần tử LDL kích thước nhỏ [70]. Tuy nhiên, mục tiêu chính trong điều trị giảm lipid vẫn là LDL cholesterol.
Tăng huyết áp rất thường gặp ở người cao tuổi, ảnh hưởng đến 50% trong số những người > 65 tuổi [2]. Thuốc điều trị tăng huyết áp phối hợp thường được dùng để hạ huyết áp đến <130/80 mm Hg [71], và điều trị tăng huyết áp thành công giúp làm giảm nguy cơ đột quỵ, các biến cố tim mạch và suy tim [71]. Hiệu quả và mức độ an toàn của các phác đồ điều trị tăng huyết áp cũng được cho thấy qua nhiều nhiên cứu ở người cao tuổi.
Nhóm các yếu tố nguy cơ chuyển hóa tim mạch, được gọi chung là hội chứng chuyển hóa, xác định những bệnh nhân cần điều trị nghiêm ngặt hơn, cũng nhằm mục đích phòng các bệnh và tàn phế do tuổi. Đặc biệt ở người cao tuổi, tình trạng của từng bệnh nhân phải được quan tâm, gồm những lợi ích, an toàn và những tác dụng phụ có thể xảy ra trong các phác đồ điều trị.
Tài liệu tham khảo
1 Rưssner S: Obesity in the elderly – a future matter of concern? Obes Rev 2001;2:183 -188.
2 Villareal DT, Apovian CM, Kushner RF, Klein S: Obesity in older adults: technical review and position statement of the American Soci- ety for Nutrition and NAASO, The Obesity Society. Am J Clin Nutr 2005;82:923-934.
3 Facchini FS, Hu N, Abbasi F, Reaven GM: In- sulin resistance as a predictor of age-related diseases. J Clin Endocrinol Metab 2001;86: 3574-3578.
4 Reaven GM: Banting Lecture 1988. The role of insulin resistance in human disease. Dia- betes 1988;37:1595-1607.
5 Eckel RH, Grundy SM, Zimmet PZ: The metabolic syndrome. Lancet 2005;365:1415- 1428.
6 Hu G, Qiao Q, Tuomilheto J, Balkau B, Borch-Johnsen K, Pyorala K: Prevalence of the metabolic syndrome and its relation to all-cause and cardiovascular mortality in non-diabetic European men and women. Arch Intern Med 2004;164:1066-1076.
7 Grundy SM: Metabolic syndrome pandemia. Arterioscler Thromb Vasc Biol 2008;28:629- 632.
8 McNeill AM, Katz R, Girman CJ, Rosamond WD, Wagenknecht LE, Barzilay JI, Tracy RP, Savage PJ, Jackson SA: Metabolic syndrome and cardiovascular disease in older people: the cardiovascular health study. J Am Geri- atr Soc 2006;54:1317-1324.
9 Yaffe K: Metabolic syndrome and cognitive disorders. Alzheimer Dis Assoc Disord 2007; 21:167-171.
10 Executive Summary of the Third Report of The National Cholesterol Education Pro- gram (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Pan- el III). JAMA 2001;285:2486-2497.
11 Alberti KG, Zimmet P, Shaw J; IDF Epide- miology Task Force Consensus Group: The metabolic syndrome – a new worldwide def- inition. Lancet 2005;366:1059-1062.
12 Despers JP, Lemieux I: Abdominal obesity and metabolic syndrome. Nature 2006;444: 881-887.
13 Monami M, Marchionni N, Masotti G, Man- nucci E: IDF and ATP-III definitions of met- abolic syndrome in the prediction of all- cause mortality in type 2 diabetic patients. Diabetes Obes Metab 2007;9:350-353.
14 Motta M, Bennati E, Cardillo E, Passamonte M, Ferlito L, Malaguarnera M: The metabol- ic syndrome in the elderly: considerations on the diagnostic criteria of the International Diabetes Federation and some proposed modifications. Arch Gerontol Geriatr 2008 (in press).
15 World Health Organization: Obesity: Pre- venting and Managing the Global Epidemic. Report of a WHO Consultation on Obesity. Geneva, WHO, 1998.
16 Willett WC, Dietz WH, Colditz GA: Guide- lines for healthy weight. N Engl J Med 1999; 341:427-439.
17 Volkert D, Berner YN, Berry E, et al: ESPEN guidelines on enteral nutrition: geriatrics. Clin Nutr 2006;25:330-360.
18 Heiat A, Vaccarino V, Krumholz HM: An evidence-based assessment of federal guide- lines for overweight and obesity as they apply to elderly persons. Arch Intern Med 2001; 161:1194-1203.
19 Harris TB, Launer LJ, Madans J, Feldman JJ: Cohort study of effect of being overweight and change in weight on risk of coronary heart disease in old age. BMJ 1997;314:1791- 1794.
20 Manson JE, Willett WC, Stampfer MJ, Cold- itz GA, Hunter DJ, Hankinson SE, Hennek- ens CH, Speizer FE: Body weight and mortal- ity among women. N Engl J Med 1995;333: 677-685.
21 Grinker JA, Tucker K, Vokonas PS, Rush D: Body habitus changes among adult males from the normative aging study: relations to aging, smoking history and alcohol intake. Obes Res 1995;3:435-446.
22 Kannel WB, Gordon T, Castelli WP: Obesity, lipids, and glucose intolerance. The Fram- ingham Study. A
m J Clin Nutr 1979; 32: 1238-1245.
23 Fogelholm M, Kujala U, Kaprio J, Sarna S: Predictor of weight change in middle-aged and old men. Obes Rev 2000;8:367-373.
24 Visser M, Langlois J, Guralnik JM, Cauley JA, Kronmal RA, Robbins J, Williamson JD: High body fatness, but not low fat-free mass, predicts disability in older men and women: the Cardiovascular Health Study. Am J Clin Nutr 1998;68:584-590.
25 Bo M, Sona A, Astengo M, Fiandra U, Qua- gliotti E, Brescianini A, Fonte G: Metabolic syndrome in older subjects: coincidence or clustering? Arch Gerontol Geriatr 2008 (in press).
26 Alexander CM, Landsman PB, Grundy SM: The inf luence of age and body mass index on the metabolic syndrome and its components. Diabetes Obes Metab 2008;10:246-250.
27 Ford ES, Giles WH, Dietz WH: Prevalence of the metabolic syndrome among US adults: findings from the Third National Health and Nutrition Examination Survey. JAMA 2002; 287:356-359.
28 Stunkard AJ, Sorensen TI, Hanis C, et al: An adoption study of human obesity. N Engl J Med 1986;314:193-198.
29 Stunkard AJ, Harris JR, Pedersen NL, Mc- Clearn GE: The body mass index of twins who have been reared apart. N Engl J Med 1990;322:1483-1487.
30 Kưrner A, Kiess W, Stumvoll M, Kovacs P: Polygenic contribution to obesity: genome- wide strategies reveal new targets. Front Horm Res 2008;36:12-36.
31 Christakis NA, Fowler JM: The spread of obesity in a large social network over 32 years. N Engl J Med 2007;357:370-374.
32 Havel PJ: Update on adipocyte hormones; regulation of energy balance and carbohy- drate/lipid metabolism. Diabetes 2004; 53: S143-S151.
33 Matsuzawa Y, Funahashi T, Kimara S, Shi- momura I: Adiponectin and metabolic syn- drome. Arterioscler Thromb Vasc Biol 2004; 24:29-33.
34 Ridker PM: Inf lammatory biomarkers and risk for myocardial infarction, stroke, diabe- tes and total mortality: implications for lon- gevity. Nutr Rev 2007;65:S253-S259.
35 Dyck DJ, Heigenhauser GJ, Bruce CR: The role of adipokines as regulators of skeletal muscle fatty acid metabolism and insulin sensitivity. Acta Physiol 2006;186:5-16.
36 Grimble RF: Inf lammatory status and insu- lin resistance. Curr Opin Clin Nutr Metab Care 2002;5:551.
37 Hotamisligil GS, Arner P, Caro JF, Atkinson RL, Spiegelman BM: Increased adipose tis- sue expression of tumor necrosis factor- in human obesity and insulin resistance. J Clin Invest 1995;95:2409-2415.
38 Moschen AR, Kaser A, Enrich B, et al: Visfa- tin, an adipocytokine with proinf lammatory and immunomodulating properties. J Im- munol 2007;178:1748-1758.
39 Gustafson B, Hammarstedt A, Andersson CX, Smith U: Inf lamed adipose tissue: a cul- prit underlying the metabolic syndrome and atherosclerosis. Arterioscler Thromb Vasc Biol 2007;27:2276-2283.
40 Boden R, Shulman GI: Free fatty acids in obesity and type 2 diabetes: defining their role in the development of insulin-resistance and -cell dysfunction. Eur J Clin Invest 2002;32(suppl 3):14-23.
41. Friedman J: Fat in all the wrong places. Na- ture 2002;415:268-269.
42. Unger RM: Lipid overload and overf low: metabolic trauma and the metabolic syn- drome. Themes Endocrinol Metab 2003;14: 398-403.
43. Slawik M, Vidal-Puig AJ: Lipotoxicity, over- nutrition and energy metabolism in aging. Aging Res Rev 2006;5:144-154.
44. Beaufrre B, Morio B: Fat and protein redis- tribution with aging: metabolic consider- ations. Eur J Clin Nutr 2000;54(suppl):S48- S53.
45. Schwartz RS: Trophic factor supplementa- tion: effect on the age-associated changes in body composition. J Gerontol A Biol Sci Med Sci 1995;50:151-156.
46. Moller N, O’Brien P, Nair KS: Disruption of the relationship between fat content and leptin levels with aging in humans. J Clin Endocrinol Metab 1998;83:931-934.
47 Kim J, Wei Y, Sowers JR: Role of mitochon- drial dysfunction in insulin resistance. Circ Res 2008;102:401-414.
48 Petersen KF, Befroy D, Dufour S, Dziura J, Ariyan C, Rothman DL, DiPietro L, Cline GW, Shulman GI: Mitochondrial dysfunc- tion in the elderly: possible role in insulin re- sistance. Science 2003;300:1140-1142.
49 Galani C, Schneider H: Prevention and treat- ment of obesity with lifestyle interventions: review and meta-analysis. Int J Public Health 2007;52:348-359.
50 Tuomilehto J, Lindstrưm J, Eriksson JG, et al; Finnish Diabetes Prevention Study Group: Prevention of type 2 diabetes mellitus by changes in lifestyle among subjects with im- paired glucose tolerance. N Engl J Med 2001; 344:1343-1350. v.v…








